摘要
关于癌症患者是否应筛查潜伏性结核感染(LTBI)存在不确定性。我们进行了系统回顾和荟萃分析,以估计癌症中结核(TB)的相对发病率。
我们在MEDLINE和Embase中搜索2016年12月21日之前发表的研究。我们包括评估实体癌和血液系统恶性肿瘤患者相对于参考组(研究对照组或普通人群)的结核病发病率的研究。合并估计发病率比率(IRR)采用标准荟萃分析方法获得。
搜索策略确定了13项独特的研究,包括921名464名患有癌症患者。成人癌症患者的TB IRR为2.61(95%CI 2.12-3.22;我2= 91%)。在血液癌中,IRR为3.53 (95% CI 1.63-7.64;我2= 96%);在成人实体癌中,该比值为2.25 (95% CI 1.96-2.58;我2= 91%)。儿童血液系统恶性肿瘤或实体癌的IRR最高(IRR 16.82, 95% CI 8.81-32.12;我2=79%).
考虑到癌症患者最大限度免疫抑制的持续时间有限,以及由于预期寿命缩短而导致结核病的累积终生风险降低,儿童(而非成人)的风险水平似乎足以保证LTBI的系统筛查。
摘要
应考虑对患有癌症的儿童进行潜伏性结核感染的筛查和治疗http://ow.ly/lpSQ30dxyam
介绍
结核病(TB)是全球疾病和死亡的主要传染性原因之一1].目前,对潜在结核病感染(LTBI)的筛查和治疗重新引起了人们的兴趣,作为控制全球结核病流行的一种可能手段[2].在大多数感染者中,结核病在临床上仍无症状,微生物学上不活跃(潜伏)。然而,在约5%至10%的潜伏感染者中,感染会在其一生中的某个时刻导致活动性结核病[3.]。在免疫功能受损的人群中,如艾滋病毒感染者,结核病再激活的风险增加[4]、慢性肾衰竭[5]还是糖尿病[6],并在免疫抑制药物上的人员,如肿瘤坏死因子-α(TNF-α)抑制剂[7,8].世界卫生组织(世卫组织)建议在高或中高收入国家筛查高风险群体,每年具有TB的<100每年<100 000 [9],因为预防性结核病治疗可以显著降低结核病复发的风险[10.].
实性癌症和血液系统恶性肿瘤的患者由于疾病本身和化疗的结果而免疫功能低下。因此,有理由认为癌症患者的结核再激活风险会增加,并考虑在这一组进行LTBI筛查和治疗。然而,关于癌症患者是否应该进行LTBI筛查的信息很少。英国国家健康和护理卓越研究所(NICE)的建议指出,“有血液恶性肿瘤”、“正在接受化疗”和“做过胃切除术”(因为胃癌或其他原因)的人患结核病的风险增加,但他们没有为这些群体提供任何具体的筛查和治疗建议[11.].美国胸科协会(ATS)和美国疾病控制与预防中心(CDC)的联合指南,由美国传染病协会理事会(IDSA)认可,确定患有“某些血液病(例如”及“其他特定恶性肿瘤(例如,头颈癌和肺癌)为高风险,建议考虑对这些人群进行LTBI治疗[12.].为这些指南提供依据的证据来自20世纪50年代至70年代进行的非正式综合研究,这些研究具有重要的方法局限性:癌症患者中结核病的发生率以比例(累积发病率)而不是发病率表示;因此不调整观察期/风险时间。相对风险估计值的计算方法是将癌症队列中结核的累积发病率除以一般人群的发病率(每年)[13.]或根本没有计算[14.].
Cheng最近发表的系统综述和荟萃分析等. [15.关于癌症患者TB的风险也具有显着的方法局限性。该分析并未排除含有关于TB累积发病率的信息的研究,并且使用年度特定的TB发病率,未被视为从谁进行比较获得的潜在混乱[15.].比较癌症患者TB的累积发病率(在一个包括在25岁的研究期间的研究中累积[16.]),这将导致高估癌症患者患结核病的风险。同样,使用普通人群作为比较组,而不对潜在的混杂因素进行任何调整,特别是年龄,将导致高估癌症患者的结核病风险。作者的研究结论是,生活在美国的血液病、头颈癌和肺癌患者将受益于靶向LTBI筛查和治疗,因此必须提出质疑。
2014年发表的另一项系统综述只关注肺癌,并评估了这些患者的结核病患病率[17.].该综述的目的不是建立因果关系(作者意识到肺癌和结核病之间存在双向因果关系[18.])。
如果有证据表明存在LTBI,癌症患者是否应进行LTBI筛查以提供预防性治疗仍然存在相当大的不确定性。尽管需要当代证据来告知关于LTBI scr的指导方针和公共卫生政策,癌症患者的结核病风险仍然无法精确量化因此,我们进行了系统回顾和荟萃分析,以评估癌症患者(实体癌和血液系统恶性肿瘤)与普通人群相比结核病的相对发病率。
方法
搜索策略和选择标准
我们搜索了电子数据库MEDLINE,包括EPUB,在印刷,进程和其他非索引引文(1946年至2016年12月21日)和EMBASE(1947年至2016年12月21日),通过OVID进行研究的研究癌症中的结核病(实体肿瘤和血液恶性肿瘤)。作者讨论并讨论了搜索战略,并从经验丰富的研究馆员寻求建议。以下搜索条文用于识别与(1)结核病,(2)风险和(3)癌症相关的引文:(1)结核,结核分枝杆菌; (2) risk, incidence, probability, proportion, frequency; and (3) neoplasm, cancer, malignancy, tumour, carcinoma, oncology and metastases. The detailed search strategy is available in the supporting information (S1 Appendix). Articles resulting from these searches and relevant references cited in those articles were reviewed. In addition, we screened reference lists of systematic reviews, literature reviews and meta-analyses identified through the search. Articles published in any language were included.
合格的研究评估了相对于参照组(研究指定的对照组,或对潜在混杂因素进行调整或不进行调整的一般人群)的癌症患者中结核病的发病率,从而可以估计癌症患者中结核病的相对风险。我们包括了肺结核病和肺外结核病的研究报告。结核病的诊断可以根据微生物学结果,也可以根据与结核病相一致的症状和胸部x光检查结果。研究包括任何年龄组的实体癌症或血液系统恶性肿瘤的报告。关于接受干细胞移植患者患结核病风险的研究被排除在外。我们排除了横断面(流行率)研究、使用未调整风险时间的累积发病率(发病率比例)的研究、结核病诊断先于癌症诊断的研究以及结核病与癌症之间的时间关系未明确的研究。此外,我们排除了仅检测了预先定义的癌症患者亚组中结核病风险的研究,这些亚组被认为在检测前结核病感染的可能性增加(例如由于胸片异常)。摘要、社论、病例报告、会议摘要、系统综述、文献综述和荟萃分析不包括在内。三名评审员(C.C.Dobler、K.Cheung和J.Nguyen)独立筛选标题和摘要,然后由至少一名评审员确定可能合格的论文全文。评审员之间的分歧通过讨论解决。该系统评审遵循PRISMA(系统评审和元分析的首选报告项目)观察性研究的荟萃分析和系统评价报告指南[19.].
数据分析
三位审稿人(C.C. Dobler, K.张和J. Nguyen)独立地将纳入研究的数据提取到标准化数据表中。每篇文章记录的变量包括:
发表年份、国家、研究设计、患者数量、癌症组结核发病率、参照组结核发病率(即。对照样本或适用的一般人口统计数据)、随访时间、患者的人口统计学和临床特征、既往TB(基于病史、胸片、等.)、基于结核菌素皮肤试验(TST)或干扰素释放试验(IGRA)的LTBI患病率、LTBI治疗、癌症类型、化疗信息和研究目的的结核病定义。纳入研究的偏倚风险采用队列研究纽卡斯尔-渥太华质量评估量表进行评估[20.].
对于未具体报道IRR的研究,通过将TB在参考组中TB的发病率分开TB的发病率来计算IRR。如果没有报告,假设观察病例的频率遵循泊松分布[21.].我们接受了危险比(HRs),危险比(即。与对照组或一般人群相比,癌症患者中的“瞬时”速率),作为IRS的估计[22.]。对于报告粗略内部收益率以及调整或标准化内部收益率的研究,我们将调整或标准化内部收益率(分别为aIRR和标准化发病率(SIR))纳入荟萃分析。我们使用DerSimonian和Laird随机效应荟萃分析[23.使用综合meta分析v3.0软件(Biostat, Englewood, NJ, USA)估算合并的内部收益率和95% CIs。我们使用我2统计量,并使用Q -统计。对年龄组(成人)进行预先指定的亚组分析对儿童),以及任何特定的实体肿瘤或血液系统恶性肿瘤。
由于在纳入的研究中,每个患者或对照组最多有一个事件(结核病诊断),IRR表示结核病的相对风险,因此这两个术语可以互换使用。
结果
搜索策略确定了11 006个唯一引用,其中42个被纳入全文审查,13个研究符合纳入和排除标准,共涉及921 464例癌症患者(图1)。表1概述所收录研究的特点[24.- - - - - -36].
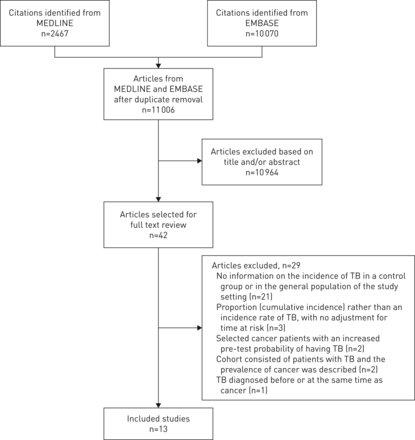
研究选择流程图。
研究特点
所有13项研究均为观察性和回顾性研究。五项研究基于国家数据库的信息,八项研究是在单一医院进行的队列研究。五项研究来自台湾,五项来自韩国,两项来自南非,一项来自美国。四项研究包括不同的血液癌和实体癌患者;各有一项研究仅分别报告了不同血液癌或实体癌患者患结核病的风险;7项研究只涉及特定癌症类型的患者(5项胃癌研究、1项肺癌研究和1项慢性髓系白血病研究)。来自南非的两项研究集中于患有不同血液学和实体恶性肿瘤的儿童(年龄在15岁以下)。研究规模从257人到855382人不等。
排除的一个常见原因(从本系统评价中)在全文回顾后评估癌症患者结核病风险的研究中,缺乏适当参考组中结核病发病率的信息。此外,一些研究被排除在外,因为它们以比例(累积发病率)表示癌症患者中的结核病病例而不是发病率,没有调整风险时间[16.,37,38].全文评论后,两项研究被排除在外,因为他们报告了癌症患者TB的风险增加了患有TB的预测概率增加(基于临床医生的评估[39或怀疑有结核的胸片异常[40])。另一项研究被排除在外,因为在大多数病例中,结核病是与癌症同时诊断的[41].在两个排除的研究中,所检查的队列由TB患者组成,描述了癌症的患病率[42,43].
荟萃分析中对混杂因素的调整概述在表1.
癌症患者结核病的相对风险
成人癌症患者结核的总体IRR为2.61 (95% CI, 2.12-3.22) (图2)。研究之间存在相当大的异质性(问统计,p < 0.001,我2= 91%)。两项研究在患有血液病和实体恶性肿瘤的儿童中进行的合并IRR为16.82 (95% CI 8.81-32.12;问= 5,DF.= 1, p = 0.030;我2= 79%) (图3)。
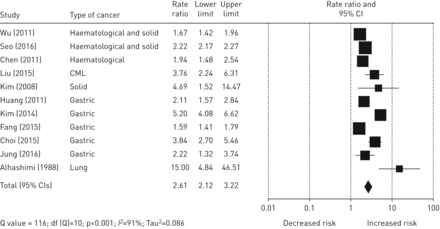
所有成年癌症研究中结核病相对风险的森林图。CML:慢性骨髓白血病。
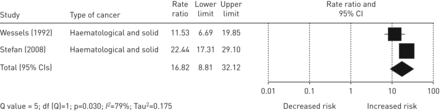
癌症儿童患结核病相对风险的森林图。
成人癌症患者的亚组分析
对血液系统恶性肿瘤和实体肿瘤的单独分析(不包括对这两组分别进行效应大小测量的研究)得出的IRR为3.53 (95% CI 1.63-7.64;Q =82年,df =3, p < 0.001;我2= 96%) (图4), IRR为2.25 (95% CI 1.96-2.58;问= 341,DF.= 29,p< 0.001;我2= 91%) (图5)。
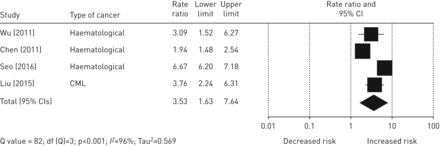
血液系统恶性肿瘤成人结核病相对风险森林图。慢性粒细胞白血病:慢性髓系白血病。
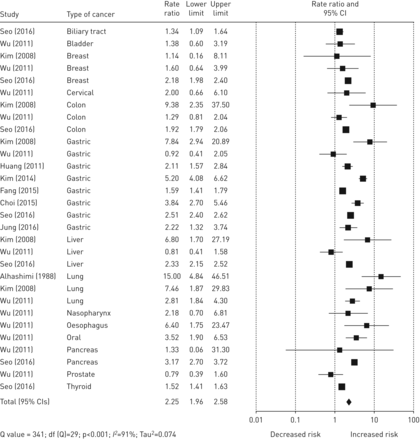
患有不同实体肿瘤的成人结核病相对风险森林图。
在至少三项研究中获得数据的实体肿瘤中,肺癌的IRR为6.14 (95% CI 1.97-19.20;我2= 76%)(图6A)胃癌的内部收益率为2.63(95%可信区间为1.96-3.52;我2= 93%) (图6B.),乳腺癌的IRR为2.17 (95% CI 1.98-2.38;我2= 0%) (图6C.),肝癌的IRR为2.02 (95% CI 0.83-4.91;我2=83%) (图6D.)结肠癌的内部收益率为2.00(95%可信区间为1.16-3.43;我2= 75%)(图6E.)。
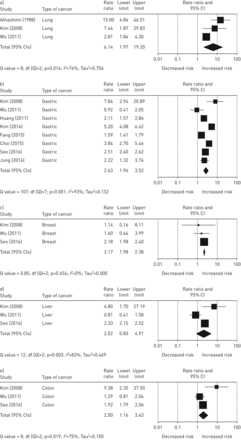
a) 肺癌患者结核病相对风险森林图。b)胃癌患者结核病相对风险森林图。c)乳腺癌患者结核病相对风险森林图。d)肝癌患者结核病相对风险森林图。e)胃癌患者结核病相对风险森林图结肠癌患者的结核病。
手术、化疗和/或放疗对结核病风险的影响
大多数经过审查的研究没有提供关于接受手术、化疗和/或放疗的癌症患者数量的详细信息,以及治疗和结核病诊断之间的时间关系。
许多胃癌研究都有治疗细节。一项来自台湾的全国性研究没有将任何治疗方式(胃切除术、化疗或放疗)作为胃癌患者结核的独立危险因素[32].台湾的另一项研究发现,与胃切除术和姑息治疗相比,化疗与胃癌患者患结核病的风险更高相关(SIR分别为2.91、2.50和1.19)[29.].韩国一项针对早期胃癌患者的全国性研究表明,与普通人群相比,接受内镜切除术的患者患结核病的相对风险没有增加;而胃切除术患者发生结核的风险比为7.92 (95% CI 1.08-58.16) [31].另一个韩国研究发现,与接受次特胃切除术的患者相比,接受全胃切除术的患者的患者有一个或3.48(95%CI 1.25-9.66)的风险[33].
纳入研究的偏倚风险评估
采用纽卡斯尔渥太华质量评估量表进行队列研究,评估偏倚风险[20.,显示该风险为中等至低(补充表S1)。偏见的风险主要是与选择的参照群体(控制队列,而不是来自同一社区,同期癌症组),以及参照群体的可比性(缺乏调整/分层最重要的混杂因素)和不确定性对后续的报道。尽管在对不同实体器官肿瘤进行亚组分析时异质性降低(但在大多数亚组中仍然很高),但所有评估结果的研究之间的异质性都很高。
只有一项研究根据研究队列中的TST/IGRA(89/257,35%)对LTBI的患病率进行了估计,并指出有五名患者接受了LTBI治疗[34].然而,这些患者被排除在分析之外。没有其他研究表明参与者是否接受LTBI治疗。6项研究,其中4项仅评估了胃癌中的结核病,包括结核病治疗史的信息和/或以前治愈的结核病的放射学证据[28.- - - - - -31,33,34],以往胸部x光片显示的结核病患病率为7% [34]至17% [28.]在研究人群中。关于艾滋病毒状况的现有资料很少。南非的一项儿科研究报告说,57名患有癌症和结核病的儿童中有6名(11%)感染了艾滋病毒[36].两项研究排除了hiv阳性人士[26.,28.].其余的研究没有披露有关艾滋病毒状况的信息。
讨论
与一般人群相比,Meta分析显示癌症患者中结核病风险的统计学显着增加。与一般人群相比,有三种或更多种研究的数据来自三种或更多种研究的数据,与其中的三种或更多种研究有关的癌症与发展结核病的风险约为两倍。这种增加对于胃,乳腺和结肠癌而言是显着的,但不是肝癌(IRR 2.02; 95%CI 0.83-4.91)。肺癌与Tb的六倍增加有关。胃癌中TB的相对风险(IRR 2.63,95%CI 1.96-3.52),通常用胃切除术治疗(与营养不良有关[44]是结核病的危险因素[45,46]),并未明显不同于其他固体癌症的相对风险。成人血液学癌症中TB的相对风险(IRR.3.53; 95%CI 1.63-7.64)仅比具有固体癌症的成人(IRR 2.25; 95%CI 1.96-2.58)中度高度高。在血液恶性恶性肿瘤或固体癌症的儿童中发现TB的相对风险最高(IRR 16.82,95%CI 8.81-32.12)。
据我们所知,这是在包括比较组(对照组或研究背景和时期的一般人群)信息的研究中,首次评估血液学恶性肿瘤和实体癌中结核病的相对风险的荟萃分析。虽然被纳入的研究之间存在显著的异质性,但应用的随机效应模型产生的估计值恰当地反映了这种差异(i、 e.通过95%的CIs)。因此,汇集估计不是一样重要的上下95%可信区间估计,考虑到相对风险是否过低(基于上面的95%可信区间)来保证LTBI检查,或者足够高(基于低95% CI)考虑LTBI筛查。
患有实体癌和血液恶性肿瘤的儿童患结核病的相对风险较高,应考虑对LTBI进行系统筛查和治疗。尽管纳入的两项儿科研究都是在南非进行的,南非是结核病再感染风险较高的地区,但这不应影响估计的结核病相对风险,因为对照组人口具有相同的暴露风险。然而,根据环境和我们的建议,实施LTBI筛查和治疗只适用于每年结核病发病率低于100 / 10万的高收入或中上收入国家[9].
这项荟萃分析的发现有助于与其他患结核病风险增加的人群的结核病相对风险进行比较,并为癌症患者潜在结核病感染和结核病化学预防提供筛查建议。癌症中结核相对风险(RR)的95%以上可信区间(3.22)低于目前LTBI筛查和治疗的目标群体的相对风险,如艾滋病毒患者(RR为50-110 [47,48]),活性TB的患者(RR为10.4次在初始医疗保健接触后60天至2年后的RR,患有1.5%的TB触点均已诊断为初始筛查[49]),慢性肾功能衰竭患者(RR为7.8[5])和TNF-α抑制剂(RR 1.8-29.3 [50])。结核病可在初次感染后的任何时候重新激活[3.]因此,估计的罹患结核病的终生累积风险对于LTBI筛查和治疗决策非常重要。在慢性疾病(如糖尿病和慢性肾功能衰竭)中,与该疾病相关的风险增加可以持续终生,而不会因结核病而显著缩短预期寿命然而,在癌症中,免疫抑制状态更可能是暂时的(例如在化疗期间)。此外,在许多癌症中,预期寿命显著降低,这降低了罹患结核病的累积终生风险。在比较癌症患者与其他免疫缺陷组的结核相对风险时,必须考虑到这一点。基于这些考虑,我们认为,在成年癌症患者中,不存在足够高的结核风险,建议对LTBI进行系统筛查和治疗,且不受其他危险因素的影响。正如世卫组织指南中所概述的,需要在个别患者的基础上权衡LTBI治疗的潜在危害和益处[9].在任何组中引入LTBI的系统筛选和治疗需要考虑本地背景,可访问性,股票,成本和实施方面[9];然而,对这些方面的讨论超出了本研究的范围。
结核病的总发病率(每年)随着癌症诊断后的时间(与早期治疗相关)而下降。这是在最大的研究证明包含在目前的荟萃分析(包括855 382癌症患者),这表明,结核病的相对风险最高,癌症的诊断,后随着时间的推移,逐渐减少先生为3.70 (95% CI 3.57 - -3.83)的前6个月;6至11个月的SIR为2.19 (95% CI 2.08-2.30);12至23个月的SIR为1.75 (95% CI 1.67-1.84);诊断后超过24个月的SIR为1.43 (95% CI 1.36-1.51) [25.].除了癌症和癌症治疗造成的免疫受损外,在癌症病程早期进行更密切的医疗随访和检查可能会导致确诊结核病病例的增加。这可能会导致高估癌症患者患结核病的风险。
关于癌症诊断后不同时期TB相对风险的考虑也与对现有结果的解释也有关。随着癌症患者的长期随访的研究将产生每人的较低的发生率估计,随着TB的风险随着诊断而过去的时间而下降。随着时间的推移在上述大型队列研究中的血液恶性肿瘤研究中的这种风险降低尤为突出,其中先生在诊断后的前6个月内先生为12.01(95%CI 10.81-13.30),并减少到2.70的先生(2.12-3.39)诊断后大于24个月[25.].在目前的荟萃分析中,由于长期随访,血液恶性肿瘤中的血液恶性恶性肿瘤(15岁或以上患者)的杂志IRR.结核病发病率显示出随后续持续时间增加的下降,反映了初步诊断和完成化疗后的结核病风险的降低[51].
我们的系统综述的优势之一是其严格的方法学,仅包括提供癌症患者中结核病发病率(而不是累积发病率或流行率)以及对照组/一般人群中的结核病发病率的研究。目前系统综述的一个局限性是它不能区分癌症本身和癌症治疗产生的风险。现有的数据也不允许我们考虑癌症阶段的影响。作为选择治疗方法基于癌症阶段,预期的预后,以及后续周期较短的晚期癌症患者,它是非常困难的,如果不是不可能的话)建立独立的治疗方法的效果和癌症阶段从队列研究结核病的风险重新激活。如上所述,不同研究的不同随访时间可能导致了对结核病风险估计的差异。纳入的研究没有区分近期传播引起的结核病和继发性再激活结核病,只有后者是LTBI筛查的指征。
使用不同的参照组(从匹配的对照组到研究环境中未经调整的一般人群)可能会增加荟萃分析中确定的异质性。最低质量的参考组是研究环境中的普通人群,没有调整潜在的混杂因素,尤其是年龄。这可能导致高估老年人结核病发病率较高人群中结核病的相对风险(更可能的情况),或低估年轻人结核病发病率较高人群中结核病的相对风险。然而,只有一项研究没有将年龄作为潜在的混杂因素进行调整[26.].
总之,这种荟萃分析显示,与一般人群相比,癌症的患者的风险增加了发展结核病的风险。具有固体癌症或止血性恶性肿瘤的儿童具有高度发育结核病的风险很高,并且应考虑用于系统的筛选和治疗LTBI,特别是当它们源于具有高结核病发病率的环境时。在患有癌症的成年人中,TB的相对风险仅适度增加。风险略有增加,与此事实相配,在许多情况下,由于初始癌症诊断以来,由于初始癌症诊断,并且由于预期寿命降低,累计寿命风险减少,表明成年患者不需要LTBI的系统筛选和治疗,独立于其他危险因素。患有患有额外危险因素的患有癌症的成年人(例如来自TB负担的国家的移民),应考虑LTBI逐案的筛查和治疗。在固体癌症中,肺癌具有Tb的最高风险之一,但预后往往是穷人[52,而较短的平均预期生存期可能表明,对许多患者来说,LTBI治疗的好处并不大于相关的不便和风险。虽然目前的指南描述患者胃切除术作为结核病的高危人群,我们的分析(包括许多最近的研究在胃癌和胃切除术)显示无显著差异在结核病患者的胃癌的风险,有或没有胃切除术,而其他固体癌症患者。
补充材料
脚注
这篇文章的补充材料可从www.qdcxjkg.com
支持声明:C.C. Dobler得到了澳大利亚国家卫生和医学研究理事会奖学金的支持(APP1090198)。资助方不参与研究设计、数据收集、数据分析、数据解释或手稿的撰写。通讯作者可以完全访问研究中的所有数据,并对提交发表的决定负有最终责任。本文的资金信息已存入交叉参考基金登记处.
利益冲突:没有宣布
- 已收到2017年1月23日。
- 接受2017年5月26日。
- 版权所有©2017















