摘要gydF4y2Ba
雌激素升高是患者发生肺动脉高压(PAH)的强烈流行病学危险因素,与代谢缺陷相关。此外,雌激素驱动携带骨形态发生蛋白受体II型(BMPR2)突变的小鼠外显率,BMPR2是大多数遗传性PAH的原因。本研究的目的是确定抑制雌激素是否有效治疗这些小鼠的多环芳烃。gydF4y2Ba
雌激素抑制剂氟维司坦和阿那曲唑被用于BMPR2突变小鼠的预防和治疗范式,他莫昔芬被用于治疗。此外,BMPR2突变小鼠被杂交到雌激素受体(ESR)1和ESR2敲除背景上,以评估受体的特异性。测量血流动力学和代谢结果。gydF4y2Ba
雌激素抑制对BMPR2突变小鼠多环芳烃均有预防和治疗作用。这与代谢缺陷的减少有关,包括氧化脂质形成,胰岛素抵抗和过氧化物酶体增殖物激活受体-γ和CD36的拯救。该效应主要通过ESR2介导,但部分通过ESR1介导。gydF4y2Ba
我们的数据表明,在人类多环芳烃中抑制雌激素的试验是有必要的,并且可能通过改善代谢缺陷来改善肺血管疾病。虽然氟维司坦和阿那曲唑比它莫西芬更有效,但它莫西芬可能对绝经前女性有用,因为它可降低诱发绝经的风险。gydF4y2Ba
摘要gydF4y2Ba
雌激素抑制逆转bmpr2相关的肺动脉高压和相关代谢缺陷gydF4y2Bahttp://ow.ly/ir6Y30b2WLHgydF4y2Ba
简介gydF4y2Ba
肺动脉高压(Pulmonary arterial hypertension, PAH)是一种包括肺血管内皮功能障碍、中、小肺动脉闭塞和脱落、平滑肌和外膜细胞肥大和增殖的疾病。这些因素共同导致肺血管阻力逐渐加重[gydF4y2Ba1gydF4y2Ba,gydF4y2Ba2gydF4y2Ba].这最终会导致右心衰和死亡;目前尚无治疗方法。gydF4y2Ba
大多数可遗传形式的(H)PAH病例与骨形态发生蛋白受体II型(BMPR2)的突变有关,BMPR2是BMP通路的2型受体[gydF4y2Ba3.gydF4y2Ba].此外,BMPR2在大多数其他形式的PAH中被抑制,即使在没有突变的情况下[gydF4y2Ba4gydF4y2Ba].BMPR2突变或缺失的小鼠会自发发展多环芳烃[gydF4y2Ba5gydF4y2Ba- - - - - -gydF4y2Ba7gydF4y2Ba].然而,BMPR2突变的小鼠和人类的外显率都是不完整的:只有20%的BMPR2突变的人类发展为临床PAH [gydF4y2Ba8gydF4y2Ba].gydF4y2Ba
许多形式的多环芳烃的最强流行病学风险因素是女性[gydF4y2Ba9gydF4y2Ba].虽然只有20%的BMPR2基因突变的人会患上PAH,但根据性别有显著差异:43%的女性会患上PAHgydF4y2Ba与gydF4y2Ba14%的BMPR2突变男性会在一生中患上多环芳烃[gydF4y2Ba10gydF4y2Ba].与这一发现一致的是,我们证明雌激素代谢是PAH外显率的一个强有力的预测因素:优先将雌激素代谢为16-雌激素的女性,如16αOHE1,发展为PAH,而优先将雌激素代谢为2-或4-雌激素的女性则没有[gydF4y2Ba11gydF4y2Ba- - - - - -gydF4y2Ba13gydF4y2Ba].雌激素代谢促进男性外显率,但与女性不同[gydF4y2Ba14gydF4y2Ba].gydF4y2Ba
女性在人类疾病中占优势的机制仍然解释不清,部分原因是在典型的多环芳烃啮齿动物模型中,如缺氧和单花百合碱,发现雌激素具有保护作用[gydF4y2Ba15gydF4y2Ba].这可能与内源性和外源性雌激素的差异有关;潜在的差异包括产生的位置(大量雌激素是在肺血管系统中产生的)和天然雌激素的周期性[gydF4y2Ba16gydF4y2Ba].我们的数据显示,与人类患者一样,用16αOHE1治疗的BMPR2突变小鼠发生了具有更高外显率和严重程度的PAH [gydF4y2Ba14gydF4y2Ba],比其他模型更能准确地再现人类现象。我们之前的工作表明,16αOHE1促进胰岛素抵抗和其他代谢问题[gydF4y2Ba14gydF4y2Ba,gydF4y2Ba17gydF4y2Ba].与这一发现一致的是,代谢缺陷越来越多地与多环芳烃有关[gydF4y2Ba18gydF4y2Ba- - - - - -gydF4y2Ba20.gydF4y2Ba],我们已经证明它们会加剧BMPR2突变小鼠的PAH [gydF4y2Ba21gydF4y2Ba,gydF4y2Ba22gydF4y2Ba].尽管代谢缺陷与多环芳烃的关联机制尚不清楚,但它可能与血管功能障碍、破坏性超氧化物的增殖或产生有关[gydF4y2Ba23gydF4y2Ba].gydF4y2Ba
因为在经典的多环芳烃模型中,雌激素抑制是有害的,目前的研究试图确定抑制内源性雌激素是否在预防或逆转已建立的bmpr2相关的多环芳烃方面具有治疗效果,以及这是否与改善代谢指标(如胰岛素抵抗和氧化脂质)有关。一项小型试验已证实阿纳斯特唑对绝经后PAH患者的安全性,并提示其疗效[gydF4y2Ba24gydF4y2Ba].因此,疗效和机制的证明是临床前模型验证这一研究链转化为患者所必需的最后一步。gydF4y2Ba
方法gydF4y2Ba
雌激素抑制实验gydF4y2Ba
我们使用Rosa26-rtTA2 × TetOgydF4y2Ba7gydF4y2Ba-Bmpr2gydF4y2BaR899XgydF4y2BaFVB/N小鼠,如前所述[gydF4y2Ba25gydF4y2Ba,gydF4y2Ba26gydF4y2Ba],称为Rosa26-Bmpr2gydF4y2BaR899XgydF4y2Ba或Bmpr2gydF4y2BaR899XgydF4y2Ba简洁。R899X是BMPRII尾域899氨基酸上的精氨酸终止突变,发现于US33家族[gydF4y2Ba6gydF4y2Ba].转基因基因的表达发生在所有类型的组织,但只有在启动多西环素。gydF4y2Ba
成年雌性Rosa26-only或Rosa26-Bmpr2gydF4y2Badelx4 +gydF4y2Ba用0.2 mg·g强力霉素激活8-10周龄小鼠的转基因gydF4y2Ba−1gydF4y2Ba,并接受载体(见后文)或治疗。实验小鼠均无外源性16αOHE1。小鼠被随机分配到一个治疗组,执行表型的个体对该组不可见,就像执行胰岛素计数等工作的机构专业实验室一样。Fulvestrant (Selleck Chemicals, Houston, TX, USA)溶解在乙醇中至100 mg·mLgydF4y2Ba−1gydF4y2Ba.阿那曲唑(Sigma, St Louis, MO, USA)溶于乙醇至2 mg·mLgydF4y2Ba−1gydF4y2Ba.用花生油稀释抑制剂溶液,每日皮下注射小鼠。氟维司坦用量为200µg·小鼠gydF4y2Ba−1gydF4y2Ba·天gydF4y2Ba−1gydF4y2Ba(∼6 mg·kggydF4y2Ba−1gydF4y2Ba),阿那曲唑剂量为10µg·小鼠gydF4y2Ba−1gydF4y2Ba·天gydF4y2Ba−1gydF4y2Ba(0.3∼mg·公斤gydF4y2Ba−1gydF4y2Ba).17-醋酸甲羟孕酮(MPA;Sigma)在乙醇中溶解至50 mg·mLgydF4y2Ba−1gydF4y2Ba.将MPA溶液稀释于花生油中,以1 mg·只的剂量肌注小鼠gydF4y2Ba−1gydF4y2Ba每3周(30毫克·公斤gydF4y2Ba−1gydF4y2Ba每3周)。他莫昔芬(Sigma)溶于乙醇至100 mg·mLgydF4y2Ba−1gydF4y2Ba然后用花生油稀释后注射到小鼠体内。注射剂量为1 mg·只gydF4y2Ba−1gydF4y2Ba·天gydF4y2Ba−1gydF4y2Ba(∼30 mg·公斤gydF4y2Ba−1gydF4y2Ba·天gydF4y2Ba−1gydF4y2Ba).gydF4y2Ba
使用的药物剂量由人体剂量换算成RgydF4y2BaeagangydF4y2Ba- sgydF4y2Ba山楂gydF4y2Ba等gydF4y2Ba.[gydF4y2Ba27gydF4y2Ba],采用比例体表面积;这导致从人类患者到小鼠的单位重量剂量增加了约12倍。使用的剂量与最近人类和动物研究中使用的剂量非常匹配;对于一个50公斤重的女性人类,我们的剂量相当于1.2毫克·天gydF4y2Ba−1gydF4y2Ba,相当于1.0毫克·天gydF4y2Ba−1gydF4y2Ba用于最近对人类多环芳烃患者的初步研究[gydF4y2Ba24gydF4y2Ba].gydF4y2Ba
在预防实验中,动物在强力霉素诱导时开始接受药物。在逆转实验中,动物只接受强力霉素4周,然后再接受2周强力霉素和治疗(或载体)。gydF4y2Ba
6周后,动物进行超声心动图检查,第二天进行血流动力学表型分析和组织收集。gydF4y2Ba
超声心动图和血流动力学表型gydF4y2Ba
采用Vivo 770高分辨率图像系统(visualsonic, Toronto, Canada)进行二维超声心动图。在异氟醚麻醉下于牺牲前一天进行b型、m型和频谱多普勒超声心动图检查。在升主动脉测量速度、时间积分和心率,在同一位置测量直径。冲程容积(SV)由公式SV=(π 2/4)×(主动脉速度时间积分)推导,其中π=主动脉直径。心输出量(CO)由公式CO=SV×heart rate [gydF4y2Ba28gydF4y2Ba,gydF4y2Ba29gydF4y2Ba].gydF4y2Ba
血流动力学表型如前所述[gydF4y2Ba6gydF4y2Ba,gydF4y2Ba25gydF4y2Ba].简单地说,用三溴乙醇麻醉小鼠,用尾袖检查全身压力,然后进行闭胸颈内右心导管插管。gydF4y2Ba
血浆雌二醇测量gydF4y2Ba
从每种治疗中随机选择4只雌性小鼠进行雌二醇测量。将25µL血浆分取至雌二醇酶联免疫吸附试验板(ES180S;Calbiotech, El Cajon, CA,美国)。雌二醇酶联免疫吸附试验按照生产厂家说明书进行;450nm处的吸光度使用微孔板阅读器(型号680;Bio-Rad,赫拉克勒斯,CA,美国)。计算血浆雌二醇浓度,以pg·mL表示gydF4y2Ba−1gydF4y2Ba从标准曲线。gydF4y2Ba
ESR1/ESR2 × Bmpr2gydF4y2BaR899XgydF4y2Ba实验gydF4y2Ba
雌激素受体(ESR)1或ESR2敲除小鼠购自Jackson实验室(萨克拉门托,CA, USA)。首先与C57BL/6背景的Rosa26小鼠杂交。然后与FVB/N背景的Rosa-R899X小鼠杂交。对照组(Rosa26-Bmpr2R899X)与ESR1和ESR2敲除的同一天进行表型,并且与其他任何实验中使用的动物不同(在任何实验中都没有“重复使用”对照值)。另外,实验与雌激素抑制实验完全相同。gydF4y2Ba
船muscularisationgydF4y2Ba
如前所述制备石蜡包埋的小鼠肺切片。小鼠单克隆α-平滑肌肌动蛋白(SMA)抗体(1:200;Dako, Carpinteria, CA, USA)在4°C过夜。PBS冲洗三次后,用Alexa 488荧光二抗(1:1000;Invitrogen, Carlsbad, CA, USA)室温1小时。PBS清洗三次后,将载玻片风干,加入安装介质(Vector Laboratories, Burlingame, CA, USA),并用盖玻璃覆盖。使用尼康Eclipse 90i直立荧光显微镜(Belmont, CA, USA)在10×视野下对sma阳性血管进行计数,每只小鼠随机选择10个视野。gydF4y2Ba
西方墨点法gydF4y2Ba
组织在500µL放射免疫沉淀试验缓冲液(PBS, 1% ipegal, 0.5%脱氧胆酸钠,0.1%十二烷基硫酸钠(SDS))中均质,并加入蛋白酶和磷酸酶抑制剂鸡尾酒(Sigma)。组织在4℃(15 000×gydF4y2BaggydF4y2Ba, 15 min),上清液采用Bradford微量测定法(Bio-Rad)测定蛋白浓度。等量的蛋白质提取物在95°C变性样品缓冲液中变性。每个样品中的蛋白质(20µg)通过4-12% Bis-Tris凝胶电泳分离,转移到聚偏二氟乙烯膜上;运行缓冲液为NuPage SDS运行缓冲液(Thermo Scientific, Rockford, IL, USA)或TRIS/甘氨酸/SDS缓冲液(Bio-Rad)。用含5%脱脂干牛奶和0.05% Tween-20的PBS在室温下阻断膜1小时,然后在4℃下用兔抗过氧化物酶体增殖物激活受体(PPAR)一抗多克隆抗体(1:1000稀释;Abcam, Cambridge, MA, USA), CD36(1:1000稀释;Novus Biologicals, Litteton, CO)和β-肌动蛋白(1:1000,Abcam, Cambridge, MA)。然后将膜与山葵过氧化物酶标记的驴抗鼠免疫球蛋白二抗(1:5000稀释;圣克鲁斯生物技术,圣克鲁斯,CA,美国)。使用SuperSignal West Pico化学发光底物(Thermo Scientific)检测辣根过氧化物酶。 Blots were imaged using either a Bio-Rad ChemiDoc Touch Imaging System or an Alpha Innotech Digital Imaging System. Densitometry was performed using ImageJ (public domain software published by the National Institutes of Health).
线粒体超氧化物检测gydF4y2Ba
使用MitoSox Red (Molecular Probes, Eugene, OR, USA)检测线粒体超氧化物。小鼠肺微血管内皮细胞(PMVECs)(野生型或bmpr2r899x)和转基因诱导如先前报道。细胞在腔室载玻片上生长至50-80%合流。MitoSOX加入终浓度为0.5µM, Hoechst染色加入终浓度为0.1µg·mLgydF4y2Ba−1gydF4y2Ba.将细胞置于37°C培养箱中20分钟,然后用汉克斯含钙和镁的平衡盐溶液洗涤三次。将安装介质(Vector Laboratories)添加到载玻片中,并用盖玻片覆盖。数码图像使用尼康Eclipse 90i直立荧光显微镜,100×油浸物镜拍摄。gydF4y2Ba
线粒体摄氧量的测量gydF4y2Ba
野生型和BMPR2gydF4y2BaR899XgydF4y2Ba如前所述,从Immortomouse背景中收获和培养小鼠PMVECs [gydF4y2Ba30.gydF4y2Ba].实验前72 h,细胞转入37°C,多西环素(300 ng·mLgydF4y2Ba−1gydF4y2Ba)诱导转基因表达。分析前24小时,用1µM 16αOHE1或载体处理细胞。细胞在基础试验培养基中清洗(Seahorse Biosciences, North Billerica, MA, USA)。分析前1小时,将细胞置于无二氧化碳培养箱中,在基础检测培养基中添加葡萄糖(1 g·L)gydF4y2Ba−1gydF4y2Ba),gydF4y2BalgydF4y2Ba-谷氨酰胺(2mm)和丙酮酸钠(1mm)在pH值7.4。然后在Seahorse XFe96细胞外通量分析仪中使用mito压力测试协议,使用以下试剂浓度(在单独实验中为这些分析进行了优化)分析细胞:寡霉素(2.5µM终孔),FCCP(0.5µM终孔),FCCP(0.5µM终孔,共1µM)和鱼藤酮和抗霉素A(0.5µM终孔),按制造商推荐浓度进行分析。报告的数据为每次实验中每个单独条件平均5到8个井,实验重复进行,每个井使用70 K PMVECs。gydF4y2Ba
测量Glut4在胰岛素作用下的动员gydF4y2Ba
Glut4-GFP表达载体购自OriGene公司(Rockville, MD, USA)。按照制造商说明书,用Lipofectamine 2000试剂(Invitrogen)转染细胞。转染4 h后用新鲜培养基替换转染液,细胞用1µM 16αOHE1或载体处理18 h。然后将细胞饥渴6小时,用10 nM胰岛素刺激1小时,固定,清洗并染色4 ',6-二氨基氨基-2-苯基吲哚(DAPI)和DY-554 phalloidin(红色)。封面被安装在vectasshield安装介质中(Vector实验室),并在显微镜下观察。gydF4y2Ba
小鼠肺中等酮蛋白加合物和神经酰胺的免疫组化分析gydF4y2Ba
在小鼠肺切片上进行了等酮蛋白加合物和神经酰胺的免疫定位。组织切片脱蜡,再水化,用0.3%双氧水处理,如前所述。对于等酮染色,切片在含有5%正常小鼠血清和5%牛血清白蛋白(BSA)的0.1 M PBS (pH 7.4)中室温孵育30分钟,以阻断二抗的非特异性结合。切片用5µg·mL孵育gydF4y2Ba−1gydF4y2BaD11单链抗体(等酮抗体)在室温下孵育2小时,然后与辣根过氧化物酶(HRP)标记的抗e标签孵育(1:500稀释;GE Healthcare, Pittsburgh, PA, USA)在室温下放置2小时。神经酰胺染色时,在10mm柠檬酸缓冲液中进行抗原提取。用5% BSA阻断切片,然后用神经酰胺抗体(Enzo Life Sciences, Farmingdale, NY, USA)在4℃下孵育过夜。第二天,切片用生物素化二抗孵育,然后用酶标链霉亲和素孵育。二氨基联苯胺被用作HRP(载体实验室)的底物。切片脱水后装入Cytoseal XYL (Richard-Allan Scientific, MI, USA)进行光镜检查。gydF4y2Ba
统计方法gydF4y2Ba
使用JMP程序进行统计检验(SAS, Cary, NC,美国)。使用单因素或多因素方差分析来确定相互作用变量的影响gydF4y2Ba事后gydF4y2BaFisher最小显著性差异(LSD)用于确定个体组之间的差异。采用相关z检验建立相关显著性。gydF4y2Ba
动物使用批准gydF4y2Ba
范德比尔特大学(Nashville, TN, USA)的动物护理和使用委员会批准了所有的动物研究。gydF4y2Ba
结果gydF4y2Ba
雌激素抑制抑制BMPR2突变小鼠肺动脉高压gydF4y2Ba
之前已经证明了16αOHE1会放大多环芳烃,我们首先试图确定雌激素抑制或雄激素暴露是否具有保护作用,以及它们是否协同工作。对于雌激素抑制,我们使用阿那曲唑和氟维司坦的组合,这是常用来抑制人类乳腺癌的雌激素。我们只将它们联合使用,而不是单独使用,因为这项初步研究的目标是在没有最强的药理学信号的情况下确定抑制雌激素信号在该模型中是否具有保护作用。对照(Rosa26)或Rosa26- bmpr2gydF4y2BaR899XgydF4y2Ba小鼠按0.2 g·kg剂量饲喂强力霉素gydF4y2Ba−1gydF4y2Ba6周(在此期间Bmpr2gydF4y2BaR899XgydF4y2Ba小鼠通常会出现右心室收缩压升高[gydF4y2Ba25gydF4y2Ba]),然后将每个基因型分为正负雄激素MPA (1 mg·小鼠)4组gydF4y2Ba−1gydF4y2Ba每3周)加上或减去芳香化酶抑制剂阿那曲唑(10µg·小鼠)的组合gydF4y2Ba−1gydF4y2Ba·天gydF4y2Ba−1gydF4y2Ba)和雌激素受体抑制剂氟维司坦(200µg·小鼠gydF4y2Ba−1gydF4y2Ba·天gydF4y2Ba−1gydF4y2Ba)(阿那曲唑/ fulvestrant)。通过多因素方差分析,使用MPA对测量的任何变量都没有显著影响,因此在剩余的研究中,这些结果与非MPA动物分组。此外,如果排除暴露于mpa的动物,结果不会改变。gydF4y2Ba
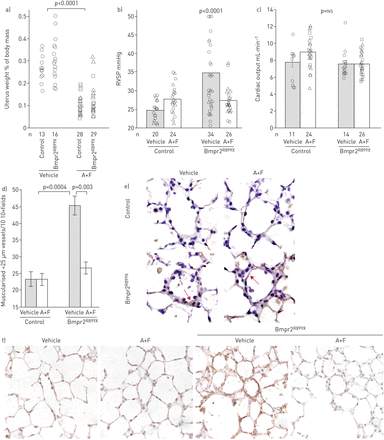
使用阿那曲唑/氟维司坦可有效抑制雌激素信号,子宫重量显著降低(gydF4y2Ba图1一个gydF4y2Ba).正如预期的那样,Bmpr2突变小鼠的RVSP升高,平均为35 mmHg,外显率为50% (gydF4y2Ba图1 bgydF4y2Ba).RVSP在Bmpr2中是可变的gydF4y2BaR899XgydF4y2Ba因为肺血管阻力是由血管损失和狭窄所驱动,而不是血管收缩[gydF4y2Ba25gydF4y2Ba].使用阿那曲唑/氟维司坦可阻止Bmpr2中RVSP的大部分增加gydF4y2BaR899XgydF4y2Ba治疗组RVSP平均为27 mmHg,外显率为~ 10%(与对照组相比p<0.0001)。对任何组的心排血量均无影响(gydF4y2Ba图1 cgydF4y2Ba).富尔顿指数(在线补充图S1)在该模型中不具有信息量;我们之前发表过Bmpr2突变小鼠(和患者)的右心室肥厚反应受损[gydF4y2Ba19gydF4y2Ba].gydF4y2Ba
a)阿那曲唑和氟维司坦(a +F)降低小鼠子宫重量(p<0.0001);经多元方差分析,R899X突变对子宫重量无影响。每个符号表示一个鼠标的测量值。b) A+F在渗透泵中通过6周BMPR2的最后4周传递gydF4y2BaR899XgydF4y2Ba转基因诱导可预防右心室收缩压升高(以转基因和药物为变量,经多元方差分析p<0.0001)。每个符号代表一个鼠标的值。以三角形为代表的小鼠另外注射了雄激素醋酸甲羟孕酮(MPA),不影响RVSP,因此这些数据未被分离。对每组小鼠进行年龄匹配,同时对对照组进行测试。c) A+F治疗或Bmpr2突变均未显著改变超声心动图心输出量。d) A+F几乎使BMPR2中常见的肌肉化血管增加正常化gydF4y2BaR899XgydF4y2Ba老鼠。通过考虑BMPR2突变和治疗作为因素的多元方差分析,BMPR2突变增加了肌肉血管(p=0.0004),而A+F则减少了肌肉血管,特别是在BMPR2突变小鼠中(p=0.003)。e)氧化脂质染色显示BMPR2氧化应激增加gydF4y2BaR899XgydF4y2Ba小鼠,A+F归一化(箭头)。f) BMPR2在肺中神经酰胺(有毒脂质)染色(棕色)增加gydF4y2BaR899XgydF4y2BaA+F降低小鼠的活性。gydF4y2BansgydF4y2Ba:不重要的。gydF4y2Ba
雌激素抑制与阿那曲唑/氟维司坦几乎正常化的肌肉血管计数(gydF4y2Ba图1 dgydF4y2Ba).因为我们之前已经证明氧化应激增加是Bmpr2突变小鼠代谢缺陷的标志,我们对氧化脂质进行了免疫组化,并发现Bmpr2突变小鼠血管壁氧化脂质增加;然而,这是正常的雌激素抑制(红色箭头gydF4y2Ba图1 egydF4y2Ba).雌激素抑制似乎不能减少浸润炎性细胞中的氧化脂质(gydF4y2Ba图1 egydF4y2Ba).我们之前已经证明Bmpr2突变会增加毒性脂质神经酰胺的积累[gydF4y2Ba31gydF4y2Ba作为代谢功能障碍的一部分。Bmpr2突变小鼠血管壁上神经酰胺再次增加,阿那曲唑/氟维司坦可降低神经酰胺(gydF4y2Ba图1 fgydF4y2Ba).gydF4y2Ba
雌激素抑制逆转BMPR2突变小鼠中建立的多环芳烃gydF4y2Ba
由于既定疾病的逆转与PAH患者群体特别相关,我们允许Bmpr2突变小鼠发生PAH 6周,然后用阿那曲唑/氟维司坦或稍弱的雌激素受体拮抗剂他莫昔芬治疗它们4周。添加他莫昔芬是因为它可以安全地用于绝经前女性而不会引起绝经。gydF4y2Ba
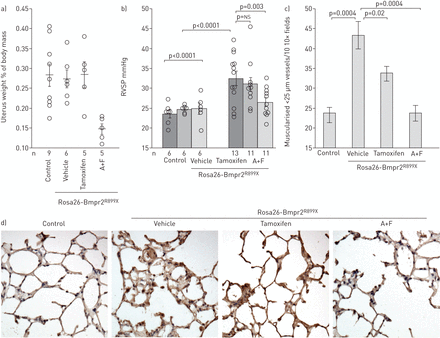
正如预期的那样,他莫西芬不影响子宫重量,但阿那曲唑/伏维司坦可降低子宫重量(gydF4y2Ba图2一个gydF4y2Ba).使用阿那曲唑/氟维司坦可降低血浆雌激素水平~ 3.5倍(在线补充图S2a)。尽管如预期的那样,他莫西芬不影响循环雌激素,但它确实降低了已知雌激素靶点FHL1和SNAT2的表达[gydF4y2Ba32gydF4y2Ba],分别减少50%和35%(在线补充图S2b)。gydF4y2Ba
a)阿那曲唑和氟维司坦(a +F),而不是他莫昔芬用于治疗可降低小鼠子宫重量(与对照组相比p=0.002;与车辆相比P =0.007)。每个符号代表一个鼠标的测量值;数据以中位数±表示gydF4y2Ba扫描电镜gydF4y2Ba.b) A+F在渗透泵中通过10周BMPR2的最后4周传递gydF4y2BaR899XgydF4y2Ba转基因诱导逆转右心室收缩压升高(RVSP)的发展(以转基因和药物为变量,多元方差分析p=0.003)。同样使用他莫昔芬对RVSP无显著影响,但RVSP呈下降趋势。每个符号代表一个鼠标的值。c) A+F治疗几乎使BMPR2中常见的肌化血管增加正常化gydF4y2BaR899XgydF4y2Ba老鼠;他莫昔芬为中间效应。经方差分析,BMPR2突变增加了肌化血管(p=0.0004),而A+F (p=0.0004)和他莫西芬(p=0.02)均降低了肌化血管。d) BMPR2在肺中神经酰胺(有毒脂质)染色(棕色)增加gydF4y2BaR899XgydF4y2BaA+F,而不是他莫西芬。比例尺bar=25µm。gydF4y2Ba
Vehicle-treated Bmpr2gydF4y2BaR899XgydF4y2Ba小鼠的外显率和压力与之前的实验相当,阿那曲唑/氟维司坦治疗在很大程度上逆转了这一结果,但他莫昔芬的效果较小(gydF4y2Ba图2 bgydF4y2Ba).肌肉化的小血管计数显示Bmpr2显著增加gydF4y2BaR899XgydF4y2Ba他莫昔芬使小鼠轻度减少,阿那曲唑/氟维司坦使小鼠正常化(gydF4y2Ba图2 cgydF4y2Ba).Bmpr2突变小鼠血管壁上神经酰胺增加,阿那曲唑/氟维司坦可降低神经酰胺,但他莫昔芬不明显(gydF4y2Ba图2 dgydF4y2Ba).gydF4y2Ba
敲除ESR1或ESR2可以部分保护BMPR2突变小鼠gydF4y2Ba
由于抑制雌激素受体的药理学方法可能缺乏特异性,且因细胞类型而异,我们使用基因敲除来试图确定雌激素效应是否通过ESR1或ESR2介导。因此,这些小鼠每只都有两个转基因和两个敲除等位基因(Rosa26-rtTA2M2, TetO7-Bmpr2gydF4y2BaR899XgydF4y2Ba,两个等位基因从ESR1或ESR2中被敲除)。成年动物喂食强力霉素6周诱导Bmpr2gydF4y2BaR899XgydF4y2Ba转基因表达。gydF4y2Ba
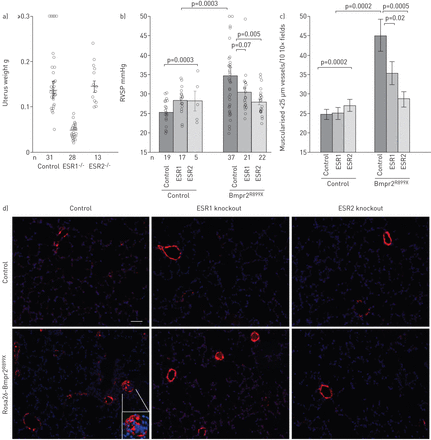
正如预期的那样,敲除ESR1而不是ESR2导致子宫重量减轻(gydF4y2Ba图3一gydF4y2Ba) [gydF4y2Ba33gydF4y2Ba].在ESR1和ESR2敲除小鼠和杂合小鼠中,针对ESR1、ESR2和非典型G蛋白偶联雌激素受体(GPER)的Western blots显示了预期的和特异性的蛋白质损失(在线补充图S3)。在敲除ESR1或ESR2基因后,GPER似乎有代偿性增加,但没有互反性ESR。gydF4y2Ba
a)雌激素受体(ESR)1,而不是ESR2敲除可降低小鼠子宫重量(p<0.0001),正如预期的那样[gydF4y2Ba33gydF4y2Ba];经多元方差分析,R899X突变对子宫重量无影响。每个符号代表一个鼠标的测量值;数据以中位数±表示gydF4y2Ba扫描电镜gydF4y2Ba.b)敲除ESR1部分和ESR2完全降低男性和女性BMPR2的右心室收缩压(RVSP)gydF4y2BaR899XgydF4y2Ba老鼠。每个符号代表一个鼠标的值。多因素方差分析显示,考虑性别、BMPR2突变和ESR状态等因素,BMPR2突变增加RVSP(多因素方差分析p=0.0003), ESR1趋于恢复(p=0.07), ESR2完全恢复RVSP (p=0.005)。性别没有显著的相互作用(所有小鼠都在泵内注射了16αOHE1)。每组小鼠的数量列在图的底部;小鼠年龄匹配,每组同时评估对照组。c) ESR1基因敲除小鼠部分和ESR2基因敲除小鼠完全减少BMPR2中的肌肉化小血管gydF4y2BaR899XgydF4y2Ba小鼠恢复正常。通过多因素方差分析,考虑性别、BMPR2突变和ESR状态等因素,BMPR2突变增加肌肉化血管(多因素方差分析p=0.0002), ESR1 (p=0.02)和ESR2 (p=0.0005)均使肌肉化血管正常化。d)平滑肌肌动蛋白(红色)用4′,6-二氨基氨基-2-苯吲哚(DAPI;蓝色)。DAPI染色的表观强度降低,以澄清肌动蛋白。在BMPR2中,肌肉化和部分肌肉化的小血管大约增加一倍gydF4y2BaR899XgydF4y2Ba小鼠,偶有血管闭塞(图中)。ESR1基因敲除减少了肌肉化,但仍有一些堵塞的血管(前两名);敲除ESR2使肌肉化正常化,堵塞的血管不再明显。gydF4y2Ba
闭胸测量自主呼吸小鼠的RVSP, 37例Bmpr2中发现20例(54%)gydF4y2BaR899XgydF4y2Ba血压>32 mmHg的小鼠(gydF4y2Ba图3 bgydF4y2Ba),而Bmpr2的这一数字较低gydF4y2BaR899XgydF4y2BaESR1敲除小鼠(21只中有7只(33%)),Bmpr2敲除22只中有3只(14%)gydF4y2BaR899XgydF4y2BaESR2敲除小鼠。Bmpr2的肌肉化趋势与此相似,有大量肌肉化的小血管gydF4y2BaR899XgydF4y2Ba小鼠几乎是对照组的两倍(gydF4y2Ba图3 cgydF4y2Ba和d),这些数字在ESR1中有所减少,在ESR2敲除中减少更多。Bmpr2中偶尔可见闭塞血管gydF4y2BaR899XgydF4y2Ba小鼠肺在ESR1敲除中仍然存在,但在ESR2敲除中不明显(gydF4y2Ba图3 dgydF4y2Ba).综上所述,这些数据表明雌激素在PAH中的作用部分是通过ESR1和ESR2介导的,其中ESR2占主导地位。gydF4y2Ba
雌激素抑制逆转BMPR2突变诱导的胰岛素抵抗gydF4y2Ba
我们和其他研究人员此前已经证明,在BMPR2突变小鼠和人类PAH患者中,PPAR-γ和CD36的表达受到抑制,胰岛素抵抗增加[gydF4y2Ba22gydF4y2Ba,gydF4y2Ba34gydF4y2Ba].gydF4y2Ba
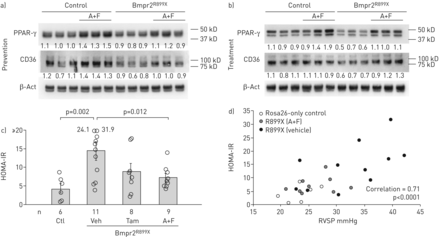
在这里我们发现这些变化被阻止了(gydF4y2Ba图4一gydF4y2Ba)和反转(gydF4y2Ba图4 bgydF4y2Ba)雌激素抑制。在反转研究中,BMPR2突变体组PPAR-γ和CD36的抑制更令人印象深刻,可能是因为动物有更长的发病时间(10周而不是6周)。通过测量血糖和胰岛素来测量胰岛素抵抗,与之前一样,BMPR2突变体的稳态模型评估(HOMA)胰岛素抵抗显著增加,阿那曲唑/氟维司坦显著降低,而他莫昔芬则呈下降趋势(gydF4y2Ba图4 cgydF4y2Ba).绘制HOMA对RVSP的胰岛素抵抗图显示两者强相关(r=0.71) (gydF4y2Ba图4 dgydF4y2Ba).这些数据表明雌激素对RVSP的抑制作用与其代谢效应密切相关。gydF4y2Ba
a)预防性使用阿那曲唑和氟维司坦(a +F)会导致全肺过氧化物酶体增殖物激活受体(PPAR)-γ (p=0.001)和CD36 (p=0.02)增加,否则R899X突变(PPAR -γ p=0.003, CD36 p=0.007)会被抑制,通过双向方差分析。数字表示上述波段的密度测量;每一条都是来自不同动物的整个肺。b) A+F治疗导致全肺PPAR-γ (p=0.019)和CD36 (p=0.027)升高,而R899X突变(PPAR-γ p=0.047, CD36 p=0.043)抑制全肺PPAR-γ升高。数字表示上述波段的密度测量;每一条都是来自不同动物的整个肺。c) A+F治疗显著降低R899X小鼠的胰岛素抵抗(p=0.012),而他莫西芬(Tam)有改善的趋势(p=0.06)。检验是Fisher方差分析后最不显著的差异(p=0.01,拒绝为空)。请注意,即使是对照组小鼠的胰岛素抵抗也相当高,因为它们是西方饮食的FVB/N小鼠。d)胰岛素抵抗与右心室收缩压(RVSP)高度相关(相关性=0.71,p<0.0001)。 β-Act: β-actin; HOMA-IR: homeostatic model assessment insulin resistance ctl: control; veh: vehicle.
此外,我们还在BMPR2突变和无BMPR2突变的ESR1和ESR2敲除小鼠中测量了PPAR-γ和CD36。ESR1基因敲除效果不一致(gydF4y2Ba图5一个gydF4y2Ba),而敲除ESR2导致对照组和BMPR2突变小鼠PPAR-γ和CD36增加(gydF4y2Ba图5 bgydF4y2Ba).这支持了血液动力学测量gydF4y2Ba图3gydF4y2Ba这表明ESR2比ESR1更容易导致雌激素对PAH的负面影响。gydF4y2Ba

a)通过双向方差分析,敲除雌激素受体(ESR)1不影响全肺过氧化物酶体增殖物激活受体(PPAR)-γ或CD36,尽管PPAR-γ被R899X突变抑制(p=0.03)。b)通过双因素方差分析,PPAR-γ在全肺中被R899X突变抑制(p=0.02),在ESR2敲除后被诱导(p=0.001);ESR2敲除也能诱导CD36 (p=−0.001)。β法:β肌动蛋白。gydF4y2Ba
雌激素在细胞水平上促进胰岛素抵抗gydF4y2Ba
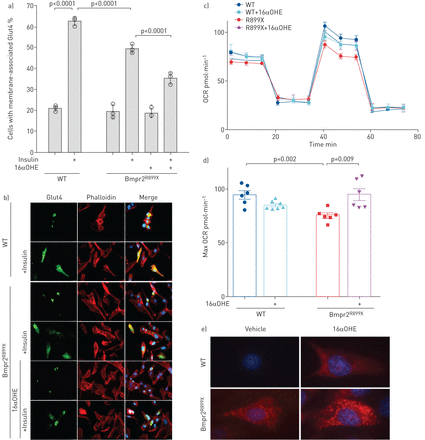
虽然葡萄糖代谢在整个生物水平上是由多个器官的相互作用调节的,但在细胞水平上,胰岛素抵抗的特征是葡萄糖转运蛋白Glut4在胰岛素反应中的动员减少。我们之前在BMPR2突变的人内皮细胞中发现了这一水平的基本缺陷;具体来说,胰岛素信号是完整的,但Glut4未能动员[gydF4y2Ba35gydF4y2Ba].在这里,我们重复了这一结果,并表明雌激素16αOHE1显著恶化了Bmpr2培养的PMVECs的胰岛素反应gydF4y2BaR899XgydF4y2Ba老鼠(gydF4y2Ba图6gydF4y2Bab).使用16αOHE1而不是E2,因为它比E2更具有雌激素性,患者体内E2优先代谢为16αOHE1 [gydF4y2Ba11gydF4y2Ba].gydF4y2Ba
a) BMPR2降低了小鼠肺微血管内皮细胞(PMVECs)中GLUT4的胰岛素动员gydF4y2BaR899XgydF4y2Ba经16αOHE1预处理后,小鼠的细胞活性进一步降低。通过计数核周来测定胰岛素动员gydF4y2Ba与gydF4y2Ba膜相关绿色荧光蛋白(GFP)标记的GLUT4在每个技术重复的100个细胞中(每个重复的百分比用圆圈表示)。每个组有三个技术重复:有些是重叠的。误差条表示标准偏差;经方差分析,p<0.0001时差异显著,比较用Fisher最小显著性差异表示。通过Wilcoxon非参数检验,差异具有显著性(p=0.01)。b)瞬时转染gfp标记的Glut4的小鼠PMVECs活细胞图像,未经处理,用16αOHE1预处理,或用载液或胰岛素处理后15分钟(胰岛素应将Glut4动员到细胞表面)。c)海马细胞外通量分析(海马生物科学,北比勒利卡,马萨诸塞州,美国)使用mito应激方案显示,FCCP处理(~ 40-60分钟)增加了最大耗氧率(OCR)。d)根据c中的数据定量最大耗氧率。e) Mitosox Red试验(Molecular Probes, Eugene, OR, USA)表明,携带16αOHE1的Bmpr2突变细胞的耗氧增加是由线粒体超氧化物产生增加所驱动的。WT:野生型。gydF4y2Ba
比较Bmpr2的最大耗氧率(OCR)gydF4y2BaR899XgydF4y2Ba使用海马细胞外通量分析,我们发现PMVEC来自Bmpr2gydF4y2BaR899XgydF4y2Ba小鼠的最大OCR显著降低(gydF4y2Ba图6 cgydF4y2Bad)在标准媒体中。然而,16αOHE1的加入增加了Bmpr2的最大OCRgydF4y2BaR899XgydF4y2Ba突变体;相反,16αOHE1降低了野生型细胞的最大OCR (gydF4y2Ba图6 cgydF4y2Bad).这些数据表明雌激素可以改变Bmpr2突变环境中已经紊乱的细胞代谢活性。gydF4y2Ba
虽然我们不清楚雌激素如何影响这些细胞的代谢,但用超氧化物检测器Mitosox Red染色活细胞表明,16αOHE1的耗氧量增加是由超氧化物产生增加引起的(gydF4y2Ba图6 egydF4y2Ba).gydF4y2Ba
讨论gydF4y2Ba
在过去的十年中,多环芳烃研究界在开发分子靶向疗法方面取得了巨大的进展。在该领域有广泛的共识,除了BMP信号被抑制外,或者可能是因为BMP信号被抑制,PAH的进展需要去分化和增殖、炎症和代谢变化。针对这些药物的试验已经完成[gydF4y2Ba36gydF4y2Ba- - - - - -gydF4y2Ba38gydF4y2Ba],正在进行中[gydF4y2Ba39gydF4y2Ba]或正在发展中[gydF4y2Ba40gydF4y2Ba];在这一点上,争论的是如何有效地干预,而不是我们需要在哪里干预。因此,该领域的目标是有效地将我们的分子发现转化为治疗方法。gydF4y2Ba
女性是PAH最强的流行病学危险因素,男女比例为3:1。然而,直到最近,其原因尚不清楚:雌激素和女性在经典的多环芳烃模型中具有保护作用,如缺氧和单花椰菜碱[gydF4y2Ba15gydF4y2Ba].然而,一系列的研究提供了关于性和多环芳烃的新信息。多环芳烃患者雌二醇水平升高[gydF4y2Ba41gydF4y2Ba],而患者多环芳烃风险的增加与雌激素优先代谢为16-雌激素(如16αOHE1)密切相关[gydF4y2Ba11gydF4y2Ba,gydF4y2Ba12gydF4y2Ba,gydF4y2Ba42gydF4y2Ba].产生母本雌激素的两种芳香化酶都存在潜在的遗传变异[gydF4y2Ba41gydF4y2Ba以及调节雌激素代谢的CYP1B1 [gydF4y2Ba11gydF4y2Ba,gydF4y2Ba43gydF4y2Ba]与门脉性肺动脉高压和特发性肺动脉高压的预后相关。16αOHE1的增加很重要,因为它以共价结合受体,因此比2-和4-雌激素更具有雌激素性。gydF4y2Ba
用16αOHE1治疗BMPR2突变小鼠增加外显率和疾病严重程度[gydF4y2Ba14gydF4y2Ba],与代谢问题增加的标志物相关[gydF4y2Ba17gydF4y2Ba].代谢紊乱的标志物,包括代谢综合征,与患者的疾病密切相关[gydF4y2Ba18gydF4y2Ba- - - - - -gydF4y2Ba20.gydF4y2Ba]和BMPR2突变小鼠的因果关系[gydF4y2Ba21gydF4y2Ba,gydF4y2Ba22gydF4y2Ba].代谢问题本身可能很重要,例如,通过促进增殖,但它们也可能很重要,因为它们导致活性氧和氮的产生增加。这些现象是紧密相连的,并且两者都在多环芳烃中被广泛研究(由FgydF4y2Ba血管gydF4y2Ba和WgydF4y2Ba美国东部时间gydF4y2Ba[gydF4y2Ba44gydF4y2Ba])。雌激素,特别是16αOHE1,最近已被证明以依赖于nadph的方式诱导活性氧的产生[gydF4y2Ba45gydF4y2Ba],支持雌激素、代谢和活性氧之间的联系。gydF4y2Ba
在本研究中,我们通过解决关键遗留问题来完成翻译准备工作。我们证明,在BMPR2突变的背景下,雌激素抑制既可以防止和逆转PAH,可能是通过典型的雌激素受体信号。我们发现雌激素抑制逆转代谢缺陷标志物,包括homa -胰岛素抵抗,雌激素在细胞水平上影响胰岛素抵抗。这些数据的组合提供了一种可能的作用机制,并在小鼠中证明了疗效,为在患者中使用雌激素抑制影响代谢轴的临床试验铺平了道路。gydF4y2Ba
一个关键的问题是雌激素是直接调节代谢,还是通过调节BMP途径间接调节代谢。雌激素抑制人肺动脉平滑肌细胞BMPR2信号转导[gydF4y2Ba46gydF4y2Ba],可能是通过雌激素受体与BMPR2启动子的直接结合[gydF4y2Ba47gydF4y2Ba],可导致细胞培养中增殖增加。由于BMP通路调节代谢,至少部分影响可能是通过ESR1 (ERα)介导的抑制BMPR2。ESR1单核苷酸多态性与门脉性肺动脉高压风险相关[gydF4y2Ba41gydF4y2Ba].然而,有些影响可能是直接的;ESR2 (ERβ)可以定位于线粒体,在那里它直接迫使支持增殖的代谢转移[gydF4y2Ba48gydF4y2Ba].因为我们之前已经证明雌激素对线粒体形态有很强的影响[gydF4y2Ba17gydF4y2Ba],很可能至少部分雌激素对代谢的影响绕过了BMPR2。因为ESR1和ESR2都有合理而独特的作用模式,其主要作用可能微妙地依赖于被研究的精确条件和器官。例如,在本研究中,由于BMPR2被基因抑制,ESR1在抑制BMPR2中的作用可能不那么重要。ESR敲除后GPER的增加也可能与结果相关:GPER已被证明在药理雌激素阻断后增加[gydF4y2Ba49gydF4y2Ba].通过GPER增加信号传递对多环芳烃有潜在益处[gydF4y2Ba50gydF4y2Ba].gydF4y2Ba
另一个有趣的问题是雌激素的来源是否重要。以往的研究大多显示雌激素对雄性啮齿动物的保护作用;相比之下,在缺氧或Sugen/缺氧模型中,阿那曲唑对雌性啮齿动物有保护作用,但对雄性啮齿动物没有保护作用[gydF4y2Ba16gydF4y2Ba].此外,在右芬氟拉明模型中,只有雌性小鼠出现肺动脉高压[gydF4y2Ba51gydF4y2Ba],卵巢切除术可以防止过度表达血清素转运体的小鼠的肺动脉高压[gydF4y2Ba52gydF4y2Ba].理论是雌激素产生的部位很重要,而生殖道外的雌激素产生可能尤其重要。为了支持这一点,我们之前已经证明雌激素代谢模式与男性多环芳烃患者的疾病外显率相关[gydF4y2Ba17gydF4y2Ba].这表明,在男性和绝经后患者中,脂肪组织等外周雌激素的产生[gydF4y2Ba53gydF4y2Ba],可能仍然是雌激素驱动疾病的病理来源。gydF4y2Ba
这些和其他科学问题仍有待解决。从长远来看,雌激素可能对PAH患者右心室功能有保护作用,这仍是进一步研究的机会[gydF4y2Ba43gydF4y2Ba,gydF4y2Ba54gydF4y2Ba- - - - - -gydF4y2Ba56gydF4y2Ba].由于绝大多数女性和糖尿病患者不会患上PAH,因此单凭雌激素或胰岛素抵抗显然都不足以引起PAH,但在BMPR2突变的背景下,这些都是发展为临床疾病的强大驱动因素。然而,我们仍然不了解具体的机制。暴露于雌激素和暴露于BMPR2突变与线粒体碎片有关[gydF4y2Ba17gydF4y2Ba],氧化应激增加[gydF4y2Ba57gydF4y2Ba]、蛋白质、糖和脂质处理的改变[gydF4y2Ba18gydF4y2Ba]和胰岛素抵抗增加[gydF4y2Ba14gydF4y2Ba,gydF4y2Ba22gydF4y2Ba].虽然所有这些现象都是相关的,但我们还没有一个自上而下的机制将这些与雌激素或BMPR2联系起来,我们也不知道哪些是致病的,哪些是旁观者。此外,我们不知道非典型雌激素信号的确切作用,如果有的话。gydF4y2Ba
虽然在科学上很有趣,但在进行翻译之前,并不是必须回答所有这些问题。特别是在男性和绝经后女性中,强雌激素抑制是安全的,可以解决许多与PAH发展有因果关系的分子病理,并在许多患者中发现的携带相同BMPR2突变的小鼠中逆转已确定的疾病。事实上,一项使用雌激素修饰形式的短期二期人体多环芳烃试验最近刚刚完成gydF4y2BaNCT01545336gydF4y2Ba);它是安全的,耐受性良好,并显示出一些疗效[gydF4y2Ba24gydF4y2Ba].临床翻译的核心问题之一是使用何种药物。我们的数据表明,虽然更强的抑制作用,如阿那曲唑和氟维司坦所达到的抑制作用更有效,因此可能更适合绝经后患者和男性,但它莫西芬具有一定的疗效,并且更容易用于绝经前女性[gydF4y2Ba58gydF4y2Ba,值得确定是否可以在这些年轻患者中进行替代,以避免诱导绝经。gydF4y2Ba
本研究为进一步证明雌激素抑制的有效性和阐明机制(包括改善多环芳烃中存在的一些代谢异常)提供了关键的背景工作。通过增加进行人体试验所需的基础工作,我们期待着继续进行额外的测试和早期转化研究。gydF4y2Ba
补充材料gydF4y2Ba
补充材料gydF4y2Ba
请注意:gydF4y2Ba补充材料不是编辑部编辑的,上传时是作者提供的。gydF4y2Ba
图S1。在预防研究(A)、治疗研究(B)和雌激素受体敲除研究(C)中,任何组的富尔顿指数(右心室重量除以左心室和中隔重量)都没有改变。富尔顿指数在这个模型中没有信息,因为Bmpr2突变小鼠(和患者)的RV具有肥厚反应受损[19]。gydF4y2Baerj - 02337 - 2016 - _supplementary_figure_s1gydF4y2Ba
图S2。(A)血浆雌激素被阿那曲唑和氟维司坦联合抑制,但不被他莫昔芬抑制,正如预期的那样。(B)他莫西芬治疗抑制了全肺已知雌激素靶点FHL1和SNAT2的表达。通过定量RT-PCR进行评估,归一化到管家基因HPRT的表达和载体值。两种情况下的误差条都是平均的标准误差;圆形符号是来自单个鼠标的值,条形标记平均值。gydF4y2Baerj - 02337 - 2016 - _supplementary_figure_s2gydF4y2Ba
图S3。western blot检测全肺雌激素受体水平,显示最接近的蛋白阶梯标记。请注意,尽管在ESR1敲除小鼠中ESR1似乎没有增加,或在ESR1敲除小鼠中ESR2似乎没有增加,但在杂合和纯合的ESR1和ESR2敲除小鼠中,g蛋白偶联雌激素受体GPER明显增加。数字表示密度测量,归一化为野生型。gydF4y2Baerj - 02337 - 2016 - _supplementary_figure_s3gydF4y2Ba
披露的信息gydF4y2Ba
补充材料gydF4y2Ba
摩根大通(J.P. FesselgydF4y2Baerj - 02337 - 2016 - _fesselgydF4y2Ba
境HemnesgydF4y2Baerj - 02337 - 2016 - _hemnesgydF4y2Ba
J.E.劳埃德gydF4y2Baerj - 02337 - 2016 - _loydgydF4y2Ba
脚注gydF4y2Ba
这篇文章有补充资料可从gydF4y2Bawww.qdcxjkg.comgydF4y2Ba
支持声明:这些研究由美国国立卫生研究院(NIH)资助,NIH P01 HL108800, NIH R01 HL 095797和HL 122417和NIH K08 HL121174;帕克·b·弗朗西斯奖学金(j·p·费塞尔);美国心脏协会教授奖#13FTF16070002 (E.L. Brittain);以及吉利德科学研究学者肺动脉高压项目(E.L. Brittain)。本研究中使用的海马生物科学细胞外通量分析仪被安置和管理在范德比尔特高通量筛查核心设施中,这是一个机构支持的核心,由NIH共享仪器拨款S10 OD018015资助。本文的资助信息已存入gydF4y2Ba交叉参考基金注册gydF4y2Ba.gydF4y2Ba
利益冲突:可以在本文旁边的网站上找到信息披露gydF4y2Bawww.qdcxjkg.comgydF4y2Ba
- 收到了gydF4y2Ba2016年5月4日。gydF4y2Ba
- 接受gydF4y2Ba2017年4月15日。gydF4y2Ba
- 版权所有©ERS 2017gydF4y2Ba
参考文献gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba