文摘
阻塞性睡眠呼吸暂停(OSA)是与癌症发病率和死亡率相关。免疫系统似乎是至关重要的贡献;然而,潜在的单核细胞和自然杀伤(NK)细胞的作用仍不清楚。
定量逆转录酶聚合酶链反应、流式细胞术和在体外分析是用来分析表型和免疫应答活动92年阻塞性睡眠呼吸暂停综合症患者(60最近诊断治疗患者和32名患者治疗6个月后持续气道正压(CPAP))和29名健康志愿者(高压)。
我们确定,单核细胞阻塞性睡眠呼吸暂停患者表现出免疫抑制表型,包括表面的表达glycoprotein-A重复主要蛋白质(GARP)和转换增长factor-β(TGF-β),相比那些从高压和CPAP组。高水平的TGF-β在阻塞性睡眠呼吸暂停综合症血清检测。TGF-β释放GARP+单核细胞受损的NK细胞毒性和成熟。这个改变表型与缺氧临床严重程度评分(CT90)。再氧化最终恢复改变表型和细胞毒性。
这项研究表明,GARP+从未经治疗的阻塞性睡眠呼吸暂停综合症患者单核细胞通过释放TGF-βNK-suppressing作用。我们的研究结果表明,单核细胞可塑性immunomodulates NK活性在这个病理,表明癌症发病率的潜在作用。
文摘
阻塞性睡眠呼吸暂停症诱发可逆变化的先天免疫反应;单核细胞NK细胞妥协http://ow.ly/q2yb309MRPt
介绍
间歇性缺氧与阻塞性睡眠呼吸暂停(OSA)已被确认为人类癌症发病率和死亡率的一个重要的决定因素(1- - - - - -6和在动物模型7- - - - - -10]。免疫系统能起到至关重要的作用在阻塞性睡眠呼吸暂停综合症和癌症之间的关系7,11- - - - - -13]。调节t细胞淋巴细胞亚群),或者激活巨噬细胞是至关重要的球员在这个免疫抑制状态(14]。事实上,巨噬细胞从老鼠暴露在活的有机体内间歇性缺氧(IH)展览专利对周围组织的免疫抑制表型分化,有利于肿瘤侵犯7,15]。
虽然缺氧对肿瘤免疫逃逸的影响仍然知之甚少,大量证据表明,缺氧可能影响表型和单核细胞和自然杀伤(NK)细胞活性(16),开着强有力的免疫反应的关键。反过来,氧气在NK细胞的发展起着至关重要的作用[17),调节重要的转录因子(RAR-related孤儿受体C (RORC) T-Box蛋白质21 (Tbet)和eomesodermin(加工))参与后期的NK细胞的成熟(18]。它也被报道,转化生长因子β(TGF-β)调节NK细胞分化和细胞毒性通过SMAD3通路(19,20.]。这个途径的激活是由释放TGF-β从其活动形式,TGF-β-latency-associated-peptide (TGF-β-LAP);在这种背景下,glycoprotein-A重复主要蛋白质(GARP)起着重要的作用在调节生物利用度和TGF-β激活细胞表面提供了一个平台21]。有趣的是,我们曾报道,低氧factor-1α(HIF-1α)调节TGF-β的表达在人类单核细胞,增强免疫抑制表型(22]。
因此我们提出,阻塞性睡眠呼吸暂停综合症患者表型的改变和改变循环单核细胞和NK细胞活性,促进免疫逃逸,最终可能增加癌症的发病率。
在此,我们报告单核细胞与阻塞性睡眠呼吸暂停综合症患者认为Treg角色,表达下调的NK细胞毒性TGF-β-dependent方式子集。我们已经识别出的相关性缺氧病理严重程度和受损的免疫反应,以及确定恢复适当的复氧后表型和免疫活动。
材料和方法
材料和方法深入细节,请参阅补充材料。
研究参与者
阻塞性睡眠呼吸暂停综合症患者前瞻性招募从La Paz-Cantoblanco大学医院的睡眠单位,马德里,西班牙。患者年龄在40 - 65年apnoea-hypopnoea指数(AHI)≥30被纳入研究。
根据之前用持续正压通气(CPAP)治疗阻塞性睡眠呼吸暂停综合症患者被分为CPAP-naive(治疗组、阻塞性睡眠呼吸暂停综合症)或已经治疗至少6个月(CPAP治疗组)与平均每天日常使用超过4.5 h,衡量运行时计数器。CPAP组最优CPAP压力是由汽车CPAP滴定装置(REMstar Pro和C-Flex M系列,飞利浦Respironics,匹兹堡,PA,美国)和反复验证了呼吸道polygraphy时加入这项研究。作为对照组,健康志愿者(高压)、均匀性、年龄、吸烟习惯和身体质量指数,被选中。这些志愿者被处理任何类型的药物,和阻塞性睡眠呼吸暂停综合症的存在被呼吸道polygraphy排除。
这项研究是由当地伦理委员会批准(pi - 1857),并从所有的参与者获得知情同意。
细胞培养
从高压组单核细胞和NK细胞培养在常氧条件下(21% O2,5%的公司2,37°C)或使用一个在体外IH的典范。在IH协议,细胞暴露于低氧室(3% O2,5%的公司2,37°C)的12个周期和改变预处理低氧介质(5分钟)常氧介质(10分钟),正如前面所描述的R严等。(23]。预先处理这些媒介的使用是必要的,以允许瞬时接触缺氧。细胞内氧含量测定氧的淬火的激发态oxygen-sensitive探测细胞内氧浓度的测定(Ab197245;Abcam,英国剑桥)。oxygen-sensitive探针的荧光寿命减少暴露于低氧介质后,在常氧条件下增加。
评估的影响,先天免疫系统恢复足够的氧化作用,外周血单核细胞(PBMCs)更多的血氧过低的治疗阻塞性睡眠呼吸暂停综合症患者培养16 h标准细胞培养条件(normoxia,在37°C在湿润的环境中组织文化孵化器有限公司5%2)。
通过定量PCR生物标志物的表达
总RNA从PBMCs和单核细胞纯化分离从罗氏诊断使用高纯RNA隔离工具(瑞士巴塞尔)。基因表达水平进行分析1毫克的反转录RNA使用高容量cDNA逆转录工具包(美国应用生物系统,福斯特,CA),然后定量PCR (qPCR;Light-Cycler,罗氏诊断),使用特定的引物。在CD14+单核细胞、HIF-1αTGF-β1,血管内皮生长因子(VEGF)和白介素(IL) -10被用作M2标记,而IL-12p40担任M1标记(24]。相对表达是基于目标基因的水平与管家基因(β-Actin)。
流式细胞术
PBMCs被染色后隔离与表示抗体(CD3、CD14 TGF-β-LAP、CD56、CD16, CD4, CD25、CD8, CD28、e, P44, P46, p-SMAD2/3和CD117)从BD生物科学(法国格勒诺布尔)。细胞内染色,细胞被贴上了forkhead盒P3(具体),Tbet, RORC,加工和穿孔素从BD生物科学(所有),后一组标准协议使用转录因子缓冲区(BD生物科学)。适当的同形像控制被用于每个实验。抗体的详细信息都包含在E1补充表。染色后,细胞获得使用BD FACSCalibur流式细胞分析仪,并使用FlowJo v10收集到的数据进行分析。
统计分析
除非另有指示,提出了数据均值±扫描电镜。使用方差分析比较组间进行克鲁斯卡尔-沃利斯检验,邓恩的非正态分布变量的多重比较。为在活的有机体内和在体外研究中,统计显著性计算使用Wilcoxon测试或一个合适的配对t检验。的相关性进行评估和斯皮尔曼等级相关的非正态分布数据。被认为是重要的差异p < 0.05和使用Prism 5.0软件进行分析(GraphPad软件公司,拉霍亚,CA,美国)。
结果
病人的人口统计
总共有92例严重的阻塞性睡眠呼吸暂停综合症患者包括60最近被诊断和CPAP-naive(阻塞性睡眠呼吸暂停综合症组)和32曾用CPAP治疗> 6个月(CPAP组);29 HVs也包括控制。表1的基线人体测量和临床数据显示三组。当时他们的诊断,患者在阻塞性睡眠呼吸暂停综合症和CPAP组显示出类似的睡眠特征。然而,研究包含的时候,即后CPAP集团经历了> 6个月的治疗,病人在这组显示恢复睡眠特征(补充表E2)。
阻塞性睡眠呼吸暂停症单核细胞对免疫抑制表型表达GARP和TGF-β两极分化
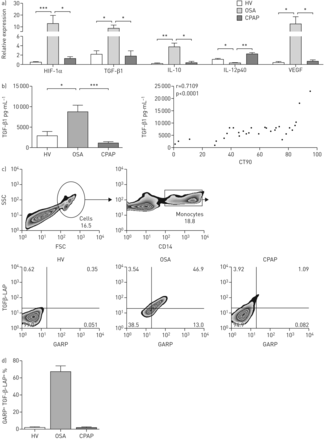
生物标志物在孤立CD14表达分析+单核细胞的三个研究小组表明,阻塞性睡眠呼吸暂停综合症单核细胞分化的免疫抑制表型。我们发现HIF-1αmRNA水平高,TGF-β1,VEGF、il - 10水平下降IL-12p40阻塞性睡眠呼吸暂停综合症组相比,高压或CPAP集团(图1一个)。
阻塞性睡眠呼吸暂停(OSA)患者单核细胞从展览一个免疫抑制表型,表达TGF-β和可能。CD14+单核细胞分离得到健康志愿者(高压)(n = 20随机选择),阻塞性睡眠呼吸暂停综合症患者(n = 20个随机选择)和患者持续气道正压(CPAP) (n = 20随机选择)。HIF-1α)表达式的分析定量PCR, TGF-β1,il - 10, IL-12p40 CD14和VEGF mRNA+单核细胞。相对表达。b) TGF-β1血清中的蛋白质含量进行分析从高压(n = 29),阻塞性睡眠呼吸暂停综合症患者(n = 30随机选择)和病人用CPAP治疗(n = 32)。TGF-β1蛋白质含量与CT90阻塞性睡眠呼吸暂停综合症患者的血清相关。斯皮尔曼相关系数(r和p值)所示。c)控制策略,单核细胞的检测。数字毗邻地区概述表明细胞和单核细胞的百分比。代表点滴TGF-β-LAP GARP CD14表达+细胞所示。外周血单核细胞从高压(n = 29),阻塞性睡眠呼吸暂停综合症患者(n = 20随机选择)和病人用CPAP治疗(n = 20随机选择)被流式细胞术分析。d)的百分比分布可能+TGF-β-LAP+在完全封闭的CD14+细胞。*:p < 0.05;* *:p < 0.01;* * *:p < 0.001为阻塞性睡眠呼吸暂停综合症利用克鲁斯卡尔-沃利斯检验邓恩的多重比较。
此外,我们的分析显示,TGF-β1阻塞性睡眠呼吸暂停综合症中蛋白质含量明显升高血清与高压和CPAP组;这个表达式与夜间动脉氧饱和度测量脉搏血氧仪(年代阿宝2)< 90% (CT90) (图1 b,r = 0.7109)。尽管TGF-βTreg人口的诱导物(25),阻塞性睡眠呼吸暂停综合症患者表现出显著减少Treg子集(补充图E1a)。我们研究TGF-β-related蛋白的表达,GARP TGF-β-LAP,扮演着重要的角色在活跃TGF-β的释放。GARP和TGF-β-LAP在阻塞性睡眠呼吸暂停综合症患者单核细胞,发现了但不是在单核细胞从高压和CPAP组(图1 cd);然而,TGF-β-LAP Treg上没有检测到细胞表面(补充图E1b)。
阻塞性睡眠呼吸暂停NK细胞表现出不成熟的子集和受损细胞毒性的活动
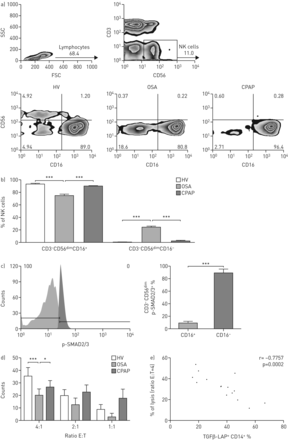
TGF-β在NK细胞的免疫抑制作用是众所周知的26- - - - - -30.]。虽然未发现差异在NK细胞(CD3的总数−CD56+)在三个学习小组(补充图ea2), NK表型的分析表明专利(CD3细胞毒性减少子集−CD56昏暗的CD16+在阻塞性睡眠呼吸暂停综合症组相比,高压和CPAP组(图2一个b)。奇怪的是,我们观察到一个新的(CD3 NK子集−CD56昏暗的CD16−)只有在阻塞性睡眠呼吸暂停综合症患者(见阻塞性睡眠呼吸暂停综合症点污点,图2一个b)。此外,我们发现p-SMAD2/3水平显著增加(图2 c),表明TGF-β通路的激活在这个新的NK子集。NK细胞毒性的能力明显受损的患者较CPAP-treated阻塞性睡眠呼吸暂停综合症患者和高压(图2 d)。NK细胞毒性与表面TGF-β-LAP单核细胞(图2 e,r =−0.7757),这表明他们的免疫抑制作用。自然细胞毒素受体的表达,包括e, p44 p46, CD3明显减少−CD56昏暗的CD16−与细胞毒性(CD3子集−CD56昏暗的CD16+)(NK子集图3一- c)。减少穿孔素表达CD3也观察到−CD56昏暗的CD16−子集(图3 d)。
患者的NK子集阻塞性睡眠呼吸暂停(OSA)表明,CD16表达下调,p-SMAD2/3调节,受损的细胞毒性与TGF-β-LAP单核细胞。从健康志愿者外周血单核细胞(高压)(n = 29),阻塞性睡眠呼吸暂停综合症患者(n = 20个随机选择)和患者持续气道正压(CPAP) (n = 20随机选择)被流式细胞术分析。)控制策略对NK细胞的检测。数字毗邻地区概述表明淋巴细胞和NK细胞的百分比。代表点墨迹CD56、CD16表情NK细胞。b) CD3的比例分布−CD56昏暗的CD16+和CD3−CD56昏暗的CD16−在完全封闭的NK细胞。* * *:p < 0.001,利用克鲁斯卡尔-沃利斯检验邓恩的多重比较。c) CD3的百分比分布−CD56昏暗的p-SMAD2/3+在CD3−CD56昏暗的CD16+(浅灰色酒吧)和CD3−CD56昏暗的CD16−(深灰色酒吧)阻塞性睡眠呼吸暂停综合症患者(n = 20随机选择)。一个标准的直方图显示。* * *:p < 0.001,采用配对t检验。d)细胞毒性活动europium-TDA释放试验2 h后的孵化NK (E)与靶细胞K562 (T)在不同的比率。显示的比例溶解。*:p < 0.05;* * *:p < 0.001,利用克鲁斯卡尔-沃利斯检验邓恩的多重比较。e)孤立的阻塞性睡眠呼吸暂停综合症患者外周血单核细胞(n = 16随机选择)被流式细胞术分析。裂解NK细胞毒性活性(%,比E: T = 4)与平均荧光强度TGF-β-LAP总CD14大门+细胞。斯皮尔曼相关系数(r和p值)。
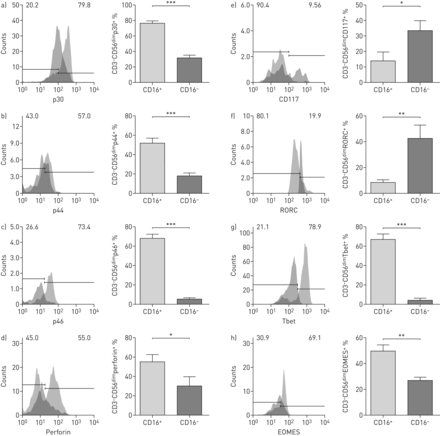
的CD3−CD56昏暗的CD16−NK子集展品不成熟状态。CD3−CD56昏暗的CD16+(浅灰色酒吧)和CD3−CD56昏暗的CD16−(深灰色酒吧)阻塞性睡眠呼吸暂停(OSA)患者(n = 20随机选择)被流式细胞术分析。对于每一个,分布和比例标准的柱状图所示。一)CD3−CD56昏暗的e+;b) CD3−CD56昏暗的p44+;c) CD3−CD56昏暗的p46+;d) CD3−CD56昏暗的穿孔素;e) CD3−CD56昏暗的CD117+;f) CD3−CD56昏暗的RORC+;g) CD3−CD56昏暗的Tbet+;h) CD3−CD56昏暗的加工+。* *:*:p < 0.05, p < 0.01;* * *:p < 0.001,采用配对t检验。
NK细胞的表型分析使用的细胞表面标记CD117、涉及的中间阶段分化的NK细胞(18),和一组转录因子(RORC, Tbet和加工)与NK细胞分化有关。的表面表达CD117 CD3明显减少−CD56昏暗的CD16−NK子集(图3 e)。而Tbet和加工与成熟的NK表型相关,RORC定义了一个不成熟的NK状态(31日]。的CD3−CD56昏暗的CD16−支持的子集表现出不成熟表型RORC upregulation和抑制Tbet和加工(图3 f- h)。其他t细胞亚群细胞毒性报道活动也进行了分析,包括CD3+CD56+,CD3+CD8+,CD3+CD28+和CD3+γδ+(补充图E2b-e)。只有CD3+γδ+阻塞性睡眠呼吸暂停患者的分组人口表现出显著增加。每个单元格的子集在高压和CPAP-treated获得病人的报道值匹配他们的年龄分布(32,33]。
GARP+单核细胞调节NK细胞毒性子集
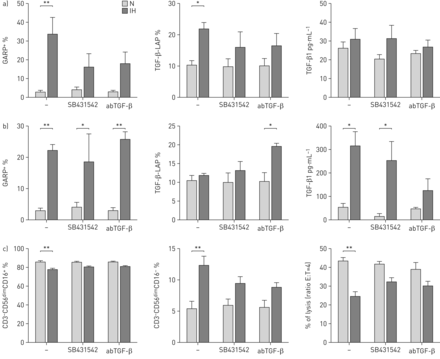
为了评估可能的含义+单核细胞在NK细胞毒性,我们执行一个在体外培养独立CD14 IH的模型+单核细胞从高压的先决条件在缺氧的先决条件中紧随其后的是常氧介质。这种模式导致细胞内氧的循环波动,模仿IH(补充图E3a)。分析HIF-1αTGF-β1,VEGF、il - 10和IL-12p40证实切换到一个免疫抑制表型(补充图E3b)。值得注意的是,HIF-1α击倒恢复的IH(补充图E3c)下观察表型。GARP的百分比+单核细胞增多IH后(图4一左面板);然而,这种效应被TGF-β稍微减轻受体抑制剂(SB431542)和TGF-β1抗体(abTGF-β1)。在单核细胞表面表达TGF-β-LAP显示一个类似的模式(图4一,中央面板)。有趣的是,我们没有观察到TGF-β1活性蛋白质在细胞中2 h后上层清液(图4一右面板)。阐明单核细胞和NK细胞之间的相互作用,我们培养CD14孤立+高压IH与孤立的同源常氧条件下单核细胞NK细胞的比例1:1 2 h。我们观察到可能的分布+单核细胞增多在IH SB431542的存在与否和abTGF-β1 (图4 b左面板)。TGF-β-LAP在单核细胞表面表达的IH减少共培养,除了abTGF-β1条件(图4 b,中央面板)。可溶性TGF-β1活跃的形式被发现只有在IH单核细胞和常氧NK细胞的存在,除了abTGF-β1条件(比较图4一,右面板图4 b右面板)。此外,CD3显著减少−CD56昏暗的CD16+NK和提高CD3子集−CD56昏暗的CD16−观察(NK子集图4 c(左)和中央面板)。这些数据在赞同降低溶解活动观察(图4 c右面板)。这种免疫抑制效应被SB431542减轻,abTGF-β1条件(图4 c)。
GARP+单核细胞释放TGF-β1,CD3调制−CD56昏暗的CD16+NK子集。CD14+单核细胞与健康志愿者在常氧条件下培养(N, N = 7)或间歇性缺氧(IH, N = 7)条件。媒体被补充了一个TGF-β受体抑制剂(SB431542 10μM)或TGF-β1抗体(abTGF-β50 ng·毫升−1)。GARP)比例分布+和TGF-β-LAP+在CD14+细胞所示;从培养媒体TGF-β1蛋白质含量2 h后进行分析。b)分离同源常氧NK细胞被添加在1:1的比例为2 h的孵化。GARP的比例分布+和TGF-β-LAP总CD14大门+细胞所示;从培养媒体TGF-β1蛋白质含量2 h后进行分析。c) CD3的比例分布−CD56昏暗的CD16+和CD3−CD56昏暗的CD16−在完全封闭的NK细胞。细胞毒性活动europium-TDA释放试验2 h后孵化与K562细胞目标。的比例溶解率E: T = 4所示。*:p < 0.05;* *:p < 0.01;使用配对t检验。
缺氧严重程度与阻塞性睡眠呼吸暂停表型改变和NK细胞毒性,而氧化还原免疫抑制表型
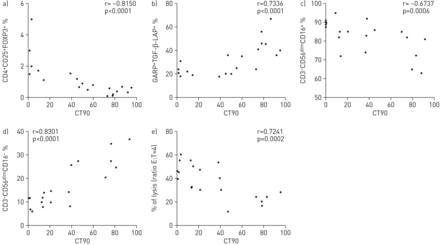
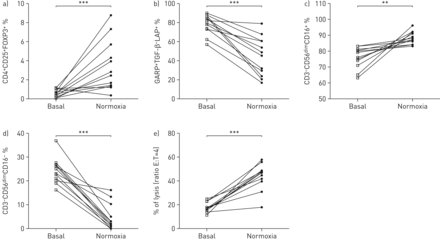
亚群的分布和表型改变,单核细胞和NK子集阻塞性睡眠呼吸暂停患者与缺氧程度评估的夜晚年代阿宝2< 90% (CT90) (图5)。此外,从最孤立的细胞血氧过低的阻塞性睡眠呼吸暂停综合症患者恢复健康的表型和细胞毒性的能力在常氧条件(16 h后图6)。符合这些发现,补充图E4显示五阻塞性睡眠呼吸暂停综合症患者的表型分析之前和之后的6个月CPAP治疗,表明CPAP治疗恢复受损的免疫表型。
夜间动脉氧饱和度测量脉搏血氧仪(年代阿宝2)< 90% (CT90)与Treg分布,单核细胞,NK表型和细胞毒性。孤立的阻塞性睡眠呼吸暂停患者外周血单核细胞(n = 20随机选择)被流式细胞术分析。相关性CT90 CD4的分布比例)+CD25+FOXP3+在完全封闭的淋巴细胞);b)分布GARP百分比+和TGF-β-LAP+在CD14+细胞;c) CD3的比例分布−CD56昏暗的CD16+在封闭的NK细胞;d) CD3的比例分布−CD56昏暗的CD16−在封闭的NK;和e) NK细胞毒性活动(%的裂解,比e: T = 4)。斯皮尔曼相关系数(r和p值)。
Normoxia恢复改变表型在阻塞性睡眠呼吸暂停(OSA)患者。患者外周血单核细胞分离出更多的血氧过低的阻塞性睡眠呼吸暂停综合症(CT90 > 60%, n = 12)分析了在基线条件(开放广场)和文化在常氧条件下16 h(黑点)。显示的百分比分布)亚群(CD4细胞+CD25+FOXP3+在完全封闭的淋巴细胞);b) GARP+TGF-β-LAP+在完全封闭的CD14+细胞;和c) CD3−CD56昏暗的CD16+和d) CD3−CD56昏暗的CD16−在完全封闭的NK细胞。e)细胞毒性活动europium-TDA释放试验2 h后孵化与K562靶细胞;溶解的百分比(比E: T = 4)所示。* *:p < 0.01;* * *:p < 0.001,使用Wilcoxon测试。
讨论
我们的研究结果表明,阻塞性睡眠呼吸暂停综合症患者免疫细胞表型改变,包括单核细胞和NK细胞。这些受损的表型没有观察阻塞性睡眠呼吸暂停患者谁收到> 6个月CPAP治疗,表明氧化作用的免疫可塑性。根据我们的调查结果,阻塞性睡眠呼吸暂停综合症调节循环单核细胞的表型向一个免疫抑制状态(高水平的HIF-1αTGF-β,il - 10和VEGF水平和减少IL-12p40)。我们曾报道,在免疫抑制重组HIF-1α起着至关重要的作用,增加TGF-β和VEGF的表达22]。此外,il - 10和衰减的upregulation IL-12p40至关重要标记分类选择表型在单核细胞(24]。据报道,一些细胞因子和代谢产物直接让免疫系统,降低细胞毒性的能力(27,34]。其中,细胞因子TGF-β在抑制免疫反应中起着重要作用[35]。奇怪的是,未经治疗的阻塞性睡眠呼吸暂停综合症的血清显示,水平的提高TGF-β与血氧过低的指数CT90,支持缺氧严重程度之间的关系和免疫抑制。我们注意到缺氧、炎症和TGF-β是肿瘤微环境的主要成分(36- - - - - -38]。在这种背景下,我们认为阻塞性睡眠呼吸暂停综合症患者基底系统性炎症和间歇性缺氧;我们也报道了高水平的TGF-β流通。因此,我们提出一个对阻塞性睡眠呼吸暂停综合症单核细胞的免疫抑制表型分化由于这个特殊的环境。
重要的是,TGF-β削弱了成熟,NK细胞的增殖和功能活动(39]。有趣的是,我们的阻塞性睡眠呼吸暂停综合症患者表现出一种新的NK (CD3子集−CD56昏暗的CD16−)p-SMAD2/3增加的情况,表明TGF-β通路的激活(26]。观察到的新NK子集的特点是减少自然细胞毒素受体和成熟的标记。NK功能还显示穿孔素水平降低与降低细胞毒性。
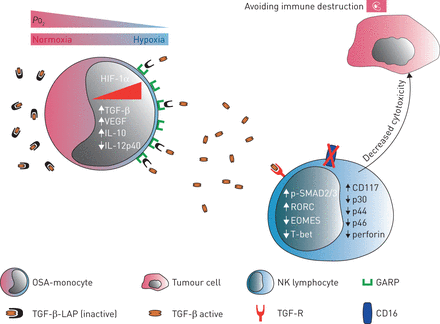
其他的研究也表明,亚减少细胞毒性NK子集通过TGF-β,支持一个不成熟的外观表型(40]。然而,我们的研究结果和之前报道的数据(12]表明,显著降低阻塞性睡眠呼吸暂停患者亚群,可能由于缺氧变弱Treg发展通过绑定FOXP3和定位变幻虫的退化(41]。因此,我们研究了TGF-β-related蛋白的表达在其他免疫细胞(GARP和TGF-β-LAP)。在我们的阻塞性睡眠呼吸暂停综合症患者,TGF-β-LAP Treg细胞表面不存在,而在单核细胞发现了GARP和TGF-β-LAP。GARP调节TGF-β的生物利用度,加入了大腿上,释放TGF-β活性形式(21,42]。其他作者报道,GARP Treg表面捕捉TGF-β-LAP从它的环境,导致当地的抑制抗肿瘤免疫反应(42]。符合这些结果,我们提出一个新颖的核心作用的单核细胞损伤患者的抗肿瘤免疫监视的阻塞性睡眠呼吸暂停综合症(图7)。我们的研究结果表明,免疫抑制单核细胞,但不是亚群,表达不活跃TGF-β-LAP和促进积极TGF-β1的释放,调节NK表型及其活动。TGF-β报道抑制NK细胞的抗肿瘤活性,抑制mTOR通路(26]。
相声单核细胞和NK细胞之间的示意图表示在阻塞性睡眠呼吸暂停(OSA)患者。间歇性低氧环境阻塞性睡眠呼吸暂停患者引起对一个免疫抑制单核细胞分化表型。此外,阻塞性睡眠呼吸暂停综合症单核细胞显示GARP和TGF-β-LAP表面表达调节NK细胞毒性彻底TGF-β激活。这NK调制显示降级从成熟到成熟阶段,影响细胞毒性表型和细胞溶解活动。总的来说,阻塞性睡眠呼吸暂停综合症条件诱导免疫抑制可能解释阻塞性睡眠呼吸暂停患者的癌症发病率。PO2:氧张力。
免疫抑制的变化描述Treg表型,单核细胞和NK细胞和NK细胞毒性与CT90阻塞性睡眠呼吸暂停患者。这些发现与之前的研究相一致的报道,CT90是唯一独立睡眠参数与癌症发病率增加(4)和死亡率(5阻塞性睡眠呼吸暂停患者。值得注意的是,在这些研究中,CT90更能预示他的癌症发病率或死亡率比你好减饱和指数(4,5]。因此,因为呼吸衰竭患者或那些接受长期氧疗法被排除在本研究慢性持续缺氧的影响降到最低,我们的研究结果似乎表明,IH先天免疫系统的影响的大小取决于缺氧而不是oxygenation-desaturation序列的数量。
我们的研究证实,恢复足够的氧化逆转免疫反应损伤的上下文中发现阻塞性睡眠呼吸暂停综合症。这些数据都和以前的观测一致,抑制tumoural缺氧的微环境逆转免疫抑制状态,减少分子如TGF-β[43]。这些影响似乎Treg NK cell-dependent,他们扩展以前的观测使至关重要的NK细胞的抗肿瘤免疫活动在正常氧条件下(44]。HVs的纵向研究,个人窝藏NK细胞自然较低细胞毒性了癌症的发病率明显高于11年之后(45]。
考虑到人类和小鼠免疫细胞子集之间的显著差异,尤其是NK细胞(46),我们的研究的主要力量是先天免疫反应的分析特征明显的阻塞性睡眠呼吸暂停综合症的病人,描述IH-dependent免疫逃逸的分子机制。
然而,目前的研究也有一些局限性。我们只选择严重阻塞性睡眠呼吸暂停综合症患者;因此,它是不可能知道确定的变化也会出现在温和形式的疾病。虽然治疗组和治疗阻塞性睡眠呼吸暂停综合症患者在基线,均匀设计张后治疗不成立(包括只有一小部分患者两组)。没有随机分配的阻塞性睡眠呼吸暂停综合症患者用CPAP治疗或控制。CPAP治疗阻塞性睡眠呼吸暂停症患者的组织包括评估先天免疫系统的可塑性和加强睡眠呼吸暂停症之间的关系,免疫抑制表型的改变,显示经济复苏时呼吸暂停是抑制。我们必须确认结果的临床意义;我们的研究结果并不允许我们建立临床对CPAP管理阻塞性睡眠呼吸暂停患者的建议。到目前为止,没有临床证据,CPAP治疗可以减少癌症的发病率或进展阻塞性睡眠呼吸暂停患者。几项研究,分析阻塞性睡眠呼吸暂停综合症和癌症死亡率之间的关系有良好的依从性CPAP治疗患者排除4,5]。我们的在体外模型不允许评估阻塞性睡眠呼吸暂停综合症的贡献的其他组件,如同情的语气或睡眠破碎,也似乎有一些先天免疫系统的影响47]。
总之,目前的研究表明,阻塞性睡眠呼吸暂停综合症引发循环单核细胞和NK细胞功能的变化,这可能有利于肿瘤的免疫逃逸。此外,我们的数据提供了新的机制间歇性低氧条件下单核细胞损害NK细胞的成熟和细胞毒性的能力。总的来说,这些发现提供生物合理性最近的流行病学资料表明,阻塞性睡眠呼吸暂停综合症是与癌症发病率增高有关。进一步的研究应该关注我们的发现之间的联系和其他报道阻塞性睡眠呼吸暂停综合症并发症,如心血管疾病、高血压和肥胖48- - - - - -50]。然而,前面提到的OSA-related病态与高水平的TGF-β有关,我们在这项研究中所示。
补充材料
确认
我们感谢献血者服务从拉巴斯大学医院,技术援助极光穆尼奥斯,ServingMed.com编辑稿件。
脚注
可以从本文的补充材料www.qdcxjkg.com
支持声明:这项工作是支持由“皇家研究院祝您健康卡洛斯三世”(ISCiii),”de Investigacion洋底疗养地”(FIS)和菲德尔(PI14/01234和PIE15/00065)大肠Lopez-Collazo和PI13/01512 f . Garcia-Rio。资金信息,本文已沉积的Crossref资助者注册表。
利益冲突:没有宣布。
- 收到了2016年12月15日。
- 接受2017年3月5日。
- 版权©2017人队