摘要
囊性纤维化(CF)的跨膜电导调节(CFTR)门控(增强器)或转运(校正器)的小分子治疗正在以一种突变特异性的方式开发。CFTR-p的药理学校正选项。Phe508del (F508del) are being extensively studied but correction of other trafficking mutants that may also benefit from corrector treatment remains largely unknown.
我们研究了折叠突变体CFTR-p的校正。Phe508del - p。Ala455Glu(A455E) and -p.Asn1303Lys (N1303K) by VX-809 and 18 other correctors (C1–C18) using a functional CFTR assay in human intestinal CF organoids.
CFTR-p的功能。Phe508del和- p。Ala455Gluwas enhanced by a variety of correctors but no residual or corrector-induced activity was associated with CFTR-p.Asn1303Lys. Importantly, VX-809-induced correction was most dominant for CFTR-p.Phe508del, while correction of CFTR-p.Ala455Glu was highest by a subgroup of compounds called bithiazoles (C4, C13, C14 and C17) and C5.
这些数据支持为优化治疗不同CFTR转运突变体而开发的突变特异性校正剂,并确定C5和双噻唑类化合物是校正CFTR-p.Ala455Glu最有希望的化合物。
摘要
CFTR校正器的疗效选择性地取决于折叠和转运突变的类型http://ow.ly/ZrrzB
介绍
细胞功能丧失突变囊性纤维化跨膜电导调节因子(雌性生殖道)基因导致常染色体隐性疾病囊性纤维化(CF)。尽管CF疗法一直针对疾病症状,但针对CFTR蛋白突变特异性缺陷的新疗法正在开发中,如1)校正器修复CFTR顶端转运(例如vx - 809) [1]和2)CFTR电位门控(例如vx - 770) [2].
大多数校正器都是使用CFTR-p从屏幕中识别出来的。Phe508del (F508del), the most common trafficking mutant expressed by ∼90% of all CF subjects [3.].最近,修正器VX-809 (lumacaftor)已被临床批准用于p.Phe508del纯合子受试者联合VX-770 (ivacaftor/Kalydeco) [4,5],首次证明突变特异性校正疗法是可行的。在P.PHE508DEL以前的屏幕中已经识别但未能达到临床阶段的多个校正器被囊性纤维化基础治疗(CFFT)(BEDFAD,MA,美国)分发用于实验目的(称为C1-C18)。6- - - - - -12].尽管目前正在对CFTR-p.Phe508del进行广泛的基于校正剂的治疗方案研究,但已知校正剂对其他转运突变体的疗效仍基本未知,迄今尚未在原代上皮CF细胞中进行研究。
我们最近在人类初级肠道类器官中开发了一种检测方法[13- - - - - -15]研究突变CFTR的残留及药物校正功能[14,16]Forskolin诱导的类有机物肿胀(FIS)以特定于受试者的方式量化CFTR功能,并用于表征VX-809和C1–C18对贩运突变体CFTR-p.Phe508del、-p.Ala455Glu(A455E)或-p.Asn1303Lys(N1303K)的校正。
方法
化合物
VX-809 (Selleck Chemicals LLC, Houston, TX, USA)和C1-C18 (CFFT)被订购为干粉。所有化合物同时制备二甲基亚砜原液(C2为10 mM,所有其他化合物为20 mM),在−80°C下储存,并在储存后6个月内使用。贮存液重新冷冻(−20°C)最多2次或在−20°C下存储,最多1个月。
人类的物质
乌得勒支大学医学中心(乌得勒支,荷兰)和鹿特丹伊拉斯谟医学中心(鹿特丹,荷兰)的伦理委员会批准了这项研究。所有参与研究的受试者均获得知情同意。健康对照组和CF受试者的类器官(雌性生殖道基因型在图1)是在1)标准CF护理期间,2)诊断目的,或3)自愿参与研究期间,通过四次直肠吸引活组织检查得出的肠道电流测量值。
直肠吸引活检的隐窝分离和器官培养
这些方法与前面描述的协议略有不同[14,16]简而言之,将隐窝分离并接种在24孔板中的50%基质凝胶(生长因子减少,无酚;BD Biosciences,Breda,荷兰)中(∼每孔3个10μL matrigel液滴中10-30个隐窝)。生长培养基[16]进一步添加Primocin(稀释1 / 500;InvivoGen,图卢兹,法国)。万古霉素和庆大霉素(均来自西格玛,Zwijndrecht,荷兰)在培养的第一周加入。每2 ~ 3天更新一次培养基,每7 ~ 10天5次传代~ 1次。
FIS的测定
以前描述的forskolin引起的类器官肿胀的测量方法[16]简言之,将7-10天龄培养物中的直肠类CF有机物(第1-30代)接种在平底96孔培养板(美国纽约州罗彻斯特市Nunc)中5分钟 μL 50%基质凝胶,通常含有20-80个类有机物,浸入100%溶液中 μL完整培养基,含或不含3 μM VX-809或C1–C18,浓度如表1所示图2.播种后1天,将类有机物培养30天 3分钟 μM钙黄绿(美国加利福尼亚州卡尔斯巴德市Invitrogen)在完整培养基中。钙黄绿染色后,按图中所示的浓度添加forskolin,并通过共聚焦活细胞显微镜(LSM710(蔡司,奥伯科钦,德国),5×物镜)直接分析类有机物60分钟 最小值(p.Phe508del/p.Phe508del和p.Phe508del/p.Ala455Glu)或120 最小值(p.Phe508del/I级和p.Phe508del/p.Asn1303Lys)。两个(图1和2)还是三个(图3)每种情况下使用一口井。每个人在三到五个不同的时间点重复每个实验。
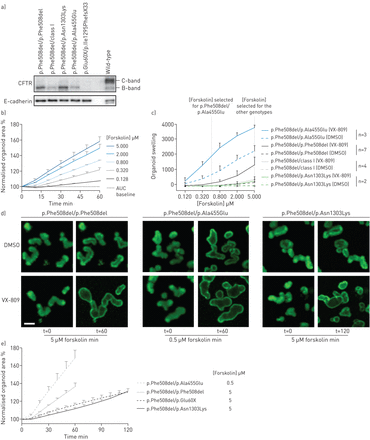
肠类有机物表达的最佳测定条件的确定囊性纤维化跨膜电导调节因子(雌性生殖道)突变。a)Western blot检测不同基因型的类器官中未成熟(B带)和成熟(C带)CFTR雌性生殖道基因型。b)相对于p. phe508del /p的t=0 min(归一化面积),forskolin诱导的表面积增加的时间示踪。不同forskolin浓度下的Ala455Glu类有机物平均值来自两个独立的井。c) forskolin诱导的各种表达的类器官肿胀雌性生殖道VX-809 (3 μM)预处理或未预处理24 h的突变,用(b)所示时间追踪计算的曲线下绝对面积(AUC)表示(基线100%,t=60 min)。I类突变包括p.Glu60X (E60X)、p.Gly542X (G542X)、p.Arg1162X (R1162X)和p.Ser18ArgfsX16 (dele2,3)。n值表示CF被试人数;每个受试者在2到5个独立的培养时间点进行测量。d)在forskolin刺激的指示时间点,VX-809预处理或不预处理24 h后,钙黄绿标记的CF类器官的代表性共聚焦图像。比例尺= 100μm。e)用0.5或5 μM forskolin刺激VX-809 (3 μM)校正的有机类物质并分析60或120分钟的示例时间跟踪,具体取决于雌性生殖道基因型。数据来自两个独立井的平均值。所有数据均以平均值±表示sd.DMSO:二甲基亚砜。
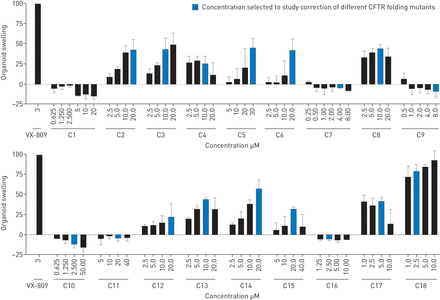
囊性纤维化跨膜电导调节剂(CFTR)的最佳校正浓度定义——p.Phe508del.Forskolin诱导的p.Phe508del纯合类器官肿胀(FIS)预处理24小时 h与VX-809(3 μM)或C1–C18的滴定,表示为根据中所示的时间轨迹计算的曲线下面积图1 b(基线100%,t=60分钟)。对二甲亚砜处理过的有机物的FIS进行了校正,并将其归一化到VX-809条件下。数据平均来自三个独立的重复实验,并以平均值±表示sd.
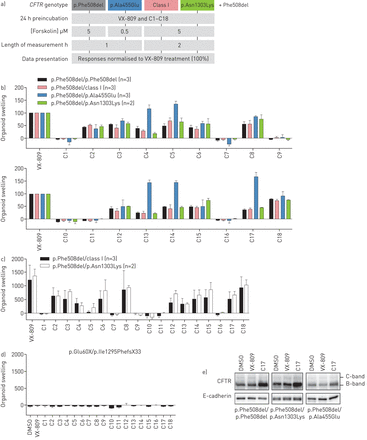
囊性纤维化跨膜电导调节(CFTR)-p的校正。Phe508del - p。Ala455Gluor -p.Asn1303Lys by VX-809 and C1–C18. a) Overview of雌性生殖道genotype-specific试验条件。b, c) forskolin诱导的类器官肿胀(FIS)表达多种雌性生殖道用VX-809 (3 μM)或C1-C18预处理24小时的突变图2.对经二甲基亚砜(DMSO)处理的类有机物的FIS的响应进行校正,并表示为曲线下的标准化(b)或绝对(c)面积,该面积由中所示的时间追踪计算得出图1 b(基线100%,t=60或120分钟)。d)表达两个I类突变的校正刺激类器官的FIS。b-d)无义突变包括p.Glu60X (E60X)、p.Gly542X (G542X)和p.Arg1162X (R1162X)。n值表示CF被试人数;每个受试者在三个重复的两个独立培养时间点进行测量。数据以平均值±表示sde)Western blot检测表达各种蛋白质的类器官中未成熟(B带)和成熟(C带)CFTR雌性生殖道DMSO、VX-809 (3 μM)或C17 (5 μM)处理后突变。结果具有代表性的3 (C17)或4 (DMSO和VX-809)独立实验,每个基因型使用来自两个不同捐赠者的器官(类似于b, c中使用的捐赠者)。
量化的金融中间人
forskolin刺激的类器官肿胀使用Volocity成像软件(Improvision, Coventry, UK)自动量化。总器官面积(xy-平面)相对于t=0的forskolin处理时间的增加,并从每个条件下的两口井中取平均值。在某些情况下,根据标准操作程序中详细描述的标准,人工排除细胞碎片和不可存活的结构。使用Prism (GraphPad, La Jolla, CA, USA)计算曲线下面积(AUC) (t=60或120 min,基线100%)。
蛋白质印迹分析
未经处理或用VX-809或C17处理的类器官在含有完全蛋白酶抑制剂片的Laemmli缓冲液中裂解(罗氏,阿尔米尔,荷兰)。裂解物通过SDS-PAGE分析,电泳转移到聚偏二氟乙烯膜(Millipore, Billerica, MA, USA)。在Tris缓冲盐水吐温(0.3%吐温,10 mM Tris (pH 8)和150 mM氯化钠)中,用5%牛奶蛋白阻断膜,并在室温下用小鼠单克隆e -钙粘蛋白特异性(1 / 10 000稀释;BD Biosciences)或cftr特异性抗体(囊性纤维化折叠联盟450、570和596;1 / 3000稀释;),然后与辣根过氧化物酶结合的二抗孵育,增强化学发光发展。
结果
确定表达不同氨基酸的肠道类器官的最佳测定条件雌性生殖道突变
确定表达不同蛋白质的类有机物的最佳分析条件雌性生殖道在5种不同的含或不含VX-809 (图1).我们首先确认了CFTR-p的折叠和贩运缺陷。Phe508del - p。Ala455Glu和-p.Asn1303Lys by Western blot analysis, which indicated highly reduced levels of complex-glycosylated CFTR (C-band) compared to wild-type CFTR organoids (图1一个).在表达两个I类突变的器官中未检测到CFTR表达,证实了CFTR的特异性(图1一个).如前所述[16],类器官肿胀以绝对值AUC表示,绝对值AUC由相对于t=0 min (图1 bc).基底和vx -809诱导的肿胀与p. phe508del /p有剂量依赖性,p. phe508del /p最高。Ala455Glu瀑样(图1 c).FIS p.Phe508del / p。Asn1303Lys和p.Phe508del/ I类器官相似,提示仅局限于无功能与p.Asn1303Lys相关。基于图1 c,我们选择了0.5 μM forskolin用于p.Phe508del/p.Ala455Glu和5 μM forskolin用于其他基因型研究C1–C18的校正效应。值得注意的是,p.Phe508del/p.Ala455Glu类有机物的FIS在0.5 μM forskolin主要由CFTR-p。Ala455Glu等位基因,因为在该forskolin剂量下,p.Phe508del/I类有机物的反应接近背景水平(图1 c).p.Phe508del和p.Asn1303Lys的类有机化合物杂合子或I类突变的FIS分析时间为120分钟,而不是60分钟,以增加检测灵敏度(图1 de)。总之,这里定义的检测条件显示了评估具有明显CFTR折叠突变的类器官校正修复FIS的最佳条件。
使用CFTR-p.Phe508del纯合类有机物确定最佳校正剂浓度
然后测量p.Phe508del/p的FIS。Phe508del organoids that were treated with VX-809 or different concentrations of C1-C18 to identify optimal compound dosages (图2).C1–C18的测试剂量基于文献中CFFT化合物顺序中描述的化合物效价数据。与未校正类有机物的FIS相比,我们观察到大多数化合物的FIS随剂量增加而增加,但C1、C7、C9、C10、C11和C16的FIS相似或减少,表明缺乏功能性CFTR-p.Phe508del由这些化合物修复(图2)。FIS降低可能表明化合物毒性。根据以下结果,每种化合物选择一个浓度进行进一步分析:图2对于与校正相关的化合物,或关于非功能校正的文献(图2).总之,我们识别了功能性和非功能性CFTR-p。Phe508del correctors, and selected optimal C1–C18 concentrations for efficacy testing using organoids with distinct trafficking mutants.
VX-809和C1-C18对CFTR-p.Phe508del、-p.Ala455Glu和-p.Asn1303Lys的修正
为了研究突变特异性CFTR修复的校正器,p.Phe508del纯合或p.Phe508del复合杂合的来自供体的类器官的FIS和无义突变,p.Ala455Glu或p.Asn1303Lys使用定义的检测条件进行评估图1和2(图3一).数据归一化为VX-809进行校正雌性生殖道突变依赖性分析差异(图3 b)通过这种方式,可以识别选择性作用于特定突变的化合物图2,除C1、C7、C9、C10、C11和C16外,所有化合物均为所有培养物校正FIS。p. phe508del /p.的相对校正模式。I类和p。Asn1303Lys类有机物具有可比性(图3 b),以及p. phe508del /class I和p. phe508del /p.的绝对校正模式。Asn1303Lys瀑样(图3 c)有趣的是,对于p.Phe508del/p.Ala455Glu类有机物而言,C4、C5、C13、C14和C17显著增加了FIS,达到了对VX-809反应的120–170%(100%),而VX-809是其他基因型最主要的校正剂(图3 b)在这些p.Ala455Glu特异性化合物中,C5含有苯基喹啉基团,C4、C13、C14和C17具有双噻唑化学结构(www.ebi.ac.uk chembl /).在表达两个I类突变的类器官中没有肿胀,表明校正剂诱导的FIS完全依赖于cftr (图3 d)Western blot研究表明,C17而不是VX-809增加了所有突变体的未成熟CFTR(B带)水平(图3 e).有无校正剂治疗,成熟CFTR-p表达。Phe508del或CFTR-p。Ala455Glu(C-band) was near background levels and difficult to evaluate. However, data suggested that VX-809 and C17 increased CFTR-p.Asn1303Lys C-band (图3 e)这与这些校正器缺乏功能性CFTR-p.Asn1303Lys修复形成对比(图3 bc).总之,这些数据表明,不同的贩运突变的最佳校正需要不同的化学校正器。
讨论
我们首次评估了原代细胞中多个CFTR贩运突变体的校正,方法是使用19种化学校正器对直肠类器官中的FIS检测进行评估[16,17].由于不同贩运突变体的剩余功能不同(图1 c和e),对分析条件进行了调整,以实现对各种突变体校正的最佳检测(图3一).含有p.a ala455 glu的类器官具有相当大的残留功能,因此减少forskolin的剂量,使校正剂疗效的最佳检测成为可能。相反,对于p. phe508del /class I和p. phe508del /p. class。Asn1303Lys, FIS测量时间从60分钟延长到120分钟,以增加检测灵敏度。将校正修复后的数据集归一化到VX-809,可以比较四种不同的基因型,并精确定位针对CFTR-p的功能校正。Ala455Glu或p。Asn1303Lys (图3 b).
该方法提示了CFTR-p的修复。Ala455Gluwas highest by a subgroup of four correctors sharing a bithiazole group and by C5, containing a phenylquinoline group (图3 b).最近的数据已经表明,校正器介导了CFTR-p.Ala455Glu功能的修复(未发表的观察)和表达[18]是可行的,但某些校正器对CFTR-p的偏好。Ala455Glu与CFTR-p相比。Phe508del has never been shown. These findings suggest that CFTR-p.Ala455Glu and CFTR-p. Phe508del contain distinct folding defects. Recent observations indicated that the bithiazole C4 acts as a class II corrector, targeting the nucleotide-binding domain (NBD)2–membrane-spanning domain (MSD)1 interface, which repairs CFTR-p.Phe508del expression and function synergistically when combined with class I correctors (VX-809) that target the NBD1–MSD2 interface [19].CFTR-p中特定的折叠缺陷和校正靶域。Ala455Glu需要进一步定义。
亲属之间的相似性(图3 b)和绝对(图3 c) p.Phe508del/p。Asn1303Lys p.Phe508del / p。Phe508del and p.Phe508del/class I organoids indicate that FIS of p.Phe508del/p.Asn1303Lys cultures most likely depends on CFTR-p.Phe508del, and that function of CFTR-p.Asn1303Lys is not restored by any C1–C18 corrector. These data support other findings demonstrating that CFTR-p.Asn1303Lys could not be functionally repaired by VX-809 or VX-770 in human intestinal organoids (unpublished observations), Fischer rat thyroid cells [20.]及人类原发肺细胞[21].与细胞系中异位CFTR表达研究一致[22], b波段升高,c波段降低。Asn1303Lys与野生型(图1一个).相比之下,CFTR-p缺乏功能性。Asn1303Lys修复,该突变体的蛋白表达水平可通过校正器部分恢复[21) (图3 e).加工校正与功能校正的不一致性提示CFTR-p的折叠缺陷。Asn1303Lys完全阻断其在顶膜上的功能,即使化学校正器或复合糖基化CFTR-p部分恢复了运输。Asn1303Lys (C-band)异常地靶向于细胞间隔而不是顶端膜。显然,需要开发新的治疗策略来修复CFTR-p的特定缺陷。阻止其功能的lys。
综上所述,我们研究了VX-809和C1-C18对不同转运突变体的原发肠道CF类器官的功能性修复,并观察了CFTR-p的修正。Phe508del和- p。Ala455Gluby 13 out of 19 compounds, while none of these compounds restored function of CFTR- p.Asn1303Lys. Most importantly, C5 and a subgroup of compounds that share a bithiazole chemical structure achieved highest repair of CFTR-p.Ala455Glu, while correction of CFTR-p.Phe508del was dominated by VX-809. These data indicate, for the first time in primary human CF cells, that the CFTR corrector efficacy selectively depends on the type of folding and trafficking defect, and support the development of mutation-specific corrector strategies that are optimal for distinct CFTR mutants.
致谢
我们感谢S.Heida Michel、M.Geerdink、M.C.J.Olling de Kok(荷兰乌得勒支大学医学中心威廉敏纳儿童医院所有儿科肺脏科)、E.M.Nieuwhof Stoppelenburg和E.C.van der Wiel(荷兰鹿特丹伊拉斯谟大学医学中心/索菲亚儿童医院儿科肺脏学系)提供肠道活检;R.J.Bridges(美国伊利诺伊州芝加哥罗莎琳德·富兰克林医学和科学大学生理学和生物物理学系)和CFFT提供C1-C18化合物;以及J.Riordan(美国北卡罗来纳州教堂山北卡罗来纳大学生物化学和生物物理学系)和CFFT提供CFTR单克隆抗体。
脚注
支持声明:这项工作得到了荷兰囊性纤维化基金会(NCFS)、威廉敏娜儿童医院(WKZ)基金会和荷兰卫生组织ZonMw的赠款的支持,赠款是hiti - cf方案的一部分。本文的资金信息已存入基金参考.
利益冲突:披露内容可与本文的在线版本一起在www.qdcxjkg.com
- 收到了2015年7月22日。
- 接受2016年3月7日。
- 版权©2016人队