摘要
在哮喘患者中,磁共振成像(MRI)和肺清除率指数(LCI)显示了持续通气的异质性,尽管其与哮喘控制的关系尚不清楚。因此,我们的目的是探讨MRI通气缺陷和LCI与严重、控制不良哮喘患者哮喘控制和生活质量的关系。
18例严重、控制不良哮喘患者(平均±sd46±12岁,6男/12女)向伦理委员会批准的方案提供了书面知情同意,并接受了肺活量测定、LCI和3.他在单次2小时的访问中进行了MRI。采用哮喘控制问卷(Asthma control Questionnaire, ACQ)和哮喘生活质量问卷(Asthma quality life Questionnaire, AQLQ)评估哮喘控制和生活质量。采用LCI和3.MRI通气缺陷率(VDP)。
所有参与者报告疾病控制不良(平均±sdACQ评分=2.3±0.9)和高度不均匀通气(平均±0.9)sdVDP=12±11%,LCI=10.5±3.0)。虽然VDP和LCI呈强相关(r=0.86, p<0.0001),但在包括1 s用力呼气量、VDP和LCI的多变量模型中,VDP是哮喘控制的唯一独立预测因子(r= 0.0001)2= 0.38, p = 0.01)。ACQ评分为bb0.2 (p=0.04)和AQLQ评分<5 (p=0.04)的哮喘患者的VDP明显加重,但LCI无明显变化;过去6个月内发作≥1次的哮喘患者的VDP有加重趋势(p=0.053),但LCI无明显变化。
在控制不良的严重哮喘患者中,ACQ和AQLQ较差的患者MRI通气而非LCI明显较差。
摘要
MRI通气缺陷,而非LCI,在哮喘控制和哮喘相关生活质量较差的患者中更严重http://ow.ly/4n9uip
介绍
哮喘治疗的主要目标是实现和维持疾病控制。不幸的是,约50%的哮喘患者控制不佳,其中高达10%的患者出现危及生命的恶化[1]。控制不良的哮喘的临床和病理生理结果是不同的,这使得治疗决策很复杂。先前的研究表明哮喘控制不佳可能与通气异质性有关[2,3.]。虽然导致通气异质性的病理生理异常尚不清楚,但这些异常可能包括腔内炎症、粘液、白蛋白和纤维蛋白、气道壁增厚、平滑肌增生/肥大和粘膜细胞化生。使用肺清除率指数(LCI)测量通气异质性在65年前首次被描述[4],并被作为一种衡量阻塞性肺病的标准。与健康对照组相比,哮喘患者的通气异质性升高[5- - - - - -7],是气道高反应性的独立决定因素[8],随着支气管扩张而改善[5,9]和吸入皮质类固醇[3.,10],并在恶化过程中恶化[11]。
通气不均匀性可以通过肺部成像方法进行区域识别和可视化[12,13]包括吸入气体核磁共振成像(MRI) [14]。在哮喘患者中,MRI通气缺陷在时间和空间上持续存在[15],支气管收缩时加重,支气管扩张后改善[16]。MRI通气缺陷在肺功能较差、气道炎症、高反应性和气道壁厚较差的老年哮喘患者中数量和大小也较大[17]。
然而,到目前为止,通气缺陷与哮喘控制和生活质量之间的关系尚未确定。超极化惰性气体MRI在评估严重哮喘患者的外周气道方面可能有特殊的应用,因为它提供了临床可用测量无法提供的区域信息。因此,本研究的目的是确定MRI和LCI测量通气异质性与哮喘控制、生活质量和恶化的关系。我们假设MRI通气缺陷和LCI与严重哮喘患者的哮喘控制和生活质量有关,这很重要,因为目前很少有哮喘控制的中间终点可用于指导治疗。
材料与方法
研究参与者和设计
参与者对当地研究伦理委员会批准的方案提供书面知情同意,该方案也已注册(西安大略大学健康科学研究伦理委员会,加拿大伦敦,批准号104200;clinicaltrials.gov标识符号码NCT02263794).根据全球哮喘倡议(GINA)治疗步骤标准,年龄在18至70岁之间诊断为严重哮喘的患者[18],并在一名呼吸科医生的护理下从两个学术三级护理中心(加拿大安大略省汉密尔顿市麦克马斯特大学费尔斯通呼吸健康研究所和加拿大安大略省伦敦市西安大略大学罗伯特研究所)招募。
在单次2小时的访问中,所有参与者都进行了支气管扩张剂前后肺活量测定、LCI和MRI。采用哮喘控制问卷(Asthma control Questionnaire, ACQ)评估哮喘控制和生活质量;七项版本)[19]及标准化哮喘生活质素问卷(AQLQ(S)) [20.),分别。记录Borg评分和修改后的医学研究委员会呼吸困难评分。严重哮喘发作、急诊就诊和因呼吸道症状住院的临床病史均为自述。如前所述[21],严重哮喘加重是指症状恶化,需要口服或静脉注射皮质类固醇治疗,或吸入皮质类固醇(ICS)剂量加倍≥3天,或服用维持性皮质类固醇(OCS)的受试者暂时增加口服皮质类固醇(OCS)剂量。在研究访视前6个月内进行甲胆碱刺激,以确定刺激浓度导致1 s内用力呼气量(FEV)下降≥20%1).
肺活量测定,支气管刺激和LCI
肺活量测定按照美国胸科学会/欧洲呼吸学会指南进行[188bet官网地址22]使用MedGraphics Elite系列容积描记仪(MedGraphics, St. Paul, MN, USA)。对于使用支气管扩张剂后的测量,使用AeroChamber Plus间隔器(Trudell Medical International;伦敦,安大略省,加拿大)。所有参与者被指示在访问前12小时(过夜)保留短效β激动剂。
LCI测量使用100%氧气进行氮气冲洗,并使用配备超声流量和摩尔质量传感器的ndd EasyOne Pro LAB系统(ndd Medical Technologies, Zurich, Switzerland)。当志愿者坐直时,冲洗阶段开始于呼气结束时从室内空气切换到100%氧气。100%氧气潮汐呼吸,直到过期氮浓度<试验开始时浓度的2.5%。功能剩余容量(FRC)由过期氮的累积体积除以冲洗开始和结束时潮末浓度之差计算。累积过期气量(CEV)是冲洗过程中累积的过期气量。如前所述,LCI为氮浓度<试验开始时浓度的2.5%时所需的FRC肺周转量(以CEV除以FRC产生)[23]。重复进行多次呼吸冲洗,LCI报告为两次操作的平均值。
图像采集
解剖质子(1H)和超极化3.如前所述,使用3T MRI系统(General Electric Healthcare, Milwaukee, WI, USA)在5分钟内获得通气磁共振图像[24]。受试者被指示吸入1.0 L气体(100% N2为1H MRI和a3.他/ N2混合物的3.在屏息条件下获取FRC的He MRI图像和冠状面图像。3.气体被极化到40% (Polarean;HeliSpin, Durham, NC, USA),用氮气稀释至每公斤体重5毫升。
使用64层光速VCT系统(General Electric Healthcare, Milwaukee, WI, USA)获得胸部计算机断层扫描(CT)体积,受试者在从FRC吸入1.0 L氮气后保持呼吸,如前所述[25]。使用制造商设置和ImPACT CT患者剂量计计算器(基于英国健康保护局NRPB-SR250软件),总有效剂量为1.8 mSv。
图像分析
定量MRI评估由一名训练有素的观察者(具有5年经验)使用半自动分割软件进行,如前所述[24]。3.MRI通气缺损百分率(VDP)为通气缺损体积归一化后的胸腔容积[24]。使用Pulmonary Workstation 2.0 (VIDA Diagnostics Inc., Coralville, IA, USA)对胸部CT图像进行分析,生成三维气道树。为了确认通风缺陷与相应气道之间的空间关系,使用3D切片软件(www.slicer.org).
统计方法
使用Shapiro-Wilk正态性检验对数据进行正态性检验,当数据不正态时,进行非参数检验。采用线性回归(r2), Pearson相关性(r),当数据不正常时,Spearman相关性(ρ)。为了确定VDP是否是过去12个月内ACQ、AQLQ和病情恶化的独立预测因子,使用逐步方法和SPSS 20.0软件(IBM, Armonk, NY, USA)生成多元回归模型。为了确定VDP是否是过去6个月恶化的独立预测因子,使用SAS 9.4软件(SAS Institute, Cary, NC, USA)中的PROC COUNTREG程序生成多变量零膨胀泊松回归模型。采用非配对t检验和Mann-Whitney检验比较按ACQ(≤2或>2)、AQLQ评分(≥5或<5)和既往6个月加重史(<1或≥1次加重)分层的受试者的通气异质性。当发生I型错误的概率<5% (p<0.05)时,所有结果均认为具有统计学意义。
结果
参与者的特征
表1提供18名参与者的摘要(每个三级学术医疗中心9名,6名男性/12名女性,平均±sd(46±12年)重度哮喘;每位参加者的资料载于表S1。均值±sd哮喘病程31±15年(范围7 ~ 57年),支气管扩张剂前平均±15年sdFEV1预测68±24%(范围33-103% pred),平均±sdFEV1/用力肺活量为65±15%(范围35 ~ 88%)。
哮喘药物和控制参数总结于表2;表S2中也提供了这些数据的清单。尽管接受了中至高剂量ICS和长效β激动剂(GINA治疗步骤4-5)[18],所有18名参与者的ACQ评分(平均±sd2.3±0.9,范围1.0-4.3)。其中,8名参与者(44%)对强的松依赖(剂量范围为2.5 - 50mg·天)−1).在过去的6个月和12个月中,分别有9名(50%)和15名(83%)参与者报告了一次或多次严重哮喘恶化。
通气异质性与哮喘控制
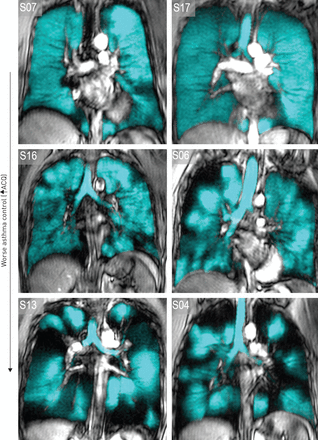
支气管扩张剂前测量用于评估通气异质性与哮喘控制之间的关系,而支气管扩张剂后通气异质性测量在补充资料中提供(图S2和S3)。3.他的MRI通气图像共配到相应的16名代表性参与者的解剖MRI显示,有较多的数量和体积3.ACQ评分较差患者的He MRI通气异常(图1).如图所示表1,所有参与者的平均VDP为12±11%(范围= 1-35%),平均LCI为10.5±3.0(范围= 6.3-17.5)。个体参与者的数据显示,13名参与者的VDP和LCI异常,5名哮喘患者的VDP和LCI正常或VDP正常和LCI异常(表S1)。
Hyperpolarised3.有代表性的重症哮喘患者的核磁共振成像(MRI)。中央冠状切片3.蓝色的核磁共振通气与解剖一致16例有代表性的重度哮喘患者的H MRI灰阶。S07: 55岁女性,用力呼气量1 s (FEV)1)=77%,哮喘控制问卷(ACQ)=1.4,肺清除率(LCI)=9.7,通气缺陷率(VDP)=2%;S17: 39岁,女性,FEV1=66% pred, ACQ=1.7, LCI=6.7, VDP=3%;S16: 48岁,男性,FEV1=78% pred, ACQ=2.3, LCI=8.6, VDP=8%;S06: 45岁男性,FEV1=34% pred, ACQ=2.7, LCI=11.5, VDP=14%;56岁,男性,FEV1pred =34%, ACQ=3.1, LCI=17.5, VDP=33%;S04: 60岁女性,FEV1=47%, ACQ=4.3, LCI=14.0, VDP=35%。
我们通过三种方式评估VDP与ACQ和AQLQ评分及既往加重的关系。首先,我们根据ACQ评分(ACQ≤2,n=7和ACQ bbb2, n=9)、AQLQ评分(AQLQ≥5,n=7和AQLQ<5, n=9)和过去6个月内自我报告的加重次数(<1次加重,n=9和≥1次加重,n=9)对患者进行分层(图S1)。VDP明显降低(18±13%)与6±5%;p=0.04), LCI为11.2±3.6与9.4±2.4;p=0.3),在ACQ评分为>.2的哮喘患者亚组中。VDP也显著降低(18±13%)与6±5%;p=0.04), LCI为11.4±3.3与9.1±2.6;p=0.2),在AQLQ评分<5的哮喘患者亚组中。VDP有恶化趋势(17±13%)与8±5%;p=0.053), LCI为11.2±3.8与9.7±1.8;P =0.30),在过去6个月内报告≥1次发作的哮喘患者中。支气管扩张剂后也有类似的结果(图S2)。第二,如图2我们还评估了VDP与LCI和ACQ评分的线性关系。图2VDP与LCI (r= - 0.86, p<0.0001)和ACQ评分(r=0.62, p<0.01)相关,LCI与ACQ评分有相关性(r= - 0.49, p=0.052)。类似的结果也显示在图S3中支气管扩张剂后的数据。最后,为了确定VDP与哮喘控制的独立关系,我们采用逐步方法,以ACQ评分为因变量,以VDP、LCI和FEV为变量,研究了一个多变量模型1作为自变量(表3).VDP是回归方程中唯一能显著影响ACQ评分的变量(β=0.62, p=0.01)。LCI和FEV1在分析的第二步中没有进入方程。AQLQ和急性加重(6个月和12个月)的多变量分析也无显著性。
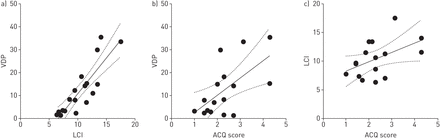
通气异质性与哮喘控制的关系。a)通气缺陷率(VDP)与肺清除率(LCI)显著相关(r=0.86, p<0.0001)。b) VDP与哮喘控制问卷(Asthma Control Questionnaire, ACQ)显著相关(r=0.62, p=0.01)。c) LCI-ACQ有相关性(r=0.49, p=0.052)。虚线表示95%置信区间。
讨论
我们试图回答这个问题:通风异质性与哮喘控制有关吗?为此,我们评估了18例重度哮喘患者的MRI通气缺陷和LCI。我们发现:1)VDP与LCI呈强相关;2) ACQ评分为bb0.2和AQLQ评分<5的哮喘患者VDP明显加重,但LCI不明显;3)包含FEV的多元模型1VDP是哮喘控制的唯一独立预测因子。
基于先前的结果,我们假设MRI通气缺陷可能与哮喘控制有关。这一观点得到了加强,因为之前的多次呼吸冲洗研究表明,哮喘控制不佳与通气异质性增加有关[2,3.]。值得注意的是,我们不认为LCI可以与通风缺陷的静态吸入MRI测量直接相关,因为这些操作可能测量不同但相关的特征。考虑到测量本身的机制差异,我们惊讶地发现VDP和LCI之间存在如此强的相关性。在严重哮喘中常见的气道狭窄或气体捕获的情况下,预计肺部填充和排空的时间常数很长。因此,考虑两种方法相对于肺段填充和排空的时间常数的时间分辨率是很重要的。例如,惰性气体冲刷测量是在数分钟的正常潮汐呼吸的时间过程中进行的。相比之下,MRI通气缺陷通常是在单次8-10秒的吸气屏气期间测量的,提供了在该时间段内吸入气体去向的视觉快照。因此,LCI异质性与较长的肺排空时间常数有关,而我们测量的MRI通气异质性反映了肺充盈延迟。值得注意的是,以前开发的区域分段通风图[26)探针3.他冲洗了~ 5次呼吸(<0.5 min)。该方法的时间分辨率由H内在的et al。(26]可以更好地反映在数分钟正常潮汐呼吸的时间过程中进行的LCI测量。除了时间分辨率的差异外,这些方法的表观空间分辨率也可能存在差异。原则上,LCI测量可能受到任何或所有传导区和腺泡区影响[27]。对于通风MRI,有一些粗糙的空间分辨率(3×3×15 mm),这可能导致对非常小的通风缺陷的低估。为了支持这一观点,受试者S07和S14报告了相对较好的疾病控制(ACQ=1.4和1.0),但LCI异常和MRI通气相对均匀(表S1)。另一个,先前提出的[27],解释表明,即使是很小的通气缺陷也可能使LCI增加远远超过正常上限,从而导致对疾病严重程度的高估。支持这一观点的是,受试者S07的LCI异常(9.7),MRI仅观察到一个小的低通气区(VDP=2%)。重要的是,这名55岁的女性服用口服强的松(7.5 mg·天)−1)和ICS(布地奈德>1000µg),控制相对较好(ACQ=1.4)。在比较VDP和LCI测量时还应考虑体位影响,因为MRI是仰卧位进行的,而LCI测量是直立获得的。在先前的一项儿童研究中,仰卧位哮喘患者的气体捕获量增加,但氮冲洗法得出的通气异质性测量结果并非如此[28]。无论如何,为了减轻潜在的姿势影响,包括肺不张,成像在5分钟内完成,这有效地减少了这些影响[29]。最后,气体物理性质的差异肯定会影响气道内的流动阻力。根据先前公布的估计,N2和3.他/ N2混合物为1.101 kg·m−30.609 kg·m−3的估计黏度2和3.他/ N2混合物是1.984×10−4姿态和1.993×10−4分别[30.]。将这些估计与空气的估计进行比较,空气的密度和粘度为1.140 kg·m−3和2.064×10−4分别表明,N2可能比空气更接近空气3.他/ N2混合物。
本研究最重要的观察结果是VDP是哮喘控制的唯一独立预测因子。ACQ评分为bbbb2和AQLQ评分<5的哮喘患者的VDP明显加重,且哮喘发作次数越频繁,VDP有加重的趋势,也支持了这一发现。使用LCI测量没有观察到这一点,可能是因为样本量小和/或LCI本身对决定哮喘控制的潜在病理生理不太敏感。我们使用MRI的结果与先前使用单光子发射计算机断层扫描(SPECT)进行的通气成像研究相矛盾,该研究报告了ACQ评分与通气之间没有关系[12]。SPECT阴性结果可能源于SPECT固有的低空间分辨率或小样本量,或者可能是因为哮喘患者的控制相对较好。
我们关于通气缺陷与哮喘控制相关的主要发现是新颖的,并引导我们推测这种关系背后的可能机制。我们认为通气缺陷可能影响哮喘控制和症状,因为这些缺陷直接反映了对类固醇不敏感的高反应气道。此外,这些患者的通气缺陷与LCI密切相关的事实也表明,困气、缓慢填充和缓慢排空区域都是这些患者的关键特征。值得注意的是,在本研究的哮喘患者中,支气管扩张剂可逆性的大小与基线VDP密切相关(r= - 0.77, p=0.0002)。不幸的是,没有足够的患者有资格接受甲胆碱刺激来研究基线VDP和高反应性之间的关系。
在全球范围内,控制不良和对皮质类固醇不敏感的哮喘患者带来了相当大的管理负担和复杂性,以及巨大的医疗负担[31]。不幸的是,这些患者的临床、生理或病理资料有限。在这里,我们观察到通气缺陷和支气管扩张反应持续存在,哮喘在一小群严重哮喘患者中没有得到充分控制,尽管接受了大剂量的ICS和/或OCS。已经提出了哮喘中皮质类固醇不敏感的几种可能机制[32],但类固醇不敏感与通气缺陷之间的关系尚待探讨。在目前的评估中,尽管接受了中至高剂量ICS和长效β2激动剂治疗,所有18名参与者的疾病控制不佳,提示治疗耐药。其中,8名参与者(44%)对强的松依赖(剂量范围为2.5 - 50mg·天)−1).强的松依赖性哮喘患者和非强的松依赖性哮喘患者的支气管扩张剂前VDP无差异(p=0.15,数据未显示)。然而,强的松依赖患者使用支气管扩张剂后VDP的改善明显更大(p=0.02,数据未显示)。此外,正如预期的那样,支气管扩张剂后VDP的变化与支气管扩张剂前VDP相关(r= - 0.77, p=0.0002),因此VDP较差的患者改善最多。综上所述,这些数据使我们假设,在大多数哮喘患者中,VDP是一种严重程度和区域性气道疾病的衡量标准,但在控制非常差的哮喘患者中,VDP区域性识别严重狭窄的气道,这些气道反应过度,极易关闭和塌陷。这种反应会导致伴随哮喘控制不良的难以忍受的症状。这也提示,在临床上,通气缺陷的严重程度和区域位置可用于指导治疗和患者管理决策,并可能改善哮喘控制。
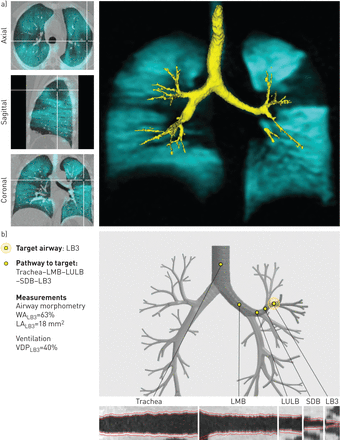
我们认为,旨在减少通气缺陷的治疗可能用于改善对严重哮喘的控制。为了强调这一点,MRI通风缺陷和气道之间的空间关系的一个例子显示在图3对于一名具有代表性的哮喘患者(S14),所有可用的药物治疗都不能优化控制(表S2)。图3一显示局灶性左上叶通气缺陷及其与左上叶前段的空间关系。没有右上肺叶或下肺叶通气异常的证据。在图3 b,一个用于临床使用的图形用户界面,识别由LB3节段支气管提供的左上叶前段,以及LB3形态测量和节段VDP的定量测量,作为区域指导和测量治疗反应的一种方法。
使用磁共振成像(MRI)识别一个典型的严重哮喘患者的潜在治疗靶点(S14)。a)共同登记3.He MRI通气(蓝色显示)和计算机断层扫描(灰色显示),气道渲染(黄色显示)。轴位、矢状位和冠状位显示左上肺叶前段局灶性通气缺陷。b)图形化用户界面显示左上肺叶通气缺损与LB3段支气管的空间关系以及通往潜在治疗靶点的支气管内通路;此外,还提供了该患者LB3段支气管的定量气道形态测量和段性通气缺陷百分比(VDP)。LMB:左主支气管;LULB:左支气管上叶;SDB:上分支气管;LB3:左支气管3条;WA:墙面积;LA:管腔区域。
我们认识到我们的研究有一些局限性,包括研究参与者的数量较少。虽然样本量很小,但我们注意到MRI通气测量对气道和炎症异常高度敏感,因此可以使用小样本量检测到显着差异。重要的是要指出临床翻译3.他核磁共振不太可能,更直接的临床影响将来自129目前正在全球范围内接受监管机构批准的MRI方法。我们还承认,哮喘患者是从两个主要的三级保健中心招募的,因此大多数患者无法获得呼出的一氧化氮分数和痰炎测量。如果这些是可用的,我们可以尝试梳理出管腔炎症对通气异质性和哮喘控制的相对贡献。此外,由于后勤原因,我们没有评估控制良好的哮喘患者或病情较轻的哮喘患者的比较组,尽管在先前对控制良好的哮喘患者的研究中,确定了通气缺陷与哮喘严重程度之间的关系[17]。
有强有力的证据表明,哮喘控制不佳与严重哮喘事件的风险增加有关[33]。目前,气道炎症是哮喘控制/恶化的中间终点[34- - - - - -36],气流阻塞也一样[37],呼吸系统电抗[38],以及在较小程度上,通风不均匀性[2,3.]。在一组相对较小的严重哮喘患者中,我们观察到VDP是哮喘控制的独立预测指标,这使我们推测通风缺陷也可能作为哮喘控制的中间终点。通气缺陷驱动症状和哮喘恶化的假说仍需要严格检验,旨在减少通气缺陷的哮喘治疗显著改善哮喘控制的假说也需要严格检验。然而,根据目前对严重的、未控制的哮喘患者的研究,我们认为通气缺陷是“煤矿中的金丝雀”,反映了气道已经变窄和高反应,区域性地识别出易发生支气管痉挛的肺区域,揭示了这些患者的症状来源和急性恶化。
致谢
我们感谢M. Kjarsgaard(加拿大汉密尔顿麦克马斯特大学凡士通呼吸健康研究所)的临床协调和临床数据库管理,H. Lim(加拿大汉密尔顿麦克马斯特大学凡士通呼吸健康研究所)对患者的识别和特征描述,A. Wheatley(加拿大伦敦西安大略大学罗巴茨研究所)的生产和配药3.他和D. Reese(加拿大伦敦西安大略大学罗伯茨研究所)对研究志愿者进行了核磁共振成像。
脚注
社论评论:Eur呼吸器2016;48: 294 - 296。
本文的补充资料来自www.qdcxjkg.com
临床试验:本研究注册于clinicaltrials.gov带标识号NCT02263794.
支持声明:本研究的开展,在一定程度上要感谢加拿大研究主席项目对P. Nair(加拿大炎症学研究主席)的支持,加拿大卫生研究院(CIHR)新研究者奖对G. Parraga的支持和加拿大呼吸研究网络对S. Svenningsen的支持。CIHR运营基金(MOP 201309)和加拿大肺脏协会的试点研究资助也得到了感谢。本文的资金信息已存入FundRef.
利益冲突:没有声明。
- 收到了2016年2月22日。
- 接受2016年4月13日。
- 版权所有©ERS 2016