抽象的
描述了一项针对轻度哮喘的新型ICS/快速起病LABA缓解疗法的现实研究http:///wly/we3yp.
到编辑:
本文介绍了新型启动(Symbicort Turbuhaler哮喘缓解疗法)的基本原理和设计,随机对照试验吸入皮质类固醇(ICS)/快速发作的长效β-激动剂(Laba)缓解治疗中的缓和哮喘。
哮喘临床研究和管理的主要重点是中度或严重哮喘的患者。几乎没有关注与哮喘的“沉默的大多数”支付,哮喘经历所谓的间歇性和轻度持久性哮喘。这些患者通常仅吸入短作用β-激动剂(SABA)治疗,以提供症状浮雕。然而,虽然单独使用SABA治疗确实提供症状浮雕,但是只有稳健的证据,支持单独用SABA治疗轻度哮喘的长期疗效和安全性,或指导临床医生和患者常规低剂量ICS治疗。此外,医生和患者发现,当症状不常见时,难以认识到ICS治疗的需要,并且在这种情况下遵守ICS是常见的。这导致对常规ICS处方的替代方案进行考虑,用于间歇性或轻度哮喘。
包含ICS和快速缺口Laba的组合吸入器,其单独使用,其仅作为释放治疗,单独优于SABA释放治疗,并且可能是常规IC的替代性,具有间歇性或轻度哮喘患者的SABA缓解疗法[1-4.]。组合IC / FAST-ONSET Laba Reliever疗法允许根据症状滴定ICS治疗。这可能会增加患者过度依赖于其SABA的患者,否则遵守维护ICS治疗的患者,并且实际上可能代表什么患者,规定的常规组合IC / FAST-BAXA治疗,采取“现实世界”[5.那6.]。
新型开始试验将研究ICS / FAST-ONSET LABA作为间歇性或轻度持久性哮喘患者唯一的缓解疗法的疗效和安全性。研究假设是IC / FAST-PANSET Laba Reliever疗法比SABA Relifever治疗和维护IC和SABA Reliever疗法更有效,所述成年患者间歇性或轻度哮喘。主要目的是比较ICS / FAST-BANSET LABA释放治疗与另外两种治疗策略的功效:SABA缓解治疗和维护IC与SABA救济疗法相结合。参与者将是仅使用SABA单药治疗和没有其他哮喘药物的成年患者。次要目标是比较每个方案的安全性,检查吸入器与随机方案的吸入器模式,并探索基线临床特征是否如T-Herper细胞(Th)2轮廓预测对随机处理的优先响应。
该研究设计为52周、开放标签、平行组、多中心、III期、随机对照试验(RCT),将在新西兰、英国、意大利和澳大利亚进行。实验治疗将采用布地奈德福莫特罗富马酸二水合物(信必可都保;阿斯利康,Sodertalje,瑞典)200µg/6µg一次吸入,可根据需要缓解症状。代表当前临床实践的两种比较疗法将首先是沙丁胺醇加压计量吸入器(pMDI) (Ventolin;(葛兰素史克,伦敦,英国)100µg, 2次吸入,根据需要缓解症状;其次是布地奈德(普米克都bubuhaler;阿斯利康)200µg,每日两次,一次吸入;沙丁胺醇pMDI(喘乐宁)100µg,根据需要两次吸入以缓解症状。将向与会者提供哮喘行动计划,其中包括何时寻求哮喘恶化的医疗审查。如前所述,所有研究吸入器都将配备电子监测装置,以记录使用情况,以便识别药物使用模式[5.]。
该研究旨在仅招募675名与会者诊断哮喘接受SABA缓解疗法的参与者。如果1)将招募潜在的参与者如果1)他们报告了在过去12个月内发生的严重加剧,并在前4周内每天平均≤2场平均使用自我报告SABA;或2)在过去的12个月中,他们没有严重加剧,自我报告SABA平均使用≥2个偶数4周[7.]但是在过去的4周内平均≤2场平均每天。患者通常在每次每场合时的动力次数将被记录。包含和排除标准,研究程序和协议的详细信息,包括统计分析计划,可以在澳大利亚新西兰临床试验登记处找到(https://www.anzctr.org.au/Trial/Registration/TrialReview.aspx?id=369311&isReview=true);试验设计总结在图1。
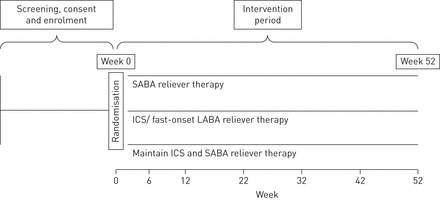
学习规划。SABA:短作用β-激动剂;ICS:吸入皮质类固醇;Laba:长效β-激动剂。
主要结果将是每年患者每位患者的恶化次数表达的哮喘发育率。
哮喘加剧的研究定义是:1)哮喘恶化,导致紧急医学审查(初级保健,急诊部(ED)访问或医院入院);和/或2)哮喘恶化,导致使用全身皮质类固醇,例如泼尼松,任何持续时间;和/或3)哮喘产生高β-激动剂使用的发作,定义为24小时内的Salbutamol或Presonide / Formoterol的8次致动。
关键二次结果包括:
1)临床结果:
a)三个标准中的每一个定义的加剧的比例,至少一个加剧的患者的比例以及第一次加剧的时间。
b)严重的恶化率和时间由美国胸部学会/欧洲呼吸协会标准定义的第一次严重加重的时间[188bet官网地址8.]。
使用系统性皮质类固醇至少3天。
因哮喘而入院或ED访问,需要全身性皮质类固醇。
c)由于治疗失败而撤出的患者的比例,定义为:
一个严重的恶化。
三个加剧,分开至少7天。
不稳定的哮喘导致随机治疗的变化。
d)哮喘控制问卷(ACQ-5得分)。
e)1 S强迫呼气量(FEV1) %预测。
f)呼出的一氧化氮的分数。
2)研究药物用途:
a)平均每天剂量(Budesonideμg·日-1);没有ICS使用的天数,否持续时间最长。
b)全口腔皮质类固醇剂量。每年口腔皮质类固醇的课程数量;每年复合全身皮质类固醇暴露,其中每年的ICS剂量转化为口服泼尼松 - 当量剂量,用于对肾上腺功能的全身影响[9.],添加到口服强的松剂量每年,如前所述[5.]。
c)高β-激动剂使用的集发作集,包括参与者的比例,至少有一个高使用的一集;在48小时内没有医学评审的高使用剧集的比例,7天和14天。
d)24小时内的最大β-激动剂致动的最大数量。
e)如先前定义的,在严重加剧前的14天内使用研究药物的使用[10]。
3)不良事件:
a)不良事件。
b)严重不良事件。
4)成本效益。医疗费用(药物,紧急医疗和急诊部门访问以及医院招生)以及非医疗费用(休假日)。收集的成本效益数据将允许外推到未来的定价模型。
5)患者态度:
a)问-12问卷[11]。
b)在120名参与者的子集中进行定性访谈,以评估药物的可接受性和效用以及药物对患者信仰的影响。这将以10名参与者组成,由随机待遇和国家选择。
统计分析将采用“意向治疗”。主要分析是通过泊松回归比较每位患者每年的病情加重率,其中对观察天数和使用SABA的固定效应以及招募前的严重病情加重次数进行了补偿。分析前应评估过分散,必要时应进行正确的分析。将进行两项敏感性分析,以说明潜在重要反应预测因子的不同分布。使用Kaplan-Meier图和Cox比例危险度的生存分析将用于计算与首次发作时间的危险度比。
对于基于药物使用的次要结果变量,事件计数将通过泊松回归分析,并在必要时对观察时间和过度分散进行校正。事件的比例将通过计算相对风险或优势比和适当的置信区间来分析。连续变量,如ACQ-5评分和FEV1将通过T检验和混合线性模型进行比较,以考虑重复的测量并检查随时间的变化模式。预先指定的子组分析将进行评估是否具体特征会影响治疗响应。
每个治疗臂的样品大小为225,占20%的掉落,具有80%的功率,α5%,其相对加剧的相对速度为0.75,每位患者每年1.2至0.9。
在对400名患者进行随机分组后,数据安全监测委员会将对所有严重不良事件进行掩蔽临时安全性统计分析。
本研究是第一个独立的调查员启动和管理的RCT进入ICS / FAST-ONSEL LABA吸入器,作为哮喘患者哮喘患者的唯一释放治疗,并将提供关于所有三种治疗的安全性和疗效的强大数据战略。该研究具有务实的开放式标签设计,使得两个潜在的“现实世界”优势ICS / FAST-ONSEL LABA REVIFEVER治疗方案,IE。在临床实践中会出现使用单一吸入器而不要求常规使用吸入器的情况。避免双假、双盲设计和广泛的纳入标准,将确保研究结果可以推广到临床实践。确定特定特征(如Th2分布)是否影响对随机治疗的反应的亚组分析将提供可能作为个体化治疗基础的数据。
我们将解决临床问题:“对于仅接受SABA缓解疗法的间歇性或轻度哮喘患者,SABA缓解疗法(继续当前治疗)的比较疗效如何?相对维护IC和SABA Reliever疗法(按照指南推荐)[7.]相对ICS/快发型LABA缓解疗法(新疗法)?”虽然这项研究并没有设计验证指南,它将使一个评估建议患者使用萨巴至少两次在前4周应定期接受ICS治疗,除了那些严重恶化在过去12个月里无论萨巴很少使用(7.]。
主要结果,哮喘加剧率,是一种复合措施,包括如前所述的高β-激动剂使用发作[5.],基于β-激动剂使用水平的阈值,要求在标准动作计划中进行医学审查,并由6μg蛋白质醇的短期支气管胆管等当量,以急性哮喘中重复给药6μg甲酚至200μgsalbutamol [12那13]。经过验证的电子监控设备,可记录吸入器用于识别其他未记录的恶化,以及使用行动计划,这些计划提供有关如何识别恶化和采取行动的书面指示,允许稳健识别恶化。主要结果措施对应于“中度至严重的加剧”;还将分析严重的恶化作为重要的二次结果。
根据需要的SABA组每年每年每年1.2患者的假定加剧率是保守的,源自两个安慰剂控制的RCT,其每年举报安慰剂维持和SABA救济治疗的加剧率为每年0.77-1.63的速度为0.77-1.63 [1那14]。加剧的定义在研究之间存在差异,但最重要的差异,我们通过电子监测研究药物使用的高β-激动剂使用时期应改善加剧的鉴定[5.]。提名的临床有意义的治疗效果为0.75的相对加油率也是保守的。
总之,新型开始研究将提供关于ICS / FAST-SAPSEABA REVIEVER治疗方案的疗效和安全性的数据,与SABA REFIFERVER治疗相比,在成年患者中的维持ICS和SABA refiever治疗方案相比轻度哮喘。
脚注
临床试验:本研究登记www.anzctr.org.au.使用标识符ACTRN12615000999538.universal试用号:U1111-1170-2118。
支持声明:本研究由AstraZeneca的授权资助(参考号ESR 14-10452)。在与Astrazeneca咨询之前,调查人员启动和设计了该研究。该研究的全球赞助商是新西兰的医学研究所(惠灵顿,新西兰)(参考号:MRINZ / 15 / A1),这将对研究行为,监测和数据管理进行全面责任。本文的资助信息已存入乐趣。
利益冲突:披露可以在本文的在线版本旁边找到www.qdcxjkg.com.
- 已收到2015年10月12日。
- 公认2015年12月12日。
- 版权所有©2016















