抽象
气道壁的厚度和肺气肿有助于气流受限。
我们检查了他们的肺功能下降和气流受限的发展协会在2021年男性吸烟者与不气流受限。气道壁的厚度和肺气肿分别上胸部计算机断层扫描进行定量,并表示为一个10毫米内腔周长(PI10)和第15百分位数法(Perc15)的壁面积的平方根。Baseline and follow-up (median (interquartile range) 3 (2.9–3.1) years) spirometry was available.
Pi10和Perc15与基线强迫呼气量1 s (FEV1)相关(r=−0.49和0.11,分别(p<0.001))。多元线性回归分析显示,基线时Pi10和Perc15与随访后FEV1较低相关(p<0.05)。为每一个SDincrease in Pi10 and decrease in Perc15 the FEV1 decreased by 20 mL and 30.2 mL, respectively. The odds ratio for developing airflow limitation after 3 years was 2.45 for a 1-mm higher Pi10 and 1.46 for a 10-HU lower Perc15 (p<0.001).
一个greater degree of airway wall thickness and emphysema was associated with a higher FEV1 decline and development of airflow limitation after 3 years of follow-up.
抽象
计算机断层扫描显示,气道壁厚度和肺气肿与肺功能下降和慢性阻塞性肺病有关http://ow.ly/DMN4h
介绍
慢性阻塞性肺疾病(COPD)的特点是气流受限和肺功能下降增加[1]。气流受限是由肺气肿引起的气道壁重塑(即。气道壁增厚和细支气管闭塞)2]。慢性阻塞性肺病是一种异质性疾病,人们认识到,肺气肿和气道壁疾病导致气流受限和肺功能损害的程度因人而异[3.,4]。
定量计算机断层扫描(CT)可以被用于量化肺气肿的程度及气道壁的厚度。一些研究发现肺气肿和气道壁的厚度与关联肺功能,COPD和临床症状的存在。以往的研究表明CT量化肺气肿和吸烟者和科目更快速肺功能下降与COPD之间的关联[5- - - - - -9]。
然而,气道壁厚度是否与肺功能更强的下降独立相关尚未被研究。在临床实践中或为筛查目的而进行的胸部CT检查可能有助于识别有COPD风险或肺功能快速下降的受试者。
The objective of the present study was to determine the association of airway wall thickness and emphysema with lung function decline or development of forced expiratory volume in 1 s (FEV1)/forced vital capacity (FVC) <0.70 after a follow-up period of 3 years in a cohort of former and current smokers without and with airflow limitation.
方法
参与者
这项研究是荷兰 - 比利时肺癌的男性参加筛查试验(NELSON)中进行10]。纳尔逊审判是肺癌的人群为基础的,CT筛查试验。入选标准已经被先前公布[8]。In short, participants meeting the inclusion criteria of having smoked >10 cigarettes·day−1for >30 years or >15 cigarettes·day−1for >25 years and who were fit enough to potentially undergo thoracic surgery were invited to participate. Potential fitness for surgery was determined by the ability to walk up two flights of stairs. Baseline details on smoking habits were gathered through questionnaires, which included questions about duration of smoking, smoking history and smoking status at enrolment (current or former smoker). At the start of the study it was decided that this study provided the opportunity to also assess lung function. To investigate this in relation to CT measurements, spirometry was performed in a random sample at the University Medical Center Utrecht (Utrecht, the Netherlands) and the University Medical Center Groningen (Groningen, the Netherlands).
NELSON试验于2003年12月23日由荷兰卫生部批准,并由两家参与医院(乌特勒支大学医学中心和格罗宁根大学医学中心)的伦理委员会(批准号为03/040)批准。NELSON试验在荷兰注册www.trialregister.nl(试验编号ISRCTN63545820)。从所有参与者获得知情同意。
肺功能测试
肺功能试验(PFTs)按照现行欧洲呼吸学会和美国胸科学会指南进行,包括FEV1、FVC和FEV1/FVC [188bet官网地址11]。没有评估气流限制的可逆性。在基线和随访时进行PFTs。PFTs与CT扫描在同一天进行。根据2012年全球肺功能倡议(GLI)方程,将气流限制定义为z分数<−1.645,根据全球慢性阻塞性肺病倡议(GOLD)的二次分析,定义为FEV1/FVC <70% [1,12,13]。预测值,标准化残差和正常的下限分别用2012 GLI方程[计算13]。
CT扫描
所有参与者均接受低剂量CT扫描,采用16排多层CT扫描仪(Brilliance 16P;飞利浦医疗系统公司,美国克利夫兰,或sens- 16;西门子医疗解决方案公司,德国福尔奇海姆)基线和随访。扫描数据采用螺旋模式,准直16×0.75 mm,灵感充足。未应用肺量计门控[14]。一个xial images were reconstructed with 1.0 mm thickness at a 0.7 mm increment. All scans were reconstructed with a soft reconstruction filter (Philips B; Philips Medical Systems, Cleveland, OH, USA; Siemens B30f; Siemens Medical Solutions, Forchheim, Germany) at a 512×512 matrix. Exposure settings were 30 mAs at 120 or 140 kVp, depending on the participant's weight. This low-dose CT protocol has previously been used to quantify emphysema in COPD patients and heavy smokers [8,15,16]。所有的量化用CIRRUS龙12.03(执行http://cirrus.diagnijmegen.nl)。
肺气肿的定量
自动分割肺部,并采用降噪滤波器来减少噪声对定量测量的影响。肺气肿严重程度采用第15百分位数法(percentile method, Perc15)。这项技术提供了低于15%的体素分布的Hounsfield单位点。Perc15值越低,即。当接近−1000 HU时,肺气肿就会增多。为了调整CT采集期间参与者之间的吸气水平变化,将Perc15调整为预测的总肺活量[17]。由适当的参考方程推导出总肺活量[13]。我们通过用CT肺总体积乘以Perc15和除以由预测总肺活量调整Perc15。在这篇文章中Perc15指的是在灵感水平的差异调整值。
气道壁的厚度的定量
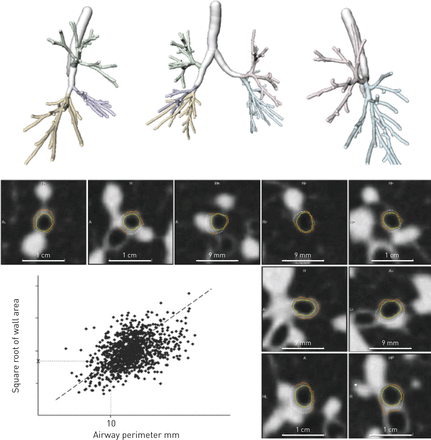
基于区域生长和形态学操作自动分割气道树[18,19]。平均而言,第8代的气道被包括在分割中。在整个分割的气道树中,将垂直于局部气道方向的截面图像平面定义为间距为1mm。由于无法进行精确测量,从气管、主支气管或分叉处获得的横断面平面会被自动丢弃。对于所有剩余的截面,通过分析从管腔中心向外指向的72条射线的强度分布来确定准确的管腔和壁边界,使用强度积分技术来解释部分体积效应[20]。每次扫描平均有800个横截面。计算每个横截面的管腔周长和管壁面积。壁面积的平方根的线性回归与周长计算了所有横截面的内腔(图。1)21]。有10毫米内腔周长(PI10)的壁面积的平方根计算,并用作气道壁的厚度的测量值。对于每一个CT扫描所检测到的气道壁的边界的截面的随机选择目视检查,以验证测量精度。
气道壁的厚度的自动定量的图示。气管树是基于区域生长和形态学操作自动分割。在整个分段气道树中,截面图像平面垂直于在1毫米间距分别定义的局部气道方向。对所有剩余的横截面,准确腔和壁边界是通过分析72个向外光线使用强度积分技术以考虑部分体积效应从腔的中心指向强度分布来确定。壁面积的平方根的线性回归与计算所有截面的管腔周长。计算10mm管腔周长的理论气道管壁面积的平方根,用于测量气道管壁厚度。从[复制21],并得到出版商的许可。
统计分析
均值±SD为正态分布数据计算值,为非正态分布数据计算中位数(四分位数范围)。采用t检验和卡方检验来适当地检验组间的差异。在基线时,皮尔逊相关性被用来建立变量之间的关联。观察期结束时的FEV1为主要终点,采用多元线性回归分析。气道壁厚(Pi10)和肺气肿(Perc15)是主要的解释因素。对基线FEV1、年龄、身高、包年和吸烟状况(当前/前吸烟者)进行了调整。在第二个模型中,增加了气道壁厚与肺气肿的相互作用项。在第三个模型中,增加了吸烟状态和包装年与Pi10和肺气肿的相互作用。
在对基线时没有气流限制的受试者进行随访后,采用多元线性logistic回归分析来检验Perc15和Pi10是否与气流限制的发展有关。对FEV1 z分数、年龄、包年和吸烟情况进行了调整。A p值<0.05被认为是显著的。所有统计分析均使用SPSS 20 (SPSS,芝加哥,IL, USA)进行。
结果
基线人口统计学和肺功能
总体而言,2211名受试者接受CT和随访肺功能检查。气道壁的厚度测量不是在190个科目可用,因为技术故障,导致被包括在这项研究2021个科目。有在年龄显著差异,包年,吸烟状况和因为被列入失踪谁气道壁的厚度测量和那些排除对象之间FEV1下降(数据未显示)。
均值±SD年龄60.5±4.9岁。根据GLI, 408名(20.2%)受试者在基线时存在气流限制。使用黄金标准,大约三分之一的受试者(n=697;34.5%)有气流限制。均值±SDFEV1为3.64±0.37 L,即−0.41±1.16标准化残差。大约一半的受试者在研究开始时是吸烟者(n=1113;55.1%)和平均值±SD的包年整个研究组为42.0±19.9。有平均一个显著差异±SDFEV1标准化残留在当前吸烟者和已戒烟者之间,分别为- 0.42±1.16和- 0.26±1.17 (p=0.02)。包年也有显著差异,分别为39.2±16.0和40.9±17.3 (p=0.045)。关于基线人口统计和肺功能的进一步细节见表1。
基线气道壁厚度和肺气肿
均值±SDPerc15为−934.8±30.1 HU, Pi10为2.42±0.59 mm。根据2012年GLI方程,有气流限制的参与者比无气流限制的参与者有更多的肺气肿和更厚的气道壁(Perc15:−945.3±18.6和−931.7±31.2 HU;Pi10: 2.83±0.59 mm, 2.31±0.55 mm;所有p < 0.001)。当使用黄金准则进行气流限制时,结果相似,但差异较小(Perc15:−942.8±17.6)与−930.6±34.3胡;Pi10: 2.70±0.61与2。27±0.53 mm; all p<0.001).
一个t univariate analysis, participants with a higher Pi10 and lower Perc15 had a lower FEV1 (r= −0.49 and 0.11, respectively, p<0.001). A 1-mm higher Pi10 resulted in a 25-mL lower FEV1 and a 10-HU lower Perc15 resulted in a 6-mL lower FEV1 (p<0.001). There was a low significant correlation between Perc15 and Pi10 (r=0.12, p<0.001). Current smokers had a higher Pi10 than former smokers; 2.53±0.61 mm and 2.37±0.58 mm, respectively (both p<0.001). Current smokers had a higher Perc15 than former smokers; −933.0±18.6 HU and −942.6±17.3 HU, respectively. No significant correlation was found between pack-years and Perc15 or Pi10.
后续计量
下降的FEV1
中位(四分位范围)随访时间3.0(2.9-3.1)年。均值±SDFEV1 decline was 197±71 mL. Multivariate analyses, with correction for baseline FEV1, years in study, height, pack-years, smoking status and age, showed that lower Pi10 was associated with a lower FEV1 after follow-up (p=0.002). A 1-mm higher Pi10 resulted in a 34-mL lower FEV1 after follow-up. Additionally, Perc15 was associated with a lower FEV1 after follow-up (p=0.006) and a 10-HU lower Perc15 was associated with a 10-mL lower FEV1 after follow-up. Smoking status, baseline FEV1, age and height were also associated with FEV1 after follow-up. The effect sizes of these parameters on FEV1 after follow-up are presented in表2。有PI10和Perc15(p值= 0.703)之间不存在显著相互作用。当标准化的FEV1比较PI10和Perc15的效果,一个效果SD在PI10变化导致在20-mL低FEV1之后的后续和一个SD在随访后,随着Perc15的变化,FEV1降低了30.2 ml。吸烟状态和包年与Pi10和Perc15的交互作用不显著(p>0.05)。
在后续的气流受限的发展
1613(79.8%)参与者根据2012 GLI方程,其中172(10.7%)的开发气流受限随访在基线没有气流受限。使用GOLD标准,这是1324(65.5%),其291(22%)发达的气流受限的随访。-937.6±17.4:谁在后续开发的气流受限(2012 GLI方程)科目相比,谁没有发展的气流受限(Perc15在基线显著更肺气肿(P <0.001)和较厚的呼吸道壁与-931.5±33.1 HU,分别;PI10:2.59±0.54与分别为2.28±0.55毫米)。
经过3年的随访,根据2012年GLI方程,Perc15和Pi10均与气流限制的发展具有显著的独立相关性。低10-HU的Perc15导致优势比为1.46,高1 mm的Pi10导致优势比为2.45(均p<0.001)。当使用黄金准则进行气流限制时,发现Pi10的比值比类似,但在Perc15时,比值比更低。低10-HU的Perc15导致优势比为1.26,高1 mm的Pi10导致优势比为2.44(均p<0.001)。根据GOLD将289名基线受试者分为气流阻塞组,而不是根据2012年GLI方程。根据2012年GLI方程,Pi10高1 mm时,气流限制的比值比为1.86,10-HU低Perc15时,比值比为1.23 (p=0.039, 0.024)。图2和3.说明显影根据Perc15和PI10的基线值气流受限(2012 GLI方程式)的多变量调整概率。年龄,包年和吸烟状况进行了独立与气流受限的发展有关。
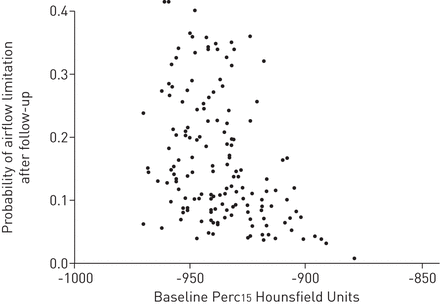
多变量调整逻辑回归分析的结果,显示在基线具有根据基线第十五百分方法(Perc15)的后续后气流受限参与者没有气流受限的概率。低Perc15主题有随访概率较高的气流受限。

示出了根据在基线到基线10毫米内腔周长中的参与者(PI10)值的壁面积的平方根没有气流受限随访后具有气流受限的概率多变量调整逻辑回归分析的结果。具有较高PI10参与者有随访概率较高的气流受限。
讨论
在这个大型研究过去和现在的男性吸烟者和不轻度气流受限的,我们发现,这两种肺气肿和厚度平均3年的随访期后,用较低的FEV1独立相关气道壁。此外,我们发现,肺气肿及气道壁的厚度也与气流受限的学科发展基线时无气流受限有关。这些结果表明,在前任和现任吸烟者肺部的CT结构变化的评估可以让医生以确定科目谁将会显示较大的FEV1下降或将开发的气流受限。
一些研究已经检查了CT气道壁的厚度和肺功能下降和慢性阻塞性肺病的发展之间的关系。Øhara等。(22研究表明,83名男性COPD受试者气道管壁面积占总管腔面积百分比的增加与FEV1的年升高相关。然而,他们只报道了单变量分析的结果,没有提供效应量。其他横断面研究表明,气道壁厚度越高,肺功能越低,存在COPD [5,23- - - - - -26]。
气道壁的厚度已经与其他成果的措施有关。Grydeland等。(27]显示,较高的气道壁厚度与呼吸系统症状(呼吸困难、咳嗽和喘息)有关。H一个等。(28的研究结果表明,相对于肺气肿而言,较高的气道壁厚度与COPD患者发生急性COPD加重的风险更高。在他们的研究中,Pi10每增加1毫米,年恶化率就增加1.8倍。米artinez等。(29]表明,较厚的气道城墙是用在圣乔治呼吸问卷得分较高,BODE指数(身体质量指数,气流阻塞,呼吸困难和运动能力)相关29]。总之,这些研究表明气道壁厚度与临床相关结果相关。
考虑到其他几个研究小组也报道了类似的发现,ct量化的肺气肿与肺功能加速下降相关的发现似乎很有说服力[5- - - - - -9]。YUAN等。(7显示,CT上自动量化的低衰减区与无COPD吸烟者的随访肺功能之间存在趋势。虽然他们的发现并不重要,但效果的方向和我们的是一样的。我们的发现补充了Vestbo等。(6,该研究报道,患有肺气肿的COPD患者(定义为>10%低衰减区<−950 HU) FEV1额外下降13 mL·年-1相较于那些没有肺气肿。在这项研究中,都包含了中度,重度或极重度COPD患者,但随着病情的早期阶段,受试者没有,不像在我们的研究。因此,我们自己的观察延伸到早期肺气肿。
COPD是由气流受限的存在定义[1]。然而,气流受限是由肺结构变化的复杂相互作用造成的,即。肺气肿和大大小小的气道疾病。随着COPD严重程度的增加,气道壁增厚的相对重要性降低,气道壁增厚在较严重的COPD患者(GOLD III/IV)中的作用似乎降低[3.]。在我们的研究中,只包括轻度COPD受试者。因此,我们不能真正检验气道壁厚度的相对重要性是否随COPD严重程度的增加而降低。此外,肺气肿和气道壁增厚可能已经存在,但尚未导致COPD。目前,无COPD患者气道壁增厚的临床相关性尚不清楚,但我们发现,气道壁厚度与FEV1相关,这可能与目前和以前无COPD的吸烟者相关。通过CT检测和量化这些结构变化可能有助于改善个体受试者的预后[三十]。
我们的研究包括吸烟者与不轻度气流受限谁可能是COPD的病理生理过程的早期阶段。最近,它表明小气道很可能影响早在COPD的病理生理级联[3.]。此外,在随访中,气道壁厚度和肺气肿都与较低的FEV1独立相关。这表明在分析胸部CT扫描时评估肺气肿和气道壁厚度是很重要的。然而,在预测吸烟者肺功能下降和/或慢性阻塞性肺病的发展方面,CT扫描相对于呼吸困难、咳嗽和喘息症状的优势需要在未来的研究中加以解决。
这项研究的优势在于大量的被纳入的参与者(n=2021)都有或没有轻度的气流限制,平均随访时间为3年。CT扫描的另一个优点是低辐射量。鉴于CT扫描的数量逐年增加,进一步了解CT扫描中肺部结构改变的预后价值可能变得越来越重要。如果肺癌筛查可以作为一种以人群为基础的筛查,那么在肺癌旁边附加的信息可能会提高(国家)筛查计划的相关性。
这项研究的局限性是使用了支气管扩张器前肺功能值。然而,由于基线和随访肺量测量均未进行支气管扩张,因此不应对FEV1下降的评估产生影响。然而,由于缺乏支气管扩张后的肺量测量值,一些受试者可能被错误地归类为气流受限。另一个限制是目前的研究没有包括女性。之前的一项研究表明,在横断面水平上,女性的Pi10比男性低[17]。然而,Pi10与肺功能下降的相关性在女性和男性之间是否存在差异尚不清楚。未来的研究将决定我们的发现是否适用于女性。不同的曝光设置被用于体重<80公斤和>80公斤的受试者,这可能会影响百分15测量值。然而,在这个没有COPD或轻度COPD的队列研究中,我们没有预见到体重和肺功能之间有很强的相关性。最后,由于分割错误,如自动识别所有支气管壁的问题,190次扫描没有被纳入分析。然而,这些受试者的临床参数与所包括的受试者没有差异。
总之,目前的研究表明CT扫描是更严重的气道壁的厚度和肺气肿是独立与加速FEV1下降和气流受限的男性吸烟者的发展相关。胸部CT扫描可能获得在有和无轻度COPD的吸烟者谁将会从更严重的肺功能下降和/或慢性阻塞性肺病的发展遭受的选择作用。
脚注
这篇文章有提供补充材料www.qdcxjkg.com
支持声明:本研究由Zorgonderzoek Nederland-Medische Wetenschappen (ZonMw;荷兰海牙)、KWF Kankerbestrijding(荷兰阿姆斯特丹)和Stichting Centraal Fonds保护区van Voormalig Vrijwillige Ziekenfondsverzekeringen (RvvZ;泽斯特、荷兰)。
利益冲突:披露能够随本文的在线版本中找到www.qdcxjkg.com
- 收到2014年1月31日。
- 接受2014年10月14日。
- 版权所有©ERS 2015年