摘要
文献中曾报道过使用干扰素(IFN) α或β治疗的患者出现肺动脉高压(PAH)的孤立病例。
本研究的目的是描述1998年至2012年在法国参考中心确诊的有IFN暴露史的所有连续PAH患者。
共有53例PAH患者被确定有干扰素治疗史。应用干扰素α治疗慢性丙型肝炎48例,其中门静脉高压占85%,HIV合并感染占56%。另外5例患者接受了IFNβ治疗多发性硬化症。66%的患者在干扰素治疗后3年内诊断为PAH。在诊断为PAH后,16例暴露于IFN的患者中有13例进行了重复血流动力学评估。13例中11例肺血管阻力>增加20%(中位数增加43%;差32 - 67%)。其中5例患者停用干扰素导致自发性血流动力学改善。
这项回顾性分析表明IFN治疗可能引发PAH。然而,这些患者中大多数存在PAH的其他危险因素。有必要进行前瞻性病例对照研究,以明确确定IFN暴露与多环芳烃之间的联系。
摘要
临床资料提示干扰素治疗可能是肺动脉高压的一个触发因素http://ow.ly/BweqG
简介
肺动脉高压(PAH)是一种严重的进行性疾病,主要表现为肺动脉压力升高和肺血管阻力升高,可导致右心衰,最终死亡[1,2].多环芳烃可能是特发性的、遗传性的,或与若干病症和疾病有关,包括结缔组织疾病、艾滋病毒感染、门脉高压、先天性心脏病和接触药物和/或毒素[3.,4].在已知与多环芳烃形成有关的药物中,只有抗厌食症药物如氨氧克斯和芬氟拉明衍生物,以及有毒菜籽油被认为是多环芳烃的“明确”危险因素[2,5].最近,法国肺动脉高压登记处发表的数据表明,达沙替尼,一种酪氨酸激酶抑制剂(TKI),也可能诱发PAH [6].
干扰素(IFN)的作用越来越被认为是多环芳烃发展的危险因素。发表的几份个案报告证实了这一点[7- - - - - -14]和实验研究[15- - - - - -18].干扰素在免疫系统中具有强大的作用,它们在抗病毒、抗菌和抗肿瘤方面发挥着关键作用。它们被分类为螺旋细胞因子,并根据其物理和功能特征分为I型或II型。I型干扰素包括α(由白细胞释放)、β(由成纤维细胞释放)、τ和ε子类型,它们可能来自一个共同的祖先基因。根据它们的作用,干扰素已被用于治疗广泛的疾病。干扰素-α已广泛用于肝炎病毒的治疗,但也用于血液、肾脏和皮肤恶性肿瘤。在过去的几十年里,IFN-α和利巴韦林的相关性被认为是目前治疗慢性丙型肝炎病毒(HCV)感染的标准。重组干扰素β被批准用于治疗复发缓解型多发性硬化症[19].
干扰素治疗的主要缺点是多种副作用的发生,导致患者依从性差,导致疗效降低。影响呼吸系统的主要不良事件是咳嗽(26%)[20.],而其他副作用则很罕见,而且通常很严重:间质性肺病(0.3%)[21]、胸腔积液、哮喘加重、肉芽肿、有组织肺炎及双侧肺浸润[14].
在文献中,有12例肺动脉高压可能与干扰素暴露相关[7- - - - - -14].此外,最近的实验研究表明,IFN可促进内皮功能障碍,增加人肺血管细胞内皮素-1的释放[16].在这些发现的基础上,为了评估干扰素和多环芳烃之间的潜在联系,我们咨询了当地的多环芳烃登记处。
本报告总结了在巴黎-南大学法国重度肺动脉高压参考中心(PH)连续出现IFN暴露史的PAH患者的临床特征和结局。
方法
病人
法国多环芳烃患者登记处是选择暴露于IFN的多环芳烃患者的主要数据库。我们将搜索限制在参考中心(巴黎-南大学)的随访患者。这项回顾性研究符合赫尔辛基宣言。尽管法国法律不要求伦理委员会批准或知情同意进行回顾性数据收集,但数据是匿名的,并符合国家医学和医学研究所的要求国家信息委员会等Liberté该组织负责法国的隐私、信息技术和公民权利。该委员会于2003年5月24日批准了用于收集和分析数据的方法(批准号842063)。
所有多环芳烃患者(即。PH值临床分类第1组)[4有IFN暴露史的人被纳入分析。PH定义为右心导管测量的平均肺动脉压(mPAP)≥25 mmHg和肺动脉楔压(PAWP)≤15 mmHg。所有经右心导管检查确诊为PH的患者都接受了广泛的调查,以确定血管疾病的其他原因或危险因素(先天性心脏病、孔肺动脉高压、艾滋病毒感染、结缔组织病、慢性血栓栓塞性PH、慢性阻塞性或限制性肺病、收缩期或舒张期左心脏病、血红蛋白病、等)。诊断时记录诊断年龄和经改良的纽约心脏协会(NYHA)功能分级评估的临床状况。按照美国胸科协会的建议,进行非鼓励的6分钟步行测试。
暴露于干扰素和达沙替尼的慢性骨髓性白血病患者被排除在外,因为达沙替尼最近被指控诱发PAH [6].
干扰素暴露
IFN暴露的具体情况是通过初次检查或检查时的详细临床病史收集的后验视具体情况而定。干扰素的类型(α或β)、初次暴露日期和总暴露时间是在与患者及其肝病医生面谈后确定的。
统计分析
数据存储在基于pc的数据电子表格中。在Microsoft Excel 2007上使用StatEL(广告科学,巴黎,法国)统计包进行分析。所有数据均以均数±表示sd或中位数和四分位范围(IQR)。在暴露于IFN的已诊断PAH患者中,对IFN暴露前、IFN暴露时和IFN停用后最后一次评估中获得的血流动力学变量进行比较,对配对组的正态分布变量使用单向方差分析,对非正态分布变量使用非参数Friedman检验。事后使用Newman和Keuls检验或非参数Wilcoxon检验进行比较。p值<0.05为有统计学意义。
结果
研究人群
从1998年到2012年,法国严重ph参考中心发现了53例有IFN暴露史的PAH患者。其中48例是在暴露IFN后诊断出PAH的。在其余5例患者中,IFN治疗是在已知PAH的情况下开始的。
使用IFN-α治疗的患者
在研究人群中,47例慢性HCV感染患者接受了IFN-α治疗,1例慢性骨髓性白血病患者接受了IFN-α治疗。IFN-α治疗的中位IQR持续时间为7.7个月(5.3-11.0个月)。80%的病例使用IFN-α2a, 20%的病例使用IFN-α2b。在这48例患者中,8例(17%)在诊断PAH时仍在使用IFN-α。48例患者中有35例(73%)在接触IFN-α后3年内被诊断为PAH (图1).
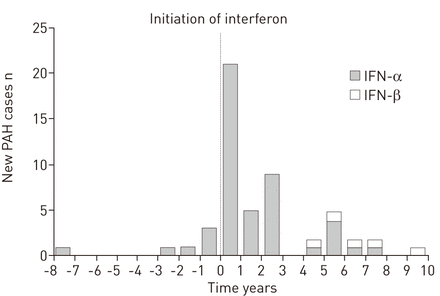
干扰素(IFN)启动和肺动脉高压(PAH)诊断之间的延迟。三分之二的PAH病例在干扰素治疗开始后3年内被诊断出来。在5名接受IFN-β治疗的患者中,多环芳烃在开始接触5-10年后被诊断出来。
在PAH诊断时评估的48例IFN-α治疗患者的临床和血流动力学特征显示在表1.所有肝硬化患者均有门静脉高压的证据,至少存在以下一种情况:腹水、食管静脉曲张或肝静脉压梯度升高(>5 mmHg)。27例(56%)患者合并感染HIV。暴露于干扰素的HCV患者,无论有无HIV合并感染,其血流动力学与法国登记的门脉性高血压患者相似(数据未显示)。
使用IFN-β治疗的患者
5例患者在诊断为PAH时接受了IFN-β治疗。在这些患者中,从开始使用IFN-β到诊断为PAH的时间从59到117个月不等(图1,表2).这5例患者的个体特征详细见于表2.其中一名患者有房间隔缺损,这是PAH的明确危险因素。其中大多数人发展为严重的多环芳烃,导致2例死亡。
干扰素对多环芳烃进展的影响
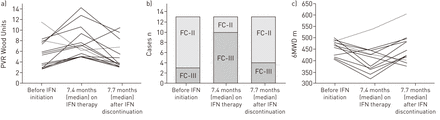
在已知PAH诊断的情况下,16例患者接受了IFN-α治疗。5名患者首次接受了干扰素治疗,而11名患者过去已经接受过治疗。在干扰素起始时,16例患者中有8例正在接受多环芳纶特异性治疗(内皮素受体拮抗剂和/或磷酸二酯酶5型抑制剂)。这些患者的临床和血流动力学特征显示在表3.在这些患者中,IFN暴露的中位持续时间为10个月(IQR 6.4-12.9)。13例患者在接受干扰素治疗(中位7.4个月;IQR 6.4-13.8)和停用IFN后(中位数7.7个月;差6.0 - -8.9)。显示NYHA功能分级、6分钟步行距离(6MWD)和肺血管阻力(PVR)的过程图2.13例患者中PVR增加超过20%的有11例(5±2.1 ~ 8.1±3.2;p < 0.05)。这种血流动力学恶化与功能和运动能力的恶化有关(图2).4例患者在使用干扰素后,临床和血流动力学恶化,需要额外的多环芳烃特异性治疗。在其他5例患者中,停用干扰素导致临床和血流动力学改善,无需任何额外治疗。相比之下,其余2例患者停用干扰素后PAH未见改善。
干扰素-α对肺动脉高压患者临床、功能和血流动力学参数的影响起始干扰素后中位7.4个月(四分位数范围(IQR) 6.4-13.8)和停用干扰素后7.7个月(IQR, 6-8.9)的临床、功能和血流动力学参数的演变。干扰素启动前的最后一次评估是在丙型肝炎病毒治疗前3.7个月(IQR, 1.2-9.2)进行的。IFN启动后,观察到b)纽约心脏协会功能等级(FC)恶化,c) 6分钟步行距离(6MWD)显著降低。有创血流动力学评估显示肺血管阻力(PVR)显著增加(p<0.05)。a)只有2例患者在IFN启动后PVR下降(虚线)。在IFN启动后,4例患者的pah特异性治疗得到加强。在停用干扰素后的功能、临床和血流动力学评估显示,5名患者的恶化情况自发缓解,无需额外的多环芳烃特异性治疗。
讨论
自1998年以来,法国严重PH参考中心在接受IFN治疗的患者中发现了53例有症状的毛细血管前PAH。绝大多数患者曾因慢性HCV感染接受过IFN-α治疗。所有患者均存在PAH的另一危险因素(门脉高压和/或HIV感染)。5例患者因多发性硬化症接受了IFN-β治疗,其中只有1例患者存在PAH的另一危险因素。
尽管在大多数患者中存在与多环芳烃相关的其他危险因素,但一些特征表明暴露于干扰素与多环芳烃的发生之间存在潜在联系。首先,我们观察到三分之二的患者在IFN开始后3年内被诊断为PAH。在接受IFN-β治疗的患者中,时间延迟更长。我们还观察到大多数暴露于IFN的PAH患者症状、运动能力和血流动力学参数的恶化。最后,对没有任何其他疾病危险因素的PAH患者的描述强调了IFN在PAH发展中的潜在作用。
文献报道了其他12例可能与干扰素治疗相关的多环芳烃[7- - - - - -13];其中只有5例是通过右心导管插入术确诊的。1993年发表的第一个病例描述了一名肾细胞癌患者在接受干扰素治疗后发生的可逆急性右心衰,首次提出了可能的致病机制[13].总体而言,10例归因于IFN-α, 2例归因于IFN-β。只有2例在停用干扰素后被认为是可逆的。相比之下,其他10例需要使用多环芳烃特异性治疗或导致死亡。有趣的是,文献中所有病例都是在干扰素治疗开始后3年内诊断的,这与我们对暴露于干扰素-α的患者的观察结果一致。在其他临床研究中,越来越多的证据表明IFN治疗可发生或加重PAH。已观察到,在使用IFN-α治疗慢性HCV感染的患者中,多达48%的患者肺部CO扩散能力至少下降15%。这表明这种治疗诱发了潜在的肺血管病变[22].此外,在接受干扰素α治疗丙型肝炎感染的患者中,血清内皮素-1水平升高,而内皮素-1是PAH发病的关键媒介[23].我们的报告的优势在于,我们有一个大型前瞻性PAH数据库,可以监测PAH危险因素的趋势,也有基线和停用干扰素后的侵入性肺血流动力学数据。
药物诱导的多环芳烃的时间模式并不总是高度提示因果作用,但不排除药物在疾病发生中的责任。使用厌食药物的经验表明,治疗开始后肺血管损伤发生的时间有时可能很长(中位为>年5年),并且可以在停止接触后发生[24,25].这一特性,再加上一小部分患者受到副作用的影响,在一定程度上解释了一些药物在多环芳烃新病例出现中作用的晚认识。最近,报道的达沙替尼诱导多环芳烃的病例表明,药物暴露与多环芳烃发生之间的时间可能更短(34个月)[6].在我们的研究中,我们观察到一个时间关联,提示IFN在PAH发病中的责任。在5例患者中,IFN的参与已被正式排除,因为在接触多环芳烃之前就已经知道。在这些患者中,我们只分析了IFN对PAH进展的影响。在大多数接受IFN-α治疗的患者中,多环芳烃在药物暴露后3年内被诊断出来。有趣的是,暴露于IFN-β和诊断为PAH之间的时间要长得多(5-10年)。然而,这些病例很重要,因为在其中4例中没有发现多环芳烃的混杂危险因素。可以提出假说来解释IFN-β暴露与多环芳烃发生之间的较长时间。IFN-α和IFN-β的生物学活性不同。我们可以认为,这些分子在诱导内皮功能障碍和肺血管重塑的潜力上存在差异。 Further experimental studies are needed to investigate this possible association.
我们还可以假设IFN-α可以在较短时间内延迟易感患者肺血管疾病的发展,从而发挥触发作用。过去,药物诱导的多环芳烃的几个特征表明,一种药物可以起到第二击的作用。这在厌食药物中表现得尤为明显。据报道,在暴露于芬氟拉明及其衍生物的相对较高比例的患者中存在与该疾病相关的其他危险因素[24,26].此外,在该人群中PAH与厌食症相关,患者携带的比例BMPR2与特发性多环芳烃患者相同[25].此外,携带乙肝病毒的患者接触药物的时间较短BMPR2与没有突变的人相比[25].同样,暴露于干扰素的患者中有高比例的患者具有PAH的另一个危险因素,不应排除干扰素在PAH发展中的责任。
IFN是一种常见的调节因子,在许多与多环芳烃发展高风险相关的情况下,如结缔组织疾病或病毒感染,IFN可能不受调节。在系统性硬皮病或系统性红斑狼疮患者的循环单核细胞中描述了以IFN调控基因表达增加和激活为特征的“IFN签名”[27].有趣的是,一项评估IFN对系统性硬皮病影响的安慰剂对照试验表明,IFN-α实际上在硬皮病的治疗中没有价值,而且可能是有害的。在接受积极治疗的患者组中,观察到肺功能和一氧化碳扩散能力的更大恶化[28].后来,有研究认为IFN可能参与了硬皮病患者纤维化或多环芳烃的发生[29].同样,有人认为HIV感染可能通过间接机制和炎症介质或生长因子的释放促进PAH。艾滋病毒感染患者会慢性产生干扰素α [30.,31]且IFN表达增加与HIV疾病进展相关[32].有趣的是,在我们的研究中,HIV合并感染患者的比例高于通常在慢性HCV感染患者中观察到的比例[33].由于内源性IFN参与了这些疾病的生理病理过程,因此IFN的外源性作用就很难定义了。因此,我们可以推测,由于潜在的易感因素,这些患者暴露于外源性干扰素时更容易发生多环芳烃。
没有任何危险因素的多环芳烃病例是不寻常的,大多与IFN-β有关。然而,这些病例非常重要,因为它们加强了干扰素暴露与多环芳烃发展之间潜在联系的观点。
分析IFN对PAH进展的影响提供了有趣的额外信息。我们获得了13例具有可用血流动力学参数的患者的全面可靠数据。暴露于IFN后,13例患者中有11例观察到血流动力学恶化,加强了IFN在PAH中的责任假设。更有趣的是,在这些患者中,大多数停用干扰素后,这种血流动力学的恶化是可逆的,在一半的病例中,无需加强多环芳烃特异性治疗。
许多实验研究加强了IFN暴露与多环芳烃发展之间存在联系的假设。绵羊的实验研究表明,IFN-α能够刺激血栓素级联,导致短暂的PH值[34],作者认为IFN可能加速由其他因素引起的亚临床现象,如人类疱疹病毒,丙型肝炎病毒本身,或未知的遗传倾向。其他研究报道了IFN与内皮素(ET-1)释放之间的联系,内皮素是参与PAH发病的关键中介。研究表明IFN可诱导TNF-α诱导的人肺动脉平滑肌细胞ET-1 [18].TNF对人肺动脉平滑肌细胞中IFN反应性的“致敏”作用的发现回避了潜在炎症条件是否会导致PAH发展的问题。这一实验发现可以解释为什么干扰素在炎症性疾病(如门脉高压或HIV感染)中似乎对肺循环产生更有害的影响。最近,已经证明I型IFN受体敲除(IFNAR1(-/-))小鼠免受右心缺氧、血管重塑和血清ET-1水平升高的影响。这些数据表明I型IFN可以介导PAH通过IFNAR1的作用[15].需要进一步研究IFN对其他PH动物模型的影响,如单野百合碱诱导的PH或慢性缺氧。
在过去十年中,国家网络的发展和基于网络的登记的创建促进了对可能与多环芳烃有关的药物的检测。通过分析病理生理学、流行病学和历史数据,该网络可能有助于发现与多环芳烃相关的潜在危险因素。然后,可以进行实验和临床研究来验证或否定假设。这种方法需要与药物警戒中心和国家药品监管机构密切合作,以便比较现有数据,评估问责水平,并确定必要的行动,以降低与该药物相关的多环芳烃风险。我们的临床研究为文献中已知的IFN暴露与多环芳烃发生之间可能存在的联系提供了额外的信息。然而,我们的研究存在一些局限性,主要是由于其回顾性和单中心的性质,例如在暴露于IFN-α的患者中存在混杂的PAH危险因素。研究病例对照研究的可行性,以建立干扰素暴露与多环芳烃发展之间的明确联系,并估计干扰素暴露患者中多环芳烃发展的发生率,可能是有用的。然而,在未来几年,这种治疗方法可能会被其他病毒性肝炎治疗方案所补充[35].
本研究结果可能为HCV感染患者IFN治疗的管理提供一些建议。在IFN开始时未诊断为PAH的患者中,IFN出现不明原因的呼吸困难和/或右心室衰竭迹象应导致PAH检测。如果PAH确诊,应停用IFN,并必须考虑PAH特异性治疗。对于诊断为PAH且有IFN治疗HCV感染适应症的患者,在开始任何IFN治疗之前必须进行广泛的检查,包括右心导管插入和运动测试。在稳定的、非严重的PAH患者中,IFN可以在密切监测肺血管疾病的同时使用。如果对多环芳烃的控制不能令人满意,在IFN启动前必须考虑加强多环芳烃特异性治疗。
综上所述,IFN可作为易发多环芳烃患者的“触发因素”。然而,在没有任何PAH危险因素并使用IFN-β治疗的患者中,已经发现了“纯”PAH病例。根据目前临床对PH的分类,IFN目前被认为是PAH的“可能”危险因素[4].我们的研究强调了临床和实验研究的必要性,以确定IFN暴露和多环芳烃的发展之间的关系,以便更好地了解其潜在机制,以防止肺血管系统的副作用。
致谢
我们感谢法国肺动脉高压药物警戒网络VIGIAPATH,该网络由法国国家机构Sécurité du Médicament et des producits de Santé (ANSM)支持。
脚注
这篇文章根据2015年12月发表的更正进行了修订欧洲呼吸杂志.
利益冲突:可以在本文的在线版本中找到信息披露www.qdcxjkg.com
- 收到了2014年3月26日。
- 接受2014年8月4日
- ©2014人队