文摘
肺癌,包括肺腺癌,是一种异质性疾病,气道上皮细胞从分子进化改变。本研究探讨肺腺癌的亚型是否表达人类呼吸道基底细胞的独特的分子特性(BCs),以及如何表达的气道BC特性与分子、肺腺癌的病理和临床表型。
三个独立的肺腺癌基因表达数据集进行分析,构成了气道BC签名。公元前的签名然后在肺腺癌相关临床和生物参数。
公元前的浓缩气道签名在肺腺癌基因被发现。肺腺癌的一个子集(BC-high腺癌)表现出高BC签名基因的表达与贫困肿瘤,血管侵犯的频率和较短的生存高于腺癌较低表达的基因。在分子水平上,BC-high腺癌显示更高的频率喀斯特突变,激活转录网络和通路与细胞周期、细胞外基质的组织,不同的分化模式抑制的纤毛和外分泌细胞细支气管(克拉拉细胞)-相关基因。
激活公元前气道的项目是不同的分子特性,激进的肺腺癌的亚型。
文摘
气道的高表达基底细胞基因有助于积极的肺腺癌的分子表型http://ow.ly/nIdJC
介绍
肺癌,全球癌症死亡率的主要原因,是一种异质性疾病,从分子进化改变气道上皮由环境致癌的压力,主要是吸烟(1- - - - - -3]。人类呼吸道上皮pseudostratified层主要由纤毛细胞和分泌,中间,基底细胞(BCs),和罕见的神经内分泌细胞(4]。
这些个体的具体贡献的气道上皮细胞类型肺癌异质性原因还不是很清楚。气道BCs,气道上皮细胞的干细胞/祖细胞群(5),被认为是候选人原产地“细胞”的肺鳞状细胞癌,部分原因是呼吸道BCs可能是鳞状细胞化生之源,鳞状细胞carcinoma-related潜在肿瘤前期病变(1]。相比之下,肺腺癌的细胞起源并不清楚(1]。集中位于表面或腺癌被认为起源于支气管腺上皮(6]。相比之下,一个外分泌细胞(克拉拉细胞)和II型细支气管pneumocyte-associated分化模式,也被称为“终端呼吸单元”(TRU),已经在外围观察到腺癌(7,8]。外分泌细支气管各亚群细胞,分泌细胞类型出现在小鼠气道上皮细胞(9),但有限的人类小航空公司(10),已与肺腺癌小鼠模型的发展(11]。然而,其他细胞类型的贡献,如BC-like祖细胞,人类肺腺癌也被提出(1,12]。
在目前的研究中,使用我们的最近的描述人类呼吸道BC转录组(13),我们分析了气道的独特的分子特性的贡献BCs肺腺癌的分子及临床表型。的数据提供了证据的肺腺癌亚型表达高水平的气道BC基因与积极的临床表型。
方法
可以找到更多细节的方法在网上补充材料。
肺腺癌的数据集
三个独立的肺腺癌组进行分析:主要群组(182 199例最初描述的Chitale等(14),重新评估组织学检查和更新最近的临床信息)和两组验证,一个被Bild等。(15](58科目)和一个年代海顿等。(16)(327 442例,即。不包括104例分析纪念斯隆凯特林癌症中心(MSKCC)(美国纽约),其中大部分出现在主群,和11大细胞神经内分泌癌样本识别基于病理重新评估(17])。病人特征列在网上补充表i代表实验研究流图所示图S1补充。
分析气道BC签名表达人类肺腺癌
公元前气道签名特征基因(862)曾在我们的实验室13]。分析基因富集微阵列芯片,然后是正常的数据中所有基因表达水平在所有样品确定。平均水平为每个基因平均水平相比都是公元前862气道签名基因,non-BC签名,明显高于表达完整的大型气道上皮细胞与纯化公元前基于全基因组芯片比较(标准高表达:叠化≥5 p < 0.01 Benjamini-Hochberg校正),50 862 -基因随机集(选择Affymetrix(美国圣克拉拉,CA) HG-U133A基因组用Excel(美国微软公司,微软,WA) RAND函数)。
比较公元前气道签名的表达在不同癌亚型(18- - - - - -24公元前)与呼吸道样本,数据集进行分析,主成分分析(PCA)使用GeneSpring版本7.3.1(安捷伦科技,圣克拉拉,CA)。
公元前指数(I公元前)计算为每个主题的累积测量气道BC签名表达式如前所述完整的气道上皮细胞(25]。分类的主题是基于我执行的公元前使用四分位数法:个人在底部四分位数被归类为“公元前低”和个人的最高四分位数被归类为“公元前高”。
确定转录组差异BC-high BC-low腺癌,我们全基因组进行比较(标准差异表达基因:叠化> 2,与Benjamini-Hochberg校正p < 0.01)。富集的通路中差异表达基因进行了分析使用大卫生物信息学资源6.7分析工具(http://david.abcc.ncifcrf.gov/)。为BC-high腺癌调节基因,分析网络中的基因在调节基因被确定使用加权相关网络分析和识别网络基因(标准:斯皮尔曼相关系数ρ> 0.6,p < 0.05),然后与气道BC-high BC签名基因调节肺腺癌基于物理蛋白质-蛋白质之间的关系与已知的转录调节使用GNCPro分析工具(http://gncpro.sabiosciences.com/gncpro/gncpro.php)。
表达的基因与人类的气道上皮的主要细胞类型(纤毛,分泌粘液,外分泌细支气管和神经内分泌细胞)和epithelial-mesenchymal过渡(EMT)比较肺腺癌亚型的主要群体。比较公元前气道签名的表达在鳞状细胞癌肺腺癌,数据集包含58腺癌和53鳞状细胞癌所描述的Bildet al。(15)进行了分析。
生存分析
评估的关系表达式的气道BC签名在肺腺癌患者生存,我们首次发现穷survival-associated基因的全基因组比较腺癌患者< 2年总生存期(可怜的幸存者)与那些> 5年总体生存率的主要群体(标准:差异表达基因与Benjamini-Hochberg校正p < 0.05)。所有使用kaplan meier生存分析方法。腺癌亚型之间的生存而使用生存率较。多变量分析了使用Cox比例风险模型。
免疫组织化学分析
活检样本独立收集的腺癌接受肺切除术的患者根据批准的协议和知情同意MSKCC机构审查委员会。肺腺癌的分类样本用于免疫组织化学到公元前高低是使用索引方法,如前所述,基于TaqMan PCR分析(美国应用生物系统公司,培育城市,CA)排名前十的表达基因BC-high腺癌> 85%的敏感性(在所有三个独立的肺腺癌的数据集;基因列表给出了在线补充表II)。免疫组织化学分析来验证微分BC-low之间选择的蛋白质的表达和-腺癌(13]。唯一的修改是样本孵化原发性肿瘤抗体蛋白63 (TP63)(2μg·毫升−1;圣克鲁斯生物技术、圣克鲁斯、钙、美国)和甲状腺转录因子- 1 (TTF-1)(3μg·毫升−1;美国DAKO Carpinteria, CA)为2 h 37°C。商用正常的肺和肺鳞状细胞癌组织样本(我们以下Inc .,罗克维尔市,医学博士,美国)被用于比较分析。
统计分析
所有分析,除了微阵列数据,进行使用SPSS统计软件包(SPSS . n:行情)、芝加哥,美国)。我之间的关系BC -和NKX2-1基因表达分析在初选中腺癌组使用皮尔逊相关分析。组织之间的关系是使用卡方或Mann-Whitney测试评估。微阵列数据的分析使用GeneSpring版本7.3.1早些时候规定执行。
结果
气道BC签名丰富在肺腺癌
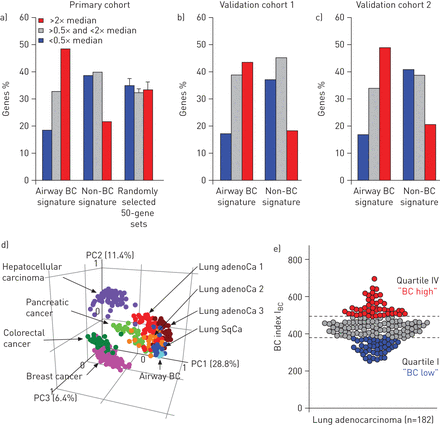
提供全面对气道BC分子特性的表达在肺腺癌,公元前862 -基因的表达气道签名(在线补充基因列表我)进行了分析。公元前862年气道的特征基因,420名(48.7%)在肺腺癌基因表达的高度(所有基因表达水平中值的两倍以上),而只有118人(22%)的544个non-BC签名基因(在线补充基因列表2)和< 35%的基因在随机选择的基因集在肺腺癌高度表达的基因(图1一个)。相比之下,< 20%的BC-signature基因导致了较低的基因表达在肺腺癌(表达水平低于中位数的一半基因)比> 35%的non-BC基因和随机选择的数据集。公元前浓缩的签名在肺腺癌基因验证使用两个独立的组(图1 b和c)。所有三个组相结合的分析显示显著富集的公元前气道签名基因在肺腺癌高度表达的基因与non-BC基因(p < 0.0006)与随机选择的基因集(p < 0.02)(在线补充表III)。
呼吸道表达基底细胞(BC)签名基因在人类肺腺癌(adenoCa)。气道BC签名的基因频率,non-BC签名基因和50 862 -基因随机集的基因导致肺adenoCa基因高表达(表达水平的两倍多的中位数表示的基因;红色),较低的基因表达在肺adenoCa(表达水平低于中位数的一半都表达的基因;与中间蓝色)和基因表达在肺adenoCa(剩余肺adenoCa-expressed基因;灰色)组(a)初选14),和验证组b) 1 (15)和c) 2 (16]。有关详细信息,请参阅在线补充表III。d)主成分分析比较各种类型的人类癌和气道BCs表达式的基础上气道BC签名。分析数据集包括肺adenoCa 1 D荷兰国际集团(ing)等。(22)(红色;n = 68);肺adenoCa 2 H欧等。(21)(深红色;n = 40), adenoCa 3 K味道等。(20.)(橙色;n = 40)、肺鳞状细胞癌(SqCa) K味道等。(20.)(深蓝色;从年代n = 18),结肠直肠癌mith等。(18)(深绿色;从L n = 55),乳腺癌u等。(19)(粉色;从C n = 129),肝细胞癌hiang等。(23)(紫色;n = 91),从B胰腺癌adea等。(24)(浅绿色;公元前n = 39)和呼吸道样本健康不吸烟(浅蓝色;n = 4)。每个圆圈代表一个单独的样品。前三个主成分的每分钱贡献(pc)观察到的变化表示。e)肺adenoCa分类为高、低气道BC基因表达者。BC指数(I公元前)是基于数量的气道BC签名基因表达高于中位数水平在肺adenoCa科目(n = 182) (14]。AdenoCa受试者分为BC-high(第四象限;红色),BC-intermediate(四分位数ii iii;灰色)和BC-low(四分位数我;蓝色)亚型。
气道BC签名是调节肺腺癌的一个子集
接下来,我们问及气道BC签名表达的模式在肺腺癌由其他癌或共享相对独特的这种类型的肺癌。主成分分析显示,肺鳞状细胞癌(20.和所有三个肺腺癌的数据集20.- - - - - -22)表现出相似的模式,使用集群接近气道BC样品比结直肠18],乳腺癌[19),肝细胞(23和胰腺24癌症(图1 d)。大多数肺鳞状细胞癌样本显示气道BC基因表达模式相似,而肺腺癌是异构的。
进一步探索肺腺癌的异质性的基础上气道BC签名表达,我公元前已经开发成一个累积基因表达参数。符合上面的主成分分析数据,分析发现显著的异质性肺腺癌患者根据公元前气道签名表达式(图1 e)。基于我公元前BC-high(最高四分位数)和BC-low(四分位数)腺癌亚型识别(图1 e)。
BC-high肺腺癌表现出不同的生物表型
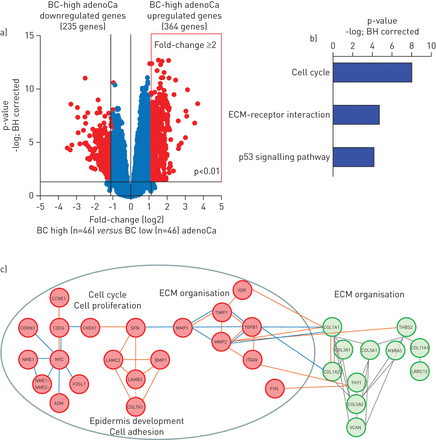
确定在BC-high腺癌生物学途径和模式丰富,我们首先BC-high的全基因组进行比较与BC-low腺癌(图2一个和在线补充基因列表III)。在364个基因上调BC-high腺癌中,有显著的富集的生物学通路与细胞周期有关,细胞外基质(ECM)受体相互作用和p53信号通路(图2 b)。符合路径分析、网络分析BC-high腺癌的调节基因转录网络元素的浓缩透露有关ECM组织(图2 c)。的BC-high adenocarcinoma-enriched中的ECM网络组件的交互合作伙伴BC签名基因调节epithelial-mesenchymal交互和肺组织内稳态,包括转变增长factor-β1 (TGFB1) metalloprotease (MMP) 1和MMP2、组织抑制剂metalloproteases 1 (TIMP) integrin-αV(ITGAV)和维生素D受体(VDR) (图2 c)。
基底细胞之间的差异表达基因(BC) -肺腺癌(adenoCa)和BC-low adenoCa。)火山阴谋的全基因组比较BC-high adenoCa (n = 46)和BC-low adenoCa (n = 46)主肺adenoCa队列(n = 182)。红色:重要基因(褶皱变化≥2;与Benjamini-Hochberg p < 0.01 (BH)校正);蓝色:基因与组之间没有显著差异。b)基因和基因组的京都百科全书通路的分析与黑洞校正显著(p < 0.05)富含BC-high adenoCa调节基因。c)内的分子网络丰富BC-high adenoCa调节基因识别使用加权相关网络分析(格林:中的BC-high肺adenoCa基因内的主数据集)和连接到公元前签名基因调节BC-high adenoCa(红色)使用GCNPro分析工具(橙色:转录调控;蓝色:物理蛋白质-蛋白质之间的关系;有关详细信息,请参阅方法部分)。ECM:细胞外基质; VDR: vitamin D receptor; CCN: cyclin E1; TIMP1: tissue inhibitor of metalloproteases 1; CDKN3: cyclin-dependent kinase inhibitor 3; CDC6: cell division cycle 6; CHEK1: checkpoint kinase 1; SFN: stratifin; MMP1: matrix metalloprotease 1; TGFB1: transforming growth factor-β1; COL1A1: collagen Iα1; THBS2: thrombospondin 2; MMP2: matrix metalloprotease 2; COL3A1: collagen IIIα1; COL5A1: collagen Vα1; MXRA5: matrix remodelling-associated 5; COL11A1: collagen XIα1; NME1: NME/NM23 nucleoside diphosphate kinase 1; LAMC2: laminin-γ2; BMP1: bone morphogenetic protein 1; ITGAV: integrin-αV;COL1A2:胶原蛋白Iα2;LRRC15:富亮氨酸repeat-containing 15;LAMB3: laminin-β3;NME1-NME2:NME1- - - - - -NME2基因readthrough;FOSL1: Fos-like抗原1;COL5A2:胶原蛋白Vα2;ADM: adrenomedullin;COL7A1:胶原蛋白VIIα1;VCAN: versican。
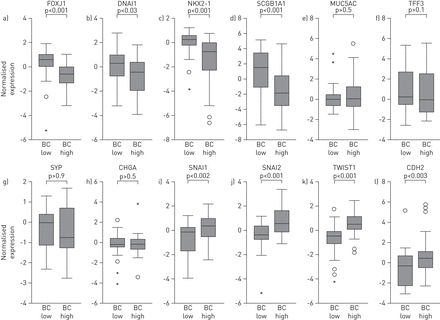
BC-high腺癌显示与分化相关的基因的差别明显对这些小气道上皮的主要细胞类型,包括纤毛细胞(forkhead盒子j - 1 (FOXJ11)和动力蛋白axonemal中间链(DNAI1))和外分泌细胞细支气管(NK2同源框1 (NKX2-1)和secretoglobin 1 a1 (SCGB1A))。典型的分泌粘液细胞和神经内分泌细胞的基因表达这两种亚型之间没有不同。有一个我之间的负相关公元前和NKX2-1基因表达(在线补充图S2)。符合这一观点,有一个趋势的低表达NKX2-1编码TTF-1 BC-high腺癌,尽管它是检测在两种腺癌亚型,与TTF-1-negative鳞状细胞癌(在线补充图S3)。相比之下,分化基因,EMT相关基因的表达,如SNAI1(蜗牛同系物1),SNAI2(蜗牛同系物2),TWIST1(转折基本helix-loop-helix转录因子1)CDH2(N-cadherin) [26),是上调BC-high,与BC-low相比,腺癌(图3)。基因与其他肺癌亚型,包括肺小细胞癌,如编码p53, retinoblastoma-1 L-MYC,之间没有差异表达BC-high和BC-low腺癌亚型(在线补充图S4)。
基底细胞differentiation-associated分子的表达模式的例子(BC) -腺癌而BC-low腺癌。纤毛细胞基因:forkhead盒j - 1 (FOXJ11)和动力蛋白axonemal中间链(DNAI1);外分泌细胞细支气管(克拉拉细胞)基因:NK2同源框1 (NKX2-1)和secretoglobin 1 a1 (SCGB1A1);mucin-producing分泌闲暇的基因:粘蛋白5 ac (MUC5AC)和三叶草因子3 (TFF3);神经内分泌细胞基因:synaptophysin (SYP)和chromogranin (CHGA);基因与epithelial-mesenchymal转型:蜗牛同族体1 (SNAI1),蜗牛同族体2 (SNAI2),扭转同族体1 (TWIST1)和N-cadherin (CDH2)。在所有的面板,日志2改变了正常基因表达水平基于微阵列分析显示;每组n = 46。离群值表示的基础上四分位范围(差):圆形,-1.5×差3×差;明星:> 3 < 3×差。
BC-high腺癌表现出积极的临床表型
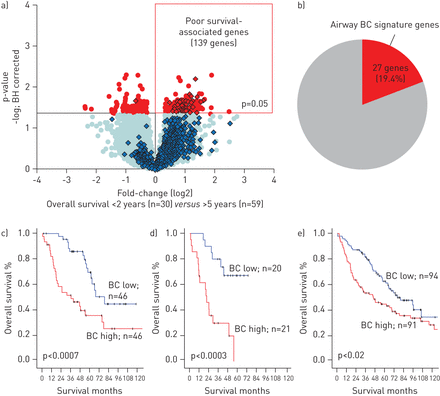
Upregulation细胞cycle-related EMT differentiation-related的基因和抑制基因表达项目BC-high腺癌表明BC签名在肺腺癌的高表达可能与更积极的肿瘤表型有关。与贫穷相关的分析显示,在139个基因在肺腺癌(生存图4公元前),∼20%基因签名基因(图4 b(四)和在线补充基因列表。
气道基底细胞之间的关系(BC)签名表达与肺腺癌患者生存。腺癌患者)全基因组比较< 2年总生存期(可怜的幸存者;n = 30)和> 5年总生存期(n = 59)在原发性肺腺癌组(n = 182)。红色:重要基因(p < 0.05与Benjamini-Hochberg (BH)校正);蓝色:基因与组之间无显著差异;钻石:公元前862气道签名的基因。b)重叠139穷人survival-associated基因(如上所述)和气道BC签名的基因。汉英)kaplan meier分析估计BC-high腺癌患者的总生存期(红色)与BC-low腺癌患者(蓝色)从c c)的主要群体hitaleet al。(14),验证群d) Bildet al。(15)和e)海顿et al。(16]。假定值是由生存率较;每组中个体的数量。
BC-low腺癌相比,BC-high腺癌是由贫困特征分化(p < 0.001),低频率的影响预后有利的腺癌lepidic模式(以前支气管肺泡癌;p < 0.001),血管侵犯的频率更高(p < 0.004)。在分子水平上,BC-high腺癌表现出更高的频率喀斯特突变和更低的频率表皮生长因子受体表皮生长因子受体突变。符合喀斯特已知突变状态,更smoking-associated腺癌的特征(1,3),有更多的吸烟者BC-high之一,与BC-low相比,腺癌患者(表1)。
符合BC签名的显著贡献给穷人survival-associated基因集(图4 b),个人BC-high腺癌有较短的总生存期相比BC-low腺癌(中位数生存36与79个月;日志等级p < 0.0007) (图4摄氏度)。多元生存分析表明,高表达的气道BC签名是一个独立的预后因素与短生存(风险比为1.59,95%可信区间1.14 - -2.22;p < 0.008) (表2)。
公元前气道签名表达式的预后相关性验证使用两个独立的肺腺癌组(15,16]。BC-high腺癌病例的比例介于36%和28%之间,而25%的主要群体。类似于主群,BC-high腺癌病例相比明显缩短整体存活率BC-low腺癌(图4 d和e)。BC-high腺癌也无病生存期较短有关相比BC-low腺癌(补充图S5)。
BC-high肺腺癌明显不同于肺鳞状细胞癌
公元前气道异常激活的基因已经先前与肺鳞状细胞癌(12]。符合这些观测之前,公元前气道签名的整体表达明显高于鳞状细胞癌与腺癌组(图5)。然而,之间没有显著差异在总体存活率BC-high和BC-low鳞状细胞癌的个人(在线补充图S6a和b)。值得注意的是,尽管公元前的整体表达基因在鳞状细胞癌和腺癌相比,更高的鳞状细胞癌患者的总生存期更长相比BC-high腺癌在分析群体(在线补充图S6c)。
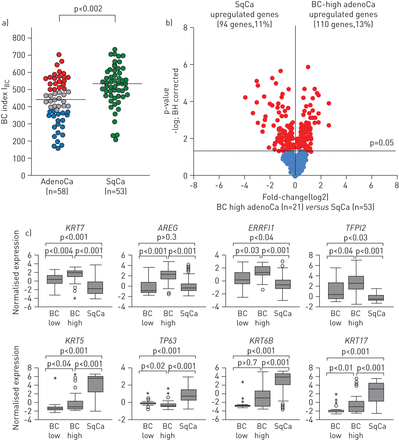
比较分析气道的基底细胞(BC)签名表达肺腺癌(adenoCa)和肺鳞状细胞癌(SqCa)。一)肺adenoCa (n = 58)和SqCa (n = 53)情况下的Bildet al。(15]数据集进行分析。BC指数(I公元前)计算基于adenoCa主题为每个基因的平均水平。红色:BC-high adenoCa;灰色:BC-intermediate adenoCa;蓝色:BC-low adenoCa;格林:SqCa。中间我公元前对于这两种类型的癌症SqCa adenoCa(436和529)突出显示水平线;假定值表示决心通过Mann-Whitney测试。b)火山情节比较公元前气道签名基因的表达(13在BC-high肺adenoCa (n = 21) SqCa (n = 53)从B的数据集ild等。(15]。红色:重要基因(p < 0.05与Benjamini-Hochberg (BH)校正);蓝色:基因与组之间没有显著差异。c)气道BC签名基因差异表达例子BC-high adenoCa (n = 21)与SqCa (n = 53)从B的数据集ildet al。(15]。在所有的面板,日志2改变了正常基因表达水平是基于微阵列分析法。离群值被表示的基础上四分位范围(差):圆:−1.5×差3×差;明星:> 3 < 3×差。KRT7:keratin-7;沙土荒漠:amphiregulin;ERRFI1反馈:ErbB受体抑制剂1;TFPI2:组织因子途径抑制剂2;KRT5:keratin-5;TP63:肿瘤蛋白63;KRT6B:keratin-6B;KRT17:keratin-17。
接下来,我们问及BC-high腺癌股票气道BC-related鳞状细胞癌的分子特征。气道BC签名基因表达的比较BC-high腺癌和鳞状细胞癌发现13%的气道BC基因高表达在BC-high腺癌和鳞状细胞癌的11% (图5 bV)和在线补充基因列表。这表明BC-high腺癌的特点是一个独特的气道BC模式基因区分从鳞状细胞癌亚型的肺癌。在公元前气道BC-high腺癌中表达主要上调keratin-7 (KRT7)、表皮生长因子受体配体amphiregulin (沙土荒漠),反馈ErbB受体抑制剂1 (ERRFI1)和组织因子途径抑制剂2 (TFFPI2)(图5度)。相比之下,公元前经典标记keratin-5 (KRT5),TP63keratin-5B (KRT6B)和keratin-17 (KRT17)鳞状细胞癌中表达明显高于相比BC-high腺癌(图5度)。符合这一观察,免疫组织化学分析显示,TP63蛋白质,通常表示在公元前气道人口,在鳞状细胞癌中,但不是在腺癌亚型(在线补充图S3)。
讨论
越来越多的证据表明,人类恶性肿瘤的生物学异质性是由特定的人群tissue-resident细胞的起源,在一组不同的致癌的影响下改变,导致特定的临床相关的表型在每个单独的组织学类型的癌症(28]。基于这个概念,我们评估人类肺腺癌的临床异质性分子和使用我们最近描述人类转录组的气道BCs,气道上皮细胞的干细胞/祖细胞群(5,13]。这一分析让我们识别一种新型生物肺腺癌的亚型,指定BC-high腺癌,特点是upregulation公元前一组不同的气道的签名基因与肿瘤侵犯的临床和病理特征。
肺癌起源于分子改变气道上皮细胞(1,3,8),纤毛细胞群组成,中间和分泌细胞(大型航空公司和杯状细胞外分泌细支气管细胞小航空公司),BCs,罕见的神经内分泌细胞(4]。根据个人肺癌亚型的独特的形态特征,候选细胞类型提出了每个组织学亚型的起源。肺小细胞癌和大细胞神经内分泌癌被认为起源于神经内分泌细胞(1]。气道BCs被认为是公认的肺鳞状细胞癌的细胞起源的基于知识的气道BCs作为鳞状化生之源,一个相关联的组织学病变的早期步骤发展的肺鳞状细胞癌(1公元前),以及过度的选择标记,如KRT5和TP63肺鳞状细胞癌(29日]。肺腺癌,细胞的起源尚不清楚,尽管外分泌细胞细支气管和II型pneumocytes已经被提议作为外围腺癌的细胞起源,和支气管上皮细胞的表面和腺源更近的腺癌(6]。在鼠标,“bronchioalveolar干细胞”,一个独特的干细胞群外分泌bronchioalveolar管结分享功能的细支气管和肺泡II型细胞,参与发起和传播肺腺癌(11]。然而,人工气道上皮的细胞成分不同于老鼠。在人类中,BCs整个航空公司的存在,而他们几乎没有老鼠的小航空公司(30.气道的作用,阻碍调查BCs肺腺癌发展使用小鼠模型。
在目前的研究中,我们评估肺腺癌的生物学异质性假说在转录水平的肺腺癌的亚型可能来自气道bc。根据公元前气道签名的表达基因,这些数据表明,肺腺癌可分为BC-high BC-low亚型,表现出明显不同的生理、病理和临床特点。数据提供洞察肺腺癌的生物学证明人类肺腺癌的表型多样性可以解释说,至少在某种程度上,通过持续激活基因表达项目或多或少与气道BCs有关。
相关的分子模式BC-high与BC-low腺癌还提供见解的激活机制,可能导致气道BC课程在肺腺癌的一个子集。首先,有一个更高的频率喀斯特突变BC-high腺癌。协会喀斯特与干细胞/祖细胞突变报道关于肺癌的发展。内胚层祖细胞与喀斯特突变表现出增强的扩散,无法区分和维持干细胞特性在体外(31日]。这些数据支持这一概念,BC-high腺癌可能是来自气道BCs携带喀斯特突变与吸烟协会(1,3]。相比之下,BC-low腺癌被更高频率的特征表皮生长因子受体突变。这与先前的观察是一致的表皮生长因子受体突变是更频繁的在不吸烟的腺癌患者3)和相关的分化模式称为TRU,高表达的基因的典型外分泌细支气管和肺泡II型细胞,如蛋白质编码TTF-1和表面活性剂(7]。
第二,BC-high肺腺癌在转录途径丰富和网络相关的ECM组织与各种交互BC签名基因编码的重要监管机构在肺组织稳态过程,包括TGFB1,MMP1,MMP2,TIMP2(组织抑制剂metalloproteases 2),ITGAV和论述表皮,以及相关的网络开发、细胞粘附、细胞周期和增殖。鉴于BCs的解剖位置立即在基底膜,有可能是BCs可能导致肺腺癌的发病机制ECM内稳态的调节和epithelial-mesenchymal交互。激活不同的生长因子信号机制,包括那些有关TGFB1和/或调解通过激活epithelial-mesenchymal矩阵metalloprotease和整合素信号的接口,可以负责浓缩的细胞粘附和细胞cycle-related网络,并有助于更激进的肿瘤特征观察BC-high肺腺癌。
第三,BC-high分化模式的比较分析与BC-low肺腺癌相关基因的差别表明对这些纤毛和BC-high外分泌细支气管细胞分化腺癌伴有EMT转录的激活计划,包括诱导转录因子,如SNAI1 /蜗牛,SNAI2 /蛞蝓,TWIST1 CDH2 [26]。激活EMT的计划被认为是一个重要的过程促进癌症入侵和转移(32]。符合这个概念,BC-high腺癌表现出更高频率的血管侵犯和淋巴结转移。此外,EMT报道生成细胞致瘤的特征(33]。本研究加强了EMT之间的关系和组织干细胞在肺腺癌的背景下发展。
最后,通过鳞状细胞癌相比,BC基因也是高度表达,我们发现,BC-high肺腺癌展品upregulation BC签名的一套独特的基因,包括EGFR通路相关的基因,如沙土荒漠和ERRFI1。EGFR通路富集在气道BCs [13)和吸烟能激活表皮生长因子受体信号在肺上皮细胞表皮生长因子受体突变,诱发细胞过程与肺癌相关的开发(34]。
虽然基因导致BC-high adenocarcinoma-enriched分子途径并不被称为经典cancer-driving致癌基因,了解他们的小说发展的互动是很重要的治疗策略,旨在调控肿瘤细胞的生存和生长,例如,使用合成杀伤力的方法。这些策略可能特别有利于BC-high肺腺癌,这是与高频率的关联喀斯特突变,没有有效的开发了具体的有针对性的方法(3]。目标之间的相互作用的一些BC-high adenocarcinoma-enriched基因,比如致癌基因MYC和细胞周期蛋白依赖性激酶,最近显示诱导治疗相关合成杀伤力积极BC-like乳腺癌[35]。此外,基于知识的生存、生长和分化的BCs是依赖于他们的附着力(ECM组件36)和ECM-related BC-high腺癌基因是丰富,有可能是针对ECM基因可能代表一个额外的方法诱导合成杀伤力交互BC-high腺癌。
在一起,本研究确定了一部小说,BC-high人类肺腺癌的亚型,与一组不同的气道BC签名基因的激活,并提供transcriptome-based证据支持这一概念,这咄咄逼人的子集人类肺腺癌可能源于公元前气道人口。
确认
我们感谢m . Ladanyi(纽约纪念斯隆-凯特琳癌症中心,纽约,美国)提供MSKCC腺癌样本,j . Salit(威尔康奈尔医学院,纽约,纽约,美国)支持微阵列分析和n·穆罕默德(威尔康奈尔医学院)帮助在准备这个手稿。
脚注
可以从本文的补充材料www.www.qdcxjkg.com
支持声明:这些研究支持,部分美国国立卫生研究院的拨款P50 HL084936 T32 HL094284和UL1 RR02499,和斯塔尔基金会/斯塔尔癌症财团。r . Shaykhiev支持,部分帕克b·弗朗西斯基金会。
利益冲突:没有宣布。
- 收到了2012年9月11日。
- 接受2013年1月21日。
- ©2013人队