摘要
在目前的研究中,我们已经开发了一个在体外建立区分正常肺细胞与肺癌细胞的三维模型,以研究肺癌的发生机制。
利用重建的富层蛋白基底膜(Matrigel),我们能够培养正常的人支气管上皮细胞和恶性细胞亚群。这两种细胞类型可以很容易地通过正常细胞在Matrigel中表达结构和功能分化的表型的能力来区分。人支气管上皮细胞单细胞包埋在Matrigel中,可形成多细胞球形集落,最终大小接近真腺泡原位.成熟球体切片显示中央管腔被极化上皮细胞包围。相反,恶性细胞、细胞系和肺活检对基底膜无腔形成反应。
这些结果证明了在体外腺瘤模型可用于支气管癌基因的研究。事实上,这些发现可能为快速检测区分正常支气管上皮细胞和恶性支气管上皮细胞提供了基础。
综上所述,三维肿瘤支气管上皮泡样球是一种新颖的方法在体外进一步研究导致肺癌的病理生理功能。
摘要
三维肿瘤支气管上皮腺泡样球是一种新发现在体外模型来调查导致肺癌的变化http://ow.ly/o8eDu
简介
肺癌是全世界癌症相关死亡的最常见原因。大多数人类癌症发生于上皮细胞和组织。在已确诊的肺癌中,80%为非小细胞肺癌(NSCLC),包括腺癌、鳞状细胞癌和大细胞癌[1].在过去的几十年里,尽管许多肿瘤抑制基因和癌基因已经被发现,但大多数非小细胞肺癌患者通常在肺癌晚期被诊断出来,并在没有成功治疗的情况下死亡[1- - - - - -3.].肺癌最常见的组织学亚型是腺癌,在大多数国家几乎占所有肺癌的一半[4,5].
为了将基础细胞研究的发现转化为临床应用,基于细胞的模型需要概括器官的三维组织和多细胞复杂性,但同时需要适应系统的实验干预。细胞外基质是正常内稳态和组织表型的关键调节因子[6].细胞在培养过程中会丢失重要的信号在体外在二维塑料基底上。许多这些关键的微环境线索可以通过三维培养来恢复[7].已经证明,在非恶性细胞中的信号转导途径在三维培养中是集成的,在细胞单层培养时没有观察到的方式。例如,在用各种信号抑制剂处理的乳腺癌细胞中,β1整合素和表皮生长因子受体的表达和活性相互下调,但仅当在三维基质上培养时[8].然而,由于缺乏足够的方法来区分培养中的正常细胞和转化细胞,研究人类支气管肿瘤发展的早期事件的努力受到了阻碍。上皮组织具有几种不同的显微特征,如极化形态、细胞与细胞之间的特殊接触以及附着在基底膜上。大多数内部上皮器官都是由排列在中央腔内的单分子极化细胞组成[9],它可以是球形的,形成腺泡,也可以像管子一样,形成分枝的管状树。所有这些特征都是正确控制细胞增殖、存活、分化和分泌所必需的[10].这种完整有序的结构在上皮性肿瘤发病过程中被破坏。先前对原发性人类肿瘤组织和肺上皮肿瘤动物模型的研究提供了有关肺癌形成的遗传事件的信息。尽管这些方法对于理解肺上皮肿瘤至关重要,但对于研究肿瘤形成过程中涉及的生化和细胞生物学途径,特别是早期肿瘤发生的机制,它们相对难以处理。到目前为止,参与致癌转化的分子信号机制主要是在二维单层上进行研究。然而,由于二维单层细胞不概括上皮的腺结构在活的有机体内,它们并没有提供一个最佳的系统,以充分了解正常细胞和早期肿瘤形成过程中增殖、细胞死亡和分化的调控。因此,从单个细胞到有序极化腺结构的形成机制仍未得到二维细胞单层培养系统的回答。因此,我们使用了正常和癌症人类支气管上皮细胞(HBECs)的三维培养模型。不同的研究使用从Englebreth-Holm-Swarm肿瘤中提取的重组Matrigel (BD Biosciences, Franklin Lakes, NJ, USA),由层粘连蛋白、IV型胶原蛋白和隐动蛋白组成,在乳房三维培养中研究人类上皮细胞的形态[11],肠[12,13],胰腺[14,15]和转移性肿瘤细胞[16].来自啮齿动物气道远端区域的肺上皮细胞也显示在Matrigel [17,18]以及最近的正常HBECs [19].在他们的研究中,Wuet al。[19]的研究表明,正常的人类支气管上皮细胞在基质上生长时可以分化成三维球体。Franzdottiret al。[20.]的研究结果也表明,人支气管上皮细胞系在三维培养中可被内皮细胞诱导形成分枝状支气管肺泡样结构。之前的一项肺癌研究使用了一个稍微不同的三维模型,胶原凝胶模型[21,也有报道。然而,其他人已经证明了这一点[21在胶原蛋白中,正常细胞和肿瘤细胞都只形成松散的聚集体,细胞间接触很少或没有接触,通常表现出成纤维细胞样的生长模式。相比之下,Matrigel强烈支持正常和球形的生长和分化。Matrigel公司的三维有机型培养系统已被用作强大的细胞模型,用于在生物学相关的背景下和高通量方式下研究癌症基因和通路的功能[10,22],但奇怪的是肺里从来没有。
本文描述了用Matrigel在三维基底膜培养中肿瘤HBECs的生长。通过比较正常和恶性细胞系的三维结构,我们能够区分正常和恶性的人支气管细胞。该系统还可用于定义分化标记物,并勾画转化试验或肿瘤前病变的早期变化。因此,我们的三维HBEC培养为检查肺癌中的生物活动提供了适当的结构和功能背景,也为发现负责将单个细胞组织成有序极化腺结构的机制和信号通路提供了基础。
材料与方法
扩充和详细的材料和方法请参考在线补充材料。
抗体和试剂
我们使用商业基质(Matrigel)进行有机型分析。这些研究中使用的一抗来源如下:β-catenin (BD Biosciences), p63(克隆4A4;Santa Cruz Biotechnology, Santa Cruz, CA, USA), aved-caspase 3 (Asp175) (Cell Signaling, Danvers, MA, USA), mucc 5B (Sigma-Aldrich, St Louis, MO, USA),溶菌酶(AZGP1;Sigma-Aldrich)和β-微管蛋白IV(克隆ONS.1A6) (Sigma-Aldrich)。每个一抗按1:250的稀释倍数使用,二抗按1:500的稀释倍数使用。使用的二抗如下:alexa -氟-488-和alexa -氟-546-偶联抗小鼠和兔igg (Molecular Probes/Invitrogen, Grand island, NY, USA)。本研究使用的试剂为二氨基苯吲哚(DAPI) (Sigma-Aldrich)和多聚甲醛(Sigma-Aldrich)。
结果
基底基质中正常HBECs和癌细胞的有机培养
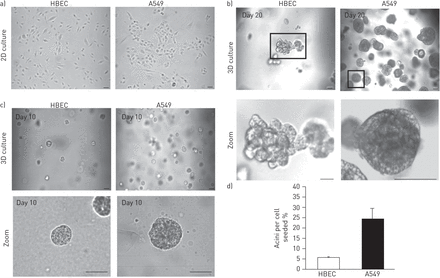
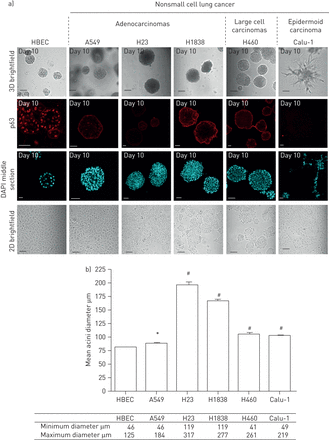
我们首先定义了正常HBECs在两种不同条件下的行为:在组织培养塑料上进行二维培养(图1一个(左图)和在Matrigel上进行三维培养(图1 b,左面板)。HBECs在二维单层培养中呈指数增长(图1一个),如上文所述[19].然后将细胞作为单细胞嵌入到Matrigel基质中(图1b和c,左面板)。在培养的10天内,基质中的细胞形成了几乎均匀的球形菌落(图1 c,左面板)。与腺泡相似在活的有机体内球体之间的小连接管道的出现进一步证实了(图1 b,左面板)。相比之下,在二维单分子层中生长的细胞不会形成球体,并且在细胞衰老之前只生长了几代(图1一个,数据未显示)。由于肺癌最常见的组织学亚型是腺癌,我们分析了腺癌(A549)细胞在类似条件下的生长模式。A549细胞在两种条件下均能在二维单层培养(图1一个,右侧面板),在矩阵内(图1b和c,右面板)。然而,与HBECs相比,HBECs在三维培养中晚时间点分化(图1 b(左图),A549仍保持腺泡状(图1 b,右面板)。这些数据表明,与A549癌细胞相比,HBECs能够分化形成形态明显不同的结构(图1 b).此外,与HBECs相比,基质中的A549细胞系形成了泡珠数显著增加的球体(图1 c).
正常和恶性支气管上皮细胞(HBECs)的有机培养。在二维(2D) (a)和三维培养(3D) (b)两种不同培养条件下培养的HBEC与相同条件下培养的A549细胞在第20天的相位对比。c)培养10天后3D场的代表图片。d)对HBECs和A549细胞进行3D培养10天后,每个细胞形成腺泡的百分比进行量化。比例尺=50 μm。
基质中正常细胞和癌细胞的分化
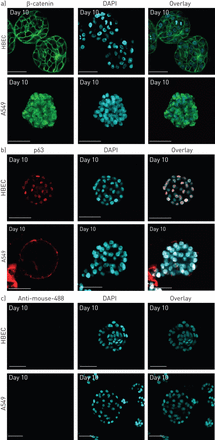
基质中正常细胞(HBEC)和癌细胞(A549)的行为被广泛用于描述组织(腺细胞)极性的标记进一步确定,例如细胞-细胞连接标记β-catenin的基底侧表达。共聚焦分析显示HBEC腺泡菌已形成细胞-细胞连接复合物(图2一个(上图),而A549腺泡蛋白则破坏细胞-细胞连接(图2一个,下面板)。人气道上皮基底细胞表达核蛋白p63,其他气道上皮细胞不表达[20.].HBEC腺泡呈p63极化核尖表达(图2 b,上面板)。相比之下,A549腺泡在细胞核中不表达该标记物(图2 b,下面板)。Alexa-488抗体的特异性在图2 c.同时,我们探索了这两个标记在二维单分子层中的定位和表达(在线补充图S1)。HBEC和A549表达β-catenin,但HBEC和A549细胞之间的细胞连接标记定位不同(在线补充图S1a)。与HBEC细胞相比,A549细胞中β-catenin的膜染色更为明显,HBEC细胞中只有少数细胞表达β-catenin的膜定位(在线补充图S1a)。基底细胞标记物(p63)在HBEC中以不同的表达强度表达(在线补充图S1b,上图),而在A549中除了极少数细胞外几乎完全不存在(在线补充图S1b,下图)。
人支气管上皮细胞(HBECs)产生的腺泡与癌症(A549)细胞系相比的免疫荧光。经a) β-catenin细胞连接标记物(绿色)和b) p63基底细胞标记物(红色)免疫染色的腺泡共聚焦横切面;c)用二氨基苯吲哚(DAPI)反染细胞核。c)阴性对照切片仅用二抗(Alexa-488)染色。图像代表了培养第10天的大多数腺泡。比例尺=50 μm。图像由尼康Eclipse 2000-C1共聚焦显微镜获取(尼康,东京,日本)。
腺泡类似于呼吸道腺体的分泌物
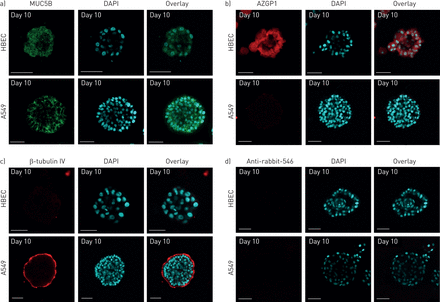
进一步鉴定分化后的腺泡细胞,并与在活的有机体内我们比较了MUC5B(一种粘膜下腺细胞标记物)的表达(图3) [23]、AZGP1(腺浆液细胞标记物)和β-微管蛋白IV(纤毛细胞标记物)[24].正如W所描述的uet al。[19],在HBECs中,MUC5B和AZGP1一般分布在小球管腔内悬浮的管腔细胞中,部分分布在根尖膜(图3a和b,上面板)。A549也表达粘膜下腺细胞标志物MUC5B (图3,下面板)。与HBEC相比,A549细胞系中未检测到腺浆液细胞标记物AZGP1 (图3 b,下面板)。如先前报道[19],在HBEC分化腺泡中未检测到β-微管蛋白IV (图3 c,上面板)。相比之下,该纤毛细胞标记物在与基质接触的A549细胞基面表达(图3 c,下面板)。球形边缘的这种染色表型已经在支气管细胞中报道过,细胞角蛋白14和β4整合素Franzdottiret al。[20.].Alexa-546抗体的特异性在图3 d.在二维单层培养中,以与三维基质培养相同的方式,MUC5B(在线补充图S2a)在两种细胞系中均有表达。与三维培养相比,AZGP1(在线补充图S2a)和β-微管蛋白IV(图S2a)标记在二维单层培养的两种细胞系中均有表达。
人支气管上皮泡泡的免疫荧光染色。在Matrigel上培养人细支气管上皮细胞(HBECs)和癌症细胞(A549),并用a)黏蛋白5B抗体(MUC5B)(绿色)、b)溶菌酶抗体(AZGP1)(红色)和c) β微管蛋白IV抗体(红色)进行染色。d)阴性对照切片仅用二抗(Alexa-546)染色。每个抗体的核与二氨基苯吲哚(DAPI)共染色(蓝色)。比例尺=50 μm。图像由尼康Eclipse 2000-C1共聚焦显微镜获取(尼康,东京,日本)。
基质中A549与HBEC生长调控的差异
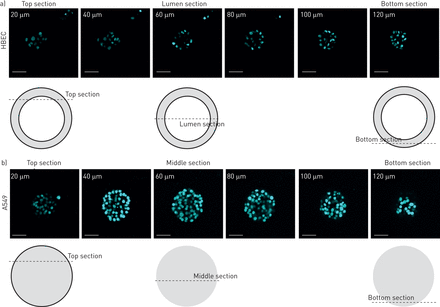
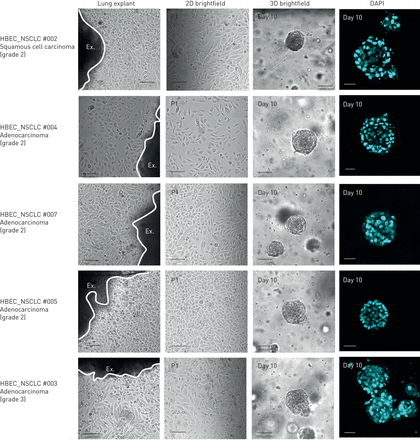
在培养的早期阶段,细胞形成被基质包围的簇。随着培养的进行,每个腺泡内出现了两个不同的细胞群:与基质接触的外层周围的极化细胞和包括内部区域的非极化细胞。随着进一步的培养,这些内部细胞经历细胞死亡和清除,导致腔的形成。HBEC细胞组织成囊状结构,其中包含一个球形细胞层,包围中央腔(图4).细胞凋亡与空化或腔腔形成过程有关,在几个三维球体模型中,固体细胞团中[25- - - - - -28].大多数腺上皮性肿瘤(乳房,前列腺,肠道,等.)是腔内空洞的缺失。许多类型的乳腺癌病变,如导管癌原位,其特点是腺泡组织丧失及腔隙充盈[29].然而,目前尚不清楚我们是否可以将这些观察扩展到肺癌细胞。为了评估与A549细胞相比,HBECs的管腔发育情况,使用DAPI作为核标记,在20 μm切片上通过腺泡监测共聚焦z-stack成像(图4).在HBECs中,观察到每个腺泡内的两种细胞群:与基质接触的外层和与基质缺乏接触的内部子集(图4).我们还观察到HBECs可以很容易地与A549细胞区分开来,因为A549细胞充满了管腔(图4 b),而HBECs则封闭腔内(图4).在几种上皮细胞类型中,细胞凋亡有助于腔的形成;的确,在发育中的唾液腺腔内存在凋亡细胞[27]及犬肾囊肿[30.],以及乳腺球状体[25,28,31].正如Wuet al。[19],我们已经在三维培养中培养细胞13天,以便能够检测caspase-3的激活。通过cleaved activated caspase-3染色检测腔隙中发生凋亡的HBECs (图5、上板和中板)。相比之下,A549细胞没有形成中空腔(图4 b), caspase-3染色阴性(图5,下面板)。这些结果表明,HBEC细胞在形态发生过程中发生了管腔凋亡,A549细胞失去了这种分化能力。我们进一步报道了三维细胞培养模型系统的发展和形态特征,利用5个肺NSCLC细胞系(在线补充表S1)。我们测试的腺癌和大细胞未分化癌细胞产生了大球体,缺乏中空腔(图6,三维亮场),而表皮样癌细胞系形成星状结构(图6,三维亮场),其特征是链细胞的迁移。我们也确认了其他恶性细胞(H23, H1838, H460和Calu-1) (图6)、A549细胞的p63和DAPI染色模式(图2 b而且6),尽管在二维单层培养中有一些明显的形态模式(图6,二维brightfield)。HBECs的最终平均直径约为82.81 μm,癌细胞A549、H23、H1838、H460和Calu-1的最终平均直径分别为87.04 μm、196.3 μm、167.2 μm、103.9 μm和103.1 μm (图6 b).HBECs腺泡的平均直径与先前Wuet al。[19].不同类型的癌细胞形成较大的腺泡,达317 μm,均充满腔。因此,这两个标准(腺泡大小和填充腔)可以很容易地区分正常细胞和NSCLC肺癌细胞。为了进一步从直接来自肺活检的细胞系中确认这些结果,我们从新分离的五种不同肺癌的人类活检中培养了原发性HBECs。图7显示细胞从外植体在培养3-4周内生长(图7,肺外植体柱)。二维亚文化(图7通过细胞角蛋白14和18染色(数据未显示)和三维Matrigel生长进行验证。在10天内,我们亦在五个测试样本中观察到球体的形成(图7、三维亮场和DAPI面板)。
人支气管泡泡内腔的形成。a)人支气管上皮细胞(HBEC)泡泡与b) A549泡泡的代表性共聚焦显微成像。连续共焦z型堆显示到第13天的腺泡。三维生长的腺泡从上到下,用二氨基苯吲哚染色核。覆盖在每个部分上的原理图说明了所述光学部分相对于所述z设在。球面结构的顶部和底部看起来像一片细胞,因为光学部分切过球面的表面轮廓。相比之下,中间部分看起来像一个环,因为该部分穿过空心腔。比例尺=50 μm。
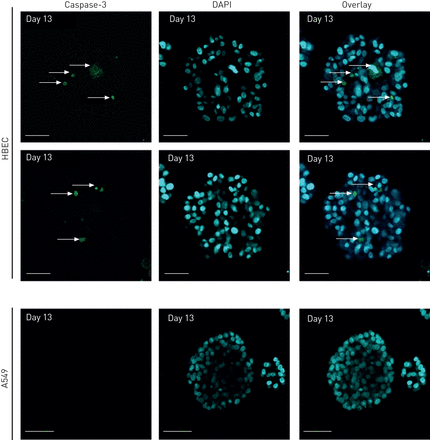
凋亡在人支气管上皮细胞(HBECs)的管腔形成过程中,而不是在A549癌细胞。细胞在Matrigel上培养13天,用激活caspase 3的抗血清免疫染色(绿色)检测细胞凋亡,用二氨基苯吲哚(DAPI)显示细胞核(蓝色)。箭头代表caspase阳性细胞。比例尺=50 μm。
上皮性肺癌细胞腔内凋亡的抑制作用。a)用二氨基苯吲哚(DAPI)染色所示细胞类型(人支气管上皮细胞(HBEC)、A549、H23、H1838、H460和Calu-1) 10日龄结构,显示细胞核(蓝色)和p63(红色)。通过每个结构的中间的代表性共焦截面(管腔切片)显示(DAPI,中间面板)。在三维(3D亮场)和二维(2D亮场)生长的细胞的相位对比显示。比例尺=50 μm。b) HBECs中腺泡直径与非小细胞肺癌细胞的比较。细胞在Matrigel上培养13天。使用EZ-C1 3.9 Nikon软件(Nikon, Tokyo, Japan)拍摄腺泡共焦图像并测量其直径。最大和最小腺泡大小(±扫描电镜)为每个细胞系报告。采用双尾t检验进行统计分析。p值<0.05为差异有统计学意义。#: p < 0.0001。*: p < 0.05。
三维(3D)腺泡形成与新分离的细胞从肺活检的非小细胞肺癌(NSCLC)患者。原代人支气管上皮细胞(HBECs)刚从五个肺癌细胞的人体活检组织中分离出来(肺外植体,最左栏)。在二维(2D亮场)中进行传代培养,然后在3D Matrigel中将细胞生长为球体(3D亮场)。通过每个结构的中间的代表性共焦截面(管腔切片)显示(二氨基苯吲哚(DAPI)面板)。比例尺=50 μm。使用EZ-C1 3.9 Nikon软件(Nikon, Yokyo, Japan)拍摄腺泡共焦图像,测量其直径。
讨论
对肿瘤特异性标记物的研究一直很激烈,这些标记物可用于诊断和治疗策略的发展,特别是肺癌。几种分化标志物,如细胞角蛋白19,已被研究用于肺腺癌的检测。然而,它们大多不是针对肺腺癌的,而是针对一般的上皮细胞或上皮细胞来源的癌症。即使是组织特异性的分化标志物,如表面活性剂肺相关蛋白A2、B、C和甲状腺转录因子-1,敏感性和特异性也不够高,无法用于分子诊断[32,33].因此,寻找特异性更高、灵敏度更高的标志物用于肺癌分子诊断是非常必要的。
在这里,我们使用了正常HBECs和NSCLC细胞的三维培养模型(在线补充表S1)。当在细胞外基质中培养时,HBECs重新获得形成腺泡样结构的能力,呈现中空腔。据推测,在管腔形成过程中死亡的细胞缺乏与基底膜的直接接触,这使得它们容易受到anoikis的影响,anoikis是上皮细胞在基质脱离时经历的一种程序性细胞死亡[34,35].与腺泡相似在活的有机体内球体之间出现连接的小导管证实了这一点(图1 b)、切面球体内腔的形成(图4)及黏液及浆液细胞标记物(图3a和b).这些结构概括了呼吸道细胞分化的许多特征[36].因此,我们可以为培养中的正常支气管组织定义标记物(在线补充表S2)。相比之下,我们还发现NSCLC细胞始终无法对这种微环境做出适当的反应。其他工作人员使用基质来区分正常和人类乳腺癌细胞[37]:研究显示,人类乳腺肿瘤细胞系在三维培养中不形成腺泡;相反,它们发展成为分化有限的非极化簇。在我们的实验中,所有NSCLC肺上皮细胞(A549、H1838、H460、H23和Calu-1)和新从肺活检中分离出来的三维生长的细胞都可以很容易地与正常的HBECs (无花果6而且7).总之,我们已经证明,现在可以很容易地从大多数临床含肿瘤的NSCLC标本中建立三维腺泡。
我们的分析显示,肺癌细胞和肺正常上皮细胞在三维培养中存在显著差异,这表明肺癌细胞与肺正常上皮细胞相比,基因普遍特异地上调或下调。随后,与肺正常上皮细胞相比,评估了五种标记物在癌细胞中被差异调节,因此可能是肺癌特异性肿瘤标记物(在线补充表S2)。迄今为止,已有几个基因被用于肺腺癌细胞的检测,如细胞因子19和癌胚抗原[38,39].然而,这些标志物检测肺腺癌细胞的敏感性和特异性都不够高,不能作为单一分子标志物应用于临床。因此,未来进一步评估本研究中使用的五种标志物与几种已知标志物联合使用肺癌细胞检测的特异性和敏感性将非常重要。在图2而且3.在Matrigel上,HBECs分化为极化腺泡细胞,表达β-catenin(细胞连接标记)、p63(基底细胞标记)、MUC5B(粘液细胞和分泌标记)、AZGP1(浆液细胞和管腔分泌标记),但不表达β-tubulin IV(纤毛标记)。A549细胞表达β-catenin (图2一个), p63 (图2 b)及MUC5B (图3),但与HBECs相比,定位不同(图2a和图b,3).相比之下,与HBECs相比,A549细胞不表达AZGP1 (图3 b)或p63 (图2 b),但β-微管蛋白IV (图3 c).p63对腺泡形成的影响已被Senooet al。[40],他们在该研究中使用了缺失p53的乳腺上皮细胞,发现缺失p53的细胞产生了球体,但数量不到野生型的十七分之一。他们提出,p53缺失克隆的三维生长的减少表明p63在上皮细胞的增殖速度或整体增殖潜力中发挥作用,而不是上皮细胞分化。
总之,在正常和NSCLC细胞系之间观察到的差异(在线补充表S1),无论是在分化动力学和凋亡的外观(图5而且6),通过腺泡标记物的表达,以及直接来自肺活检的生物学相关结构的形成,表明该模型将为研究肺癌病理通路中的重要机制提供强大的工具。因此,我们的实验已经说明了正常细胞和肿瘤细胞在三维培养中的对比,尽管当相同的细胞作为二维单层培养时,细微的表型差异是明显的(图6,二维brightfield)。蛋白质组学方法已经证明了这一点[41传统的单层培养很难概括肿瘤三维生长的特征在活的有机体内.多细胞球形培养是单层培养和肿瘤之间的中间产物在活的有机体内与细胞增殖、分化和细胞环境更密切相关的情况,即。细胞-细胞接触和不同的生长区域。球体比单层培养更好地反映了肿瘤的组装,因此可能提供了一种先进的模型系统在活的有机体内肿瘤。例如,小鼠EMT6癌细胞在荷瘤小鼠治疗后表现出耐药,在多细胞球体中再现了这种耐药表型,而在单层培养中则没有[42].因此,AZGP1和β-tubulin IV在二维上的表达不同也就不足为奇了(在线补充图S2b和c)。与三维(在线补充图S3b和c)。使用三维模型增强了我们对中空腔的形成和维持及其在癌细胞中的破坏的癌症生物学的理解。在人类肺上皮组织的背景下,这一生理相关模型的实施,使内在细胞调节途径的研究成为可能,也为间质室在指导上皮细胞功能和功能障碍中的作用提供了令人信服的证据。因此,在三维培养中生长的癌细胞腺泡作为实验工具的实用性主要是由于能够分析关键生物学过程的空间和时间方面(如。增殖和凋亡),以及形态发生过程中的信号转导事件。完整的腺结构的破坏,包括顶端-基底极性的丧失和腔隙的填充,是上皮性癌的标志,即使在其早期阶段也是如此,然而对于肺癌形成过程中引起这些变化的机制知之甚少。在三维基底膜培养中,上皮性肺癌腺泡的形态发生为测定癌基因对支气管结构的影响提供了一个生物丰富的系统和适当的结构背景。值得注意的是,研究通过特定基因在三维培养细胞中的过表达或沉默,为在肺上皮细胞中使用功能获得/丧失方法提供了令人兴奋的可能性,从而促进了对支气管结构上的肿瘤抑制因子的分析。
HBECs在基质中的三维培养可形成极化的、生长停滞的腺泡样球体,这概括了支气管结构的几个方面在活的有机体内.综上所述,这样的发展在体外该模型将为从生物学角度深入了解肺癌进展过程中促进支气管结构破坏的机制提供新的机会,并有助于建立一个寻找肺癌新诊断标志物和治疗靶点的机制框架。因此,这项研究说明了从细胞系和新鲜活检标本中提取的三维上皮细胞培养模型的能力在体外肺癌形成早期事件的模拟方法。
脚注
这篇文章有补充资料可从www.www.qdcxjkg.com
支持声明:这项工作得到了来自杰出主席INSERM-Université波尔多(批准号CRE08PREST)和Comité阿基坦法国防癌协会(批准号2012-0038)。
利益冲突:没有声明。
- 收到了2012年7月30日。
- 接受2012年12月22日。
- ©2013人队