摘要
本研究的目的是研究在长期氧疗的低血氧型慢性阻塞性肺疾病(COPD)患者中,氦高氧(HeHOx)是否比高氧(HOx)更能耐受最大和次最大运动量。
在一项双盲研究中,24男性慢性阻塞性肺疾病功能类的全球倡议IV(用力呼气量在1 s 35.2±10.1%预测动脉氧张力和56.2±7.5 mmHg)提交增量和恒定负载循环在70 - 80%最高工作效率而呼吸HOx(60%的氮,40%的氧气)或HeHOx氦(60%和40%氧气)。
除2例患者外,HeHOx均改善了静息气流阻塞和肺恶性膨胀(p<0.05)。HeHOx组24例中17例(70.8%)比HOx组高,21例中14例(66.6%)比HOx组高(p<0.05)。尽管有较高的通气反应,但HeHOx组呼气末肺容积较低(p<0.05)。HeHOx运动时吸氧动力学加快了~ 30%,特别是在残疾和过度充气的患者中。无脂质量是HeHOx高峰值工作率的唯一独立预测因子(r2.= 0.66, p < 0.001);相比之下,任何静息特征或运动反应都与运动不耐受的改善时间无关(p>0.05)。
对于大多数长期依赖氧气治疗的晚期COPD患者,氦是一种有价值的能源辅助物质。
介绍
接受长期氧疗(LTOT)的终末期慢性阻塞性肺疾病(COPD)患者的运动耐量严重降低[1.]运动障碍进一步降低了他们在日常生活中的活动能力,甚至可能与较低的生存率有关[2.]此外,这些患者经常无法以足够高的强度进行运动,以从训练中获得充分的生理益处[3.]因此,人们对评估非药物辅助物以提高氧依赖患者对动态运动的耐受性重新产生了兴趣[4.].
在这种情况下,增加吸入氧(高氧(HOx))已被理解为提高LTOT患者运动耐受性的护理标准[5.]这是有充分证据证明HOx可以降低通气需求、动态性恶性通货膨胀和呼吸困难的发生率[6.,7.]同时加强心脏循环调节以适应运动[8.].最近,向HOx中添加氦(HeHOx)[9–13]为进一步提高这些患者的运动耐受性开辟了一个新的视角。值得注意的是,HeHOx还延迟了动态过度充气和降低了通气驱动力,至少在非低氧患者中是如此[9–13].此外,氦在常氧状态下显著加速氧吸收(v′O2.)动力学[14,15]减少肌肉疲劳[16,这一效应可能与其泄气效应有关,可改善中枢血流动力学和对流氧气输送[14,17].
不幸的是,HeHOx仍然是一种昂贵的气体混合物,与单独的HOx相比,其管理相当繁琐。此外,有报道称运动对氦的反应存在显著的异质性[18,19]而一些对非低氧血症患者的研究明确显示为阴性[20.–22].我们还应该承认,单独使用HOx对低氧患者的运动能力有显著的有益影响[5.],任何补充性干预的效果大小都应该是巨大的,以产生可衡量的差异。尽管H乌桑等[13在严重气流阻塞的患者中,LTOT无低氧血症发生。因此,据我们所知,在这个相当大的患者亚群中,没有研究对比了HeHOx和HOx对运动耐受性的有益影响。
本研究首次对HeHOx和HOx在休息时和运动时低氧血症的慢阻肺患者以及LTOT下增强运动能力进行了头对头的比较。我们假设,与单独的HOx相比,向HOx中加入氦会加速v′O2.动力学,减少动态恶性膨胀,提高对增量和持续负荷锻炼的耐受性。这些假设的证实将为氦和HOx结合作为终末期COPD的助能剂提供新的支持。
方法
主题
51名久坐不动且患有严重至非常严重COPD的男性[23]来自圣保罗医院(巴西圣保罗)呼吸疾病科LTOT门诊部的患者被邀请参与该研究。27名患者因严重心血管合并症、气管造口术、骑自行车的骨肌肉限制、近期病情恶化、药物状态变化(1个月内)或对运动研究缺乏兴趣而被排除在外。其余24名患者没有缺血性心脏病、左心室功能不全(多普勒超声心动图评估射血分数<60%)或严重肺动脉高压(估计收缩肺动脉压<40mmHg)的证据。所有受试者签署了书面知情同意书,研究协议得到了S Paulo大学联邦医学伦理委员会的批准。在线补充材料中提供了关于这一主题的其他方法学信息。
研究协议
这是一项随机、交叉、双盲的研究。在第一次就诊时,患者接受肺功能测试和人体测量。然后,他们被随机分配在第2次和第3次随访时接受HeHOx或HOx,分别进行增量和恒定工作速率(IWR和CWR)测试。在给定的一天,每种混合物的试验间隔60分钟的休息时间。研究方案的详细论证在在线补充材料中提供。
测量
身体成分的评估
用四极电生物阻抗仪(BIA 450生物阻抗分析仪;生物动力学,西雅图,WA,美国)。
肺功能测试
气压表(防止气压表;医疗图形公司(MGC), St Paul, MN, USA)在每次肺量测定前用实验气体混合物(HeHOx或HOx)进行校准。使用代谢车(CardiO)的流量模块进行肺活量测定、最大自愿通气(MVV)和吸气容量(IC)操作(以估计呼气末肺容量(EELV))2.系统;MGC)。静态肺活量(总肺活量(TLC)和残余肺活量)由等容体容积描记术(CPF系统;MGC)和动脉血气(abl330;辐射计,哥本哈根,丹麦)测量患者呼吸室内空气。
心肺运动试验
对气体混合物(HeHOx或HOx)进行了定向通过一个闭合电路到一个120-L乳胶氯丁橡胶气球(道格拉斯袋),然后到一个低阻双向阀的吸气口(2700系列;Hans-Rudolph公司,肖尼,KS,美国)。气压表(预防气压表)串联安装在阀门和面罩上。为了使陪同医生和患者对正在研究的混合物进行盲视,在气瓶前放置了一个屏幕,并指示患者在整个实验过程中避免说话(即。避免吸入氦气时声调的特征性变化)。受试者吸入实验混合物进行呼吸≥每次试验前15分钟,使肺内分布最大化。试验在电子制动循环测功仪(Corival;Lode,Groningen,德国)上进行,转速为50±5 rpm,由心脏控制2.系统(MGC)。在IWR试验中,功率增量速率为5 W·min−1.对所有参与者进行CWR试验,直到耐受极限(Tlim),峰值工作率为70-80%。运动能力极低的病人(即。峰值工作速率<40 W),测试在30 W进行,以确保av′O2.足以进行动力学分析的振幅[24]假设静息TLC在运动期间保持不变,IC的变化反映EELV的变化(TLC–IC)[25].运动诱发的动态恶性通货膨胀的发展被定义为运动期间IC的渐进性降低。患者在IC操作前2分钟使用0-10 Borg评分对呼吸短促和腿力进行评分。在线补充材料中提供了关于这个主题的更多方法信息。
数据分析
由于一些患者对IWR运动极度不耐受,我们对大多数患者(等功率)和峰值功率下诱发反应振幅的最低次最大功率下的生理数据进行了分析。在CWR试验中,在isotime(患者耐受试验的最短时间)和Tlim.动力学分析,呼吸v′O2.每秒对数据进行插值(SigmaPlot 10.0;美国加利福尼亚州圣何塞市Systat软件公司),并通过以下单指数方程进行拟合[28]:
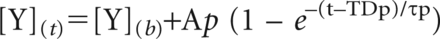
在哪里B和P分别参考基线空载循环和主要成分,A、TD和τ分别是指数响应的振幅、时间延迟和时间常数。整体动力学由平均响应时间(MRT=τ+TD)确定.由于所有患者的血流动力学数据值均未遵循单指数反应模式,因此计算了一半时间。
统计分析
使用SPSS 15.0版统计软件进行数据分析(SPSS,芝加哥,伊利诺伊州,美国)。结果以平均值±表示sd或中值(范围)。然而,意味着±se用于某些图形,以提高可读性。为了对比HOx和HeHOx的运动反应,使用配对t检验(或非参数数据的Wilcoxon检验)。混合设计方差分析模型(split-plot ANOVA (SPANOVA))对比了随时间推移的反应和干预之间的反应。重复测量的总体方差和所有测量相等(球形)对之间的总体相关性采用Mauchly检验,相互相关性的同质性采用Box检验M统计。皮尔森乘积矩相关被用来评估连续变量之间的关联水平。采用逐步向后回归分析建立HeHOx改善运动耐受性的独立预测因子。所有检验的显著性水平均设定为p<0.05。
结果
学科特点
患者在1s内出现严重的用力呼气量(FEV)1.) 49 - 30%预测;n = 13)至非常严重(FEV1.<30%pred;n=11)气流限制[23]、静肺容积增加和慢性呼吸困难(医学研究委员会呼吸困难评分≥3)。与纳入标准所预期的一样,所有患者在休息时均为低氧血症,其中24例患者中有10例(41.7%)为高碳酸血症(动脉二氧化碳张力>45 mmHg) (表1).
HeHOx对肺活量变量的影响
与HOx相比,除两名患者外,所有患者的FEV都更高1.和使用HeHOx强制肺活量(通常分别在100 - 200ml和200 - 400ml范围内增加(两者均为基线的10-25%);p < 0.05)。因此,HeHOx显著增加了最大呼气流量,与容量募集成比例,即。氦增大了最大流量-容积回路。此外,EELV降低,允许更大的潮气量(vT)扩展(数据如在线补充表E1所示)。
HOx患者对渐进运动的反应
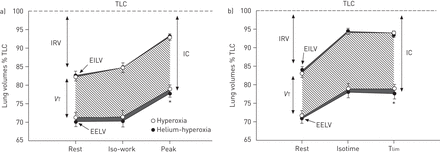
所有HOx患者的最大运动能力均中度至重度下降(峰值工作率<70% pred) [29],与通气储备减少有关(高分钟通气(v′E)/MVV)及EELV进一步增加(表2和图1一个).潮末二氧化碳张力显著增加(P埃科2.)所有患者从休息到运动高峰(表2).呼吸困难、腿部用力以及两者的结合分别是8例患者的限制症状。
根据a)增量(n = 24)和b)常数(n = 21)工作速率试验,高氧和氦高氧对手术肺容量的影响。数据以平均值±表示se.TLC:肺活量;集成电路:吸气量;vT:潮汐卷;IRV:吸气储备容积;EILV:吸气末肺容积;EELV:呼气末肺容积;Iso-work:大多数受试者所达到的最低次最大工作率;Isotime:患者耐受试验的最短时间;Tlim:公差极限。*:在给定时间点,干预间差异p<0.05。
HeHOx对增量运动反应的影响
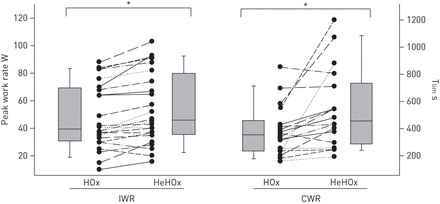
与HOx相比,HeHOx改善了24例患者中的17例(70.8%)的峰值工作率,其中大多数患者显示5- 10-W增加(中位数(四分之一范围)6 W (3-9 W)或基线的9% (6 - 23%);p < 0.05) (表2和图2左面板)。这与较低的二氧化碳排放量有关(v′一氧化碳2.), EELV下降(图1一个),更大vT,减少占空比,更大的平均吸气和呼气流量和更高v′E/v′一氧化碳2.低P埃科2.(表2在线补充图E1)。在等功速率为30 W (n = 19)时,HeHOx的心输出量也更大,这与更大的卒中量相关(表2).HeHOx的主要限制症状(呼吸困难或和/或腿部用力)基本没有改变(数据未显示)。
高氧(HOx)和氦高氧(HeHOx)对增量功率试验中峰值功率的影响(IWR,左;n = 24),并按时进行运动不耐受(Tlim)在一个恒定的工作速率测试(CWR,右;n = 21)。*: p < 0.05。
HeHOx对持续负荷运动反应的影响
由于技术或合作的原因,3名患者没有进行CWR测试。HeHOx增加Tlim21例患者中有14例(66.6%)的观察获益差异较大(109.5 s (20.5-204.8 s)或32.5%(7.3-77.3%)的基线;p < 0.05) (表3和图2右面板)。HeHOx在同时和Tlim与IWR测试中发现的一致,包括较低的EELV(表3和图1 b).值得注意的是,HeHOx导致了更快的速度v′O2.与心输出量相似趋势(p=0.07)相关的动力学(表4).HeHOX对车辆的加速作用v′O2.动力学与低峰有中度相关v′O2.在HOx下,TLC和功能剩余容量较高(r = 0.48-0.61, p<0.05)。
HeHOx改善运动耐受性的预测因素
较高的静态肺体积和更多的脂肪-无质量与HeHOx的峰值工作率改善相关(r = 46-0.72, p<0.05)。在多元回归分析中考虑了薄层色谱和无脂质量;然而,只有最后一个变量仍然是峰值工作速率(r2.=0.61,p<0.01)。相比之下,没有任何感觉神经系统(即。Borg评分)或生理反应与较高的TlimHeHOx;事实上,T的改进lim静息时EELV降低100 - 200ml变化超过5倍(p>0.05)。
讨论
这是首个比较低氧血症COPD患者接受LTOT时纠正运动相关性低氧血症(HOx)的标准疗法与HeHOx在改善运动耐受性方面的疗效的研究。与我们的假设一致,HeHOx组的最大和次最大运动耐量大于HOx组。如前所述非低氧血症患者[10,12,18, HeHOx提高了最大呼气流量率,并降低了EELV约100毫升,尽管在低代谢需求下有较高的呼吸反应,但这种效果在整个运动周期中都保持着。HeHOx也加速了运动中的主要部分v′氧气动力学。这些数据提供了新的证据,表明在HOx中加入氦可以使低氧COPD患者接受LTOT,达到更高的工作速率,并维持更长时间。从临床角度来看,这可能有助于提高患者的灵活性(使用便携式输送系统)和运动训练的耐受性。
人们对使用辅助工具提高严重残疾COPD患者的运动耐受性重新产生了兴趣[30.].这些策略包括无创正压通气等新方法[27和神经肌肉电刺激[31]到“较老”的辅助药物,如补氧剂(HOx) [6.,7.]及低密度气体呼吸(氦)[9–13].在这种情况下,目前的结果是令人鼓舞的,在低氧患者中加入氦对HOx的好处,因为三分之二的患者最大和次最大运动能力进一步提高。然而,尽管HeHOX持续改善了静息气流限制和肺恶性膨胀,但HeHOX在耐力时间增加的幅度上有很大的变异性。这种可变性部分可能与电力持续时间关系的双曲线性质有关[32,这决定了Tlim随着单个工作速率接近渐近线(“临界功率”)而增加[33].值得注意的是,静息生理变量很难预测T的变化limHeHOx。以前的研究表明,HeHOx的任何益处都将在中央气流限制更大的患者中特别观察到[13,34,35],这将允许他们在较低的EELV下保持相同的通气(或更高的通气,如本研究中所示)。然而,在实践中,我们的数据表明,如果HeHOX用于LTOT下的晚期慢性阻塞性肺病患者,其积极作用应在个体患者中明确证明。
关于HeHOx对呼吸系统的生理作用,我们的研究结果证实了E大等[10]症状较轻的患者和H乌桑等[13具有相似肺活量严重程度的非低氧血症患者。我们可以合理地假设,氦气的泄气作用与克服摩擦阻力的较低压力相结合[13]可能与HOx诱发的较低通气驱动有关[3.,4.]减少呼吸的弹性和阻力[6.].阻力性吸气功也可能减少[34,35].事实上,氦气改善呼气流量限制的潜力随着疾病的严重程度和更高的流速而增加[34],即。在本研究中发现的精确条件。尽管HeHOx提高了呼吸反应,但呼吸困难评分保持不变,因此强调了呼吸对个体压-容关系中更顺应部分的重要后果[25].
与之前报道的非低氧患者数据一致[14,15),氦加速v′O2.动力学在过渡到运动。然而,与这些研究相比,这是在相似的动脉氧含量下实现的,这表明对流氧输送改善和/或提高肌肉利用氧的潜力。在这方面,我们不能排除更快的心血管反应的作用,因为HeHOx在伴随加速心输出动力学中有一个明显的趋势。事实上,在增量试验中,HeHOx组的每搏量和心输出量高于HOx组的等功率组。部分心输出量也可能从无负荷的呼吸肌转移到工作的外周肌[27].Louvaris等[35[,例如,最近描述了与室内空气中常氧螺旋线相比,在类似心输出量的情况下,表现出动态恶性膨胀的COPD患者的股四头肌血流增加。此外,是否心输出量介导的脑血流量增加仍有待研究[36]含氦[37会增加这些患者运动时脑氧输送。
本研究的另一个有趣发现是无脂块(腿部肌肉块的一种可能替代物)的独立作用预测患者在改善峰值工作率方面受益于HeHOx的程度。这表明,一旦使用HeHOx改善了通气限制,外周肌肉质量就成为达到更高工作率的限制因素。这一解释与Butcher等[38报告说,更多的高气胀患者在HeHOx特别有效时,神经肌肉表现表明运动停止时出现肌肉疲劳。走路时是否也会这样还不确定。
本研究存在一定的局限性。由于伦理原因,患者在正常缺氧状态下不能进行运动,因为所有患者都在进行LTOT。然而,我们认识到这排除了对HOx的生理效应的分析本质上。作为一项横断面研究,我们无法解决HeHOx是否构成了一种成本效益策略,以改善患者在康复和/或日常生活活动中的表现,这是一个仍有争议的问题[8.,17,19].然而,Tlim在CWR测试中,HeHOx可以使患者继续进行更高水平的训练。最后,尽管在峰值工作率和Tlim在低氧血症患者中,观察到的中位改善接近于在较轻患者中建立的MCID,即。10 W (39]和基线的33%[40),分别。
总而言之,氦在加速过程中增加了HOx的效益v“阿2.在大多数LTOT依赖的晚期COPD患者中,降低手术肺容量,增强最大和次最大运动耐受性。这些发现表明氦对这些患者来说是一种有价值的补充性能量生成辅助物。我们的研究为更大规模的随机试验奠定了基础,以确定HeHOx在改善严重残疾人群日常生活活动能力和肺康复期间的运动耐受性方面的辅助作用。
致谢
作者感谢Brian Whipp (为纪念)和Leonardo Ferreira(佛罗里达大学,Gainesville, FL, USA),以表彰他们对动力学分析的贡献。作者还感谢自愿参加这项研究的患者。Fernando Queiroga Jr感谢美国胸科学会的流行病学、临床和操作研究课程(MECOR)团队在方案设计和数据分析方面的宝贵贡献。
脚注
这篇文章的补充材料可从www.www.qdcxjkg.com
支持声明:本研究由高级管理人员协会(CAPES)(巴西利亚,巴西),美国Fundação de Amparo à Pesquisa do Estado de São Paulo(巴西圣保罗)和Conselho Nacional de Desenvolvimento Científico e Tecnológico巴西巴西利亚(CNPq)()。
利益冲突:未声明任何利益冲突。
- 收到了2012年6月4日。
- 认可的2012年10月25日。
- ©ERS 2013