文摘
最近的分子分型研究表明相互传染的潜在收购途径之一铜绿假单胞菌囊性纤维化患者(CF)。在澳大利亚,只有有限的证据不相关的病人分享无异铜绿假单胞菌菌株。因此,我们调查了时点患病率、分布、多样性和临床的影响铜绿假单胞菌在全国范围内菌株在澳大利亚CF患者。
983名患者参加18澳大利亚CF中心提供了2887痰铜绿假单胞菌隔离型的enterobacterial重复基因间consensus-PCR化验确认通过茎序列类型。人口统计学和临床细节为每个参与者都被记录下来。
总体而言,610名(62%)患者怀有至少一个38共享基因型。大多数菌株在共享小病人从有限数量的集群中心。然而,两个主要基因型,AUST-01 AUST-02,分布广泛,被发现在220年(22%)和173名(18%)患者参加17个和16个中心,分别。AUST-01治疗需求明显大于独特铜绿假单胞菌菌株。
多个集群的共享铜绿假单胞菌菌株在澳大利亚CF是常见的中心。至少有一个主要的和广泛的基因型与医疗利用率增加。纵向研究现在需要确定这些发现的感染控制的影响。
慢性铜绿假单胞菌感染是囊性纤维化的临床恶化主要原因(CF)和预防策略需要帮助病人管理全球(1,2]。尽管大多数CF患者被认为拥有自己的独特的环境压力,最近打字在几个国家研究中心报告无关的病人分享不可区分的基因型,表明相互传染也可能发生(3- - - - - -7]。一些共享基因型与加速肺功能的下降,增加医疗需求,和更大的死亡风险或肺移植3,8,9]。因此,确定共享菌株在更广泛的人群为病人管理有重要意义。
CF中心练习常规分子监测和患者隔离减少了共享的发病率铜绿假单胞菌医药相关的菌株,为进一步间接证据传输(10,11]。然而,这些措施都是有争议的,因为成本和复杂性的12]。这特别适用于成人中心照顾人口老龄化,越来越多的患者并没有感染铜绿假单胞菌(13]。在发展中更严格,潜在的复杂和昂贵的感染控制政策,因此重要的是提高我们的理解铜绿假单胞菌基因型流行,分布和多样性,并确定临床影响病人健康。
到目前为止,所有澳大利亚调查发现证据对CF患者共享一个或多个铜绿假单胞菌压力(4,5,14,15]。一些报告还发现了一个共同的基因型和贫穷的临床结果之间的联系(4,5,10,14,15]。然而,这些研究代表< 25%的澳大利亚CF人口,包括只有6个中心、四个城市和三个主要基因型从澳大利亚的东南角落。有趣的是,这些调查还发现了几个小患者基因型集群共享其他小说。因此,我们的目的是检查时点患病率、分布、多样性和临床的影响铜绿假单胞菌菌株在澳大利亚CF患者。
材料和方法
患者,收集数据和孤立
参与者参加了18个澳大利亚CF中心之一(悉尼儿童医院囊性纤维化诊所,悉尼;悉尼皇家王子阿尔弗雷德医院囊性纤维化诊所;韦斯特米德儿童医院的囊性纤维化治疗中心,悉尼;约翰亨特成人囊性纤维化诊所,纽卡斯尔;约翰亨特囊胞性纤维症儿童医院单位,纽卡斯尔;墨尔本皇家儿童医院的囊性纤维化,墨尔本;墨尔本阿尔弗雷德医院囊性纤维化服务;墨尔本莫纳什大学医学中心囊性纤维化单位,;皇家儿童医院的囊性纤维化,布里斯班;查尔斯王子医院成人囊性纤维化中心,布里斯班; Mater Children’s Cystic Fibrosis Unit, Brisbane; Mater Adult Cystic Fibrosis Unit, Brisbane; Gold Coast Hospital Adult Cystic Fibrosis Centre, Southport; Gold Coast Hospital Children’s Cystic Fibrosis Centre, Southport; The Royal Adelaide Hospital Cystic Fibrosis Program, Adelaide; Women’s and Children’s Hospital Cystic Fibrosis Clinic, Adelaide; Sir Charles Gairdner Hospital Cystic Fibrosis and Bronchiectasis Unit, Perth; Tasmanian Adult Cystic Fibrosis Unit, Hobart), including 2677 patients (1300 aged ≥18 years; centre size 25–294 patients), representing 91%, 89% and 90% of the paediatric, adult and total CF population, respectively [16]。
在门诊或住院患者提供单一的痰标本2007年9月至2010年6月(表S1)。临床资料包括年龄、性别、数量注射。抗生素课程和诊所访问在过去12个月的记录。由于物流原因,最好的记录在1 s (FEV用力呼气量1)历年的样本收集和它配对用力肺活量(FVC)和身体质量指数(BMI)在同一天获得澳大利亚CF的每个病人数据注册(ACFDR) [16]。选择最好的肺量测定法是调整差异的研究临床状态条目(诊所访问与住院)。年龄调整肺功能预测方程使用(17,18),和标准偏差计算z分数使用美国国家卫生统计中心和疾病控制中心和Preventionnormalised增长BMI值的引用。
痰标本被医院诊断实验室培养使用标准技术概述之前(19]。当铜绿假单胞菌被确认,三个殖民地代表不同形态类型从每个样本(在可能的情况下)被科学家研究的独立选择,单独孤立的研究实验室和运输存储在-80°C,直到进一步的测试19]。
基因分型
DNA提取后,隔离被确认铜绿假单胞菌由一个双实时PCR试验之前进行DNA指纹分析使用enterobacterial重复基因间的共识(ERIC) PCR打字技术(19,20.]。聚类分析和基因型的ERIC-PCR指纹进行分配使用FPQuest™软件(版本4.5;Bio-Rad实验室企业有限公司、大力神、钙、美国)如前所述20.]。茎序列输入(MLST)也表现在所有共享ERIC-PCR独特的基因型和一个随机选择的子集ERIC-PCR基因型铜绿假单胞菌MLST网站(http://pubmlst.org/paeruginosa/)协议。代表隔离先前描述的高度流行澳大利亚和国际压力作为控制ERIC-PCR和MLST化验(表1)。地理空间基因型之间的关系和邮编是评估使用ArcGIS 10软件(Esri澳大利亚企业有限公司,布里斯班,澳大利亚)。
统计分析
残差为FEV1、FVC和FEV1/ FVC线性回归估计的高度,高度的平方,年龄、年龄的平方,性爱,性和交互与高度,高度的平方,年龄,和年龄的平方。这些残差作为因变量,分析预测肺功能。
ERIC-PCR基因型对肺功能的影响进行评估后囊性纤维化跨膜电导调节ANCOVA(雌性生殖道状态。肺功能的最小二乘均值值变量比较独特的菌株和5个病人患者组之间的最高度流行菌株。两两比较的意义被Dunnett的调整事后修正。ERIC-PCR基因型与治疗协会(黏液溶解的,阿奇霉素和吸入抗生素)和治疗负担(注射。抗生素treatment-days,数量注射。抗生素课程和诊所访问)是由物流和负二项回归估计的调整后的雌性生殖道地位和中心,和分别表示为概率和速度比率具有独特的菌株作为参考类别。Yates-corrected卡方(2×2)为多个比较分析与调整是用来评估ERIC-PCR基因型之间的关系和其他微生物分离研究痰标本。
结果
病人
18岁的2677名患者参加CF中心,1294年(48%)提供了文化和痰液样本铜绿假单胞菌是孤立的从1023年(79%)的1294个参与者(图1)。一至三铜绿假单胞菌隔离被运送到了研究实验室,2887年(96%)从983年的2993个可行的隔离患者可用于基因分型后确认铜绿假单胞菌通过实时PCR。

流程图的病人招聘、样本收集和分离分析。铜绿假单胞菌:铜绿假单胞菌;埃里克:enterobacterial重复基因间的共识。
表2提出了983年的研究参与者的特征铜绿假单胞菌阳性患者中列出ACFDR [16]。参与者年龄,体重指数得分(儿童)和肺功能比ACFDR病人。伴随co-pathogens孤立样本集合的时候列出在表S2。
参与者的年龄中位数(四分位范围(差))在初始铜绿假单胞菌感染的隔离和持续时间是8(差4-15)和10(6 - 15位差)年,分别。他们经历了14中值(差0-32)注射。抗生素治疗的日子,一个(差0 - 2)注射。抗生素和五(差3 - 8)诊所访问前的12个月内样本集合。总的来说,807人(82%)的983个黏液状的铜绿假单胞菌隔离从痰培养,80%的样本收集在诊所访问。
ERIC-PCR
所有2887铜绿假单胞菌隔离被ERIC-PCR typeable,产生531种不同的基因型。的931名患者提供了三个分离株,790(85%)、130(14%),11(1%)有一个,两个和三个基因型,分别。
表3显示,493独立ERIC-PCR基因型(或单菌株),另有38基因型是由两个或多个共享(范围2 - 220)的病人。总的来说,373人(38%)的983名患者只有独特的菌株和剩余的610(62%)至少有一个共同的基因型,包括与多个共享45株。成人(476(66%)717)比儿童更有可能(134(50%)266)共享铜绿假单胞菌基因型(或1.95,95%可信区间1.45 - -2.62)。的461名(47%)患者的年龄在他们的数据铜绿假单胞菌隔离,23了铜绿假单胞菌孤立在12个月内研究样本收集的日期。20患者感染独特ERIC-PCR基因型,而剩下的三个患者感染AUST-01 AUST-04 AUST-14,分别。
五个共享ERIC-PCR基因型在集群从31到220例,发现14参与集群的3-19参与者和进一步19集群涉及两个病人(表3)。总体而言,220名(22%)患者从17个中心铜绿假单胞菌从AUST-01隔离无异,而来自16个中心的173名(18%)患者隔离AUST-02区分开来。其他基因型遇到经常包括AUST-04(47名患者,12中心和六个州),小说ERIC-PCR基因型AUST-05(37例,六个中心和四个州)和AUST-06(31名患者,四个中心和三个州)(表1和3])。小集群涉及< 20例包括先前描述菌株,如AUST-03 AUST-07 AUST-11,以及一些新颖的菌株。病人从英国利物浦的流行毒株(LES)痰,但没有其他的通常共享基因型的区域,包括Midlands-1或曼彻斯特菌株,被检测到。有趣的是,三个病人克隆C,它是广泛地分布在整个北半球CF患者和在自然环境中(21]。
兄弟姐妹关系
39个兄弟姊妹,31(79%)共享ERIC-PCR所用至少一个基因型。21兄弟组(20条和一个三)共享AUST-01 (n = 14), AUST-02 (n = 5)和AUST-06 (n = 1),和一对姐妹都AUST-01 AUST-05基因型。进一步九兄弟对基因型检测两簇,和一对兄弟姐妹有一个基因型中观察到另一个不相关的主题生活号州际公路。总的来说,兄弟姊妹占19日的9个基因型共享由两个病人。
地理分布的基因型
广泛分布的独特ERIC-PCR基因型相比,我们观察到各种地理高流行基因型之间的关系(图2)。AUST-01患者常见的澳大利亚东南部,而大多数在昆士兰和西澳AUST-02隔离观察。先前描述的塔斯马尼亚菌株(AUST-03和AUST-04)也发现经常在病人在维多利亚。AUST-06几乎完全被发现在昆士兰和大多数AUST-05 AUST-08隔离来自南澳大利亚。
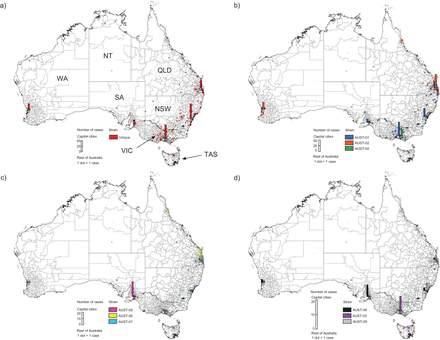
地理空间关系enterobacterial重复基因间的共识(ERIC) pcr基因型患者和住宅邮政编码:a)独特;b) AUST-01, -02年和-04年;c) AUST-05, -06年和-07年;和d) AUST-08, -03和-09株。新南威尔士州:新南威尔士州;NT:北部地区;昆士兰:昆士兰;山:南澳大利亚;助教:塔斯马尼亚;维克:维多利亚; WA: Western Australia.
与基因型相关的临床数据
参与者窝藏五种最常见的集群组(AUST-01、-02、-04、-05和-06年)是相似的年龄,性别和具有独特的营养状况铜绿假单胞菌压力(表4)。肺量测定法也类似这些人群相比,那些有独特的菌株。然而,AUST-01患者明显更可能使用阿奇霉素和吸入抗生素在前4周,有,去年,一个更大的数量和持续时间注射。抗生素课程和诊所的次数,相比之下,那些有独特的菌株(表4和5)。患者AUST-02 AUST-06有数量的增加的证据注射。抗生素的课程,到医院看病,但不是维护抗生素治疗而独特铜绿假单胞菌基因型。治疗负担的差异未见有其他两个最常见的共享集群(AUST-04和-05年)。
MLST
MLST于139年进行隔离(138名患者)代表所有共享ERIC-PCR基因型和70隔离(69名患者)和独特的ERIC-PCR基因型。分析209年的隔离了108种不同序列类型(STs)的高度整合(85%)与ERIC-PCR指纹结果(表S3和S4)。之间的差异观察ERIC-PCR MLST九次,MLST表示单或double-locus变体STs AUST-05为隔离ERIC-PCR讲,-08,-09,-11,-19,-34或-38基因型。也有八个实例涉及STs 12日27日,155年,179年,274年,275年,822年和905年MLST确认所用菌株,但ERIC-PCR发现不同基因型。进一步六隔离生产与分配不相符的STs的MLST网站AUST-02 (n = 1), AUST-11 (n = 4)和AUST-13 (n = 1)。
讨论
> 60%的澳大利亚CF患者铜绿假单胞菌从他们的痰培养菌株的至少一个其他的CF患者。尽管多个共享菌株被发现,他们主要是在小集群和从数量有限的中心和地区。相比之下,AUST-01和-02年非常普遍,发现病人从地理上分散的地区。一个或两个菌株中所有18个CF中心调查,影响> 40%的研究参与者。此外,那些窝藏AUST-01特别是医疗利用率大于那些独特的菌株。这些发现强化担心一些铜绿假单胞菌基因型是引起广泛的在澳大利亚大陆和CF中心之间相互传染。
发现通常共享菌株在澳大利亚CF社区从先前的较小规模的研究结果是一致的。病人参加CF中心维多利亚州和塔斯马尼亚有很高的患病率AUST-01和-03 (4,15),而那些在新南威尔士和昆士兰AUST-01集群,少-02和其他几个流行的基因型(5,14]。其他铜绿假单胞菌菌株也普遍在病人参加CF中心在北半球。849年的一项调查显示,病人隔离从31日英格兰和威尔士CF中心,LES发现在11%的患者和48%的中心(6]。最近,莱斯还发现15%的病人参加成人CF中心在安大略省,加拿大(3]。此外,一项研究涉及两个大荷兰CF中心报道70%的病人包庇铜绿假单胞菌共享基因型与至少一个其他病人从相同的中心7]。然而,并不是所有的研究发现的证据非常流行的基因型。报告来自比利时,不列颠哥伦比亚(加拿大)和新西兰只有识别基因相似的小集群隔离在流行病学无关的病人22- - - - - -24]。
常见的基因型在CF中心和地理区域显示罹患卫生保健相关传播病或暴露于占主导地位的环境基因型,说明了克隆C [21]。有趣的是,我们也发现克隆C三个病人。然而,随着大量参与CF中心之间的距离,似乎不太可能常见曝光可以完全占高度流行株的广泛传播,AUST-01到-02年,到目前为止还没有发现在环境调查(4,25]。相反,一些研究提高人际传播的可能性。CF患者在咳嗽,可以产生呼吸道气溶胶含有可行的细菌(26]。共享铜绿假单胞菌菌株被发现在空气样本肺量测定法,nebulisation和气道间隙接近感染患者(27]。最后,一些CF中心共享菌株的发病率减少了病人实施严格的隔离(10,11]。在一起,这些观察结果表明,大应变集群,如AUST-01和-02年最有可能收购相互传染。
最近加拿大的纵向研究相比临床结果患者LES那些窝藏独特的菌株(3]。在营养状况没有差异,肺功能下降,或肺恶化率或住院治疗。然而,3年以上,患者LES有死亡或肺移植的风险增加有关。相比之下,一项研究比较患者共享和独特的菌株在曼彻斯特成人CF中心没有显示出不同的生存8年后,但那些共享菌株表现出增加治疗需求9]。然而,这一发现可能是影响菌株基因型的知识介绍了常规分子监测后导致改变治疗实践。
AUST-01患者有更多的诊所访问和更大的治疗负担比那些独特的基因型。只有一个中心进行常规的分子指纹铜绿假单胞菌隔离。除了吸入抗生素使用,重复分析没有这个中心的数据并没有改变这些研究结果,表明AUST-01可能更致病性,而不是简单地增加治疗后应变类型的识别。增加注射。抗生素课程和诊所访问也观察到在AUST-02患者和-06年。然而,类似的肺量测定法之间的主要基因型患者组和独特的菌株(4]。我们的研究提出了重要的问题在澳大利亚CF感染控制中心。然而,其他比AUST-01,直到纵向收集的数据清楚地表明特定共享相关的副作用铜绿假单胞菌压力,应该小心谨慎。尤其在CF中心相关共享多个品种,实现复杂和资源密集型cohort-segregation政策风险不良心理后果为病人和他们的家庭不可能的好处(28]。与此同时,在澳大利亚CF中心,加强当前仍然是重要的标准的感染控制措施,包括隔离CF患者铜绿假单胞菌从所有其他的CF患者29日]。
本研究也有一些局限性。我们无法确定参与者间歇性或慢性铜绿假单胞菌感染。然而,正如大多数人与黏液状的成年人铜绿假单胞菌,很可能是慢性感染。同样,我们依靠痰标本,老年患者更严重的疾病是不成比例的招募。因此我们205年进行基因型分析铜绿假单胞菌隔离从上呼吸道和支气管肺泡灌洗的样本81名儿童在一个澳大利亚学前CF患者队列(30.]。AUST-01和-02株中发现只有一个病人,而常见的环境压力(ST-27、圣- 155和st - 179)经常被确定。因此我们不可能严重低估了病人的数量具有的一个主要基因型集群和研究应该广泛代表性的CF患者建立铜绿假单胞菌感染。从我们的研究是重要的,只有一个病人识别感染AUST-01作为第一铜绿假单胞菌隔离,尽管这些信息是可以在< 50%的研究参与者。
横断面研究设计有限的能力来识别风险因素获得共享铜绿假单胞菌菌株(包括是否高医疗利用本身就是一个因素),和全面评估特定的临床影响铜绿假单胞菌基因型。因此,病人现在形成一个纵向队列研究来确定收购的风险因素和长期高流行的影响铜绿假单胞菌在事故情况下压力。不幸的是,信息中心转移和个人医院和社会互动是本研究的范围之外。
另一个可能的限制是使用ERIC-PCR作为我们的主要基因分型工具,为分析pulsed-field凝胶电泳和MLST不切实际的近3000隔离。符合我们之前的观察,提供的一致性和程度的歧视ERIC-PCR MLST相比相对较高,因此我们有信心在我们的整体应变识别(20.]。然而,关联性被ERIC-PCR偶尔高估,重申我们之前推荐的确认ERIC-PCR类型之间的关系和分类输入技术(20.]。我们还发现附加多个ERIC-PCR基因型轴承相同的圣的证据,这常常涉及小集群内个体CF中心和兄弟姐妹组(20.]。例如,隔离来自13个病人显示一个独特的和四个共享ERIC-PCR基因型都由MLST st - 179。同样,st - 155和圣- 274多个ERIC-PCR基因型有关。有趣的是,STs 155年、179年和274年广泛分布于欧洲和北美的CF患者和经常遇到的其他生态环境包括自然环境(25]。相比之下,主要分享AUST-01菌株和-02显示有限的基因型变异,通常是发现在个人CF中心和大型集群,到目前为止,还没有发现在其他生态位,如自然环境和非人类动物25]。
最后,我们选择三个殖民地代表不同形态类型从每个标本进行基因型分析。不同基因型可能是低估了使用此策略。然而,我们相信,足够的多样性已经被抓获,85%的患者三隔离分析显示,只有一个ERIC-PCR基因型,只有1%有三个不同的基因型鉴定。同样的,萨尔我指纹分析的五个隔离每个病人在新西兰最近的一份研究显示有限的病人多样性(23]。
据我们所知,这是迄今最大的研究检查CF基因型的关系铜绿假单胞菌隔离和最全面的流行病学调查铜绿假单胞菌CF感染中心覆盖大型地理土地质量。参与者由∼75%的澳大利亚CF患者记录被感染的铜绿假单胞菌在国家注册,包括几乎所有CF整个大陆中心。共享铜绿假单胞菌菌株在澳大利亚的CF患者中很常见,虽然许多基因型可能是最初从环境中,相互传染也可以解释最广泛分散的共享基因型。这些主要的传播途径及临床意义菌株在澳大利亚CF患者仍未知,迫切需要确定。
确认
ACPinCF侦探小组的成员如下。南卡罗莱纳州贝尔(首席研究员;昆士兰儿童医学研究所,查尔斯王子医院,布里斯班)、T.J.基德(首席研究员;布里斯班昆士兰儿童医学研究所),k . Grimwood(首席研究员;布里斯班昆士兰儿童医学研究所),科学博士阿姆斯特朗(墨尔本莫纳什医学中心),p再见(首席研究员;皇家王子阿尔弗雷德医院、悉尼),P.J.库珀(儿童医院在威斯特、悉尼),C.J. Dakin(板牙儿童医院、布里斯班),核磁共振Elkins(首席研究员;皇家王子阿尔弗雷德医院、悉尼),I.H.羽毛(黄金海岸医院,南安普顿),h . Greville(皇家阿德莱德医院、阿德莱德),c .港口(悉尼大学、悉尼)、h·胡(首席研究员;悉尼大学、麦考瑞大学、悉尼),a·贾菲(悉尼儿童医院、悉尼),A.J.马丁(妇女和儿童医院,阿德莱德),快速出拳麦凯(儿童医院在威斯特、悉尼),G.B.标志(首席研究员;Woolcock医学研究所),J.M.莫顿(墨尔本莫纳什医学中心),医学博士尼森(病理昆士兰和昆士兰儿童医学研究所,布里斯班),d .价格(黄金海岸医院,南安普顿),k·拉姆齐(首席研究员;布里斯班昆士兰儿童医学研究所),D.W.里德(皇家霍巴特医院,霍巴特和查尔斯王子医院,布里斯班),P.J.罗宾逊(首席研究员; Royal Children's Hospital Melbourne, Melbourne), B.R. Rose (principal investigator; The University of Sydney, Sydney), G. Ryan (Sir Charles Gairdner Hospital, Perth), D.J. Serisier (Mater Adult Hospital and University of Queensland, Brisbane), T.P. Sloots (Queensland Children's Medical Research Institute, Brisbane), D.J. Smith (The Prince Charles Hospital and University of Queensland, Brisbane), C.E. Wainwright (principal investigator; Queensland Children's Medical Research Institute, Royal Children's Hospital, Brisbane), P.A. Wark (John Hunter Hospital, Newcastle), B.F. Whitehead (John Hunter Children's Hospital, Newcastle) and J.W. Wilson (principal investigator; The Alfred Hospital, Melbourne, all Australia).
我们感谢所有的参与者,研究和临床工作人员和临床微生物实验室在每个澳大利亚研究的网站。研究试验负责人包括:m .木材(查尔斯王子医院、布里斯班),m·杰克逊和j·切尼(皇家儿童医院,布里斯班),p .蓍草(板牙儿童医院、布里斯班),m·齐默尔曼(黄金海岸医院,南安普顿),j·克拉克和诉麦当劳(约翰亨特医院,纽卡斯尔),l .奶酪和r .天(约翰亨特儿童医院,纽卡斯尔),r·斯特(悉尼儿童医院、悉尼),r . Dentice和t·德怀尔(皇家王子阿尔弗雷德医院、悉尼),Giddon和m . Laporte(墨尔本莫纳什医学中心),a .罗宾逊和r . Carzino(墨尔本皇家儿童医院),e·威廉姆斯和d·克拉克(墨尔本阿尔弗雷德医院),r .球员(皇家阿德莱德医院、阿德莱德),d .蔡尔兹(妇女和儿童医院,阿德莱德)和美国莫雷(查尔斯爵士Gairdner医院,珀斯)。参与实验室包括:昆士兰病理学;母亲健康服务病理学;在尼克莱德斯沙利文病理学;猎人区病理服务;南东部地区实验室服务;悉尼西南病理服务;病理学的部门,在韦斯特米德儿童医院;实验室服务,墨尔本皇家儿童医院; Southern Cross Pathology Australia; CentrePath; Institute of Medical and Veterinary Science; Division of Laboratory Medicine, Women's and Children's Hospital; PathWest Laboratory Medicine WA (all Australia). We thank E. Charles-Edwards and M. Bell (Queensland Centre for Population Research, The University of Queensland) for their expertise with GIS mapping, and G. Sims (Cystic Fibrosis Australia) for his assistance with ACFDR data. Control strain isolates were kindly provided by M. Syrmis (Queensland Children's Medical Research Institute, Brisbane, Australia), J. Govan (University of Edinburgh, Edinburgh, UK), and B. Tümmler (Hannover Medical School, Hannover, Germany). This publication made use of the铜绿假单胞菌MLST网站(http://pubmlst.org/paeruginosa/)由k·乔利和选址在牛津大学。这个网站的发展已经由威康信托基金会资助。
脚注
可以从本文的补充材料www.www.qdcxjkg.com
支持声明
的国家卫生和医学研究委员会的项目(455919)昆士兰儿童健康的基础(50007)昆士兰州卫生办公室卫生和医学研究,澳大利亚囊性纤维化研究信任格兰特(2009 - 06)查尔斯王子医院基金会和旋转澳大利亚支持这个项目。的资金来源没有参与这项研究的设计和实施,分析或解释的数据,准备手稿的最后批准或决定提交出版的手稿。
感兴趣的语句
利益冲突的信息可以发现与本文的在线版本www.www.qdcxjkg.com
- 收到了2012年4月11日。
- 接受2012年7月22日。
- ©2013人队















