抽象的
慢性阻塞性肺疾病(COPD)患者骨骼肌受损会降低运动能力。与氧化肌肉纤维相似,这些患者的肌肉对训练的血管适应可能会钝化,就像其他慢性疾病一样。因此,我们比较了COPD患者和久坐健康受试者(SHS)训练后的肌肉功能反应和血管适应。
24例COPD患者(1 s内强迫呼气量45.6±17.5%)和23例SHS (<150 min·周)−1完成一项为期六周的康复计划,该计划是基于个别的中等强度耐力训练。训练前后进行组织形态学肌肉分析,检测促血管生成血管内皮生长因子(VEGF)-A和抗血管生成血栓反应素(TSP)-1。
COPD患者和SHS显示出改善的症状限制氧气消耗和肌肉耐力,尽管COPD患者的改善较低(+ 0.96±2.4与+ 2.9±2.6 ml·kg−1·Min.−1,p <0.05,+ 65%与分别为+ 108%,p = 0.06)。COPD患者的毛细血管对纤维(C/F)比SHS患者增加较少(+16±10%)与+ 37±20%,P <0.05),COPD患者发生纤维型开关。VEGF-A / TSP-1比率在COPD患者和SHS中增加(+ 65%与+ 35%, p < 0.05)。C/F变化与症状限制耗氧量相关(r=0.51, p<0.05)。
除了缺乏纤维开关外,COPD患者还显示出对训练的钝血管生成反应。
骨骼肌功能障碍在许多慢性疾病(慢性心力衰竭(CHF)、糖尿病、外周动脉疾病)中具有重要意义[1),肥胖,等。).在慢性阻塞性肺病(COPD)中,骨骼肌功能障碍影响患者的预后,运动耐受性和与健康相关的生活质量[2].这种肌肉损伤的特征是细胞变化,I型氧化纤维、氧化酶的比例减少[3.]和毛细血管[4].特别是,毛细管供应的改变[4与患者肌肉功能和有氧运动能力受损密切相关。
COPD患者骨骼肌受损与缺乏体育活动有关,尽管运动训练是这些患者骨骼肌功能障碍最有效的治疗方法[5],它从未被证明完全逆转过这种功能障碍[6].系统因素可以解释这种不完整的恢复[2]但是在细胞水平缺乏肌肉适应也被归因于令人报约。例如,在COPD患者的Quadriceps运动训练后,若干研究表明了I型纤维比例的增加[7- - - - - -10.],与健康受试者的观察结果相反[11.].
符合毛细血失化在肌肉功能中的作用,培训诱导的血管生成有可能还可以解释COPD患者中肌肉功能的不完全恢复。因为运动训练显着增加了这些患者中的肌肉毛细血肿[7,8,12.,可以假设肌肉对训练的血管生成反应是存在的,但在慢性阻塞性肺病中是钝化的,就像其他具有类似骨骼肌损伤的慢性疾病(糖尿病[13.]和chf [14.])。不幸的是,没有研究比较训练诱导的COPD患者毛细血管化与久坐的健康受试者(SHS)。此外,COPD对训练诱导的骨骼肌血管适应主要分子因子(如促血管生成血管内皮生长因子(VEGF)-A或抗血管生成血栓反应素(TSP)-1)表达的影响尚不清楚。
因此,我们的研究目的是确定COPD患者是否会在其肌肉血管血管自适应容量中经历特定的改变。为此,我们在COPD患者和SHS中的中等强度训练计划中比较了功能反应,Myofibre改造,毛细血管和主要血管生成因子,具有相同的物理不活动模式。
材料和方法
请参阅在线补充材料中的附加信息和参考资料。
研究人群
从2008年3月到2009年2月,我们招募了24名SHS(年龄50-75岁),他们没有疾病,每周进行中等到高强度体力活动的时间小于150分钟(对应于健康改善的推荐阈值[15.])和24例COPD患者由呼吸困难,慢性咳嗽或痰液产生和/或暴露于疾病的风险因素的历史,并且支气管扩张剂强制呼气量为1 S /强制呼吸能力比<70%[16.].排除标准包括其他呼吸道诊断,失代偿合并症,在过去3个月内加剧,并以前参与锻炼培训计划。所有受试者和患者分别在奥斯秘和奥斯秘州和法国Lodève的肺部康复中心进行Inserm U-1046获取知情书面同意,从所有科目获得,研究议定书由蒙彼利埃大学医院(2008年 - Eesss-V2和2009-04-BPCo-V2)的机构伦理委员会批准,并按照赫尔辛基宣言和欧洲良好临床实践指南。
体育活动
为了评估我们久坐选择的健康人口的身体活动,我们使用了vooorrips调查问卷(修改了巴西的调查问卷),在此指示中验证和使用的身体活动调查问卷[17.].在20个COPD患者和20个SHS中评估了“目标”身体活动水平(Trittac RT3研究跟踪器; Stanthealthy,Monrovia,CA,USA),在COPD中验证[18.,连续7天。
量化DE L'ActivitéMeatherique(Quantap)采访的调查是一种计算机辅助工具,旨在确定四个维度(学校,休闲运动,职业和日常活动的体育)的身体活动。该问卷在评估终身体力活动方面是可靠的,并且已被验证用于老年人法国科目以及各种病例的背景下,包括最近在COPD中[19.].
肺功能测试
所有受试者都接受了全身体积描记法(透气箱2800; Sensomedics,Yorba Linda,CA,USA)。将值与正常值进行比较[20.](在线补充材料)。
运动测试和肌肉功能评估
6分钟步行试验在一个30米的走廊进行。将测试期间的步行距离(6MWD)与参考值进行比较[21.].参与者在电动制动的自行车功率计(Ergoselect 200P;测定症状限制耗氧量(德国比茨)(V′O2sl)及通气阀阈值[22.](在线补充材料)。如果呼吸困难阈值不能被检测到,我们通过每分钟对呼吸困难进行评分来评估呼吸困难阈值,使用患者自己的词汇[23.](在线补充材料)。采用等距最大自主收缩(qMVC)和耐力时间(t林).估计无脂肪和肌肉质量,具有多频生物电阻抗(Quadcan 4000; Bodystat,Douglas,UK)。在线补充材料中提供了附加信息。
运动训练
运动培训课程是多组分和综合肺康复课程的一部分,包括教育计划[5].20次耐力训练,每周进行3 - 4次,持续6周。运动强度设置为呼吸或呼吸困难阈值时的心率[5,22.,23.].每一组持续45分钟,每两组中有一组以每次最大重复次数的40%进行30分钟的力量锻炼。所有课程都由经验丰富的临床医生监督,培训强度在培训方案期间增加。
肌肉活组织检查分析
在运动训练计划之前在Quadriceps的夸脱侧面进行肌肉活组织检查,并在最后一次培训期间后48小时进行[24.].
肌肉免疫组织化学
在从肌肉活组织检查中的冷冻切片(10μm厚)上的免疫组化后评估肌纤维型和平均横截面积(CSA),使用针对每种肌蛋白重链同种型的抗体(爱荷华州爱荷华大道,IO,美国IO大学)[4,25.].用CD31单克隆抗体(#550389;BD生物科学,富兰克林湖,新泽西州,美国)。在对每个肌肉活检的1 - 2个冷冻切片上的毛细血管和肌纤维计数后,测定CSA、毛细血管密度和毛细血管纤维比(在线补充材料)。
西方墨点法
探测VEGF-A(克隆VG-1#05-1117; Millipore,Etobicoke,Canada)和TSP-1(克隆A6.1#399300; Invitrogen,Burlington,Canada)的污点。还测量β-肌动蛋白蛋白作为我们的负载控制(在线补充材料)。
统计分析
数据以平均值±表示SD..通过Kolmogorov-Smirnov测试测试分配正常性。Pearson系数描述了相关性。我们使用了多元线性回归模型。通过混合线性回归建模进行组之间的训练效果的比较[26.].每次患者/受试者评估两次(重复措施)。因此,使用线性混合效应模型调整测量变量,以考虑重复措施作为随机变量的重复措施。患者组和测量时间被用作模型中的固定效应。然后用混合线性模型测试组效果。P值为<0.05被认为是统计学上显着的。使用R.2.13.0软件进行分析数据(www.r-project.org).
结果
COPD患者和SHS的基线特征
所有SHS都有一个<9.4的voorrips得分,表明他们都是久坐不动。COPD患者和SHS根据年龄和身体活动水平很好地匹配(表格1).此外,COPD患者和SHS在过去的15年里,COPD患者和SHS之间没有显着差异(代谢当量14 949±9470与12 341±5201,p = 0.26)。在形态学水平上(在线补充图E1), COPD肌肉中I型纤维的比例明显低于SHS (表2.).在线补充材料中提供了其他详细信息。
运动训练诱导的功能和组织形态学适应
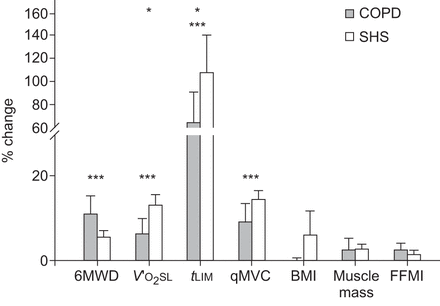
在COPD患者和SHS的透气或呼吸困难的强度(24名COPD患者中的6例)的强度(24名COPD患者6例)进行运动培训(12.7±1.9ml·kg−1·Min.−1预测48.7±11.4%和15.4±3.5 ml·kg−1·Min.−1,分别为63.5±10.1%,p<0.001)。以最大心率%表示,相对强度在COPD患者和SHS中差异无统计学意义(分别为66±6.8%和69±6.3%,p=0.27)。表示为%V′O2最大限度,COPD患者的相对强度略高与SHS(66±6%与60±5%,分别为p = 0.05)。显示所有功能参数的相对改进图1.两组训练显着改善6MWD(COPD:+ 37±35 m和SHS:+ 31±35米,P <0.001;无花果。1).这V′O2最大限度在组和时间之间显示出显着的相互作用(P <0.05)。最后,大幅增加t林两组(COPD:+ 121±169 s和SHS + 334±274 s,P <0.001)发生,几乎达到意义之间的相互作用(P = 0.06)。
慢性阻塞性肺疾病(COPD)患者和久坐健康者(SHS)运动训练后功能参数的相对变化(%)6MWD:步行距离6分钟;V′O2sl:症状限制摄氧量;t林:持续时间;qMVC:四头肌最大自愿收缩;BMI:身体质量指数;FFMI:无脂肪质量指数。数据以平均值±表示扫描电镜.*:组-时间交互作用,p<0.05;***:时间效应,p<0.001。
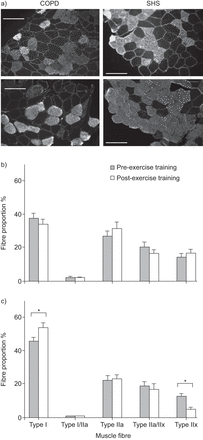
慢性阻塞性肺病患者和SHS中I型纤维比例的代表性变化见图图2一个.SHS组I型纤维比例显着增加(+ 8±11.6%,P <0.01;图2 c), IIx型纤维百分比下降(−8±10.0%,p=0.001)。相反,COPD组无明显变化(图2 b).我们观察到COPD患者的纤维CSA减少(从5107±1375 μm)2到4565±1477μm2, p<0.05), SHS组(4409±1679 μm)无明显变化24629±1670μm2,p = 0.51)。在COPD患者中看到I型和IIA型纤维CSA的这种减少(从5905±1588μm2到5260±1493μm2,p <0.05,5400±2012μm24657±1460μm2, p < 0.05)。
a)慢性阻塞性肺疾病(COPD)患者和久坐不动的健康受试者(SHS)在运动前(上排)和运动后(下排)进行了I型肌球蛋白重链(MHC)同型抗体染色的代表性股外侧肌横切冰冻切片。注意在SHS中I型MHC纤维比例的增加。b) COPD患者(n=21)和c) SHS患者(n=23)运动训练计划前后肌纤维类型比例(%)。数据以平均值±表示扫描电镜.秤杆=100μm。*:P <0.05,运动培训后。
运动训练诱导的肌肉血管适应
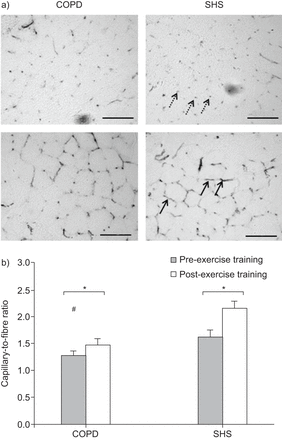
在内皮标记物CD31的免疫检测后可视化毛细血管(无花果。3A).在两组中,运动训练刺激血管生成,通过增加毛细血管纤维比(COPD 16±10%和SHS 37±20%,P <0.001)(无花果。3B.).然而,组和时间之间存在显着的相互作用(P <0.01),表明COPD患者的改善较小。在两组(COPD 29±28%和SHS 9±17%,P <0.01)中观察到毛细密度的改善,没有群时间相互作用(P = 0.11)。
a)在慢性阻塞性肺病(COPD)患者(COPD)患者中染色内皮标记CD31,在(上排)和(下排)锻炼之后,在慢性阻塞性肺病(COPD)患者和久坐活性的健康受试者(SHS)中染色。注意在运动前训练中围绕Myofibre(虚线箭头)的横向毛细血管,锻炼培训后毛细管 - 纤维接口的尺寸增加(黑箭头)。b)COPD患者的平均值和标准误差和SHS培训毛细血管与纤维比之前和SH。秤杆=100μm。*:P <0.05,运动培训后。#:P <0.05,在组之间。
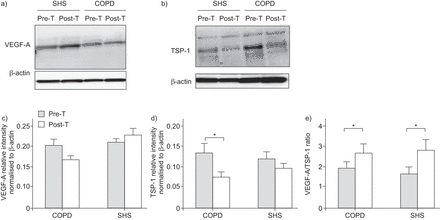
运动培训对健康受试者或COPD受试者的VEGF-A蛋白质水平没有显着影响。TSP-1蛋白表达响应于两组运动训练(P <0.05),在COPD人群中观察到44%降低(0.134±0.022 AU预训练与培训后0.075±0.013 AU,P <0.05)(图4 d).有趣的是,COPD组和SHS组的VEGF-A/TSP-1比值均通过运动训练显著增加(分别为+65%和+35%,p<0.05) (图4 e),有利于血管生成反应。
a)血管内皮生长因子(VEGF)-a和b)血压性肺炎(TSP)-1蛋白表达在慢性阻塞性肺病(COPD)患者(COPD)患者(COPD)和久坐不动的健康受试者(SHS)中(PRE-t)和之后(t)培训。β-肌动蛋白用作负载控制。C)VEGF-A和D)TSP-1蛋白的密度测定分析;e)COPD患者的Passus Landlis和SHS培训前后的VEGF-A / TSP-1比例。数据以平均值±表示扫描电镜.*:组之间的P <0.05(训练后)。
血管生成功能关系
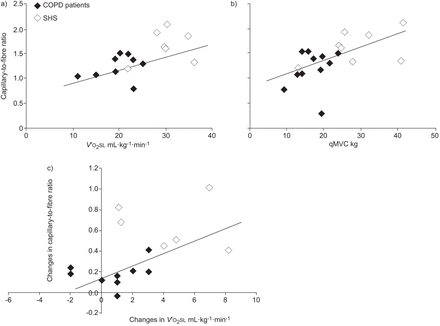
在基线时,毛细血管纤维比显著正相关V′O2最大限度COPD患者和SHS中的QMVC(r = 0.60,p <0.01和r = 0.67,p <0.01,p <0.01)(无花果。5A和B.).毛细血管密度与I型纤维比例无显著相关性(p=0.07)。训练引起的毛细血管纤维比的绝对变化与血管内的变化显著相关V′O2最大限度在两组(r = 0.51,p <0.05)(无花果。5C).
毛细血管纤维率与A)症状限制氧气摄取呈正相关(V′O2sl)(r = 0.60,p <0.01)在慢性阻塞性肺疾病(COPD)患者和久坐不动的健康受试者(SHS)和B)在基线时,Quadriceps最大自愿收缩(QMVC)(QMVC)(R = 0.67,P <0.01)。c)毛细血管 - 纤维比变化与变化呈正相关V′O2sl(r = 0.51,p <0.05)在COPD患者和SHS训练后。
讨论
我们的研究的主要发现是COPD患者的骨骼肌对肌肉毛细血管反应方面的训练表现出了良好的反应,这与较低的功能改进相关联。我们还观察到两组VEGF-A / TSP-1比的增加,有利于血管生成过程。最后,在COPD患者中观察到缺乏对训练的纤维型切换响应,而COPD患者与年龄和身体活动匹配匹配的健康受试者相比。
训练刺激的效果
我们适度强度的运动培训计划显着提高了COPD患者和SHS的运动能力。在线补充材料中提供了其他详细信息。有趣的是,组和时间效应之间存在显着的互动V′O2最大限度和t林,表明COPD患者的功能变化较低,用于这些参数。与SHS相比,COPD患者的这些较低的功能性改进与缺乏运动诱导的肌肉纤维类型变化相容[27.].
关于运动培训的强度,所有参与者都在自己的透气(或呼吸困难)阈值上培训,这是一种针对培训刺激到个体肌肉有氧能力的方法[28.].在最大心率的百分比方面,相对强度是相似的,这是靶向相对运动强度的另一种经典方法[5,22.].学习训练有素和未经训练的健康科目,似乎相对但不是绝对强度是肌肉基因对运动训练的转录激活水平的决定因素[29.].以相似的相对强度进行连续运动后,肌肉反应更强(50%和65%)V′O2最大限度)甚至在COPD患者中与健康受试者进行了比较,特别是过氧化物酶体增殖物激活受体-γ共激活物-1α,它是纤维类型开关的主要调节器[30.].因此,在我们的研究中,很可能在肌肉水平时,培训刺激在COPD患者和SHS中至少相似。
COPD患者肌肉组织形态和功能对训练的反应
同意以前的作品,COPD患者的肌肉毛细血管化的基线水平较低[4,7],且与肌肉功能障碍和O2在培训之前消费[4].我们观察到毛细血管对纤维的比例增加,这可能表明训练诱导的转移O的能力的提高2在COPD患者和SHS中的Myofibres。事实上,最近的工作表明o2转移到单元格主要是毛细管 - 光纤接口的函数[31.],由毛细血管纤维比反射[32.].我们的许多冷冻液都突出显示,这表明毛细管接触长度增加,因此界面的长度(无花果。3A).
此外,肌肉毛细血管纤维比的增加(即。毛细血管到纤维的界面,因此O2转移能力)可能是O型肌的主要驱动力2摄取性,从而提高了COPD患者中等强度运动训练后的耐久性。这将是一致的证据表明o的关键作用2在最大o的毛细管中转移到细胞2来自健康受试者的肌肉吸收[33.].事实上,在我们的研究中,我们发现Myofibres消耗o的能力没有变化2.与SHS相比[34.] COPD患者没有向更多氧化型I纤维的转变[7,12.[我们COPD患者(n = 10)中的初步数据表明,无透化纤维的氧气消耗的最大速率没有改善(参见在线补充材料中的方法和结果部分)。最后,毛细血管纤维比和v'之间的显着和正相关性O2sl如前所述在健康受试者中观察到的变化[35.],加强对毛细血管作用的可信度在最大o的改善中2在我们的COPD患者中吸收。
COPD患者血管生成因子的训练诱导反应
血管生成是一种复杂和多步生物过程,通过促抗血管生成因子之间的平衡来紧密策划。因此,我们选择针对具有良好特征的临床影响的关键促进和抗血管生成因子,即。VEGF-A [36.]和TSP-1。在转基因小鼠的Myofibres中删除VEGF-A显着降低了肌肉毛细血管毛细血管,并降低了〜80%的运动耐久性时间[37.].靶向VEGF基因表达的基因治疗改善了肌肉毛细血管[38.].TSP-1是一种大的基质糖蛋白,其作用主要是抑制血管生成[36.].与野生型相比,TSP-1基因敲除小鼠的肌肉毛细血管增加和耐力提高了67%,从而突出了其临床影响[39.].总共,VEGF-A / TSP-1比率出现为肌肉血管自适应平衡的最相关标记[36.].后肢卸荷后[40], VEGF-A/TSP-1比值增加,与毛细血管化增加一致。因此,评估VEGF-A/TSP-1比值似乎比单独分析分子因子的表达更准确[36.].在我们的研究中,我们还观察到这两个群体中这种比例的显着增加,这表明我们患者的血管生成平衡转移有利于血管生成,这与毛细血管的增加一致。
COPD患者肌肉细胞受损对训练的反应机制是什么?
在COPD患者中锻炼训练的缺陷肌肉适应性的特征在于缺乏纤维型移位和钝化毛细血管反应。因此,我们可以假设脂肪阶病原生物机制。在COPD中,在外周肌功能障碍中,系统性因素(在运动期间所有增强的氧化应激或全身性低级炎症都增强)已被归功化[2].尽管如此,调节肌肉血管生成的细胞途径和纤维类型之间的分子联系是不能消除的。
临床意义
我们研究中的一个关键观察是功能减退(四头肌)之间的联系t林和V′O2sl)和capillarisation。此外,我们的研究表明,钝化的肌肉毛细血管反应对训练在减少的作用V′O2slCOPD患者的改善,因为血管生成也显示出对改进的影响V′O2sl在另外两种慢性疾病中:CHF [41.]及外周动脉疾病[42.].因此,我们对毛细管至纤维比率的降低改善似乎是临床显着的。COPD肌肉的钝化血管生成能力与其他慢性疾病的观察结果一致,具有类似的外周肌功能功能障碍(糖尿病[13.]和chf [14.])。在与下肢缺血相关的疾病中,肌肉血管生成可以是用于改善肌毛细血管的治疗干预的相关靶标[43.].但是,虽然o2转移到肌肉似乎至关重要,没有COPD患者慢性下肢缺血的证据表明[44.].然而,低氧血症和/或合并疾病(血管和/或糖尿病)的患者可能经历慢性缺血,在这种情况下,治疗干预与运动训练可能是一个适当的方法。
总之,运动训练增加了COPD患者的肌肉毛细血管化,这可能推动了功能的改善。尽管血管适应平衡的最相关参数(即。VEGF-A / TSP-1比率增加了COPD患者和SHS中的血管生成过程,毛细血管的增加仍然在患者中显着钝化。除了缺乏纤维型开关之外,还原的血管生成构成了在COPD患者训练中改变的肌肉反应的另一个特征。
致谢
作者感谢A. Bourret和G. Hugon(Montpellier大学,法国)在实验室和所有团队中的技术支持,肺康复中心“La Salane”和“La Vallonie”的贡献工作。G. Caris(肺部康复中心,奥赛杰,法国)和A. Suc(蒙彼利埃大学,蒙彼利埃,法国)被承认他们的肌肉活检。作者谨此感谢G. Carnac(Montpellier大学,法国蒙彼利埃大学)为管理蒙彼利埃和多伦多团队,C. Notarnicola(蒙彼利埃大学,法国蒙彼利埃大学)为她的专业知识和C. Stott为他对稿件的批判性阅读。
脚注
这篇文章有补充资料可从www.www.qdcxjkg.com
支持声明
该研究得到了中心住院机构区域大学蒙彼利尔和患者协会和协会倒L'援助等的联合拨款支持的支持,援助等人(APARD)。F. Gouzi和A. abdellaoui由公约Industrielles De Chareation Par La Recherche(CIFRE)提供支持Fontalvie Corporation以及法国的Ministère Délégué à la Recherche et aux Nouvelles Technologies。O. Birot得到了加拿大自然科学和工程研究委员会(NSERD DG 341258-2011)。
兴趣表
利益冲突信息可以在本文的在线版本旁边找到www.www.qdcxjkg.com
- 已收到2012年3月31日。
- 接受2012年6月18日。
- ©2013人队