抽象的
俱乐部细胞(Clara细胞)参与支气管伤口修复和再生。它们位于支气管中,它们在特发性肺纤维化(IPF)中的肺泡损伤期间活化,并迁移到受影响的肺泡中,是一种称为肺泡支气管化的方法。这种迁移的目的和俱乐部细胞在肺泡伤口修复中的作用是有争议的。本研究旨在探讨俱乐部细胞在肺泡上皮伤口修复和肺纤维化中的作用。
直接联络共同文化在体外模型用于评估俱乐部细胞(H441细胞系)对肺泡上皮细胞(A549细胞系)和小气道上皮细胞(SAEC)伤口修复的作用。免疫组织化学在IPF患者的肺组织样本上进行,以复制在体外发现离体.
我们的研究表明,俱乐部细胞通过肿瘤坏死因子相关凋亡诱导配体(TRAIL)依赖机制诱导肺泡上皮细胞和SAECs凋亡,从而显著抑制创伤修复。此外,在IPF肺中,在纤维化区域的受累肺泡上皮内检测到trail表达俱乐部细胞,并伴有广泛的肺泡上皮细胞凋亡。
从这些发现中,我们假设与IPF相关的广泛的亲纤维化重塑可以通过抑制肺泡上皮细胞诱导细胞凋亡的脑凋亡的机制来驱动。
特发性肺纤维化(IPF)是一种慢性渐进性纤维化患者未知的病因,主要是在老年人身上发生并限于肺部[1].这种疾病的病理生理过程尚不清楚。然而,最近已经假设对肺泡上皮细胞的多重微损伤,不平衡的免疫应答和异常伤口修复是IPF发病机制的关键介质,其中炎症可能不是启动触发[2- - - - - -4].肺泡损伤后,通过肺泡上皮细胞迁移、增殖和分化,使脱落的肺泡基底膜迅速再上皮化,恢复肺泡的完整性和功能至关重要。在IPF中,这种愈合过程似乎受到了损害[2];虽然其确切机制尚不清楚,但可能涉及反复损伤和大量I型肺泡上皮细胞丢失的多因素交互过程[2,5],增加肺泡上皮细胞凋亡[6- - - - - -8,失调的上皮-间充质串音[9]偏振免疫反应[4,10.和肺泡细支气管化[11.,12.].
肺泡细支气管化是俱乐部细胞(Clara细胞)和其他细支气管上皮细胞异常增殖和肺泡迁移的过程,已在IPF肺组织和肺纤维化动物模型中得到证实[11.- - - - - -18.].这些俱乐部细胞的一个亚群表现为功能性细支气管祖细胞,参与细支气管创面修复和再生[19.- - - - - -21.].然而,动物模型研究的谱系追踪表明,俱乐部细胞可能不参与肺泡损伤修复[22.].此外,在岩土霉素诱导的鼠肺纤维化中,肺泡支气管灭绝的废除不会恶化疾病状态[15.].尽管这些发现,肺泡支气管化仍然是IPF肺部的恒定的组织学特征,伴随着肺泡架构和功能恢复失败[11.,12.,14.].我们假设具有IPF的发作,俱乐部细胞的激活迁移到肺泡区及其与其相互作用原位肺泡上皮细胞对随后的异常修复响应和随后的纤维化组织重塑枢转。阐明这种关键的俱乐部细胞 - 肺泡上皮细胞相互作用可以解开有利于IPF的药理学操作的可利用靶,仍然没有有效治疗的疾病。
因此,在这项研究中,我们开发了一种双细胞共培养伤口修复模型,以阐明俱乐部细胞在肺泡上皮细胞伤口修复中的作用。通过使用该模型,我们证明了俱乐部细胞的直接接触显着抑制肺泡上皮细胞和小气道上皮细胞(SAEC)伤口修复通过肿瘤坏死因子相关的凋亡诱导配体(TRAIL) - 依赖性凋亡。通过扩大IPF患者肺组织样本的发现,我们证明了在持近熟纤维化的肺泡区中展示了Trail表达俱乐部细胞的定位原位肺泡上皮细胞广泛凋亡。这些在体外和离体调查结果引导我们假设IPF期间的广泛的亲纤维化重塑是可能在肺泡上皮细胞中诱导肺泡上皮细胞中凋亡的诱导症凋亡的推动。
材料和方法
人体细胞系
Human type II alveolar epithelial cell line A549, club cell line H441, normal human lung fibroblasts CCD-8Lu (all from ATCC, Rockville, MD, USA) and human primary SAECs (Lonza, Wokingham, UK) were cultured according to the manufacturers’ protocol. As human primary type II alveolar epithelial cells (ScienceCell Research Laboratory, Carlsbad, CA, USA) do not form confluent monolayers, a primary criterion for wound repair models, we used prosurfactant protein (proSP)-C (a type II alveolar epithelial cell marker) -expressing A549 cells (online supplementary figure E1). Experiments were replicated on the confluent monolayer-capable proSP-C-negative SAECs (online supplementary figure E1) to exclude the potential for cancer cell line-related bias. Due to the unavailability of primary human club cells, the H441 cell line, which originated from human club cells and is widely used in club cell functional studies [23.- - - - - -25.], 被选中。
人体组织样本
21例IPF患者和19例因其他原因行肺叶切除术但无IPF证据的对照组患者的肺组织样本。IPF组织诊断由一名独立病理学家根据美国胸科学会(ATS)和欧洲呼吸学会(ERS)的组织病理学标准确诊[188bet官网地址1].
在体外上皮细胞伤口修复测定
的在体外伤口修复测定是先前描述的方法的修饰[26.].简而言之,在标准条件下培养A549和H441细胞作为单层作为单层的单层汇集,以在标准条件下为单体化的完整Dulbecco的改性鹰培养基(DMEM)。在细胞单层上制备线性卷,然后用无血清(SF)-DMEM,10%FBS补充的DMEM或SF条件培养基(CM)补充24小时(无花果1和2A).采用Image J软件(National Institutes of Health, Bethesda, MD, USA)测量周向创面间隙,计算24 h后创面修复百分率。
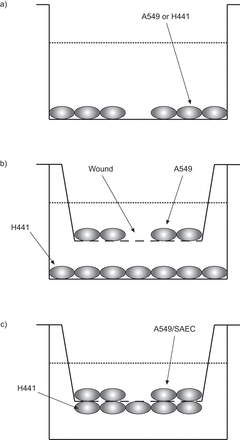
在体外上皮伤口修复和共培养系统。a)在24孔板上缠绕在A549或H441细胞单层上缠绕。b)间接接触共培养模型。在Transwell(上层)的0.4微米多孔聚乙烯对苯二甲酸乙二醇酯(PET)与H441细胞(底层)的受伤A549;两个细胞层之间的间隙为0.8mm。c)直接联络共同培养模型。DII标记的伤口A549细胞或小型气道上皮细胞(SAEC)(上层),具有在3μm多孔Transwell膜上生长的未伤口的DIO标记的H441细胞(底层)。伤口后,将直接和间接接触样品在无血清基底介质中培养24小时。
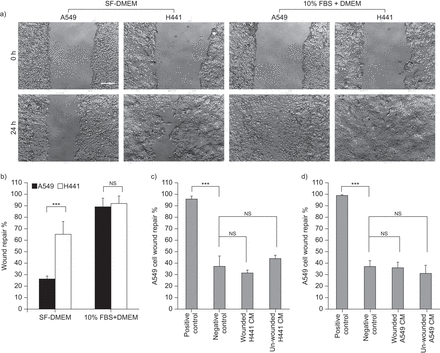
A549和H441细胞在体外伤口修复。a)A549和H441细胞伤口修复与无血清(SF)的改性鹰培养基(DMEM)和10%胎牛血清(FBS) - 在0小时和24小时后甲型DMEM。秤条=200μm。b)24小时后SF和10%FBS的A549和H441细胞的伤口修复A549和H441细胞(n = 4,5或更多的重复)。c)24小时后A549伤口修复伤口和未受伤的H441细胞(n = 3,每个重复)。d)24小时后A549细胞伤口修复伤口伤害和未受伤的A549细胞(n = 3,每次重复)。阳性和阴性对照分别代表伤口修复,分别具有10%的FBS补充和SF培养基。* * *: p < 0.001。ns:不显著。数据以平均值±表示SD..
直接和间接接触共培养伤口修复测定
对于直接接触共培养伤口修复实验,DII标记的A549细胞或SAECS和DIO标记的H441或CCD-8LU细胞(yvybrantTM值多色细胞标记套件;Invitrogen,佩斯利,英国)生长为3-μm多孔聚对苯二甲酸乙二醇酯(PET)Transwell膜(BD Bioscience,Franklin Lakes,NJ,USA)的对侧表面上的汇合无花果1 c,3de).间接共培养:0.4-μm PET多孔transwell膜上表面培养A549细胞,孔板底表面培养H441或CCD-8Lu细胞(图1 b).在A549细胞或SAEC单分子膜上作线性创面。然后将损伤的A549细胞或SAECs在无血清的基础培养基中培养24小时。在直接接触模型成像之前,用棉签从PET膜下表面小心地取出H441或CCD-8Lu细胞。在0和24小时,用激光扫描共聚焦显微镜(Olympus, Southend-on-Sea, UK)获得直接接触共培养的图像。如前所述,用倒置光学显微镜拍摄间接接触共培养伤口的图像。伤口间隙测量和伤口修复分析如前所述。
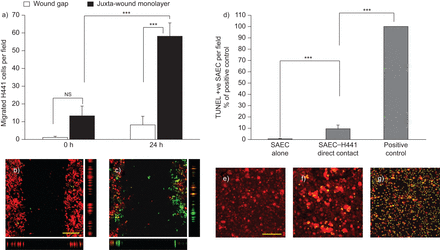
A549-H441直接和间接联络共同培养伤口修复。a)与H441细胞直接和间接接触共培养的24小时后A549细胞伤口修复。阳性和阴性对照代表伤口修复,分别用10%胎儿血清补充和无血清介质(n = 4,三,重复)。b)将H441细胞迁移到A549 Juxta伤口单层和伤口间隙(n = 5)中。c)在24小时后与H441细胞直接接触共培养的Juxta伤口单层的每种域A549细胞的数量(n = 5)。D,E)激光扫描A549-H441的共聚焦微观图像分别为0和24小时直接接触共培养。DII标记的红细胞是A549,DIO标记的绿色细胞是H441。垂直侧杆通过相应的Juxta缠绕的单层表示Z-SliCing,而水平杆通过伤口间隙表示Z切片。在伤口24小时后,在A549细胞的Juxta伤口单层中注意到大量迁移的H441细胞。*:P <0.05; **: p<0.01; ***: p<0.001. Data are presented as mean±SD..比例尺= 150 μm。
用于评估A549-H441或SAEC-H441细胞直接接触共培养的H441细胞迁移,在0小时和24小时后在各个伤口位点计算DIO标记的H441细胞和DII标记的A549细胞或SAEC伤害(图3 d和e)。进行共聚焦Z扫描以确认迁移。
肺泡A549细胞和SAECs对细胞凋亡的评估
通过使用重组人可溶性小径或Fas配体(FASL)(Peprotech,Rocky Hill,NJ,USA)评估配体A549细胞单层中的凋亡,其也被其特异性受体阻断单克隆抗体(MAB)缺失-R1(HS101,10μg·mL−1)和/或TRAIL-R2(HS201,10μg·mL−1)、Fas (SM1/23, 10 μg·mL−1)(Enzo Life Science,Lausen,Switzerland)。在SAECS中也评估了可溶性痕迹诱导的细胞凋亡。为了评估H441或CCD-8LU细胞直接接触诱导的凋亡在A549细胞或SAEC中,DII标记的A549细胞或SAEC在直接接触伤口修复设置中与未标记的H441或CCD-8LU细胞共同培养描述。为了阻断H441细胞诱导的细胞凋亡,用Fas预处理样品(SM1 /23,10μg·mL−1)或TRAIL-R1 / R2(HS101,HS201;10μg·mL−1)受体阻断的拮抗mab。24小时后,由TUNEL(末端脱氧核苷酸转移酶介导的脱氧尿苷三磷酸三磷酸镍缩末标记)测定方法在24小时后评估细胞凋亡原位荧光素细胞死亡检测试剂盒(罗氏诊断有限公司应用科学,Burgess Hill,英国)。阳性对照采用200 μM过氧化氢(H2O2)用SF基础培养基处理阴性对照。
进一步的实验程序
在线补充材料中描述了其他详细的实验程序。
统计分析
两组间差异的显著性采用配对双尾t检验。三组或三组以上的差异用非参数单因素方差分析后HOC.Tukey的多重比较分析。通过Wilcoxon匹配对分析患者数据签名等级测试或Mann-Whitney U-Test。P值为<0.05表示表示统计学意义。在体外数据以平均值±表示SD.患者数据显示为平均值±扫描电镜.使用GraphPad Prism Version 5.00软件进行统计分析(GraphPad Software,San Diego,CA,USA)。
研究批准
人体组织研究获得了南斯塔福德郡地方研究伦理委员会的批准(08/H1203/6)。
结果
H441(Club)细胞通过旁静脉因子不刺激A549细胞伤口修复
建立肺泡和支气管细胞分泌产物之间的串扰,我们首先使用A549和H441细胞的伤口修复模式研究在体外伤口修复模型(无花果1和2A)[26.].H441细胞A549细胞生长缓慢的相比在科幻和10% serum-supplemented媒体(在线补充图ea2和b)。A549和H441细胞的倍增时间计算在旧金山召开的媒体是22和100 h,分别和18和50 h,分别在10% FBS-supplemented媒体(在线补充图E2c)。尽管存在这种差异,但在10%血清的情况下,伤口修复模式没有观察到显著差异(图2一个b)。然而,在SF培养基中,H441细胞伤口修复的速率比为A549细胞所见为2.5倍(65%H441与26%A549,P <0.001;图2 b).
接下来,我们在A549细胞伤口修复上测试从受伤和未伤口的H441和A549细胞单层获得的SF-CM。来自伤员和未受伤的H441细胞的SF-cm不影响A549细胞伤口修复(32%SF-CM与38%SF,44%SF-CM与分别为38%科幻小说;图2 c).同样,来自肺泡A549细胞的SF-CM,无论是否损伤,都不会刺激A549细胞创伤修复(图2 d).相反,SF-CM的伤口和未受伤的A549细胞没有刺激H441细胞伤口修复(在线补充图E3)。连同,这表明俱乐部细胞(H441细胞)可以在SF条件下自动刺激伤口修复,但不能刺激肺泡上皮细胞伤口的修复。
H441细胞在A549-H441共培养伤口修复系统中抑制A549细胞伤口修复
为了进一步探讨H441细胞在肺泡A549细胞创面修复中的作用,我们开发了一种直接和间接接触共培养创面修复系统(图1 bc). H441与损伤单层A549直接或间接接触共培养可显著降低创面修复率(直接接触:11%,p<0.01;间接接触:20%,p < 0.05;控制:36%;图3).
与A549细胞伤口中的修复速率的降低相结合,我们还观察到基本的H441细胞迁移到受伤的A549细胞单层中,其中与伤口间隙相比,在Juxta伤口单层部位位于Juxta-andlable onolayers部位时4.25倍较大的迁移的H441细胞。本身(p <0.001;图3 b和e)。结合这种迁移,还注意到了Juxta伤口单层A549细胞的55%降低(图3 ce).在类似的直接接触共培养实验中,H441细胞没有迁移到未损伤的肺泡上皮细胞单层(在线补充图E4),在A549细胞缺失的情况下,H441细胞迁移可以忽略不计(在线补充图E5)。相反,在A549 - CCD-8Lu直接和间接接触共培养中,正常的人肺成纤维细胞CCD-8Lu没有抑制A549细胞创伤修复(在线补充图E6a)。此外,在直接接触模型中,CCD-8Lu细胞向A549细胞创伤部位的迁移可以忽略不计(在线补充图E6b)。综上所述,这些结果表明,H441(俱乐部)细胞,而不是正常的肺成纤维细胞,以一种依赖于近距离的方式抑制肺泡A549细胞的创伤修复,至少在直接接触模型中,创伤修复抑制是由于肺泡上皮细胞群的直接中断和破坏。
可溶性TRAIL和FasL诱导A549细胞凋亡
我们推测,近伤部位A549细胞数量的减少可能是由于h441诱导的凋亡。为了验证这一假设,我们首先检测了A549细胞对已建立的凋亡诱导配体TRAIL和FasL的敏感性[27.- - - - - -30.].800 ng·mL的TRAIL或FasL均可诱导A549细胞单层凋亡−1或3.2μg·毫升−1, 分别 (图4).通过抗落后受体(R)1和/或抗追踪-R2拮抗MAb(图4 b).证明了FasL诱导的细胞凋亡特异性通过使用抗FAS拮抗MAB(图4摄氏度).这表明肺泡A549细胞上存在功能性Fas和TRAIL受体。
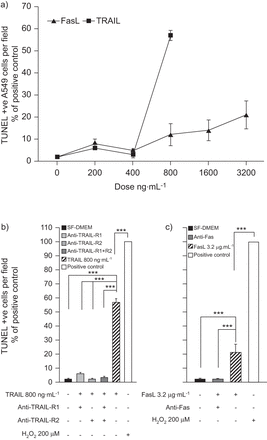
A549细胞单层细胞凋亡的评估。a)具有可溶性Fas配体(FasL)和肿瘤坏死因子相关凋亡诱导配体(TRAIL)的A549细胞中凋亡诱导的剂量响应。b)通过抗追踪受体(R)1或抗润落-R2或组合单克隆抗体(MAb)阻断A549中的血迹诱导的细胞凋亡。c)用抗Fas mab(n = 3)阻断可溶性FasL诱导的凋亡。阳性对照在200μmH诱导的A549细胞中代表细胞凋亡2O2.数据图和列代表均值实验值±SD..TUNEL:末端脱氧核苷酸转移酶介导的脱氧尿苷三磷酸镍骨贴图;SF:无血清;DMEM:Dulbecco的改良鹰媒体;H2O2:过氧化氢。* * *: p < 0.001。
H441细胞的直接接触通过依赖于依赖依赖机构在A549-H441直接接触式共培训伤修复系统中诱导A549细胞中的细胞凋亡
为了确认我们之前的假设,我们在用H441细胞进行直接接触模型中的A549细胞伤口进行了TUNEL测定。我们在A549-H441直接接触伤口修复模型中观察到A549细胞中A549细胞(52%标准化为阳性对照)的凋亡率大幅度(无花果。5A和d)在等效的直接接触A549-CCD-8LU共同培养(在线补充图E6C)中未观察到。迁移H441细胞对TUNEL没有染色,因此不被认为是凋亡(在线补充图E7)。在使用H441细胞播种到与H441细胞的直接接触模型中之前,具有特异于Fas的阻断抗体的预孵育A549细胞,未能阻断凋亡反应(无花果。5B.f)。然而,用抗trail R1/R2单克隆抗体预孵育A549细胞在直接接触模型中完全阻断了h441诱导的凋亡(p<0.001;无花果。5B.e)并改善A549细胞伤口修复在其未经处理的对应物(32%的抗追踪受体MAbs治疗与8%未经处理的样品;P <0.05;无花果。5h.和我)。这些结果表明,H441细胞在受伤的肺泡A549细胞中诱导细胞凋亡,并通过直接接触共培养伤口修复系统中的依赖依赖机制抑制伤口修复。
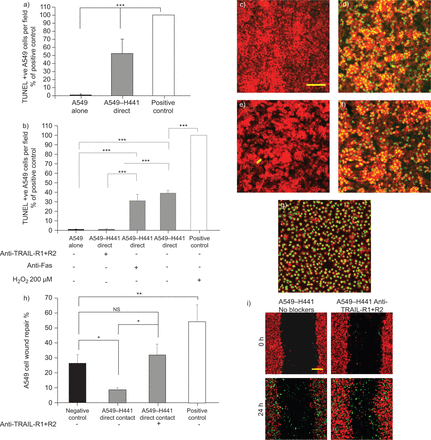
A549-H441直接联络共同培养中凋亡和伤口修复评估。a)在A549-H441直接接触共培养伤口修复(N = 3)中,在24小时后A549细胞在A549细胞中的细胞凋亡(n = 3)。b)A549-H441直接接触共培养诱导凋亡凋亡,抗肿瘤坏死因子相关的凋亡诱导配体(TRAP) - 重量(R)1 + R2和抗Fas单克隆抗体(MAb)。对于阳性对照,在A549细胞单层中诱导细胞凋亡200μmH2O2c-g)激光扫描共聚焦显微镜图像,对A549 - h441直接接触共培养进行末端脱氧核苷酸转移酶介导的脱氧尿苷三磷酸镍末端标记(TUNEL)检测。红色为dii标记的A549细胞,绿色细胞核为tunel阳性A549细胞核。c) A549细胞单株培养(阴性对照)。d) A549-H441细胞直接接触共培养。e) A549-H441与anti-TRAIL-R1和-R2单克隆抗体直接接触共培养。f) A549-H441与抗fas单抗直接接触共培养。g)阳性对照:200 μM H单培养A549诱导细胞凋亡2O2.h)A549伤口修复在存在和不存在抗-R1 + R2 mAb(10μg·mL−1)在24小时后的A549-H441直接接触共培养。阴性和阳性对照在单殖民中的Transwell膜上代表A549细胞伤口修复,分别用SF和10%胎牛血清(FBS) - 甲型DMEM(n = 3)。i)代表性激光扫描共聚焦微观图像A549-H441直接联络共同培养伤口修复。DII标记的红细胞是A549,DIO标记的绿色细胞迁移H441细胞。结果显示为平均值±SD..ns:不重要;H2O2:过氧化氢。*:P <0.05;**:P <0.01;* * *: p < 0.001。秤条=100μm(C,D,E,F和G)和150μm(i)。
TRAIL在H441和A549细胞中的表达谱
转录分析证实了TRAIL, TRAIL- r1和TRAIL- r2 mRNA在未损伤的H441和A549中的表达(无花果。6A).免疫细胞化学在未受伤的肺泡A549细胞中检测到较高水平的TRAIL-R1和-R2表达,而不是H441细胞,而逆转是足迹(无花果。6B.).
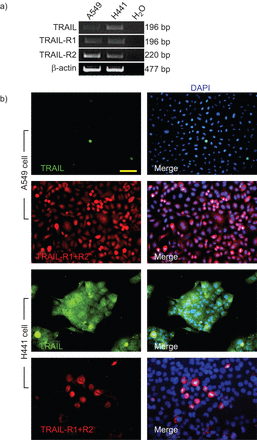
肿瘤坏死因子相关的凋亡诱导配体(TRAIL)和TRAIL受体(R)表达谱。a)A549和H441细胞的TRAIL,TRAIL-R1和TRAIL-R2的RT-PCR。b)A549和H441细胞中的TRAIL,TRAIL-R1和TRAIL-R2的免疫细胞化学。4',6-二氨基-2-苯基吲哚(DAPI)用于核的反染色。秤条=50μm。
H441细胞迁移到Saec伤口部位,并在SAEC-H441直接联络共同培养伤口修复系统中诱导细胞凋亡
虽然SAECS是PROSP-C阴性(数据未显示),并且由于它们适用于伤口修复模型的适用性,但不代表II型肺泡上皮细胞[31.我们复制了一系列使用A549细胞进行的主要实验,以排除结果中可能存在的癌症细胞系相关偏差。首先,我们评估了H441细胞向损伤SAEC单层细胞的迁移特性。有趣的是,我们的实验总结了A549-H441直接接触共培养模型的观察结果。有相当一部分H441细胞在创面24小时后迁移到SAEC创面部位,其中迁移到近创面单层的H441细胞数量是创面间隙的7.25倍(每个场58个细胞)与每场八个细胞,P <0.001;无花果。7A,b和c)。径至与相关对照相比,径至A549细胞的凋亡响应诱导,虽然与A549细胞相比,但与A549细胞相比显着显着(在线补充图E8)。类似地,与SAEC单一栽培相比,表达TRAIL表达H441细胞在SAEC-H441直接接触共培养中诱导伤者SAEC的显着细胞凋亡(9.54%)与0.38%,p <0.001;无花果。7D-F.).SAEC trail阴性(在线补充图E9),共聚焦显微镜证实tunel阳性细胞核为SAEC,未迁移H441细胞(在线补充图E10)。在没有损伤的情况下,可忽略的H441细胞向SAEC层迁移(数据未显示)。
小气道上皮细胞(SAEC)-H441直接联络共同培养伤口修复。a)H441细胞将H441细胞迁移到SAEC JUXTA型单层和伤口间隙(n = 3)中。b,c)激光扫描SAEC-H441直接接触共培养的共聚焦微观图像B)0 H和C)24小时。DII标记的红细胞是SAECS,DIO标记的绿色细胞是H441细胞。垂直侧杆表示通过相应的Juxta卷绕单层和水平杆表示通过伤口间隙的Z切割。d)在SAEC-H441直接接触共培养伤口修复(N = 3)中24小时后苏克达卷绕单层的肝细胞凋亡。对于阳性对照,通过治疗200μM过氧化氢(H.)在SAEC单层中诱导细胞凋亡(H.2O2)24小时和阴性对照,仅使用无血清小气道基础培养基处理Saec单层。E-G)激光扫描末端脱氧核苷酸转移酶介导的脱氧酰氨氨酸三磷酸镍骨蛋白末端标记(TUNEL)测定对SAEC-H441直接接触共培养。红细胞是DII标记的SAECS,绿核是TUNEL-正阳性的核核。e)阴性对照,SAEC单一栽培。F)SAEC-H441细胞直接接触共培吸伤口修复。g)阳性控制。结果显示为平均值±SD..ns:不显著。* * *: p < 0.001。秤条=200μm。
在IPF肺的纤维化肺泡中检测到Trail表达表达的俱乐部细胞,其具有肺泡上皮细胞凋亡的关联
组织学上,所有IPF活检标本均表现为与普通肠道肺炎一致的特征;具体来说,是正常的未受影响的肺与重塑的纤维化肺交替出现的一种典型的斑块,累及I型肺细胞破坏,II型肺细胞增生,并伴有成纤维细胞灶和胶原型瘢痕。纤维母细胞灶反映了活跃的正在进行的纤维发生的部位。
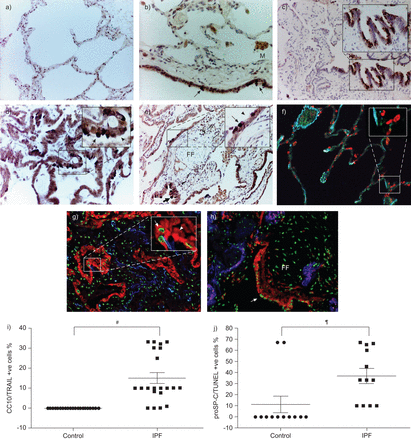
通过双免疫组织化学与俱乐部细胞标记物(CC)10和TRAIL抗体,研究了对照和IPF肺组织中的肺泡区域中表达肺泡区域的定位和IPF肺组织。在对照肺的肺泡区域未检测到双标记的CC10 / TRAIL Club细胞(无花果。8A)但在支气管墙上观察到(无花果。8B.).然而,在学习的21例IPF病例中有18个,在过溶血性上皮区域内容易检测到CC10 / TRAIL阳性俱乐部细胞(无花果。8D.)在肺泡上皮直接覆盖成纤维细胞上皮(无花果。8E).定量分析在IPF病例上平均呈15%CC10 /尾标上皮细胞(P = 0.0004;无花果。8i.).
肿瘤坏死因子相关的凋亡诱导配体(TRAP)和俱乐部细胞标记物(CC)10免疫组化和末端脱氧核苷酸转移酶介导的脱氧尿苷三磷酸镍缩镍骨贴标签(TUNEL)测定正常对照和特发性肺纤维化(IPF)肺组织中的免疫荧光样品。a)用CC10 / TRAIL抗体染色的对照肺双抗体的肺泡区域。在肺泡区中检测到没有CC10标记的俱乐部细胞。肺泡上皮细胞是阴性的。b)与正常对照肺的支气管肺泡区域的CC10 /痕迹的双免疫染色显示了支气管上皮(箭头的CC10标记的球杆细胞(用非常强烈的紫色(VIP))。巨噬细胞簇用痕迹标记,用3,3'-二氨基苯甲酸(DAB)(DAB)(DAB)可视化。没有肺泡上皮细胞用足迹标记。c)俱乐部细胞用IPF肺的增生肺泡区域的上皮内的CC10抗体标记(用DAB可视化)。d)在IPF肺的增生肺泡区域(箭头染色的箭头染色,用于CC10的DACK和VIP的箭头染色)中检测到双标记的CC10 / TRAIL俱乐部细胞。 Type II alveolar epithelial cells also showed positive to TRAIL immunostaining but negative to CC10 (arrowhead). e) CC10/TRAIL dual-labelled club cells were detected in the epithelium overlying the fibroblastic foci (FF) and hyperplastic regions (arrows). Alveolar epithelial cells were TRAIL-positive and CC10-negative (arrowhead). (Continued on following page). f) Pro-surfactant protein (SP)-C/TUNEL dual staining of control lung. TUNEL-positive nuclei were not detected in proSP-C-positive type II alveolar epithelial cells (red fluorophore-labelled). g) proSP-C/TUNEL dual-labelled cells (arrow) were detected in the hyperplastic regions of IPF lung tissue. A heterogeneous pattern of TUNEL-positive alveolar epithelial cells was observed. The arrowhead indicates a proSP-C-only cell. Notable numbers of inflammatory cells in the interstitial spaces were also TUNEL-positive. h) Apoptosis was detected in alveolar epithelial cells overlying the fibroblastic foci in IPF lung (arrow). Magnification: ×200 for all images. i) Quantitative analysis of CC10/TRAIL dual-positive cells in the alveolar region of normal and IPF lungs (21 IPF patients and 19 controls). j) Quantification of proSP-C/TUNEL-positive cells in the alveolar regions of IPF and healthy control lungs (12 IPF and 12 controls). Data are presented as mean±扫描电镜.#: p = 0.0004 (Wilcoxon配对符号秩检验);¶:P = 0.0035(Mann-Whitney U-Test)。
接下来进行双PROSP-C / TUNEL标记以鉴定IPF肺中凋亡肺泡上皮细胞的存在和定位,并与对照组织相比(图8 f-h).在IPF肺的成纤维灶和重塑的纤维化区域中,检测到TUNEL标记的pro - c阳性肺泡上皮细胞数量增加(IPF病例中平均37%的pro - c /TUNEL细胞与控制中11%;p = 0035;无花果。8J.).显着大,10次输出的12例对照病例未显示出对抗肺泡上皮细胞;然而,两种病例显示出大量的TUNEL阳性PROSP-C标记的细胞,无明显的组织学原因,因为检查的控制组织在形态上是健康的(无花果。8J.).尽管有这一发现,但综合这些数据,为肺泡上皮细胞凋亡和trail表达俱乐部细胞与肺纤维化纤维化的传播的潜在关联提供了证据。
讨论
俱乐部细胞在IPF中肺泡上皮损伤修复中的确切作用仍然未知。由于在表观增殖和迁移到IPF中受伤的肺泡后,恢复正常建筑和肺功能的恢复失败,因此不太可能是不可能的。11.,12.].在这项研究中,我们通过使用一种方法阐明了俱乐部细胞在肺泡上皮细胞伤口修复中的可能作用在体外伤口修复模型,致力于临纤纤化过程中的俱乐部细胞。第一次演示通过依赖于依赖的机制,俱乐部细胞诱导肺泡上皮细胞凋亡提供了以前未被发现的细胞行为的证据,这具有对肺病理生理学的影响。我们进一步证明,表达迹线表达的俱乐部细胞不仅诱导了肺泡上皮细胞系中的细胞凋亡,而且诱导了原发性人的SAEC。肺泡上皮细胞上的俱乐部细胞行为是特定的细胞类型,如图所示通过正常肺成纤维细胞在肺泡上皮细胞上的对比行为。此外,在IPF肺中肺泡细支气管俱乐部细胞表达TRAIL并与肺泡上皮细胞凋亡相关的观察表明,俱乐部细胞可能通过TRAIL介导的肺泡上皮细胞凋亡诱导,驱动异常的肺泡创伤修复事件级联,并传播随后的纤维形成。独立的内部研究表明,在IPF肺的肺泡上皮细胞中TRAIL-R1和-R2受体显著上调,进一步支持trail介导的IPF肺泡上皮细胞凋亡的可能。
IPF的特征在于由于凋亡,多发性上皮 - 间充质稳态,基底膜破坏,不平衡的免疫应答,肺泡上皮细胞损失和肺泡支气管化而导致异常的肺泡伤口修复2,4- - - - - -12.].肺泡细支气管化在异常创面修复中的作用以及俱乐部细胞和肺泡上皮细胞之间相互作用的确切性质都是相对不明确的。细支气管化被假定为化学诱导肺纤维化和人IPF肺组织中异常肺泡创伤修复的指标[11.,12.].
在IPF中的纤维发生期间,俱乐部和其他支气管细胞出现在已建立的纤维化区域的肺泡区域中,直接接触肺泡上皮细胞。虽然精确的机制是未知的,动物模型和离体IPF组织的研究表明,Caveolin-1的下调(抑制上皮增殖的膜蛋白)刺激了支气管和俱乐部细胞增殖[11.[基质金属蛋白酶-9的上调促进其迁移到受影响的肺泡中,导致肺泡支气管溶解[15.].最近的一项研究表明在IPF肺部的支气管化和肺重塑过程中提出了Neuregulin1α依赖性异位粘液细胞分化[32.].在我们的模型中证实了俱乐部细胞行为的迁移方面,其中H441细胞迁移到受伤的肺泡A549细胞和SAEC层,大部分可能由趋化机制驱动,因为在没有A549或SAECS的情况下,未观察到俱乐部细胞迁移。这种迁移伴随着对肺泡上皮细胞伤口修复的抑制作用通过肺泡上皮细胞的血迹介导的凋亡。痕迹是肿瘤坏死因子超家族的成员,可以通过与小路径-R1和TRAIL-R2受体的相互作用诱导细胞凋亡(或者分别称为DR4和DR5)[27.- - - - - -29.].虽然在许多稳态人类细胞类型中检测到TRAIL及其受体的表达[33.,人们对它们的生理功能知之甚少。然而,TRAIL已被证明在t细胞介导的免疫调节功能和肠道上皮稳态中发挥重要作用[34.,35.].在这里,俱乐部细胞可以在肺泡A549细胞中诱导凋亡的观察结果为我们在IPF中发现的异常肺泡伤口修复中的Trail表达俱乐部细胞参与的假设提供了支持。
病理学上,IPF的特征在于其区域和时间异质性。受到近距离纤维细胞灶和胶原沉积的影响肺泡区域显示出延长的表达俱乐部细胞数(与对照健康肺活检相比),并且与升高的肺泡上皮细胞凋亡相关。此外,在IPF肺中,迹阳性肺泡上皮细胞显着存在于过增殖型立方体化的肺泡和上皮细胞覆盖的纤维细胞焦点。相比之下,对照肺的肺泡上皮细胞没有表达踪迹。在其他慢性疾病状态下报道了痕迹介导的细胞凋亡。例如,在慢性胰腺炎中,胰腺星状细胞过表达迹线,通过诱导实质细胞中凋亡的诱导术后直接导致缩醛回归通过患道受体介导的凋亡机制[36.].据报道,trail介导的凋亡是人类糖尿病肾病进展的关键媒介,肾小管上皮细胞中trail过表达与严重的肾小管萎缩和间质纤维化相关[37.].其他研究表明,通过介导的凋亡和炎症性肠病等炎症性细胞凋亡和进展,如溃疡性结肠炎和克罗恩病的进展相关的肠上皮细胞的肠道上皮细胞的上调性上调,而下调与疾病的难治阶段相关[38.,39.].慢性内质网应激和fas - fasl介导的肺泡上皮细胞凋亡及其与IPF中异常肺泡创面修复的关系已有报道[7,40].将文献证据与我们的研究结果相结合,在这里,我们建议小径介导的细胞凋亡可能在IPF中的肺泡上皮细胞凋亡和纤维生殖繁殖中发挥至关重要的作用;这可能是介导的通过在肺泡支气管化上会导致活化的TRAIL-CLOB细胞。这些发现者解开了危急的目标,用于进一步调查新型治疗剂的发展,也许与组织工程伤口修复建模组合。
脚注
本文提供了补充材料www.www.qdcxjkg.com
根据呼吸杂志编辑委员会的决定,现在推荐使用“俱乐部细胞”的名称,并将在《呼吸杂志》中取代“克拉拉细胞”欧洲呼吸杂志.
支持声明
该研究由北斯塔福德郡大学医院(斯托克-on- trent,英国)多萝西·霍奇金医学研究委员会研究生奖和呼吸医学胸部基金理事会联合资助。
感兴趣的语句
没有宣布。
- 已收到2011年12月5日。
- 接受2012年6月22日。
- ©2013年