摘要
MicroRNAs (miRNAs)是一类内源性非编码小RNA分子,通过转录后抑制基因表达调控生理和病理过程。它们最初被认为是蠕虫和果蝇发育的调节器。近年来,广泛的研究探索了它们在人类疾病发病机制中的关键作用。迄今为止,已经发现了1000多个人类mirna;然而,大多数的生物学功能和蛋白质靶点仍未被揭示。在呼吸系统中,mirna在正常肺发育和维持肺内环境平衡中非常重要。最近的研究也开始揭示,改变的miRNA表达谱可能与肺内的病理过程有关,并导致各种肺部疾病的发展,从炎症性疾病到肺癌。进一步了解mirna在呼吸系统中的作用将有助于为疾病机制提供新的视角,并揭示呼吸疾病有趣的治疗靶点和诊断标志物。
人类基因组曾被预测含有>10万个蛋白质编码基因,这是基于我们作为复杂生物将拥有大量基因的假设。我们现在知道,人类基因组中有少于30,000个蛋白质编码基因——只比不复杂的线虫略多一点秀丽隐杆线虫[1].然而,在过去的十年中,我们也了解到,蛋白质编码基因(转录为mRNA)只占人类基因组的2%,而绝大多数被转录为非蛋白质编码RNA (ncRNA) [2].这些NCRNA在我们的体内涉及许多重要的角色,包括蛋白质合成(转移RNA和核糖体RNA),mRNA(抗乳糖体RNA)的剪接和基因表达调节(microRNA)。
microrna (mirna)是一种小的ncRNA分子(长度约为22个核苷酸(nt)),构成了广泛的基因调控层。它们通常通过翻译抑制和mRNA降解作为内源性基因活性抑制因子。它们对包括细胞增殖、凋亡和分化在内的许多生物学过程都是至关重要的。事实上,计算分析表明,mirna可能调节60%的人类基因组[3.那4.].尽管它们是1993年在线虫中首次发现的秀丽隐杆线虫[5.],“microRNA”一词直到2001年才被引入[6.].超过1,000人miRNA序列现在被认定,其中有许多在其他生物体是高度保守的,这表明它们代表了相对较老的和重要的管制途径[7.-9.].MiRNA与敲击单一基因的转录的更熟知的小干扰RNA(siRNA)不同,因为单一miRNA可以靶向几百个不同的mRNA。表1总结了miRNAs和sirna之间的一些区别。
从代谢性和炎性疾病到恶性肿瘤,一些人类疾病与miRNA表达的失调有关[11-15].mirna对适应性和先天免疫也至关重要,对细胞分化和免疫功能具有调节作用[16].然而,尽管我们越来越认识到它们在人类疾病中的作用,但对于它们的功能靶标、生物学相关性和在发育和疾病中的多因素作用,我们仍有许多了解。本文就mirna在呼吸系统疾病中的新作用进行综述。
microrna的生源论
miRNA生物生成涉及一系列复杂的步骤(图1),开始于细胞核,完成于细胞质。miRNA基因定位于基因组DNA中蛋白质编码基因的非编码区或内含子中。在细胞核内,初级miRNAs (pri-miRNAs;一般>1 kb长)主要由RNA聚合酶II转录[9.].pri-miRNA经历一系列内核水溶步骤,包括核RNase III酶的切割称为“DROSHA”[17-19].由此产生的70 nt pre-miRNA被积极运输到细胞质中,并被一种称为“Dicer”的细胞质RNase III酶加工成一个22 nt的双链miRNA。其中一条代表成熟miRNA的双链被纳入rna诱导沉默复合体(RISC),而另一条链则被降解。miRNA组装到RISC中,通过翻译抑制或mRNA降解来调控基因表达,这依赖于miRNA 5 '区(种子序列)和mRNA 3 '非翻译区(3 ' utr)之间的序列互补[9.那20.那21].最近已经表明,靶mRNA降解或不稳定是用于降低蛋白输出的主要机制:通过左右的miRNA介导的靶抑制的84%是由于降低的mRNA水平,这超过先前的估计[22].
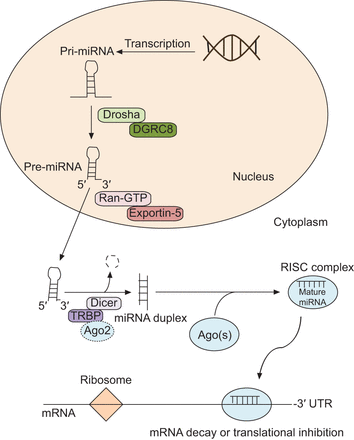
微rna (MicroRNA的)生物起源。Pri-miRNA:初级microrna的;DGRC8:迪乔治综合征关键区基因8;Ran-GTP: ras相关核蛋白-鸟苷-5'-三磷酸;TRBP:反式激活反应rna结合蛋白;前:Argonaute蛋白质;RISC: rna诱导沉默复合物;UTR:翻译区。
分析miRNA表达和靶基因鉴定的策略
miRNA是从传统的RNA在结构上不同(例如用于分析和量化传统rna的方法需要改进和适应mirna的研究。早期,Northern blotting和cDNA arrays被用来研究mirna。最近,出现了一系列的技术,在表2.
定量PCR, 2004年首次发展[23],通常用于确定两个组的样品,通常是一个“正常”控制和“疾病”样品之间的差异。这个评估的准确性是关键依赖于数据的适当的归一化,以除去尽可能多的变化,因为这些基团除了之间可能的变化是疾病本身[的结果24].理想地,规范器是单个核酸始终在所有样品中表达,并且证明了等效的存储稳定性,萃取和定量功效作为靶miRNA。偶尔,多于一种miRNA规范器/内源控制,以便用于提高精度和鲁棒性。对于微阵列,其他数据驱动标准化方法是经常使用的,并且包括平均表达归一化和分位数标准化[25].最后,当比较样本组时,除了相对表达外,考虑绝对的miRNA水平也是有用的:从1000到2000单位的变化可能被认为比从5到10单位的变化更具有生物学相关性[26].
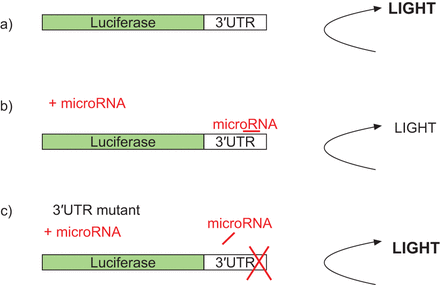
每个miRNA都有数百个进化保守的目标和数倍于其数量的非保守目标[27].还认识到,多个miRNA可以靶向相同的基因,表明它是确定基因表达和相互作用的生物学意义的所有这些活性的组合[28].计算算法是预测miRNA靶标的主要驱动力,大多数研究人员使用诸如Pictar,Targetscan,Mirana,Mirbase和Mirgen的目标基因预测数据库[29].不同的算法可能产生不同的miRNA-mRNA预测,并且必须必须有人知道,可能存在可能存在误报(对统计上显着但无法验证的对)和假否定(结果中缺少的真实对)。常见的做法是专注于多种算法预测的目标。用于验证miRNA靶基因的一种常用技术是过表达或抑制所选细胞中的miRNA,评估这是否对应于靶mRNA编码的蛋白质量的可预测变化,并证明这相当于生物功能的变化.为了补充并确认miRNA和mRNA之间的直接分子链路,靶mRNA的3'UTR可以克隆到荧光素酶报告中。然后将重组质粒以及感兴趣的miRNA转染到细胞和荧光素酶活性或测量的发光[30.那31](图2).
荧光素酶测定。对应于靶基因的3'未翻转区域(UTR)的DNA序列克隆到荧光素酶报告中,使其能够对荧光素酶蛋白的翻译进行控制。将重组质粒转染到细胞中,其中表达荧光素酶蛋白的mRNA和融合的3'UTR,含有miRNA结合位点。a)可以通过测量发光来评估荧光素酶的表达。b)将重组质粒与感兴趣的miRNA一起转染到细胞中。miRNA对3'UTR的结合将抑制荧光素酶报告蛋白的产生,并产生较少的“光”。c)进一步证实结果,可以将疏忽患者的突变版本与感兴趣的miRNA进行转染到细胞中的荧光素酶报告器构建体。由于缺乏序列同源性,MiRNA无法与3'UTR结合并不能对荧光素酶报告蛋白的翻译产生抑制作用;未观察到“光”生产的减少。
米兰航空的调节
大多数mirna被预测会靶向数百个mrna,同时靶向多个基因通路,以微调基因表达。因此,在转录、miRNA加工、靶标相互作用等多个层面上,miRNA的功能受到多种机制的严格调控[32].在转录水平上,已经确定了一些直接与miRNA启动子元件结合并控制其表达的调控因子。例如,肿瘤抑制基因p53已被证明与miR-34家族的启动子区域结合并激活它们的表达。miR-34过表达体外导致细胞周期阻滞和凋亡,其效果类似于单独强迫p53表达[33-35].miRNA的转录似乎也受表观遗传控制,并依赖于甲基化状态。这是由观察到的miRNA基因的子集驻留在CpG岛的支持。这与肺癌的发展有潜在的相关性,与正常肺中let-7a位点的广泛甲基化相反,在一些肺腺癌患者中,let-7a位点是低甲基化的。这些发现表明,某些miRNA位点的表观遗传控制缺失可能导致恶性转化[36].miRNA的成熟一旦被转录,就受到调控因子的严格控制,在Drosha核加工水平上都有阳性和阴性的控制[37那38,以及对pre-miRNA转运出核的影响[39]和/或Dicer的细胞质加工[40那41].
靶mRNA 3'UTR区域内的多态性也可能损害miRNA的调控和结合[42].例如,人类白细胞抗原(HLA)G的3'UTR单核苷酸多态性影响了3个mirna对该基因的靶向,表明这些mirna的等位基因特异性靶向可以解释HLAG是哮喘易感性基因的观察[42那43].免疫应答本身也有可能调节miRNA水平[44].L.国际单位等等。[45]的研究表明,细菌内毒素诱导miR-147的表达,miR-147可减弱巨噬细胞中toll样受体(TLR)刺激诱导的炎症反应,防止过度炎症反应。白介素(IL)-13是哮喘气道中的一种主要细胞因子,已被证明可下调支气管平滑肌细胞中miR-133a的表达,从而改变这些细胞的表型[46].mirna也可能受到环境因素的调控,如吸烟、污染物和饮食[32那47那48].让人着迷,这可能对后代的影响,因为它已经在小鼠模型中得到证实,产妇高脂肪食物导致关键miRNA的表达改变后代[49].
参与呼吸系统疾病
已被证明MiRNA以组织特异性和发育阶段特异性方式表达[50.-52.].肺已经被证明有一个非常特殊的miRNA表达谱这些miRNA对肺发育和维持肺内环境平衡非常重要[53.那54.].通过肺部特异性缺失的MiRNA的全球降低导致肺部发展期间的异常细胞凋亡和气道分支[55.].miR-17 -92簇(包含miR-17, -18, -19, -20和-92)被认为调节肺发育,因为它在胚胎肺中表达高,并在发育到成年后稳步下降[56.].miR-17-92簇缺陷的小鼠肺发育不良,而miR-17-92簇过表达导致末端细支气管缺失,这些细支气管被增殖的、未分化的上皮所取代[56.那57.].除了参与健康和发展之外,还表明MiRNA的病程可能使一系列肺病症提出。
肺癌
肺癌是全球癌症相关死亡的主要原因。尽管医疗保健和技术取得了进步,但自20世纪70年代以来,5年生存率并没有显示出显著的改善,这强调了对早期检测、预测和靶向治疗的新模式的需求。miRNA的错误表达已经在一些实体和血液系统的恶性肿瘤中被证实。观察到约50%的miRNA基因位于与癌症相关的基因组区域或脆弱位点,这些基因在肿瘤发生过程中经常被放大或删除,这突出了它们在癌症中的重要性[58.].随着我们对mirna理解的不断加深,我们越来越清楚,mirna不仅参与肺癌的发展和进展,而且可能作为诊断、预后和治疗反应的生物标志物。肿瘤中常见的miRNA失调有两种模式。第一个发生在实体肿瘤中,其中一组mirna被解除调控,这表明这些mirna可能参与了关键的细胞通路,如细胞粘附和信号传递,细胞周期调控和凋亡。其次,某些miRNA仅在特定肿瘤中被解除调控,这表明某些肿瘤特异性微环境可能有利于特定的miRNA谱,允许它们作为生物标志物使用。
肿瘤抑制miRNAs和致癌miRNAs
癌基因和肿瘤抑制基因的癌症的发病中的作用是众所周知的,miRNA的不仅控制已知蛋白质编码癌基因和肿瘤抑制基因的表达,而且还充当直接癌基因和肿瘤抑制基因[59.].
与正常肺相比,一些mirna在肺癌中表达水平较低。其中,let-7家族因其肿瘤抑制活性而被广泛研究。这是在肺癌中发现的第一组下调的mirna。Let-7已被证明负调控RAS癌基因的表达[60.]并且,当鼻内给药时,减少肺癌RAS小鼠模型中的肿瘤形成[61.].Let-7在肺癌细胞系中的过表达体外抑制癌细胞生长[62.],而在肺癌切除术病例中let-7表达降低与术后生存差相关,且与疾病分期等其他预后因素无关[63.].此外,Let-7在肺癌细胞中的过度表达体外已经被证明可以抑制放射抗性,这表明它也可以作为一种工具来加强目前的癌症治疗[64.].
miR-17-92簇已被证明在肺癌中显著过表达,特别是小细胞肺癌[65.].当过度表达时,它能够通过提高细胞增殖,抑制细胞凋亡和增加肿瘤脉管系统来靶向多种细胞途径以青睐肿瘤内酯[66.].这些血管效应与通过这个miRNA簇抑制抗血管生成蛋白血栓反应蛋白-1和结缔组织生长因子有关[67.].相反,在肺癌细胞系中,抑制该群集的某些成员已被证明可诱导凋亡并减少细胞生长[68.].
肺癌生物标志物、诊断与预后
mirna作为生物标志物特别有吸引力,因为它们在可获得的体液中保持稳定的形式,而且它们的表达模式很容易在血液、唾液和尿液中检测到[69.那70].例如,有报道称血清中mirna表达模式的差异可以正确区分健康受试者和肺癌和结直肠癌患者[71.].在体液中,MiRNA被认为是自由循环的并且浓缩在外泌体(细胞分泌的小微泡,包括上皮细胞,淋巴细胞,树突细胞和神经元)[72.那73.].
由于与一些这些治疗相关的严重有时危及生命危及生命的并发症,生物导向疗法的最新进展需要更准确的NSCLC次分类。使用福尔马林固定组织,已经开发了一种基于miRNA的诊断测定,可以将具有高灵敏度(96%),特异性(90%)和再现性分类的NSCLC [74.].MiRNA测定的敏感性和特异性有利地与组织学诊断相比,使其成为未来有前途的工具。此外,MiRNA还可用于区分源自其他原发性肿瘤的原发性肺肿瘤和肺转移[59.].
最后,MIRNA可用于帮助预测预后和癌症生存期。它已在112例NSCLC患者中显示,其中五分之一签名(Let-7a,miR-221,miR-372,miR-137和miR-182 *)与生存和癌症复发相关[75.].在他们的肿瘤标本中,这5个mirna标记的高风险评分的患者增加了癌症复发和缩短了生存期,甚至在按分期或组织学亚组对患者进行分层之后。此外,已有研究表明,8种mirna的表达与腺癌患者的生存相关[76.],而最近,成熟miR-21和在的miR-196A-2中的单核苷酸多态性已被发现与生存在NSCLC患者[相关联77.那78.].
其他相关的生物学功能
P53蛋白是众所周知的主要肿瘤抑制剂,其编码基因在大约一半的人类癌症中突变,而在大多数剩余部分中的剩余部分是灭活的。证据开始出现,P53的许多作用包括细胞凋亡和衰老,由miRNA介导[79.].
已知异常表皮生长因子受体(EGFR)表达导致正常细胞生长过程中的异常并引发癌症。在几个恶性肿大中指出,EGFR表达增加,它已成为目标疗法的焦点[80].它被miR-128下调,miR-128是一个在肺癌中经常缺失的miRNA。W.eis等等。[81研究表明,在58例NSCLC患者的肿瘤样本中,miR-128b杂合度缺失是常见的,并且与egfr -酪氨酸激酶抑制剂治疗后的临床反应和生存显著相关。
miRNA和免疫反应
呼吸上皮不断地暴露于许多异物,包括毒素和潜在病原体。人类免疫系统已发展成为一种高度复杂和适应性的防御机制,可保护我们免受这些外国和有害物质。在适应性和先天免疫中,MIRNA已被证明是枢转,包括控制各种免疫细胞亚集的分化以及其免疫功能[16那57.那82-91].
mirna和先天免疫反应
先天免疫反应提供了抵御外部病原体感染的初始防御,主要是介导的通过骨髓细胞,如巨噬细胞,树突细胞,单核细胞和中性粒细胞。几种miRNA,包括miR-155,miR-146和miR-223,在通过TLRS识别病原体后调节急性炎症反应[92].例如,响应于内毒素的巨噬细胞系中,miR-132,miR-146和miR-155在巨噬细胞系中进行上调[93].miR-146诱导由识别细菌成分和促炎细胞因子如IL-1β的TLR触发。通过促进炎症的分辨率,它似乎在严重炎症期间提供了重要的反馈机制[94].这可能与mir -146诱导的与促炎转录因子核因子(NF)-κB活化相关的关键成分下调有关。miR-155被认为在巨噬细胞中上调是暴露于广泛的炎症介质和病毒和细菌产物的结果[44那95].一旦被诱导,它调节炎症介质的释放,并提高肿瘤坏死因子(TNF)-α的产生[95].mir - 155也起着至关重要的作用在宿主防御传染病,因为它已经被证明可以调节的成熟树突状细胞(DC)的能力和影响这些专业结合病原体的抗原递呈细胞表达下调DC-specific的表达细胞间粘附molecule-3抓住non-integrin [96].miR-223已被发现在调节粒细胞增殖和激活中发挥关键作用[91那97-99,尽管就其影响而言,存在着相互矛盾的结果。单独的研究已经确定miR-223是粒细胞分化的正调控因子和负调控因子[98那99].尽管这些结果自相矛盾,但miR-223被认为在调节炎症反应中发挥着不可或缺的作用,这得到了功能研究的支持。暴露于雾化内毒素的小鼠肺和气道上皮中miR-223表达迅速增加[100.],而miR-223敲除小鼠在内毒素刺激后自发发生肺病理和过度组织破坏[97].这些结果表明,miR-223可能也是肺炎症反应的负调控因子。
mirna和适应性免疫反应
适应性免疫反应包括通过激活抗原特异性淋巴细胞和随后的克隆扩增来选择性识别和清除入侵的病原体。
t细胞
miRNA的表达随着t细胞发育阶段的不同而不同,miRNA也调节抗原刺激t细胞的分化状态[101.那102.].的miR-181微调T细胞的灵敏度和阳性选择和通过调节T细胞受体的信号传导调节强度T细胞应答的抗原定量水平[101.那103.].miR-155也参与T细胞分化和激活。在miR-155-null小鼠中,CD4 + T细胞显示朝向T-辅助细胞(TH)2型表型的内在偏压,具有增强的TH2细胞因子IL-4和IL-5水平[90].此外,miR-155在调节性CD4 t细胞(Treg)的产生和功能中发挥重要作用[16].Treg细胞是CD4+ t细胞,负责抑制Th细胞潜在的有害活动,其功能包括维持自身耐受性和抑制呼吸道疾病,如哮喘和过敏。
miRNA和香烟烟雾
全世界约有13亿人吸烟,吸烟是包括肺癌和慢性阻塞性肺病(COPD)在内的呼吸系统疾病的一个重要危险因素。烟草烟雾已被证明影响支气管上皮miRNA的表达,其中28个miRNA在当前吸烟者与终身不吸烟者中表达不同[47].在吸烟人群中,大多数都被下调了。由于这些mirna中的一些(miR-218, miR-15a, miR-199b和miR-125b)也被证明在其他癌症中下调,这些变化,通过暗示,与烟草相关的恶性肿瘤的发展有潜在的相关性[76.那107.-109.].
基于动物的研究也有联系卷烟烟雾暴露,miRNA改变和癌症发育。暴露于香烟烟雾的大鼠在肺部miRNA表达中发挥广泛的改变,大部分观察到的改变涉及下调[110].最显着下调的miRNA属于调节应激反应,细胞凋亡,增殖和血管生成的家庭,致癌物中的所有枢轴过程。例如,卷烟烟雾已被证明是下调Let-7家族的MiRNA。如前所述,已发现Let-7在人肺肿瘤中表达不当,其抑制导致肺癌细胞的增加体外[111],低let-7表达的肺癌患者生存时间短于高表达的肺癌患者[76.].在啮齿类动物中香烟烟雾暴露也被证明下调参与沉默血管生成活动,提供的证据表明,香烟烟雾刺激肺血管生长[几种miRNA110].值得注意的是,这些变化在癌症发生前就很明显,是对环境致癌物暴露的早期反应。最后,在啮齿动物研究中,香烟烟雾下调了参与NF-κB通路的几种mirna,从而导致NF-κB激活、核易位和炎症[110].
miRNA和COPD
COPD是由气流受限限定的异质性疾病,是不是完全可逆的和肺的伤害性刺激,特别是香烟烟雾[异常持续性炎性反应112].miRNA在改变的免疫反应和COPD的稳态机制中的作用开始出现。发现34个miRNA与来自烟草的诱导的痰液差异表达,与当前没有COPD的吸烟者相比,当前吸烟者八个MiRNA与COPD的吸烟者显着降低了,而不是吸烟者(MIR-34C,MIR-218,MIR-34B,Let-7c,miR-342-3p,miR-125a-5p,miR-30e-3p和miR-125b)[113].let-7c水平与TNF受体II型(TNFR-II)蛋白水平显著负相关,这与COPD的发病机制有关。在COPD小鼠模型中,敲除TNFR-II可防止卷烟诱发的炎症和肺气肿的发展[114].有趣的是,与从不吸烟的人相比,let-7c仅在当前COPD吸烟者中降低,而在已戒烟的COPD吸烟者或非COPD吸烟者中没有降低,这表明let-7c参与了吸烟导致的COPD的发展,但与戒烟后气道炎症的持续存在无关。
来自COPD受试者和非COPD吸烟者肺组织的表达谱显示了70个差异表达的mirna,包括miR-223, miR-127a, miR-424和miR-15b [115].该组浓缩在miR-15b上,发现表达与Spiromatry评估的COPD的严重程度相关[115].有趣的是,的miR-15B能够调节转化生长因子(TGF)-β途径,在气道重塑COPD牵连的关键生长因子的组成部分。
目前公认的是,异常修复反应参与了COPD的发病机制。COPD患者的成纤维细胞已被证明在炎症细胞因子的反应中低表达miR-146a体外,导致环氧合酶-2的过度表达和前列腺素(PG)E的增加2[116].铂族元素2是否已知在COPD患者的肺部增加炎症调解蛋白,也是肺成纤维细胞修复功能的有效抑制剂[117那118].通过气流限制和扩散能力评估,细胞因子刺激的miR-146a表达也与COPD的临床严重程度相关。
哮喘
哮喘是一种常见的呼吸系统疾病,其特点是可逆的气流限制、慢性气道炎症和组织重塑。该疾病的发病机制涉及遗传因素和环境触发因素,其特征是Th2反应异常。尽管有研究强调了mirna在炎症过程中的作用,但很少有人专门研究它们在哮喘发病机制中的作用。本研究小组的研究表明,miR-155通过调节人巨噬细胞对IL-13的反应,在Th2表型的获取和维持中发挥着核心作用[119].IL-13是一个关键的TH2-衍生的效应细胞因子,被认为与哮喘发病机制相关,并诱导过敏气道炎症。显示MIR-155的抑制导致涉及Th2微环境的转录因子的增加,这意味着该miRNA在哮喘发病机制中。还提出了IL-13可以通过下调miR-133a水平来调节支气管平滑肌细胞的表型,并导致RhoA蛋白的表达增加[120那121].RhoA的是在平滑肌收缩的关键蛋白质和其上调与支气管平滑肌的增强收缩相关[122那123].
一项在哮喘小鼠模型上的实验研究发现,在过敏性气道炎症小鼠和对照组小鼠之间有差异表达的21个mirna [124].特别是,miR-21的过表达和miR-1的抑制在IL-13转基因小鼠中很明显——这些小鼠以肺特异性的方式过表达IL-13。miR-21被认为靶向IL-12,这是一种巨噬细胞来源的细胞因子,参与涉及Th1细胞极化的适应性免疫反应。miR-21的升高会导致IL-12的降低,并可能引发Th2和il -13相关的反应。IL-12的下调也被证明会影响Treg细胞的功能,导致促炎表型。miR-1被鉴定为下调幅度最大的miRNA。它被认为是一种肌肉特异性miRNA,对正常肌肉生理很重要[125那126].miR-1下调与心脏和骨骼肌肥大有关[127那128,有趣的是,推测它也可能导致哮喘中的平滑肌肥大和重塑。
在屋尘螨引起的过敏性哮喘的小鼠模型中,的miR-16水平,以及-21 -126已经报道相比于对照动物被显著升高。的miR-126的相关性还建议在急性过敏性炎症的小鼠模型中,其中RNA拮抗剂的鼻内给药抑制的miR-126导致的气道高反应性的抑制对乙酰甲胆碱,粘液分泌过多和嗜酸性粒细胞的抑制的衰减招聘 [129].然而,在房屋粉尘敏感模型中,被认为反映慢性哮喘,同样的治疗方法只能抑制嗜酸性粒细胞招募到气道,对气道壁炎症或改造没有影响[130].这表明并强调了多种mirna可能调节慢性疾病,如哮喘。
如前所述,miR-146被认为在先天免疫系统激活后炎症的负反馈调节中发挥关键作用。在哮喘气道中,miR-146被认为发挥了类似的作用。据报道,miR-146水平的升高可减少气道平滑肌细胞和肺泡上皮细胞il -1β诱导的IL-6和IL-8的释放[94那131].重要的是,这种负调节仅在高IL-1β浓度下观察到,表明它可能是严重炎症期间的重要反馈机制。
其他研究小组已经开始在哮喘患者和正常对照组之间寻找miRNA表达谱的差异。其中一项研究调查了轻度哮喘患者和非哮喘健康对照组的支气管活检中227个miRNAs的表达,发现没有miRNAs的表达有差异[132].有趣的是,这项研究还表明,尽管皮质类固醇治疗改善了肺功能,但并不影响miRNAs的表达。值得注意的是,气道内不同的细胞类型有不同的miRNA表达谱,这提高了在哮喘患者气道中出现不同miRNA表达的可能性,但在特定的细胞类型中。
其他呼吸系统疾病
最近,MiR-126表达已显示在囊性纤维化(CF)中下调相对非cf气道上皮细胞,其预测蛋白靶点TOM1 (Myb1的靶点)表达的交互增加[133].作者认为TOM1可能在CF肺中发挥抗炎作用,并推测其表达的增加可能是在这种情况下补偿高促炎负担的一种尝试。TOM1作为IL-1β和TNF-α诱导的信号通路的负调控因子,过表达TOM1抑制NF-κB活性[134].
人们的注意力集中在miR-21与肺纤维化的关系上。已经发现miR-21在博莱霉素诱导纤维化小鼠的肺中上调,在特发性肺纤维化患者的肺中也上调[135].另外,已经显示MIR-21通过TGF-β,纤维化疾病的关键病理介质,以及扩增电路中的功能来上调,以增强TGF-β1的促纤维化活性并促进纤维化肺病。miR-21抑制显着降低了脑膜霉素处理的小鼠肺中的胶原沉积,使其成为在治疗纤维化疾病治疗新疗法的潜在目标。可能预期的那样,这不是纤维化肺病中报告的唯一调控miRNA,另一项研究鉴定了18 miRNA,包括Let-7d,在特发性肺纤维化中显着降低[136].TGF-β可以降低Let-7D的表达,这导致上皮间充质转换体外在小鼠肺中增加胶原沉积和肺泡隔膜增厚体内.MiR-155也复杂地参与肺中的上皮-间充质相互作用,并特别减弱肺成纤维细胞释放的炎症细胞因子介导的角质形成细胞生长因子[137].这支持MIR-155在肺纤维化发病机制中的作用,并表明改变的miR-155表达在急性肺损期间也可能具有重要的病理生理学影响。与年龄匹配的对照相比,miR-155敲除小鼠的气道发育自发重塑,其特征在于胶原沉积增加和平滑肌质量[90].我们实验室的研究表明,过表达miR-155可减弱TGF-β诱导的促纤维化基因的表达[138].
结论
miRNA在基因调节中具有基本作用,具有调节多种基因途径的能力。它们在一系列生物过程中起重要作用,包括胚胎发生,分化,增殖,细胞凋亡,信号转导和致癌作用。近年来,还爆炸了MiRNA参与一系列人类疾病的报告,包括肺部的疾病和恶性肿瘤。这对潜在利用治疗剂中的疾病特异性miRNA和辅助诊断和预期产生了很多兴趣;因此,使用适当可靠的研究方法至关重要。我们仍然对MIRNA初步了解,并且尚未了解MIRNA在呼吸系统疾病中的具体和复杂作用。作为单一的miRNA可以靶向几百个基因,确定要专注于功能性研究的miRNA-mRNA对可能是挑战性的,并且即使一旦确认了分子相互作用,必须证明生物相关性。这可能极其艰巨且耗时,因为它不是需要研究的单一miRNA-mRNA连接,但多个miRNA靶向单一感兴趣的基因的影响。频繁地体外系统被用来验证miRNA的相互作用,需要小心避免错误的数据解释。然而,人们对这一激动人心的领域非常感兴趣,miRNA的成功翻译研究必将加深我们对疾病发病机制的认识,并影响呼吸系统疾病的预防、诊断、预后和治疗。
脚注
感兴趣的语句
没有宣布。
- 已收到2011年12月2日。
- 公认2012年6月21日。
- ©2013年