文摘
环前列腺素的保护作用及其稳定模拟iloprost介导细胞内的高程环腺苷酸(cAMP)导致增强外围的肌动蛋白细胞骨架,和胶粘剂的结构。本研究测试的假设iloprost可能出现对肺损伤的保护作用和内皮屏障功能障碍引起的细菌壁脂多糖(LPS)。
内皮屏障功能障碍被transendothelial渗透率的测量评估,形态和LPS-activated炎症信号的分析。在活的有机体内C57BL / 6 j小鼠,挑战与有限合伙人或没有iloprost 8-bromoadenosine-3′, 5′环一磷酸(Br-cAMP)治疗。肺损伤是由测量监控支气管肺泡灌洗蛋白质含量、细胞计数和伊文思蓝外渗。
Iloprost和Br-cAMP减毒的破坏内皮单层,并抑制p38增殖作用的激活蛋白激酶(MAPK),核因子(NF) -κB通路,ρ信号,细胞间粘附分子1 (ICAM)表达和嗜中性粒细胞迁移后有限合伙人的挑战。在活的有机体内,iloprost有效对抗LPS-induced蛋白质和中性粒细胞积聚在支气管肺泡灌洗液,并降低髓过氧物酶激活,ICAM-1表达和伊文思蓝溢出在肺部。抑制Rac活动取消iloprost和Br-cAMP barrier-protective和抗炎作用。
Iloprost-induced海拔细胞内营触发Rac信号,变弱LPS-induced NF-κB p38 MAPK炎症通路和Rho-dependent内皮通透性机制。
急性呼吸窘迫综合征常与脓毒症和仍然是发病率和死亡率的主要原因,30 - 40%的总体死亡率(1,2]。感染性肺损伤的急性期的特点是血管渗透性增加,表面粘附分子的表达,如细胞间粘附分子(ICAM) 1激活内皮细胞,促进白细胞粘附和招聘到肺,受损的液体平衡,富含蛋白质的液体在空中空间,积累和积累激活中性粒细胞在肺组织炎性细胞因子(综述(3,4])。总之,这些机制可能会导致严重的肺部炎症和肺水肿。然而,对细胞内的过程,确定肺内皮细胞屏障保护和减少炎症的急性肺损伤(ALI),和有效的阿里barrier-protective物质治疗仍有待确定。
临床观察和动物实验显示有益的升高细胞内环腺苷酸(cAMP)浓度在不同的肺疾病(5,6]。前列腺素我2或环前列腺素是环氧合酶(COX)的产物。内皮Aerosolised显示明显的防止氧肺损伤和肺损伤引起的缺血/再灌注。水平的提高稳定环前列腺素代谢产物与不太严重的呼吸窘迫相关(7,8]。然而,环前列腺素的影响在感染性肺损伤的模型没有被调查。
我们之前的作品描述的barrier-protective内皮的影响在人类肺内皮和ventilator-induced肺损伤的动物模型9,10]。大环前列腺素的生物效应及其稳定细胞内营浓度的模拟iloprost与海拔高度有关,这触发cAMP-activated蛋白激酶A (PKA)端依赖(11,12)和PKA-independent Epac-Rap1-Rac肺血管内皮屏障机制增强,涉及cAMP-induced激活鸟嘌呤核苷酸交换因子Epac导致激活的小gtpase Rap1和Rac19,13,14]。除了cAMP-mediated Epac-Rap1激活,Rac1可能是另外的刺激通过PKA-dependent机制和最近的报告描述了Rac1作为一个中心协调barrier-protective信号从PKA Epac-Rap1 [15]。
在这项研究中,我们使用生化、分子和功能描述iloprost效果的方法在体外和在活的有机体内LPS-induced肺损伤的模型。尽管iloprost-mediated承认PKA的潜在作用影响,在本研究中,我们关注Rac1保护作用的机制和研究它的作用iloprost对感染性炎症。
材料和方法
细胞培养和试剂
人类肺动脉内皮细胞(HPAECs)和细胞培养基获得Lonza Inc .(美国新泽西州Allendale),并在章节5 - 8细胞被使用。Iloprost得到从开曼群岛(美国安阿伯市MI)。Di-phospho-myosin轻链(多层陶瓷),phospho-heat休克蛋白(HSP) 27日,核转录因子(NF) -κB和抑制剂的NF-κB (IκB)α抗体从细胞信号(美国贝弗利,MA);phospho-vascular内皮(VE)钙粘蛋白和ICAM-1抗体从圣克鲁斯生物技术(圣克鲁斯、钙、美国);并从BD VE-cadherin抗体转导实验室(美国圣地亚哥,CA)。nsc - 23766和8-bromoadenosine-3′, 5′环一磷酸(Br-cAMP)从Calbiochem购买(La Jolla、钙、美国)。所有试剂免疫荧光分子探针买来(尤金,或者美国)。除非指定,生化试剂获得从σ(圣路易斯,密苏里州,美国)。
内源性Rac1枯竭
预先设计Rac1-specific小核RNA)的标准纯度被命令从Ambion(美国奥斯汀,得克萨斯州)。内皮细胞的转染核进行了如前所述[16]。非特异性,不属预定目标的核被用作控制治疗。转染48 h后,细胞用于实验或收获的免疫印迹验证特定蛋白质的消耗。
transendothelial电阻的测量
细胞屏障属性进行分析的测量transendothelial电阻(TER)支流HPAEC使用电子细胞基质层阻抗传感系统(应用生物物理学、特洛伊、纽约、美国)如前所述[16]。
Transwell渗透和迁移化验
渗透率为异硫氰酸荧光素(FITC)标记右旋糖酐在肺动脉内皮细胞单层生长在渗透过滤器在transwell化验使用评估在体外血管通透性试验设备(美国马Billerica Chemicon国际),根据制造商的指示。中性粒细胞趋化性测量在96 -趋化性室(美国马里兰州盖瑟斯堡Neuroprobe,,)如前所述[17]。初步实验建立了细胞的数量(4×104细胞)允许使用最优比例的细胞迁移没有堵塞的毛孔transwell上院的过滤器。数据迁移细胞的百分数表示。
免疫荧光
内皮单层镀在玻璃盖的过失受到免疫荧光染色如前所述[18]。幻灯片进行分析使用尼康视频成像系统(尼康Instech有限公司东京,日本)。图像处理与图像J(美国国家卫生研究院,马里兰州贝塞斯达)和Adobe Photoshop 7.0(美国加利福尼亚州圣何塞Adobe系统)软件。
差异蛋白质分离和免疫印迹
支流HPAECs与LPS刺激有或没有iloprost核分数是孤立使用S-PEK工具包(美国新泽西州EMD化工、Gibbstown)。免疫印迹检测感兴趣的蛋白质如前所述执行(16]。蛋白质提取物小鼠肺或内皮细胞被dodecylsulfate-polyacrylamide钠凝胶电泳分离,转移到聚乙二烯二氟化物膜和膜孵化与特定的抗体。平等蛋白质加载验证了通过reprobing膜β-actin或β-tubulin抗体。增强化学发光检测系统检测了免疫反应性的蛋白质根据制造商的协议(Amersham,小都,英国)。
动物研究
所有动物护理和治疗程序是由芝加哥大学的批准机构动物保健和使用委员会(美国芝加哥,IL)。动物被处理根据美国国立卫生研究院的指导的护理和使用实验动物。详细描述实验过程中提供了在线数据补充。
统计分析
数据均值±sd三到八个独立的实验。刺激样本相比,控制未配对t。多集团比较、单向方差分析和图基事后多重比较检验。p < 0.05被认为是具有统计学意义。
结果
iloprost对LPS-induced内皮细胞的影响研究进展
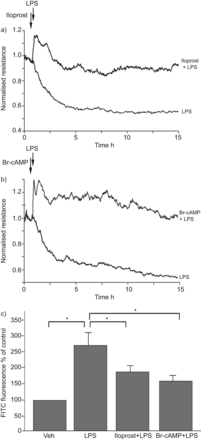
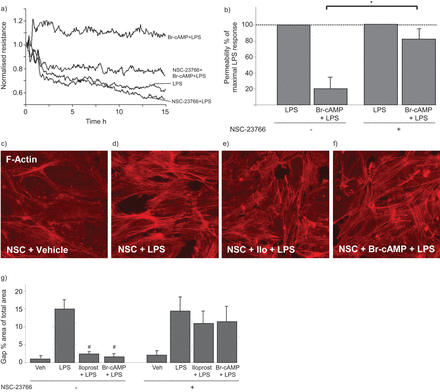
测试iloprost对内皮细胞屏障功能障碍的影响与感染性炎症有关,我们使用LPS-induced内皮细胞通透性的典范。有限合伙人和iloprost减少治疗废除这一效应(图1一个)。iloprost的保护作用主要是高度相关的细胞内营的水平,因为类似的保护作用是由内皮细胞复制治疗稳定的模拟,Br-cAMP (图1 b)。影响iloprost和Br-cAMP LPS-induced内皮细胞研究进展进一步测试溶质通量化验。iloprost和Br-cAMP减毒LPS-induced渗透率FITC-labelled右旋糖酐(图1 c)。
iloprost和8-bromoadenosine-3′, 5′环一磷酸(Br-cAMP)对脂多糖(LPS)全身的血管内皮细胞的通透性。人类肺动脉内皮细胞对微电极镀预处理与车辆(阿明费),ng) iloprost(200毫升−1ng)或b) Br-cAMP(500毫升−1),15分钟后用LPS刺激(300 ng·毫升−1),如箭头所示。Transendothelial电阻监控超过15 h . c)肺动脉内皮细胞与iloprost pre-incubated (200 ng·毫升−1ng)或Br-cAMP(500毫升−1)15分钟紧随其后的是一个有限合伙人(300 ng·毫升−1)5 h挑战和测量渗透率的异硫氰酸荧光素(FITC)标记右旋糖酐。渗透率数据均值±sd八个独立的实验。*:p < 0.05。
Iloprost变弱LPS-induced内皮细胞单层破坏
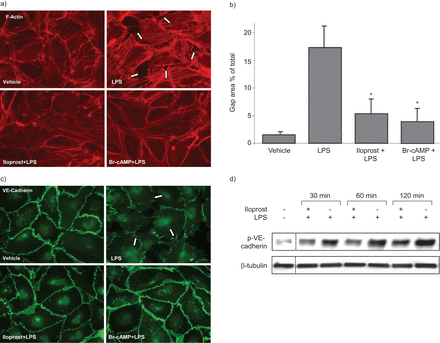
iloprost在LPS-induced内皮细胞破坏的影响被分析肌动蛋白细胞骨架改建计划和监控adherens结完整性的变化。LPS诱导肌动蛋白应力纤维的形成和细胞收缩与paracellular缺口的出现有关。这些变化是减少内皮细胞预处理与iloprost或Br-cAMP (图2 a和b)。免疫荧光分析adherens结改造确认中断响应有限合伙人的信息联系。反过来,iloprost和Br-cAMP预处理保存连续adherens结模式LPS-challenged内皮细胞(图2 c)。在Y731 Iloprost也减毒LPS-induced VE-cadherin磷酸化(图2 d),这是已知的促进adherens拆卸连接复合体(19,20.]。这些结果证明有效的保护作用对LPS-induced iloprost内皮细胞屏障功能障碍由阵营。
iloprost和8-bromoadenosine-3′, 5′环一磷酸(Br-cAMP)对脂多糖(LPS)全身的细胞骨架改建和差距的形成。内皮单层膜与车辆,预处理iloprost (200 ng·毫升−1ng)或Br-cAMP(500毫升−1)15分钟与LPS刺激(300 ng·毫升−1)5 h . a)分析肌动蛋白细胞骨架重排是由与德克萨斯州Red-phalloidin细胞免疫荧光染色处理车辆,有限合伙人,iloprost和有限合伙人,Br-cAMP和有限合伙人。Paracellular缺口的箭头。b)定量分析paracellular差距形成的控制和治疗人类肺动脉内皮细胞(HPAECs)。数据均值±sd四个独立的实验。*:p < 0.05相比,有限合伙人。c)免疫荧光染色法对血管内皮钙粘蛋白(VE)进行想象在细胞粘合连接处并且处理车辆,有限合伙人,iloprost和有限合伙人,Br-cAMP和有限合伙人。LPS-induced中断是粘合连接处并且箭头所示。d)免疫印迹分析时间VE-cadherin磷酸化与LPS有或没有iloprost HPAECs刺激预处理。β-tubulin染色被用作控制正常化。箭头长度对应5μm。
Iloprost抑制LPS-induced激活炎性信号
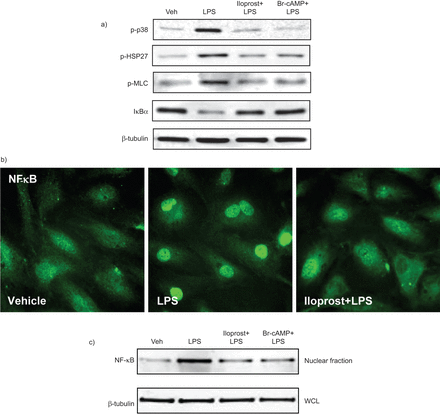
大量的信号分子,如压力激发了p38增殖蛋白激酶(MAPK) RhoA GTPase NF-κB复杂,LPS激活(21,22]。在接下来的实验中,我们测试了iloprost是否能够抑制这些barrier-disruptive通路。LPS激活p38 MAPK导致磷酸化p38 MAPK的下游目标HSP27和增加下游RhoA目标多层陶瓷的磷酸化。有限合伙人也引发了规范化的炎症通路和诱导退化IκBα抑制亚基主要NF-κB信号激活。这些影响被iloprost抑制或Br-cAMP (图3)。LPS-induced NF-κB-dependent炎症基因表达的激活需要核易位NF-κB p65亚基。免疫荧光分析(图3 b)和亚细胞分离分析(图3 c)核易位NF-κB有限合伙人的挑战后,由iloprost减毒或Br-cAMP。
iloprost和8-bromoadenosine-3′, 5′环一磷酸(Br-cAMP)对脂多糖(LPS)全身炎性信号。人类肺动脉内皮细胞)与车辆(阿明费),预处理iloprost (200 ng·毫升−1ng)或Br-cAMP(500毫升−1),15分钟后用LPS刺激(300 ng·毫升−1)1 h。p38增殖蛋白激酶的磷酸化,热休克蛋白(HSP) 27和肌球蛋白轻链(多层陶瓷)是通过免疫印迹检测到相应phospho-specific抗体。退化的抑制剂的核因子(NF) -κB (IκB)α使用nonphosphorylated蛋白抗体检测。证实了平等蛋白质加载完整的细胞溶解产物β-tubulin含量测定(水控制法)。细胞预处理与车辆或iloprost紧随其后的是一个有限合伙人挑战(300 ng·毫升−1)1 h . b) NF-κB核易位是评估与一个特定的抗体免疫荧光染色细胞处理车辆,有限合伙人,iloprost和有限合伙人。c)进行分离鉴定和内容的NF-κB核分数是由免疫印迹分析与特定的抗体。β-tubulin含量测定相应水控制法是用来确保平等的加载。
激活的血管内皮炎症因子刺激中性粒细胞粘附在血管内皮细胞衬里其次是中性粒细胞通过内皮细胞单层轮回,导致中性粒细胞炎症肺组织招聘。在接下来的研究中,我们评估了iloprost对内皮细胞激活的影响。免疫印迹分析ICAM-1表达式,内皮表面分子参与中性粒细胞粘附,显示时间增加LPS-induced ICAM-1表达式(图4)减毒iloprost或Br-cAMP预处理(图4 b)。因为LPS诱导血管内皮细胞,促炎细胞因子的生产促进中性粒细胞轮回,我们下一个评估前提中收集的影响从刺激内皮细胞中性粒细胞迁移。LPS刺激显著增加中性粒细胞迁移,而iloprost或Br-cAMP预处理抑制这种效应(图4摄氏度)。额外的实验显示LPS-induced interleukin-8肺动脉内皮细胞表达,由iloprost废除或Br-cAMP预处理(数据没有显示)。总的来说,这些数据表明iloprost的有力保护作用与激活的炎症信号引起的肺内皮有限合伙人。
iloprost和8-bromoadenosine-3′, 5′环一磷酸(Br-cAMP)对脂多糖(LPS)全身肺动脉内皮细胞的激活。)免疫印迹分析时间细胞间粘附分子1 (ICAM)表达在人类引起的肺动脉内皮细胞(HPAECs)有限合伙人(300 ng·毫升−1)。b) HPAECs与车辆(阿明费),预处理iloprost (200 ng·毫升−1ng)或Br-cAMP(500毫升−1),15分钟后用LPS刺激(300 ng·毫升−1)为4 h。ICAM-1表达式通过免疫印迹检测ICAM-1抗体。β-tubulin染色被用作控制正常化。c)细胞预处理与车辆,iloprost或Br-cAMP LPS刺激(20 ng·毫升紧随其后−1)为4 h。嗜中性粒细胞迁移试验方法部分中描述。数据意味着±sd三个独立的实验。*:p < 0.05相比,有限合伙人。
Iloprost——cAMP-stimulated Rac1信号变弱LPS-induced内皮细胞屏障功能障碍
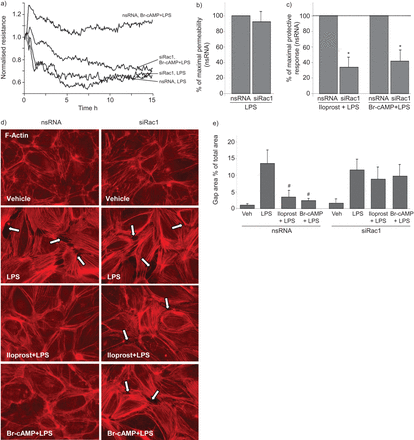
之前的作品展示的作用iloprost-activated Rac1信号增强内皮细胞屏障通过具体的外围细胞骨架重塑和增加信息连接的组装9,13]。以下实验测试Rac1机制参与iloprost抑制炎症的信号。siRNA-induced Rac1击倒并没有显著改变渗透独自应对有限合伙人,但减毒Br-cAMP的保护作用和iloprost LPS-induced渗透率(图5 a - c)。
影响的小核RNA)的Rac1 iloprost击倒——和8-bromoadenosine-3′, 5′环一磷酸(Br-cAMP)全身的内皮细胞屏障保护。人类肺动脉内皮细胞转染与小干扰rna (nsRNA)或非特异性Rac1-specific siRNA (siRac1) 48 h . a)细胞对微电极镀处理车辆(阿明费)或Br-cAMP (500 ng·毫升−115分钟)其次是脂多糖(LPS)刺激(300 ng·毫升−1)。Transendothelial电阻(TER)监测时间。汇集数据额,实验用细胞预处理Br-cAMP和iloprost有限合伙人之前治疗:b)有限合伙人影响TER比较与nsRNA细胞转染或siRac1;c)的保护作用iloprost或Br-cAMP LPS-induced渗透率在内皮细胞治疗nsRNA观察5 h后为100%。iloprost Rac1击倒减毒保护作用(200 ng·毫升−1ng)和Br-cAMP(500毫升−1针对LPS-induced渗透率)。数据均值±sd三到五个独立的实验。*:与nsRNA相比p < 0.05。d)细胞治疗与车辆或Br-cAMP LPS刺激(300 ng·毫升紧随其后−1)5 h。细胞骨架改建计划评估与德州Red-phalloidin f -肌动蛋白的荧光染色法。Paracellular缺口的箭头。e)定量分析paracellular差距形成的控制和Rac-depleted HPAECs。数据意味着±sd三个独立的实验。#:与有限合伙人相比p < 0.05。
Rac1在内皮细胞barrier-protective iloprost-induced阵营海拔引发的效应细胞骨架改建计划的进一步评估分析控制和Rac1-depleted HPAECs pre-incubated iloprost或Br-cAMP与LPS刺激。类似于nontransfected内皮细胞(图2),预处理与iloprost或Br-cAMP减毒LPS-induced应力纤维单层的形成和破坏完整性与非特异性细胞转染核而Rac1击倒抑制这些保护作用(图5 d和e)。接下来,我们使用了药理抑制剂nsc - 23766作为替代方法来抑制Rac1函数。nsc - 23766抑制Br-cAMP或iloprost内皮细胞的保护作用研究进展(图6 a和b),应力纤维的形成和paracellular的差距LPS-challenged单层内皮细胞(图6 c g)。
药理效应Rac1抑制iloprost——(Ilo)和8-bromoadenosine-3′, 5′环一磷酸(Br-cAMP)全身的内皮细胞屏障保护。)人类肺动脉内皮细胞(HPAECs)治疗车或Rac1抑制剂nsc - 23766(100μM, 30分钟)其次是脂多糖(LPS) (300 ng·毫升−1ng)挑战有或没有Br-cAMP预处理(500毫升−1)。Transendothelial电阻(TER)监控。b)汇集TER实验显示的数据。Br-cAMP的保护作用LPS-induced渗透率在内皮细胞nsc - 23766治疗观察5 h后为100%。数据均值±sd三个独立的实验。*:p < 0.05。控制或nsc - 23766 preincubated HPAECs治疗c)汽车(阿明费),d)有限合伙人(300 ng·毫升−15 h), e) iloprost (200 ng·毫升−1,15分钟)和有限合伙人,f) Br-cAMP (500 ng·毫升−1,15分钟)和有限合伙人。的f -肌动蛋白细胞骨架改建计划被荧光染色法评估德州Red-phalloidin。g) paracellular差距形成的定量分析。数据表示为均值±sd三个独立的实验。#:与有限合伙人相比p < 0.05。
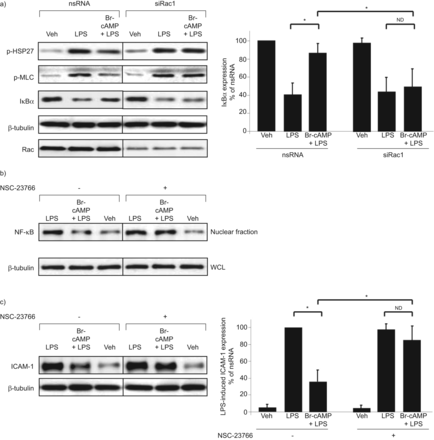
接下来,Rac1在集中营被评估的抗炎作用实验与分子或药物抑制Rac1。Rac1击倒的保护作用也废除了Br-cAMP p38 MAPK LPS-induced激活,ρ和NF-κB信号(图7)监测HSP27的磷酸化和多层陶瓷,分别和IκBα退化。亚细胞分离的抑制作用研究表明,Br-cAMP LPS-induced积累的NF-κB p65亚基核分数被废除的nsc - 23766 (图7 b)。此外,抑制Rac1活动nsc - 23766也减毒Br-cAMP的保护作用LPS-induced ICAM-1表达式,炎症激活内皮细胞的一个特点。(图7 c)。
Rac1抑制效果的抗炎作用8-bromoadenosine-3′, 5′环一磷酸(Br-cAMP)。)人类肺动脉内皮细胞(HPAECs)与非特异性(nsRNA)或转染Rac1-specific小干扰RNA (siRac1) 48 h与车辆(阿明费)或治疗Br-cAMP (500 ng·毫升−1)15分钟,其次是脂多糖(LPS)刺激(300 ng·毫升−1)1 h。磷酸化的热休克蛋白(HSP) 27和肌球蛋白轻链(多层陶瓷)是通过免疫印迹检测到相应phospho-specific抗体。退化的抑制剂的核因子(NF) -κB (IκB)α使用nonphosphorylated蛋白抗体检测。证实了平等蛋白质加载完整的细胞溶解产物β-tubulin含量测定(水控制法)。Rac1 Rac1抗体免疫印迹结果验证了损耗。b) HPAECs治疗如上所述,NF-κB易位核分数被西方墨点法监控。β-tubulin含量测定相应水控制法是用来确保平等的加载。与车辆或c) HPAECs pre-incubated Rac1抑制剂nsc - 23766(100μM) 30分钟服用Br-cAMP (500 ng·毫升−1)15分钟,其次是刺激与有限合伙人(300 ng·毫升−1)为4 h。细胞间粘附分子(ICAM) 1表达与ICAM-1抗体检测到免疫印迹。β-tubulin染色被用作控制正常化。ND:没有区别;*:p < 0.05。
Iloprost抑制LPS-induced肺屏障功能障碍和炎症在活的有机体内
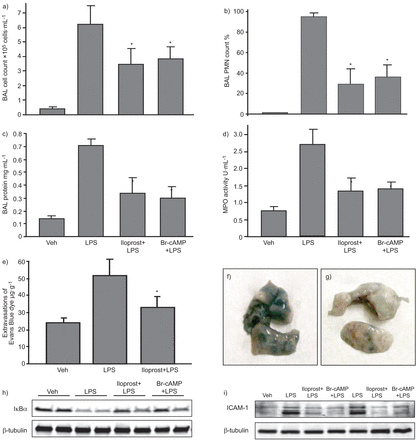
iloprost的保护作用是进一步测试了阿里的脓毒性模型引起的气管内的有限合伙人的滴注法。静脉注射iloprost或Br-cAMP落下帷幕总细胞计数和嗜中性粒细胞计数,显著降低和减少蛋白质含量在LPS-treated老鼠(图8模拟)。肺损伤和炎症的严重程度也监视测量肺组织髓过氧化酶(MPO)活动的样本。有限合伙人显著增加MPO活性以组织匀浆,虽然iloprost或Br-cAMP治疗减毒这种效应(图8模拟)。
全身的iloprost对脂多糖(LPS)肺部炎症,肺部炎症和屏障功能障碍的障碍。C57BL / 6 j小鼠与车辆的挑战(阿明费)或有限合伙人(0.63 mg·公斤−1气管内的)有或没有并发iloprost(20μg·公斤−1静脉注射,在0和90分钟后有限合伙人管理)或8-bromoadenosine-3′, 5′环一磷酸(Br-cAMP)治疗(μg·20公斤−1注射。有限合伙人管理后,在0和90分钟)。控制动物用无菌生理盐水治疗或iloprost孤单。细胞总数,b)多形核中性粒细胞(中性粒细胞)计数和c)蛋白质浓度测定在支气管肺泡灌洗(BAL)流体收集18 h后治疗。d)髓过氧化酶(MPO)活动以肺组织匀浆中描述的方法部分。数据均值±sdn = 6 - 10 /条件。伊文思蓝染料(30毫升·公斤−1注射。)注射2 h之前终止实验。肺血管通透性是由伊文思蓝评估肺组织中的积累。e)的定量分析埃文斯blue-labelled白蛋白外渗是由伊文思蓝的光度分析提取肺组织样本。数据均值±sd(n = 4 /条件。*:p < 0.05相比,有限合伙人的待遇。埃文斯blue-labelled从小鼠肺组织接受f)有限合伙人和有限合伙人和iloprost g)。核factor-κB h)抑制剂(IκB)α退化和我)后细胞间粘附分子(ICAM) 1表达有限合伙人挑战有或没有iloprost或Br-cAMP治疗测定肺组织匀浆免疫印迹分析与特定的抗体。平等的蛋白质加载证实了膜re-probingβ-tubulin抗体。
iloprost对肺血管的影响泄漏引起的有限合伙人被测量评估伊文思蓝外渗进肺部组织。Iloprost显著降低LPS-induced伊文思蓝积累在肺实质(图8 eg)。与细胞培养的研究一致,iloprost或Br-cAMP治疗抑制LPS-induced IκBα退化(图8 h)和ICAM-1表达式(图8我)在肺癌、肺组织匀浆免疫印迹分析探测到。这些结果进一步支持的抗炎和barrier-protective影响iloprost对感染性炎症和血管内皮屏障功能障碍LPS-induced肺损伤的细胞培养和动物模型。
讨论
临床研究主要集中在测试产生的内源性花生四烯酸代谢物考克斯在脓毒症患者,增加相关肺血液动力学和气体交换的变化(23- - - - - -26]。结果表明,在急性呼吸窘迫综合征(ARDS),但不是在脓毒症患者的肺器官衰竭,环前列腺素和血栓素平衡的变化2调制气体交换通过干扰缺氧性肺血管收缩(23]。试图环前列腺素和血栓素水平降低COX抑制剂布洛芬治疗导致减少发热、心动过速、耗氧量、乳酸酸中毒,但无论是预防休克或急性呼吸窘迫综合征的发展,也提高生存(27]。
其他研究用药物管理局环前列腺素类似物达到快速prostacyclin-induced改善肺血液动力学、血液气体参数和血管张力。使用这种方法的研究还表明,改善气体交换吸入性伊洛前列素由于减少肺分流的长期影响,建议iloprost在减少肺部水肿形成的潜在影响(28]。然而,特定内皮药理管理对炎症的影响参数在ALI / ARDS尚未系统地分析。我们研究解决这一重要点和研究内皮保护作用的内皮屏障监管炎症信号与阿里的先天免疫炎症反应有关。
先前的研究描述barrier-enhancing合成环前列腺素类似物的影响内皮细胞培养和保护作用在活的有机体内在无菌性肺损伤的模型,包括机械通气在高潮汐卷和thrombin-related激活肽(9,10,13,15]。这些影响与衰减RhoA-dependent机制的细胞骨架重塑和内皮细胞内营的研究由于海拔9,15]。然而,环前列腺素的影响在阿里和炎症的脓毒性模型尚不清楚。本研究的主要发现是iloprost的保护作用在阿里的LPS模型和肺血管内皮屏障功能障碍。这项研究的结果表明,iloprost治疗抑制,LPS-induced的细胞骨架内皮细胞屏障功能障碍的机制和LPS-induced炎性信号。
我们的结果也显示Rac1-dependent机制的关键作用的提高LPS-induced肺损伤和炎症信号的衰减和血管iloprost泄漏。然而,Rac激活报道LPS-stimulated巨噬细胞和中性粒细胞29日,30.]。在这些细胞中,Rac激活触发烟酰胺腺嘌呤二核苷酸磷酸氧化酶活动导致活性氧(ROS)生产和氧化应激,感染性肺损伤的主要病理机制之一。ROS增加生产也可能刺激NF-κB炎症和细胞因子的生产导致恶化的信号级联的组织炎症,血管泄漏和恶化的肺损伤(31日]。相比之下,激活Rac1信号在肺血管内皮barrier-protective受体激动剂会导致增强内皮细胞单层完整性和肺血管屏障保护起着至关重要的作用[16,32- - - - - -34]。这些报道效应之间的明显差异可以解释为Rac的多样性功能不同的细胞,和微分Rac1的角色Rac2亚型在病理条件。例如,抑制Rac2 Rac2 - / -中性粒细胞功能损害粘附、趋化性、吞噬作用和活性氧的生产(35,36),而淘汰赛的Rac1中性粒细胞对活性氧(没有影响37]。反过来,Rac1是一个关键的球员在保护血管内皮屏障ALI模型(15,16,38]。Rac1独立和Rac2功能也由不同的鸟嘌呤核苷酸交换因子(gef)。Rac1激活内皮细胞介导的gef T-lymphoma入侵,metastasis-inducing蛋白质(Tiam) 1, Vav2和β-PIX与内皮屏障增强有关9,39,40]。此外,Tiam1和Vav2是Rac1信号引起的阵营的主要催化剂高度(12,13]。反过来,在中性粒细胞Rac2优先激活磷脂酰肌醇3,4,5-trisphosphate-dependent Rac换热器(P-REX) 1和Vav1 [30.,41),和双基因敲除P-REX-1和Vav1中性粒细胞可以显著降低Rac活动和损害pathogen-induced活性氧的形成,附着力和趋化性41]。综上所述,这些数据说明在内皮细胞-和上下文相关机制的Rac功能和免疫细胞,并强调Rac角色发展的复杂性和肺损伤的衰减。
RhoA信号的作用在控制NF-κB活动仍然是一个有趣的问题。持续NF-κB激活细胞和组织中观察到的遗传模型,调节ρ活动(42]。研究表明,持续的激活Rho-NF-κB串级调节慢性皮肤炎症。其他研究也间接表明,激活ρ可能刺激NF-κB活动(43),虽然精确这样的激活机制还有待阐明。因此,先前的报道(42,43),这项研究的结果表明,长期ρLPS引起的激活可能是隐含的额外刺激NF-κB肺部发炎的信号模型。之前报道持续由有限合伙人(ρ激活44)也可能刺激p38 MAPK通路(45,46],RhoA效应蛋白激酶Nα(PKNα)最近提出的一种新型传感器的RhoA信号压力p38 MAPK级联(47]。产生激活p38 MAPK途径移植促炎症基因的表达,导致内皮细胞通透性增加通过p38-induced监管HSP27蛋白肌动蛋白的磷酸化。
我们的结果表明,在LPS-induced iloprost肺功能障碍的保护作用与Rac1-dependent有关保护肺内皮细胞屏障的完整性和衰减LPS-induced IκBα退化,NF-κB核本地化,p38 MAPK活性。这样的炎症信号衰减iloprost抑制LPS-induced ICAM-1表达在人类肺内皮细胞和培养LPS-challenged肺,和减少渗透激活中性粒细胞在肺,伴随着减少炎症和改善肺损伤参数在活的有机体内。除了对炎症信号的影响,iloprost减毒LPS-induced内皮细胞屏障破坏通过抑制LPS-induced多层陶瓷磷酸化,肌动蛋白细胞骨架改建和paracellular缺口的形成受控于RhoA内皮屏障破坏的途径。涉及的iloprost屏障保护和抗炎作用所需的阵营和高程Rac1活动,在实验与Rac1击倒在这项研究中执行。基于这项研究的结果和发布数据,我们推测iloprost-induced, cAMP-activated Rac1信号有助于在感染性肺保护条件通过拦截Rho-mediated肺动脉内皮细胞的屏障功能障碍,细胞骨架机制和抑制压力p38激酶和NF-κB-dependent炎性级联。
因此,这项研究的结果证明有利影响环前列腺素类似物的感染性肺损伤的模型并提出进一步的临床测试的重要性iloprost作为潜在的治疗肺部炎症和屏障功能障碍的治疗。
脚注
可以从本文的补充材料www.www.qdcxjkg.com
支持声明
这项研究受到了美国国家心脏,肺和血液研究所(NHLBI)拨款HL87823 HL076259和HL058064 kg。Birukov, NHLBI赠款HL089257 HL107920和美国中西部心脏协会下属A.A. Birukova补助金。
感兴趣的语句
没有宣布。
- 收到了2011年8月26日。
- 接受5月4日,2012年。
- ©2013人队