抽象的gydF4y2Ba
气道重塑,其特征在于气道平滑肌(ASM)质量,耻骨上纤维化,戈尔特细胞增生和粘液腺肥大,是慢性哮喘的特征。增加的氨基酶活性可能导致这些特征gydF4y2Ba通过gydF4y2Ba增加了多胺的形成gydF4y2BalgydF4y2Ba-脯氨酸精氨酸酶产物的下游gydF4y2BalgydF4y2Ba鸟氨酸,gydF4y2Ba通过gydF4y2Ba还原氧化氮合成。gydF4y2Ba
利用特异性精氨酸酶抑制剂2(S)-氨基-6-硼己酸(ABH),我们用慢性哮喘豚鼠模型研究了精氨酸酶在气道重塑中的作用。用ABH或PBS治疗卵清蛋白致敏的豚鼠gydF4y2Ba通过gydF4y2Ba在12周变应原或生理盐水刺激前进行吸入,并在最后刺激24小时后研究精氨酸酶活性、气道重塑、炎症和反应性指标。gydF4y2Ba
反复致敏豚鼠肺精氨酸酶活性升高。变应原刺激还会增加ASM的质量和脱落的气管环的最大收缩,而ABH可以阻止这些。此外,ABH还能减轻变应原诱导的肺羟脯氨酸(纤维化)和腐胺、黏液腺肥大、杯状细胞增生、气道嗜酸性粒细胞增多和白细胞介素-13gydF4y2BalgydF4y2Ba- orithine /gydF4y2BalgydF4y2Ba-瓜氨酸比值恢复正常。此外,ABH能完全消除致敏原诱导的气管灌注高反应性。gydF4y2Ba
这些发现表明精氨酸酶显著参与了变应原诱导的气道重塑、炎症和慢性哮喘的高反应性。gydF4y2Ba
过敏性哮喘是一种慢性气道炎症性疾病,其特征是过敏原诱导、免疫球蛋白(Ig) e介导的早期和晚期支气管阻塞性反应,在这些反应和炎症细胞(特别是嗜酸性粒细胞和t辅助细胞(Th) 2型淋巴细胞)进入气道后,急性和短暂的气道高反应性(AHR) [gydF4y2Ba1gydF4y2Ba,gydF4y2Ba2gydF4y2Ba].此外,还观察到气道壁的结构变化,包括基底膜增厚、气道平滑肌(ASM)肿块增加、上皮下纤维化、杯状细胞增生、粘膜下腺肥大和血管增生。这可能导致慢性哮喘患者肺功能的进行性下降和AHR的持久性[gydF4y2Ba2gydF4y2Ba,gydF4y2Ba3.gydF4y2Ba].gydF4y2Ba
最近,氨基酶,水解酶gydF4y2BalgydF4y2Ba精氨酸为gydF4y2BaL-gydF4y2Ba鸟氨酸和尿素,已被确定为急性过敏性哮喘病理生理学的关键角色[gydF4y2Ba4gydF4y2Ba].已鉴定出两种精氨酸酶亚型,胞质精氨酸酶I和线粒体精氨酸酶II [gydF4y2Ba5gydF4y2Ba],两者都在气道中表达,特别是在上皮细胞中,(Myo)成纤维细胞,内皮细胞和巨噬细胞[gydF4y2Ba6gydF4y2Ba- - - - - -gydF4y2Ba8gydF4y2Ba].从各种过敏性哮喘动物模型获得的气道和肺组织中观察到精氨酸酶的表达和/或活性增加[gydF4y2Ba9gydF4y2Ba]来自患者[gydF4y2Ba10gydF4y2Ba- - - - - -gydF4y2Ba12gydF4y2Ba].消费的增加gydF4y2BalgydF4y2Ba-精氨酸通过限制急性变应性哮喘的生物利用度,促进了变应性原诱导AHR的发展gydF4y2BalgydF4y2Ba-精氨酸到一氧化氮合酶(NOS)同工酶[gydF4y2Ba13gydF4y2Ba- - - - - -gydF4y2Ba15gydF4y2Ba],将氨基酸水解成一氧化氮和gydF4y2BalgydF4y2Ba瓜氨酸。这导致支气管扩张性一氧化氮缺乏,并增加高反应性促炎和促收缩性一氧化氮代谢产物过氧亚硝酸盐的形成,这两者都是过敏性哮喘动物模型AHR的基础[gydF4y2Ba13gydF4y2Ba- - - - - -gydF4y2Ba18gydF4y2Ba].在过敏性哮喘的豚鼠模型中,吸入特定的氨基酶抑制剂2(s) - 氨基-6-硼己酸(ABH)急性逆转过敏原诱导的AHRgydF4y2Ba在活的有机体内gydF4y2Ba无论是早期和晚期的哮喘反应后,治疗的程度与吸入相同gydF4y2BalgydF4y2Ba精氨酸(gydF4y2Ba19gydF4y2Ba].此外,在过敏原激发前30分钟和激发后8小时吸入ABH可防止早期和晚期梗阻性反应、反应后AHR和气道炎症的发生[gydF4y2Ba19gydF4y2Ba].gydF4y2Ba
由于醇酶活性增加,减少的一氧化氮合成也可能有助于慢性哮喘中的气道重塑,因为一氧化氮抑制ASM增殖[gydF4y2Ba20.gydF4y2Ba- - - - - -gydF4y2Ba23gydF4y2Ba]及纤维化[gydF4y2Ba24gydF4y2Ba].此外,精氨酸酶活性升高可诱导气道重塑gydF4y2Ba通过gydF4y2Ba增加多胺的合成(Putrescine,Feperminine和Femermine)和gydF4y2BalgydF4y2Ba脯氨酸的下游gydF4y2BalgydF4y2Ba- orithine [gydF4y2Ba5gydF4y2Ba,gydF4y2Ba9gydF4y2Ba,gydF4y2Ba25gydF4y2Ba].多胺参与细胞增殖和分化[gydF4y2Ba5gydF4y2Ba而多胺水平的增加已在过敏原刺激的小鼠中得到证实[gydF4y2Ba10gydF4y2Ba]及气喘病人[gydF4y2Ba26gydF4y2Ba].gydF4y2BalgydF4y2Ba-脯氨酸是胶原蛋白的前体[gydF4y2Ba5gydF4y2Ba因此,可以在过敏原诱导的纤维化中发挥作用。这是通过观察到抑制原子酶活性降低转化生长因子(TGF)-β-诱导的原发性小鼠肺成纤维细胞的胶原合成来支持这一点[gydF4y2Ba27gydF4y2Ba].因此,我们假设,除了急性哮喘,精氨酸酶活性的增加在慢性哮喘的病理生理学中也起着关键作用。在慢性变应性哮喘动物模型中观察到精氨酸酶表达和活性的增加[gydF4y2Ba11gydF4y2Ba,gydF4y2Ba28gydF4y2Ba].gydF4y2Ba
在本研究中,我们通过研究吸入ABH对反复变应原诱导的豚鼠气道重塑、炎症和AHR的影响,研究精氨酸酶在慢性哮喘中的作用。gydF4y2Ba
方法gydF4y2Ba
动物和致敏程序gydF4y2Ba
如前所述,体重200-250 g的非杂交、雄性、指定无病原体的Dunkin Hartley豚鼠对卵清蛋白(OVA)敏感[gydF4y2Ba29gydF4y2Ba].这些动物被一群一群地安置在单独的笼子里,笼子里有气候控制的动物区,并给予水和食物gydF4y2Ba自由gydF4y2Ba,虽然保持了12-H on / 12-H偏光循环。gydF4y2Ba
本研究中描述的所有方案均由格罗宁根大学动物实验委员会(格罗宁根,荷兰)批准。gydF4y2Ba
试验协议gydF4y2Ba
致敏4周后,动物每周接受一次生理盐水(对照组)或变应原(OVA)的刺激,持续12周。盐水和过敏原刺激是通过吸入雾化溶液,使用DeVilbiss星云器(646型;DeVilbiss Healthcare, Somerset, PA, USA),在一个特别设计的动物笼子里,豚鼠可以自由移动[gydF4y2Ba29gydF4y2Ba].通过吸入浓度不断增加的OVA于生理盐水中(0.05,0.1,0.3,0.5和0.7% w/v),每次3分钟,如前所述间隔7分钟[gydF4y2Ba29gydF4y2Ba- - - - - -gydF4y2Ba31gydF4y2Ba].当观察到呼吸窘迫的第一个迹象时,停止过敏原吸入。不需要抗组胺剂来防止过敏性休克的发展。对照组动物每周注射生理盐水3分钟。gydF4y2Ba
将这些动物在PBS中吸入的ABH(25mm雾化器浓度为15分钟)或PBS(15分钟)在每个过敏原或盐水攻击后8小时之前(15分钟)0.5小时。如前所述合成ABH [gydF4y2Ba32gydF4y2Ba].gydF4y2Ba
组织习得gydF4y2Ba
在最终挑战后24小时,通过实验脑震荡,豚鼠被急剧放血,然后快速放血。立即切除肺部并保存在冰上以进一步加工。将气管快速除去并转移到克雷布-Henseleit(KH)溶液(37°C; pH 7.4)中,预先加热5%COgydF4y2Ba2gydF4y2Ba/ 95%啊gydF4y2Ba2gydF4y2Ba.gydF4y2Ba
等长张力测量gydF4y2Ba
如前所述进行等距收缩实验[gydF4y2Ba30.gydF4y2Ba].简单地说,气管的制备使它没有浆液结缔组织。在含有KH溶液(37°C, pH 7.4)、5% CO气体的器官浴中,将剥去上皮的单环开环标本放置进行等距记录gydF4y2Ba2gydF4y2Ba/ 95%啊gydF4y2Ba2gydF4y2Ba.在平衡后,将静止张力调节至0.5g,然后使用20和40mm KCl进行预收缩。在洗涤出和30分钟的另一个平衡周期之后,使用甲素构建累积浓度响应曲线。gydF4y2Ba
气管灌注gydF4y2Ba
气管被准备成没有浆膜结缔组织,并被切成两半,每半约16毫米。将准备物附在灌注固定器上,并置于器官浴(37°)中,如前所述,其中含有20 mL气体化KH溶液(腔外腔室)[gydF4y2Ba17gydF4y2Ba].气管腔内以恒定流速从单独的20 ml浴液(腔内腔室)中灌注再循环KH溶液,并使用轴向中心侧孔导管在气管近端和远端测量静压。压差(ΔgydF4y2BaPgydF4y2Ba)记录;ΔgydF4y2BaPgydF4y2Ba反映气管段对灌注的阻力,该阻力是各压口之间气管平均直径的函数[gydF4y2Ba33gydF4y2Ba].gydF4y2Ba
在45分钟的平衡周期之后,用新鲜的KH洗涤三次(内部和喹内泻),将1μM异戊酮加入到外后腔室中以评估基调。在三次洗涤后(每次10分钟),将气管暴露于40mm KCl中的KH(喹啉)以获得受体无关的参考反应。用KH洗涤45分钟后,用腔内甲胆碱进行累积浓度响应曲线。气管管制剂与甲素的腔内应答被表达为通过喹啉酮施用40mM KCl诱导的反应的百分比,以校正基线δ的差异gydF4y2BaPgydF4y2Ba在δ中gydF4y2BaPgydF4y2Ba由于所用制剂的内部直径的变化,对收缩刺激的反应变化。gydF4y2Ba
氨基酶活性gydF4y2Ba
肺匀浆中精氨酸酶活性的测定是通过测量[gydF4y2Ba14gydF4y2BaC) -gydF4y2BalgydF4y2Ba精氨酸(gydF4y2Ba14gydF4y2BaC]-尿素,如前所述[gydF4y2Ba15gydF4y2Ba].精氨酸酶活性表达为每mg蛋白每分钟产生的pmol尿素。gydF4y2Ba
Interleukin-13测量gydF4y2Ba
采用抗豚鼠IL-13(库萨比奥,纽瓦克,DE,美国),根据制造商的方案,采用ELISA法测定肺匀浆中白细胞介素(IL)-13的水平。gydF4y2Ba
组织化学gydF4y2Ba
来自左右肺裂片两者的主要支气管的横向横截面(4μm)用于形态学分析。Sections染色为平滑肌特异性肌蛋白重链(NeoMarkers; Thermo Fisher,Fremont,Ca,USA)和粘蛋白5亚型A和C(MUC5AC; NeoMarkers)。使用辣根过氧化物酶连接的第二抗体和二氨基苯甲胺来视化初级抗体。此外,计算ASM束内的血清毒素染色的核。在血红素和嗜酸盐染色的肺切片中鉴定嗜酸性粒细胞,并使用过期酸 - 席夫(PAS)染色产生粘液细胞。部分内的气道被数字拍摄和将作为软骨或非甘油的分类。所有免疫组织化学测量都是使用量化软件(Imagej;国家健康机构,Bethesda,MD,MD,美国)。对于所有研究的参数,每只动物分析每种分类的三到六个气道。gydF4y2Ba
氨基酸分析氨基酸和腐凝液gydF4y2Ba
通过加入相同的冷乙腈沉淀肺匀浆(50μL)。离心后(5分钟为16,000×gydF4y2BaggydF4y2Ba),将30μl透明上清液与4μl氘代的内标溶液混合(10gydF4y2Ba−5gydF4y2Bam),并直接用于分析氨基酸gydF4y2BalgydF4y2Ba精氨酸,gydF4y2BalgydF4y2Ba鸟氨酸和gydF4y2BalgydF4y2Ba-瓜氨酸和腐胺。gydF4y2Ba
通过使用涡轮喷雾电喷雾电离界面(AB Sciex,Concord,ON)耦合到API-4000三弦孔质谱仪(AB Sciex,Concord,ON)的LC-4000 Triple-Quadruprole Mass光谱仪进行定量分析。加拿大)。在使用SIL-10自动进样器(Shimadzu)上的自动试剂添加之前,在分析之前,用40μLSymdaq试剂(Brainlink,Groningen,Netherlands)衍生样品,并在100×3-mm Synergi MAX-RP上解决(2.5-μm粒度)柱(现象,托兰,Ca,USA),水在水中的线性梯度,每种含有0.1%(v / v)甲酸。使用八点校准曲线(用于腐蚀的0.1-50μm,氨基酸为0.01-25μm)进行定量。肺部匀浆中氨基酸和腐凝物的浓度表示为每毫克蛋白质的微粒。gydF4y2Ba
羟脯氨酸测定gydF4y2Ba
确定肺组织的羟脯氨酸含量估计胶原含量,如先前的减数[gydF4y2Ba34gydF4y2Ba].将右下肺叶在液氮下粉碎,10 mL PBS超声。匀浆用1.25 mL 5%三氯乙酸在冰上孵育20分钟。样品离心,颗粒在10 mL 12 N盐酸中重悬,在110°C加热至烧焦和干燥。将干燥后的微球溶于2ml超纯水中,在室温下间歇涡旋培养72 h。每个样品取5 μL转移至96孔板,加入100 μL氯胺- t溶液(1.4%氯胺- t in 0.5 M乙酸钠/10%异丙醇)。30分钟后,100μL埃利希的解决方案(1.0米4-dimethylaminobenzaldehyde 70%异丙醇/ 30%高氯酸)添加和样本孵化为30分钟65°C。样品冷却到室温和量化了羟脯氨酸的含量比色测量(光密度在550海里;Biorad 680版读卡器,Biorad, Veenendaal,荷兰)。gydF4y2Ba
数据分析gydF4y2Ba
在等长收缩和灌注实验中,对methachine的最大收缩反应定义为最大效应(EgydF4y2Ba最大限度gydF4y2Ba).使用这个EgydF4y2Ba最大限度gydF4y2Ba,敏感性(有效浓度的负对数,导致50%的最大收缩反应(pECgydF4y2Ba50gydF4y2Ba))评估致甲胆碱。gydF4y2Ba
所有数据代表平均值±gydF4y2Ba扫描电镜gydF4y2Ba从n个单独的实验。使用单向ANOVA评估差异的统计显着性,然后是BonferonigydF4y2Ba事后gydF4y2Ba测试。P <0.05,差异被认为是统计学意义。gydF4y2Ba
结果gydF4y2Ba
重复变应原刺激豚鼠肺匀浆中的精氨酸酶活性是盐水刺激对照组的1.6倍(p<0.01;gydF4y2Ba无花果。1AgydF4y2Ba).gydF4y2Ba在活的有机体内gydF4y2Ba吸入ABH的处理完全阻止了多次攻击动物中的氨基酶活性(P <0.05),但在盐水攻击对照中没有影响氨基酶活性(gydF4y2Ba无花果。1AgydF4y2Ba).gydF4y2Ba
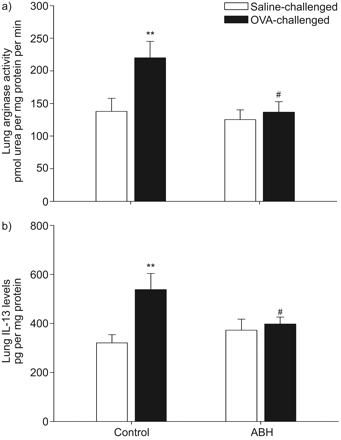
a)反复盐水和变应原(卵清蛋白(OVA))激发豚鼠肺匀浆中精氨酸酶活性和b)白介素(IL)-13水平,对照组为吸入PBS或2(S)-氨基-6-硼己酸(ABH)。数据显示为平均值±gydF4y2Ba扫描电镜gydF4y2Ba7 - 8的实验。gydF4y2Ba#gydF4y2Ba:与ova激活的对照组相比,p<0.05;**:与盐水对照组相比,p<0.01。gydF4y2Ba
为了深入了解这些原子化酶活性的可能机制,我们确定IL-13的肺水平,已知在肺中诱导氨基酶活性的TH2细胞因子[gydF4y2Ba35gydF4y2Ba].如图所示gydF4y2Ba图1 bgydF4y2Ba,肺中IL-13水平与精氨酸酶活性的变化相对应。因此,与盐水刺激对照组相比,慢性过敏原刺激导致IL-13增加了1.7倍(p<0.01;gydF4y2Ba无花果。1B.gydF4y2Ba).用ABH治疗归一化过敏原诱导的IL-13增加(P <0.05),留下基底IL-13水平不受影响(gydF4y2Ba无花果。1B.gydF4y2Ba).gydF4y2Ba
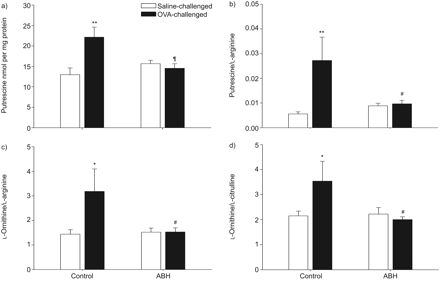
肺动脉gydF4y2BalgydF4y2Ba-Arginine和gydF4y2BalgydF4y2Ba在反复过敏原攻击后 - 碳水氨酸水平降低(P <0.01和P <0.05;gydF4y2Ba表1gydF4y2Ba),而gydF4y2BalgydF4y2Ba-鸟氨酸无显著变化,多胺腐胺升高(p<0.01;gydF4y2Ba表1gydF4y2Ba和gydF4y2Ba图2a).因此,Putrescine /gydF4y2BalgydF4y2Ba精氨酸,gydF4y2BalgydF4y2Ba- orithine /gydF4y2BalgydF4y2Ba-Arginine和gydF4y2BalgydF4y2Ba- orithine /gydF4y2BalgydF4y2Ba-瓜氨酸比值在过敏原刺激后显著增加(gydF4y2Ba图2b–d), 这gydF4y2BalgydF4y2Ba- orithine /gydF4y2BalgydF4y2Ba-瓜氨酸比表明肺中精氨酸酶活性的增加与NOS活性竞争,减少NO的产生。与此一致的是,所有过敏原引起的变化均被ABH (gydF4y2Ba图2gydF4y2Ba和gydF4y2Ba表1gydF4y2Ba).ABH对盐中毒动物体内的氨基酸和多胺水平没有影响(gydF4y2Ba图2gydF4y2Ba和gydF4y2Ba表1gydF4y2Ba).gydF4y2Ba
a)putrescine水平,b)putrescine /gydF4y2BalgydF4y2Ba精氨酸,c)gydF4y2BalgydF4y2Ba- orithine /gydF4y2BalgydF4y2Ba精氨酸和d)gydF4y2BalgydF4y2Ba- orithine /gydF4y2BalgydF4y2Ba用吸入PBS(对照)或2(S)-氨基-6-硼己酸(ABH)处理的反复生理盐水和变应原(卵清蛋白(OVA))刺激豚鼠的肺匀浆中-瓜氨酸的比值。数据显示为平均值±gydF4y2Ba扫描电镜gydF4y2Ba7 - 8的实验。*:与盐水对照组相比,p<0.05;**:与盐水对照组相比,p<0.01;gydF4y2Ba#gydF4y2Ba:与ova激活的对照组相比,p<0.05;gydF4y2Ba¶gydF4y2Ba:P <0.01与OVA攻击对照相比。gydF4y2Ba
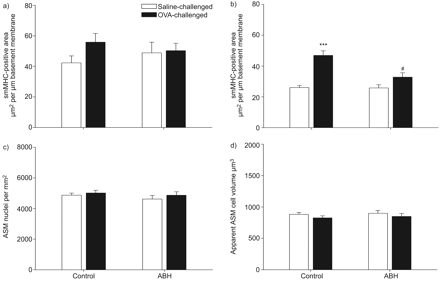
与盐水刺激对照组相比,反复过敏原刺激导致软骨气道中ASM肿块增加(p = 0.08;gydF4y2Ba无花果。3AgydF4y2Ba),而在非软骨性气道中观察到ASM肿块显著增加(p<0.001;gydF4y2Ba无花果。3B.gydF4y2Ba).吸入ABH治疗在很大程度上阻止了这种增加(p<0.001;gydF4y2Ba无花果。3B.gydF4y2Ba).相比之下,用ABH的治疗不影响盐水攻击动物中的ASM肿块。为了确定ASM含量的过敏原诱导的变化是否与细胞数和/或细胞尺寸变化的变化相关,相对于总ASM区域计数并表达ASM层内的核数。从这些数据和所有部分的厚度,还计算了ASM细胞的表观细胞体积。OVA挑战没有改变每平方毫米平滑肌区域的核数量(gydF4y2Ba无花果。3CgydF4y2Ba)或ASM细胞体积(gydF4y2Ba无花果。3dgydF4y2Ba),提示细胞大小没有变化,变应原引起的ASM质量增加是细胞数量增加所致。ABH处理对ASM细胞大小也没有影响(gydF4y2Ba无花果。3CgydF4y2Ba和gydF4y2Ba3dgydF4y2Ba).gydF4y2Ba
气道平滑肌(ASM)质量在a)软骨和b)来自反复盐水和过敏原(卵磷酸铵(ova)) - 攻击的豚鼠,用吸入的pbs(对照)或2(s)-amino-6处理硼己酸(ABH)。c)来自上述动物的非胆管气道中的表观ASM细胞的核数和D)。数据显示为平均值±gydF4y2Ba扫描电镜gydF4y2Ba7 - 8的实验。smMHC:平滑肌肌球蛋白重链。***:与盐水刺激对照组相比,p<0.001;gydF4y2Ba#gydF4y2Ba:P <0.001与OVA攻击对照相比。gydF4y2Ba
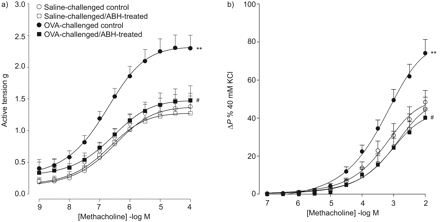
与先前的研究一致[gydF4y2Ba30.gydF4y2Ba,gydF4y2Ba31gydF4y2Ba],重复过敏原刺激可使切除上皮的气管开环制剂对乙酰胆碱的最大收缩增加1.7倍(p<0.01;gydF4y2Ba无花果。4AgydF4y2Ba和在线补充材料中的表S1),没有对敏感度的影响(PECgydF4y2Ba50gydF4y2Ba)朝向激动剂。如前所述,这表明由于受体远端发生变化,出现了过度收缩ASM表型[gydF4y2Ba30.gydF4y2Ba,gydF4y2Ba31gydF4y2Ba].ABH治疗完全防止了过敏原引起的高收缩性(p<0.01),而盐激动物的ASM收缩性没有受到影响(gydF4y2Ba无花果。4AgydF4y2Ba以及在线补充材料中的表S1)。gydF4y2Ba
a)上皮剥伤的气管开环制剂的甲胆碱诱导的等距收缩和b)完整灌注的豚鼠血管硬化反复盐水和过敏原(卵磷酸铵(OVA)) - 攻击的豚鼠,用吸入的PBS(对照)进行攻击的豚鼠(对照)或2(s)-氨基-6-硼己酸(ABH)。数据显示为平均值±gydF4y2Ba扫描电镜gydF4y2Baa) 6-8个或b) 6-10个实验。ΔgydF4y2BaPgydF4y2Ba:压差。**:与盐水对照组相比,p<0.01;gydF4y2Ba#gydF4y2Ba:P <0.01与OVA攻击对照相比。gydF4y2Ba
除了ASM的内在变化外,过敏原挑战还可能影响测量ASM音调的气道壁中的调节过程,包括(上皮)一氧化氮稳态[gydF4y2Ba16gydF4y2Ba,gydF4y2Ba17gydF4y2Ba,gydF4y2Ba28gydF4y2Ba].因此,我们也测定了完整的气管灌注制剂对乙酰胆碱的反应性。这些制剂的反应性与kcl诱导的气道收缩成正比,因此,在脱落的环中,由于受体后变化而诱导的过度收缩ASM表型并不影响这种气道反应性。有趣的是,EgydF4y2Ba最大限度gydF4y2Ba在与来自盐水攻击对照的那些(P <0.01)的那些相比,在从过敏原挑战的豚鼠获得的灌注气管段中观察到(P <0.01),而不会对收缩激动剂的敏感性(gydF4y2Ba无花果。4B.gydF4y2Ba以及在线补充材料中的表S2)。用ABH处理过敏原激发的动物可以防止AHR的发展(p<0.01),而ABH对盐激发的动物的气道反应性没有影响(gydF4y2Ba无花果。4B.gydF4y2Ba以及在线补充材料中的表S2)。gydF4y2Ba
在气道壁中增加了细胞外基质蛋白,包括胶原蛋白,包括胶原蛋白的沉积是慢性哮喘中气道重塑的特征[gydF4y2Ba36gydF4y2Ba,gydF4y2Ba37gydF4y2Ba].由于抗体可用,免疫组化检测豚鼠气道中的胶原蛋白是不可行的,因此对肺中的羟脯氨酸含量进行分析,作为对总胶原蛋白的估计。重复过敏原激发可使羟脯氨酸含量增加1.5倍(p<0.01), ABH处理的动物可完全防止羟脯氨酸的增加(p<0.05),而ABH对盐激发的动物羟脯氨酸含量没有影响(gydF4y2Ba图5gydF4y2Ba).gydF4y2Ba
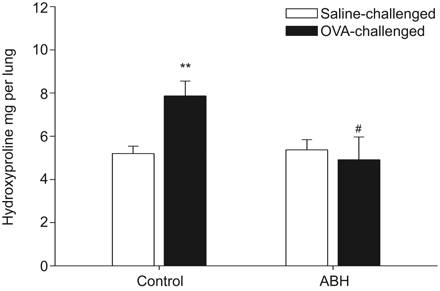
PBS(对照)或2(S)-氨基-6-硼己酸(ABH)处理的效果gydF4y2Ba在活的有机体内gydF4y2Ba对多种生理盐水或变应原(卵清蛋白(OVA))激发豚鼠肺羟脯氨酸含量的影响数据显示为平均值±gydF4y2Ba扫描电镜gydF4y2Ba4 - 6的实验。gydF4y2Ba#gydF4y2Ba:与ova激活的对照组相比,p<0.05;**:与盐水对照组相比,p<0.01。gydF4y2Ba
在盐水处理的动物中,与盐水攻击对照(所有P <0.001)相比,重复过敏原挑战诱导粘膜下粘膜下,ASM和非胆管呼吸道的菌落和非胆管的过滤器中含量gydF4y2Ba表2gydF4y2Ba).ABH治疗不影响盐水攻击动物中的气道嗜酸性粒细胞数,但在软硬片和非硅基呼吸道的所有隔室中,大量防止过敏原诱导的嗜酸性粒细胞(所有P <0.001;gydF4y2Ba表2gydF4y2Ba).gydF4y2Ba
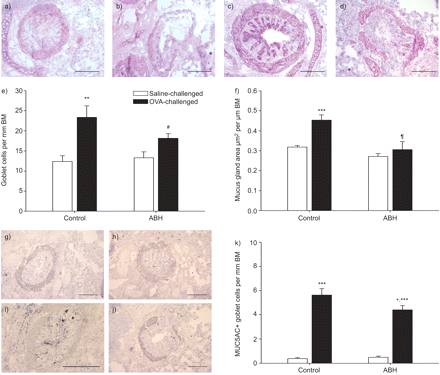
与之前使用同一慢性哮喘豚鼠模型的研究一致[gydF4y2Ba31gydF4y2Ba],反复刺激过敏原导致软骨性气道杯状细胞增生(p<0.01;gydF4y2Ba图6gydF4y2Bab),经精氨酸酶抑制剂抑制后降低(p<0.05)。此外,重复的过敏原刺激导致同一气道粘液腺面积增加(p<0.01;gydF4y2Ba图6 cgydF4y2Ba).通过ABH处理大大防止这种粘液腺体肥大(P <0.01;gydF4y2Ba图6 cgydF4y2Ba).同样,ABH可减弱muc5ac阳性杯状细胞中过敏原诱导的增加(p<0.05;gydF4y2Ba图6 dgydF4y2Ba).在盐中毒动物中,ABH治疗并不影响产生粘液细胞的数量(gydF4y2Ba图6gydF4y2Ba).gydF4y2Ba
对a)盐水激发,pbs处理,b)盐水激发,2(S)-氨基-6-硼己酸(ABH)处理,c)卵清蛋白(OVA)激发,pbs处理,d) OVA激发,ABH处理的豚鼠的肺内软骨气道切片进行周期性酸-希夫(PAS)染色。的影响gydF4y2Ba在活的有机体内gydF4y2Ba用PBS(对照)或ABH处理e)roblet细胞数和f)粘液腺面积。粘蛋白5亚型A和C(MUC5Ac)染色肺炎心碎气道部分G)盐水攻击,PBS处理,H)盐攻击,ABH处理,I)OVA攻击,PBS处理和J)OVA-挑战,ABH治疗的豚鼠。K)来自盐水或OVA挑战的豚鼠的颅骨或OVA挑战性豚鼠的颅内气道中的MUC5Ac阳性脚耳细胞数。PAS和MUC5AC染色的代表性实例分别以面板A-D)和G-J)示出。秤杆=100μm。数据显示为平均值±gydF4y2Ba扫描电镜gydF4y2Ba7 - 8的实验。BM:基底膜。gydF4y2Ba+gydF4y2Ba:与ova激活的对照组相比,p<0.05;**:与盐水对照组相比,p<0.01;***:与盐水刺激对照组相比,p<0.001;gydF4y2Ba#gydF4y2Ba:P <0.01与OVA攻击控制相比;gydF4y2Ba¶gydF4y2Ba:P <0.001与OVA攻击对照相比。gydF4y2Ba
讨论gydF4y2Ba
通过明确定义的豚鼠慢性变应性哮喘模型,我们证明了精氨酸酶活性的增加有助于过敏原诱导的气道重塑、炎症和AHR。因此,吸入精氨酸酶抑制剂ABH对过敏原诱导的ASM增生和过度收缩、粘液腺肥大、杯状细胞增生和纤维化有相当大的保护作用。此外,gydF4y2Ba离体gydF4y2Ba在ABH处理的动物中,反复过敏原攻击诱导的AHR致甲胆碱和呼吸道嗜酸性粒细胞凋亡也大大降低。gydF4y2Ba
在我们的豚鼠模型中,重复过敏原挑战导致肺中的氨基酶活性增加1.6倍,这与最近在慢性哮喘的小鼠模型中的最近发现一致[gydF4y2Ba11gydF4y2Ba].值得注意的是,gydF4y2Ba在活的有机体内gydF4y2Ba用ABH治疗完全防止了过敏原引起的精氨酸酶活性的增加。精氨酸酶活性的变化主要通过酶的变化来反映gydF4y2BalgydF4y2Ba- orithine /gydF4y2BalgydF4y2Ba-Arginine和Putrescine /gydF4y2BalgydF4y2Ba-精氨酸含量。由于ABH处理不影响盐碱刺激动物精氨酸酶的活性,其作用不能归因于肺中残留的ABH,提示精氨酸酶抑制可防止过敏原刺激后酶的诱导。精氨酸酶的表达受到Th2细胞因子的强烈诱导,包括IL-13 [gydF4y2Ba35gydF4y2Ba];ABH显着减弱了我们模型中的过敏原诱导的IL-13升高,表明ABH的增加的酶活性和ABH的抑制作用可能导致IL-13的变化。这与最近在急性哮喘的小鼠模型中发现的一致性,显示鼻内施用氨基酶抑制剂ngydF4y2BaωgydF4y2Ba-羟基去精氨酸(nor-NOHA)可防止室内尘螨诱导的肺部Th2细胞因子表达和精氨酸酶活性升高[gydF4y2Ba38gydF4y2Ba].我们很容易推测,以前观察到的吸入ABH的抗过敏作用[gydF4y2Ba19gydF4y2Ba]下潜Th2细胞因子释放和随后的氨基酶诱导。gydF4y2Ba
ASM增重是哮喘气道重塑的一个特征性特征,可能是ASM细胞增生和肥大共同导致的[gydF4y2Ba39gydF4y2Ba].与先前的研究一致[gydF4y2Ba30.gydF4y2Ba,gydF4y2Ba31gydF4y2Ba[反复过敏原攻击诱导我们的模型中的ASM质量增加,特别是在非硅基气道中,其特征在于ASM细胞增生。用ABH治疗抑制过敏原诱导的ASM细胞增生。这可能涉及恢复过敏原诱导的一氧化氮缺乏,因为一氧化氮抑制促介质诱导的培养人的增殖[gydF4y2Ba20.gydF4y2Ba- - - - - -gydF4y2Ba22gydF4y2Ba]和豚鼠[gydF4y2Ba23gydF4y2BaASM细胞。因此,我们证明了gydF4y2BalgydF4y2Ba- orithine /gydF4y2BalgydF4y2Ba-瓜氨酸比值在重复过敏原刺激后显著增加,并通过ABH治疗恢复正常。精氨酸酶抑制抑制ASM增生的第二个机制是gydF4y2Ba通过gydF4y2Ba抑制gydF4y2BalgydF4y2Ba鸟氨酸生产。gydF4y2BalgydF4y2Ba- orithine是多胺(Putrescine,Fepermidine和Femermine)的前体,其参与细胞增殖[gydF4y2Ba5gydF4y2Ba,gydF4y2Ba9gydF4y2Ba,gydF4y2Ba25gydF4y2Ba,gydF4y2Ba40gydF4y2Ba].为了支持这一观点,arginase I转染增加了血管平滑肌细胞的多胺水平和细胞增殖[gydF4y2Ba41gydF4y2Ba].精氨酸酶和鸟氨酸脱羧酶(ODC)都能转化gydF4y2BalgydF4y2Ba- 在腐凝茎中,在气道上皮细胞中表达[gydF4y2Ba42gydF4y2Ba[已经描述了导致多胺水平增加的生长因子诱导酶的诱导[gydF4y2Ba4gydF4y2Ba].此外,过敏原刺激小鼠肺部多胺水平升高[gydF4y2Ba10gydF4y2Ba]及哮喘病人的血清[gydF4y2Ba26gydF4y2Ba].我们现在表明,过敏原诱导的氨基酶活性的增加导致多胺普雷氏菌素的产量增加,这完全被ABH完全废除。除了增加的形成gydF4y2BalgydF4y2Ba- 作为一氧化氮抑制ODC,一氧化氮缺乏氧化氮的缺乏也可能有助于增加的过敏原攻击后的多胺水平增加gydF4y2Ba通过gydF4y2BaS-nitrosylation [gydF4y2Ba43gydF4y2Ba].gydF4y2Ba
重复的过敏原刺激也增加了气管单环制剂对乙酰胆碱的最大收缩。先前使用同一动物模型的实验表明,ASM的过度收缩是由于收缩蛋白表达增加[gydF4y2Ba31gydF4y2Ba].有趣的是,我们的研究结果表明,增加的氨基酶活性有助于诱导超助诊ASM表型。这可能是由于在多种过敏原挑战后的过氧尼酸盐增加而导致的gydF4y2Ba28gydF4y2Ba],因为这种氮种增加了人胎儿肺成纤维细胞中收缩蛋白的表达[gydF4y2Ba44gydF4y2Ba].需要注意的是,除了过度收缩的ASM表型外,包括一氧化氮在内的过敏原诱导的ASM音调刺激变化可能导致慢性哮喘中AHR的诱导[gydF4y2Ba28gydF4y2Ba].因此,之前使用同一豚鼠模型的实验表明,重复的过敏原激发可诱导的一氧化氮合酶(NOS)解偶联导致过氧亚硝酸盐合成增加,从而导致灌注气管段对methacholine的高反应性gydF4y2BalgydF4y2Ba-ARGINASE的杀菌消耗[gydF4y2Ba28gydF4y2Ba].目前的发现表明gydF4y2Ba在活的有机体内gydF4y2Ba用ABH治疗反复被过敏原激发的豚鼠可以防止iNOS的解偶联,以及随后的过氧亚硝酸盐的形成和AHR。gydF4y2Ba
慢性哮喘的气道纤维化也可能由较高的氨基酶活性引起,gydF4y2Ba通过gydF4y2Ba增加生产gydF4y2BalgydF4y2Ba脯氨酸的下游gydF4y2BalgydF4y2Ba鸟氨酸。支持这一观点的是,促纤维化因子TGF-β已被证明在小鼠肺和成纤维细胞中诱导精氨酸酶活性[gydF4y2Ba45gydF4y2Ba].此外,氨基酯I和II的表达增加与胶原蛋白诱导的小鼠肺纤维化的胶原I和羟脯氨酸表达的表达密切相关[gydF4y2Ba27gydF4y2Ba,gydF4y2Ba46gydF4y2Ba].通过吸入ABH,我们现在证明精氨酸酶活性的增加也有助于过敏原诱导的纤维化。同样,ABH的抗纤维化作用可能是由于抑制精氨酸酶诱导的一氧化氮缺乏,而一氧化氮具有抗纤维化作用[gydF4y2Ba24gydF4y2Ba].因此,过敏原诱导的胶原沉积显示来自InOS的肺部gydF4y2Ba-/-gydF4y2Ba小鼠和用NOS抑制剂长期治疗的小鼠gydF4y2BalgydF4y2Ba- ngydF4y2BaGgydF4y2Ba-硝基精氨酸甲酯[gydF4y2Ba47gydF4y2Ba,gydF4y2Ba48gydF4y2Ba].gydF4y2Ba
慢性变应性哮喘的另一个特征是气道炎症,推测在气道重塑中起着重要作用[gydF4y2Ba2gydF4y2Ba].我们目前的研究表明,精氨酸酶活性的增加可能参与了这一过程,因为ABH治疗显著减少了反复过敏原刺激后嗜酸性粒细胞在气道壁不同区域的浸润。ABH的抗炎作用与之前在豚鼠急性哮喘模型中的观察结果一致[gydF4y2Ba19gydF4y2Ba,这可以解释为一氧化氮的产生增加和促炎过氧亚硝酸盐的形成减少。因此,在过表达内皮NOS的小鼠中,过敏原诱导的炎症反应减弱[gydF4y2Ba49gydF4y2Ba, iNOS升高gydF4y2Ba-/-gydF4y2Ba老鼠(gydF4y2Ba50gydF4y2Ba与野生型小鼠相比。与我们的观察一致,arginase inhibitor nor-NOHA治疗减少了变应原刺激小鼠支气管肺泡灌洗(BAL)中的炎症细胞数量[gydF4y2Ba38gydF4y2Ba,gydF4y2Ba50gydF4y2Ba].但是,氨基酶抑制剂S-(2-硼乙基) -gydF4y2BalgydF4y2Ba-半胱氨酸不影响BAL中的炎症细胞数量或细胞因子水平,甚至进一步增强了另一种急性过敏性哮喘小鼠模型的细支气管周围和血管周围炎症[gydF4y2Ba51gydF4y2Ba].值得注意的是,来自骨髓源性细胞的精氨酸酶I似乎不是过敏原诱导的炎症细胞聚集到肺部所必需的[gydF4y2Ba52gydF4y2Ba,提示精氨酸酶在结构细胞,特别是气道上皮细胞中的作用。gydF4y2Ba
粘液分泌增多可能是粘液腺肥大和杯状细胞增生的结果,是慢性哮喘气道阻塞的另一特征[gydF4y2Ba53gydF4y2Ba].我们证明,增加的氨基酶活性也调节粘液细胞和MUC5Ac表达中反复过敏原挑战的豚鼠的变化。增加的氨基酶活性可能有助于这些特征gydF4y2Ba通过gydF4y2Ba多胺形成增多,可诱导细胞增殖和分化[gydF4y2Ba5gydF4y2Ba].有趣的是,gydF4y2BalgydF4y2Ba-Arguginine治疗患者增强过敏原诱导的老虎叶增生[gydF4y2Ba54gydF4y2Ba,这可以用增加来解释gydF4y2BalgydF4y2Ba鸟氨酸合成的gydF4y2BalgydF4y2Ba精氨酸,精氨酸酶。ABH的抗炎和抗过敏作用[gydF4y2Ba19gydF4y2Ba]还可以影响粘液过度,因为许多炎症细胞因子和介质,包括IL-13,涉及气道中的粘液分泌,戈尔特细胞增生和粘膜表达[gydF4y2Ba53gydF4y2Ba].此外,一氧化氮的合成已被证明可以减少粘液的过度分泌[gydF4y2Ba55gydF4y2Ba],而过氧基酯强烈诱导muc5ac表达[gydF4y2Ba56gydF4y2Ba].gydF4y2Ba
总之,我们的研究结果表明,精氨酸酶活性的增加在变应原诱导的气道重塑、炎症和慢性哮喘AHR中具有关键作用。吸入ABH治疗有效地抑制了这些特征,表明精氨酸酶抑制剂在治疗该病方面有治疗潜力。gydF4y2Ba
脚注gydF4y2Ba
本文提供了补充材料gydF4y2Bawww.www.qdcxjkg.comgydF4y2Ba
支持声明gydF4y2Ba
这项研究得到了默克-夏普公司和荷兰Oss的Dohme公司的资助gydF4y2Ba
感兴趣的语句gydF4y2Ba
J. Zaagsma和H. Meurs的兴趣陈述,并为研究本身就可以找到gydF4y2Bawww.www.qdcxjkg.com/site/misc/statements.xhtml.gydF4y2Ba
- 收到了gydF4y2Ba2010年3月14日。gydF4y2Ba
- 接受gydF4y2Ba2011年1月12日。gydF4y2Ba
- ©ers 2011.gydF4y2Ba
参考文献gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba