文摘
胆碱能拮抗剂已经使用自1900年代初以来作为支气管扩张剂慢性阻塞性肺疾病(COPD)。本研究调查是否口服毒蕈碱的M3-selective抗胆碱能代理(OrM3)将提供一种改进的治疗优势而在COPD患者的吸入抗胆碱能代理。
六周,多中心、随机、安慰剂active-controlled,与这些相应平行的组织研究了56个网站在美国。总共412名男性和女性患者(年龄在35 - 86岁),临床病史符合COPD是随机获得OrM3 0.5, 2、3或4毫克每日口服一次,四次被吸入溴化ipratropium 36μg每日或安慰剂。
OrM3表现出明显的剂量改善连环一秒钟用力呼气量和剂量相关的改善趋势patient-reported症状与安慰剂比较。然而,在剂量提供功效小于ipratropium,剂量相关的发病率,机理副作用为ipratropium OrM3超过这些观察到的。
在慢性阻塞性肺疾病患者,口服M3-selective代理没有提供对吸入ipratropium治疗的优势。这些结果不支持假设的高选择性毒蕈碱的M3受体在气道神经M2受体将代表一个更有效的治疗比目前吸入抗胆碱能类阻塞性气道疾病。
慢性阻塞性肺疾病(COPD)的第四大原因是长期在美国的发病率和死亡率1。一项调查估计,2000年被诊断出的慢性阻塞性肺病影响∼1000万人在美国,和2400万名成年人气流限制的证据2。全球慢性阻塞性肺病的发病率正在上升,世界卫生组织预计这种疾病将第五最普遍的疾病和第三个2020年死亡的最常见的原因3。
吸烟慢性阻塞性肺病的发展中扮演着重要角色在大多数病人。戒烟干预是唯一经过验证修改的自然病程慢性阻塞性肺病4。尽管积极的戒烟计划,改善了患者的药物治疗和咨询坚持禁欲吸烟5,许多人要么是不能或不愿意戒烟,和许多人做最终退出复发。
当前的药理治疗慢性阻塞性肺病不降低肺功能下降的速率,但可以改善病人的健康状况4,6。支气管扩张剂,包括短期和长效β-adrenergic受体激动剂和毒蕈碱的胆碱能拮抗剂(抗胆碱能类),是治疗的中流砥柱。对于后者,三个毒蕈碱的胆碱能受体(M1, M2和M3)在人类的航空公司有相关的生理作用。M3亚型表达在气管平滑肌和唾液腺和调解支气管收缩通过副交感神经信号转导7,8。相比之下,prejunctional M2受体表达在神经支配心脏和肺和副交感神经信号的函数作为负反馈监管机构;抑制这些受体可能会增加心跳过速的风险和支气管收缩9。
抗胆碱能药物,如溴化ipratropium(定喘乐®;勃林格殷格翰集团、州、美国CT)和溴化tiotropium (Spiriva®;勃林格殷格翰集团/辉瑞,纽约,纽约,美国),由吸入路线,已经证明了有效性在慢性阻塞性肺病支气管扩张剂10,11。代理都是功能选择性毒蕈碱的M1、M3受体亚型和电离迅速从M2受体11。有人提出M3-selective拮抗剂的使用可以减少副作用的发生率,从而允许更高的风险,增加了疗效,改善治疗。但是,没有大型研究迄今为止测试这个假说。
几个4-acetamidopiperidine衍生品研究开发一种新型支气管扩张剂与高水平的选择性M3受体,从而减少副作用9。这样的一个代理,口服M3 (OrM3),表现出高度的选择性(120倍)M3受体(K我在M2受体(= 4.2海里)K我= 490海里)9。提出,这种化合物也会选择性的M3受体的航空公司。与现有吸入抗胆碱能支气管扩张剂,OrM3被制定为口服片剂,可能更方便配方,尤其是不兼容使用气溶胶疗法的病人和那些有困难。给口头,药代动力学数据表明OrM3有很长的半衰期(t1/2= 14到20 h),这可能会允许一个每日一次给药方案。
当前研究的目的是确定是否口服M3-selective抗胆碱能代理将提供一种改进的治疗在目前吸入抗胆碱能类保证金。目前的作者,因此,相比的安全性和有效性与吸入口腔OrM3 ipratropium溴在慢性阻塞性肺病患者。
材料和方法
病人的选择
男性和女性患者年龄≥35岁和≥1年历史的症状与慢性阻塞性肺病和吸烟史≥10 pack-yrs原本健康的人都有资格参加。最低等级的资格,2(表明气短的时候匆匆略山)上的潜油电泵医学研究理事会呼吸困难量表是必需的12。
患者被排除在参与如果他们有哮喘或青光眼,总外周血嗜酸性粒细胞计数或> 440·μL > 6%1,平均需要< 1泡芙·天1β-agonist,白天室内空气氧饱和度小于90%或使用除了夜间使用所必需的氧气疗法(最大2 L·分钟1),或者前列腺病态症状。而扣缴β-agonist至少6小时,病人被要求证明一秒用力呼气量(FEV1)≥0.70 L和≤65%的预测13和一个FEV1/用力肺活量(FVC)≤70%的比例至少两次每个预研访问和安慰剂试车期间。患者还需要证明反应抗胆碱能药物至少一次在预研和安慰剂试车时间就是明证FEV的增加1≥10%的45 - 60分钟后吸入溴化ipratropium(36μg)。
病人被允许采取伴随慢性阻塞性肺病治疗,包括吸入短效β-agonist在“根据需要”的基础上;吸入或口服糖皮质激素(吸入倍氯米松≤2000天μg·1,吸入fluticasone≤1000天μg·1、口服强的松≤10 mg·1或等效)稳定剂量开始≥4周之前预先研究访问;每天两次,口服短效茶碱(配方),在一个稳定的剂量,开始≥5天前预先研究访问。
研究设计
这是一个随机、多中心、双盲、与这些相应平行的组织,dose-ranging研究56门诊中心在美国。书面知情同意,各自的机构审查委员会批准了为每个患者或在预先研究访问。最初,412例患者进入研究,开始2周,单盲、安慰剂试车期(阶段1)。
完成后,单盲安慰剂试车期间,患者进入第二阶段,被分配给一个六双盲治疗使用电脑随机分配计划:OrM3 4.0 (n = 67), 3.0 (n = 69), 2.0 (n = 73),或0.5毫克(n = 72)每天一次在早晨;溴化ipratropium 36μg每天四次(标准吸入剂量;n = 63);或安慰剂(n = 68;图1⇓)。
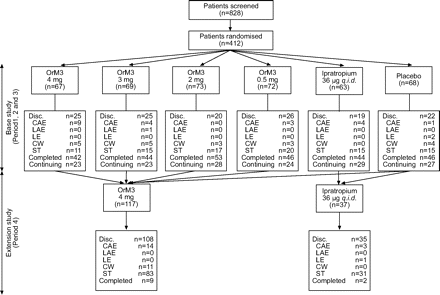
研究设计评价口服,M3-selective胆碱能受体拮抗剂(OrM3)在慢性阻塞性肺疾病患者。阀瓣。:discontinues; CAE: clinical adverse experience; LAE: laboratory adverse experience; LE: lack of efficacy; CW: consent withdrawn; ST: site terminated.
期2之后2周,双盲,安慰剂对照,治疗/冲刷时期(阶段3),在此期间的四个OrM3武器和ipratropium臂2:1的比例根据原来的分配计划。三分之一的每个手臂放在安慰剂时期3期间,三分之二继续第二阶段的治疗。这三个时期被认为是基础研究。完成时间3,所有剩余的患者提供知情同意进入期4,一个16周的双盲、安全扩展研究。
患者没有意识到这项研究包括不同时期和没有被告知当他们进入治疗期。精确匹配的安慰剂为口服和吸入抗胆碱能药物在double-dummy赞助商和分布式制造的时尚。此外,所有患者提供一个调查员沙丁胺醇吸入器的使用在一个“根据需要”的基础上。
患者将回到诊所每2周期间的研究评估肺功能和不良的经验。
肺功能测试
肺功能测试是使用标准执行肺活量计(清教徒贝内特PB100 / PB110;美国堪萨斯城,Nellcor KS)据美国胸科学会的标准13。肺活量的演习进行了一式三份,FEV最大的结果1和FVC被记录了下来。预测患者正常的值基于年龄、身高和性别13。确保标准化条件对所有肺功能测试天,患者需要保留茶碱和短效抗组胺药≥24 h和β-agonist和口头/吸入糖皮质激素≥6 h每个访问之前。
串行肺量测定法测量在诊所进行计量和1,2,4,6和10 h后给药2周后开始第二阶段的积极治疗。病人花了他们的第二个研究剂量吸入器10 h后post-dose测量,紧随其后的是第三个晚上剂量;没有额外的研究药物(平板电脑或吸入器)是在之前完成24小时连续呼吸量测定法。如果β-agonist救援需要串行肺活量的测量期间,肺量测定法是尝试过β-agonist救援,30分钟后再次。肺量测定法电子数据传输到肺量测定法的质量控制中心每周数据质量和遵守的严格审查肺量测定法入选标准14。
除了上面的串行肺量测定法测量中,基线(槽)肺量测定法测量被访问2和3(阶段1),和FEV1上午9点和FVC 06:00时h之间的测量及h后在基线和2,4,6,8周的治疗。
呼吸困难评级
改变呼吸困难的评估使用基线呼吸困难指数(BDI)完成随机,和过渡呼吸困难指数(TDI)完成后2、6和8周治疗15。BDI的焦得分计算总和的三个领域:功能障碍、任务级,级的努力。总基准分数范围从0(严重呼吸困难)12(无呼吸困难的限制)。TDI焦分数被定义为一笔9的三个领域使用规模(主要恶化)+ 9(重大的改进)。
患者日记卡
慢性阻塞性肺病患者记录其症状,早晚呼气流速峰值(病人),β-agonist使用,夜间醒来由于慢性阻塞性肺病每天的日记。日记包括6个COPD症状的问题集中在整体时间症状由于慢性阻塞性肺病,气短、咳嗽、粘液生产,实现了日常活动困难(光),和困难在做活动,要求moderate-to-high物理运动。6个尺度是用来评估这些patient-reported端点(0 =没有时间/没有/不困难,5 =所有的时间/一个非常大的或大量/所以困难不能这样做)。
慢性阻塞性肺病急性加重的信息也被记录在病人的日记。COPD恶化被定义为COPD恶化症状需要:调用一个医生;访问医生或急诊室;住院;或治疗皮质类固醇和抗生素。
的生活质量
慢性呼吸道问卷(CRQ) COPD生活质量指标,是一个20问卷四个领域:呼吸困难,疲劳,情绪功能,掌握疾病的感觉16。问题在每个域被病人规模级(1 =贫穷7 =最佳函数)。CRQ完成后在同一访问BDI和TDI。
全球评估
到达诊所,所有患者完成了为期6个月的全球评估作为第一个程序访问中。病人和医生独立评估的整体感知的变化通过选择最合适的慢性阻塞性肺病患者的反应使用级Likert-type规模(7 =非常好1 =非常糟糕)。
安全性和耐受性评价
不良经历记录和监控所有时期的研究。病人进行临床评估,包括生命体征,身体检查,眼科检查,心电图,不良经验监测和实验室安全测试(完整的血细胞计数、血清化学和尿液),随机和指定的访问之前,所有四个时期的研究。最终安全评估进行了最后的计划访问期间在停药3或4(扩展)或访问。
统计分析
主要功效是基于意向性治疗分析方法,定义为人口患者基线值和至少一个治疗周期测量。缺失值没有估算端点。对于FEV1,每个病人的端点被定义为所有测量的平均值。例如,如果一个病人只有星期2槽FEV1然后停止研究,平均槽设置是星期2的值。统计分析是基于双尾测试在0.05显著性水平;数据提出了最小二乘方法(95%置信区间),除非另有说明。
主要疗效终点是意味着串行FEV的群体间的比较1评为FEV的平均值1测量值超过24 h后2周的治疗,这是使用一个ANCOVA模型分析与治疗和研究网站因素和基线FEV1协变量和ipratropium可逆性。分段线性对比测试基于ANCOVA模型被用来检查0.5 -的剂量反应关系,2 -,3 -和4 mg剂量的OrM3和提供一个更有效的剂量的比较与安慰剂。
特定的群体间的比较(即。每个OrM3 OrM3剂量,剂量与ipratropium, ipratropium与安慰剂)是基于特定的两两对比从ANCOVA模型。其他功效端点以类似的方式进行分析,使用ANCOVA模型,包括治疗和研究网站因素,和基线作为协变量(如适用)。此外,全球评估分为三类(更好,没有变化,更糟)Cochran-Mantel-Haenszel测试和分析17。一个事后分析患者的比例至少有一个慢性阻塞性肺病恶化。临时分析OrM3获得初步的安全性和有效性的信息。
的样本量85例每组估计提供80%的电力检测(α= 0.05,两面)0.094平均FEV - l群体间的差异1测量值超过24 h后2周的治疗。这个样本大小也有80%功率检测(α= 0.05,两面)百分之7.8%的群体间的差异变化的基线pre-dose FEV(槽)1。
结果
病人
共有828名患者的筛选试验,与412年随机进入积极治疗期(图。1⇑)。最常见原因患者不是随机包括无法满足肺功能标准,使用排除药物和前列腺病态症状的历史。它的目的是在每个治疗组85例。然而,临时分析412名患者被随机进行的,研究是比原计划提前终止由于副作用的发生率和缺乏明确的卓越功效OrM3与标准治疗(ipratropium)。
275年的412名患者随机完成了基础研究(图。1⇑)。总共21个病人停止由于临床不良体验(OrM3 4毫克,n = 9;3毫克,n = 4;0.5毫克,n = 3;ipratropium, n = 4;安慰剂,n = 1)和一个病人3毫克OrM3集团停止由于实验室不良经验(AE)。总共22名患者退出同意(n = 20)或停止由于缺乏功效(n = 2), 93名患者停止研究终止时在不同网站基于临时的结果分析。
的275名患者完成了积极治疗期间,一直持续到154年扩展时期(OrM3 4毫克,n = 117;ipratropium n = 37;图1⇑)。的主要原因中止前伸展期的起始终止网站和病人的同意撤军。持续到扩展研究的154例患者,143年停止在那段时期,主要是由于终止研究的发起人,撤回同意,或临床AEs;11个病人完成伸展期的所有16周(图1所示⇑)。
412名患者随机,387名患者完成了≥2周的研究治疗和有效的串行肺量测定法在星期2包含在主要终点分析。所有其他的分析,包括安全分析,包括数据从所有随机患者到终止点招生。
大多数患者分配severe-to-very严重的慢性阻塞性肺病(慢性肺部疾病的全球倡议阶段iii iv)18;均值±sd预测FEV百分之1在基线值为40.8±14.2。Ipratropium可逆性在所有组类似,意味着±sdFEV的变化121±13%,36μg ipratropium溴离子。基于均值焦BDI分数,所有组在基线和中度损伤类似由于呼吸困难(表1所示⇓)。所有六个治疗组类似的人口和其他基线特征(表1所示⇓)。
肺功能
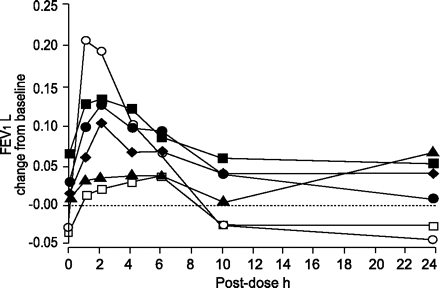
OrM3证明剂量提高串行FEV的主要终点1超过2周的治疗后24小时(表2⇓)。平均串行FEV的改善1测量的3 - 4 mg剂量与安慰剂相比具有统计学意义(p = 0.01和0.018,分别),而0.5 - 2 mg剂量没有不同于安慰剂(表2⇓)。峰均值变化从基线(峰值效应在2 h(治疗)在4毫克组三分之二ipratropium组中观察到的影响。4毫克剂量的效果还是明显的24小时post-dose(图2所示⇓);相比之下,对病人接受ipratropium, FEV1在10 h post-dose回到基线。FEV的探索性分析1曲线下的面积与平均串行FEV的结果是一致的1分析(数据未显示)。
平均变化在一秒用力呼气量(FEV1)从pre-randomisation基线值,测量24 h后2周的治疗。早晨剂量的研究药物后被第一次连环肺活量的测量(小时0,pre-dose)。3和4毫克口服M3-selective代理(OrM3)明显不同于安慰剂组(p < 0.05)。▪:OrM3 4毫克;•:OrM3 3毫克;♦:OrM3 2毫克;▴:OrM3 0.5毫克;○:ipratropium;□:安慰剂。
槽(pre-dose) FEV的平均百分比变化1从基线治疗6周表现出谦虚,尽管显著改善4毫克组与安慰剂比较(表2⇓)。在冲刷时期,没有任何证据表明反弹恶化后撤军的药物(数据未显示)。
其他有效性测量
呼吸困难的评估、TDI焦得分没有显著差异在任何治疗组与安慰剂比较(表2 6周的治疗⇓;图3⇓)或任何功能域的TDI(功能障碍、任务级和级的努力;数据未显示)。然而,剂量与观察OrM3改进的趋势意味着TDI分数(表2⇓)。
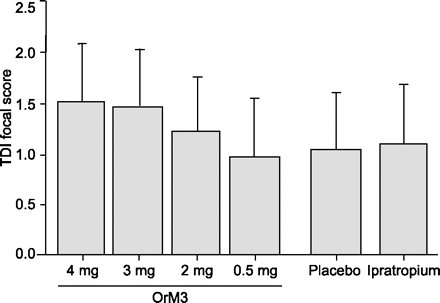
平均过渡呼吸困难指数(TDI)焦得分超过6周的治疗。数据提出了均值和95%置信区间。没有显著差异在积极治疗的安慰剂组,剂量相关的趋势,虽然在一秒钟用力呼气量一致的结果,可以看到。OrM3:口服M3-selective胆碱能受体拮抗剂。
有统计上显著的增加意味着(95%置信区间)病人在早上2毫克(11.07 (5.93 - -16.22),p = 0.017), 3毫克(10.52 (4.93 - -16.11),p = 0.029),和4毫克(14.14 (8.66 - -19.62),p = 0.002) OrM3组超过6周的治疗与安慰剂比较(2.18 (-3.34 - -7.71))。早上病人安慰剂,ipratropium组之间没有不同(图4所示⇓)。晚上病人反应显著提高仅供4毫克OrM3组(10.29 (4.42 - -16.16),p = 0.041)与安慰剂比较(1.89(-4.04 - -7.81),图4⇓)。
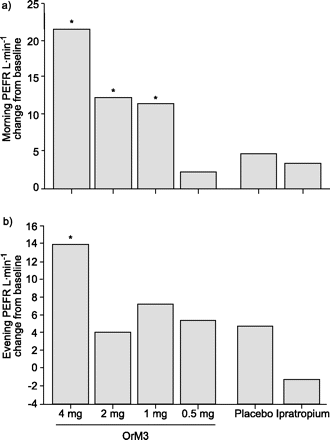
意味着变化)早上和b)晚上呼气流速峰值(病人)超过6周的治疗。2、3和4毫克口服M3-selective胆碱能受体拮抗剂(OrM3)组与安慰剂比较,表现出显著的改善在早晨病人。4毫克OrM3集团还演示了一个显著的改善与安慰剂相比在晚上病人。*:p≤0.05。
没有显著差异在每日总β-agonist使用的任何治疗组与安慰剂相比,尽管OrM3 2、3和4毫克,ipratropium显示数值减少每日β-agonist使用(表2⇓)。
根据每日日记分数,病人的整体慢性阻塞性肺病治疗组症状评分下降数值在所有活跃,最大的进步发生在4毫克OrM3集团(平均-0.15)与安慰剂比较(意思是-0.01;p = 0.018;表2⇓)。个别症状,每日呼吸困难评分显著提高只4毫克OrM3组与安慰剂比较(p = 0.033)。没有明显改善咳嗽、粘液生产和困难执行例程(光)或moderate-to-high OrM3物理活动或ipratropium组与安慰剂相比。
在六周的治疗期中,两组之间没有显著差异在夜间醒来。
大约17%的患者至少有一个慢性阻塞性肺病恶化超过8周的治疗(表2⇓)。总体而言,治疗OrM3与轻微减少慢性阻塞性肺病急性加重的发生率与安慰剂或ipratropium相比,但剂量效应并没有观察到。只有两个病人(4毫克OrM3组)住院治疗期间因COPD恶化的症状。
活性药物表现出任何影响整体的生活质量(CRQ),个人域的呼吸困难、疲劳,或者掌握疾病的六周积极治疗期间与安慰剂比较(表2所示⇓)。情感功能域显著提高3毫克OrM3组与安慰剂比较(p = 0.043),但没有明显不同的其他治疗组与安慰剂相比。
病人的全球评估的最后六周治疗期是4毫克OrM3组显著提高(平均(95%置信区间)的区别与安慰剂-0.49 (-0.93 - -0.05),p = 0.029)。没有观察到医生的区别安慰剂全球评估OrM3(平均差4毫克与安慰剂-0.17 (-0.54 - -0.20),p = 0.374),或ipratropium(平均差与安慰剂-0.02 (-0.35 - -0.39),p = 0.921)。
讨论
本研究的主要目标是测试假设一个高度M3-selective抗胆碱能代理的口服药物将提供一个优越的治疗优势在目前观察吸入抗胆碱能药物,通过改进的有效性和/或改进的安全性和耐受性。虽然吸入疗法已经证明了可接受的有效性和安全性/耐受性在慢性阻塞性肺病,大量研究证明提高病人满意度和符合口服与吸入的药物19。机理的副作用,如口干、心动过速和视觉障碍,抗胆碱能药物的效果有限,因此,这些药物主要由吸入的路线目前交付减少系统性风险。因为平滑肌收缩主要是由平滑肌M3受体表达,推测一个M3-selective拮抗剂可能避免的一些机理与转学至对手相关的副作用,从而获得更高的系统性风险和潜在的更大的功效,而恶化的副作用而非选择性拮抗剂。每日一次,口服生物利用率OrM3高度选择性M3抗胆碱能代理,是理想的位置测试这个假说。
从目前的研究数据表明,OrM3在慢性阻塞性肺病的治疗有效,对串行FEV改进指出1槽,FEV1全球评估,病人和病人。然而,口服OrM3不如吸入ipratropium作为支气管扩张剂最高OrM3剂量测试(4毫克);的改善意味着改变从串行FEV的基线1不到,观察ipratropium 2 h post-dose (0.13 L 4毫克OrM3吗与0.19 L ipratropium)。ipratropium响应(FEV峰值的大小1从pre-randomisation基线∼208毫升后一个36μg剂量)与其他地方的报道是相一致的20.,因此未能观察到类似的功效与OrM3在当前试验不太可能由于患者选择或研究设计。
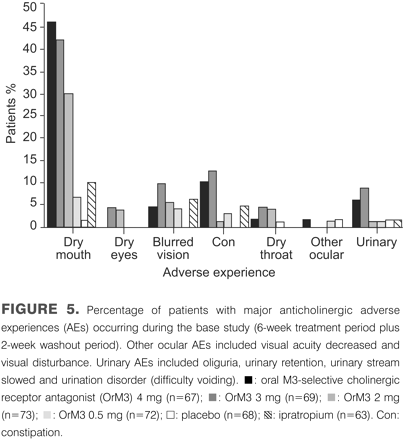
系统副作用,特别是口干,高4毫克OrM3比ipratropium治疗组治疗组。因此,改善M3-selectivity OrM3没有提供一种改进的保证金对支气管扩张剂治疗COPD患者的影响。政府可能吸入OrM3的路线可能会产生更好的疗效和/或更少的副作用;然而,这并不是这项研究的假设,因此需要额外的调查来评估这种可能性。
而OrM3不如ipratropium支气管扩张剂,积极的疗效数据支持M3-cholinergic受体的概念确实是主要的受体介导气道影响人类。相反,这些数据也证实M3-receptor封锁是主要负责副作用,如口干。这一发现表明,这将是很难识别系统管理抗胆碱能药物,还有效避免重大dose-limiting系统毒性。例如,darifenacin口服M3-selective拮抗剂批准用于治疗尿失禁,据报道有剂量相关事件的口干(13.2 -31.3%的患者)在临床试验中21。
总之,这个概念验证研究表明选择性M3受体拮抗作用引起的改善病人的气道功能没有M2 receptor-based副作用的发生,如心动过速。然而,dose-limiting副作用,如口干,可能由于在唾液腺M3受体拮抗作用,导致减少治疗相对于吸入抗胆碱能代理保证金。因此,增加了M3胆碱能受体选择性不太可能允许发展与改进的口服抗胆碱能药物治疗的慢性阻塞性肺病的利润。
确认
作者要感谢LX。魏和n .刘统计贡献。以下是相关研究人员。顶替Amgott、健康推进研究所、墨尔本、FL;m .艾尔沙德威斯康辛临床研究中心,LLC密尔沃基WI;FL F.J. Averill、诊断诊所,庄严的;j·伯恩斯坦,伯恩斯坦临床研究中心、公司、辛辛那提哦;W.W.会,威斯康星大学麦迪逊分校,麦迪逊,WI;j•卡尔霍恩,匹兹堡大学,宾夕法尼亚州匹兹堡;亚利桑那州图森市亚利桑那大学美国坎贝尔; F.J. Candal, North Shore Research Associates, Slidell, LA; J. Corren, Allergy Research Foundation, Inc, Los Angeles, CA; R. Dalal, R/D Clinical Research, Inc, Lake Jackson, TX; D. Doherty, University of Kentucky Medical Center, Lexington, KY; J.D. Epstein, Southern California Clinical Trials, Lakewood, CA; C.M. Fogarty, Spartanburg Pharmaceutical Research, Spartanburg, SC; J.T. Given, Allergy & Research Center, Canton, OH; T. Glinkowski, Breco Research, Inc, Houston, TX; G. Greenwald, Advances in Medicine, Rancho Mirage, CA; A. Heller, San Jose Clinical Research, Inc, San Jose, CA; R.T. Huling, Desoto Family Medical Center, Olive Branch, MI; M. Jacobs, Bend Memorial Clinic, Bend, OR; R.E. Kanner, University of Utah, Salt Lake City, UT; N. Kao, ICSL-Clinical Studies, Peoria, IL; E. Kerwin, Clinical Research Institute of Southern Oregon, PC, Medford, OR; K. Kim, Allergy, Asthma, & Respiratory Care Center, Long Beach, CA; C. LaForce, North Carolina Clinical Research, Raleigh, NC; R. Lapidus, Rocky Mountain Pulmonary & Critical Care Medicine, Wheat Ridge, CO; T. Lee, New Horizons Health Research, Atlanta, GA; M. Littner, VA Greater Los Angeles Healthcare System, Sepulveda, CA; R.F. Lockey, University of South Florida, Tampa, FL; D.A. Mahler, Dartmouth-Hitchcock Medical Center, Lebanon, NH; W. Campbell McLain III, Carolina Pulmonary & Critical Care, Columbia, SC; J. Melamed, Chelmsford, MA; R. Menendez, The Allergy & Asthma Research Center of El Paso, PA, El Paso, TX; S.D. Miller, New England Clinical Studies, North Dartmouth, MA; A.S. Nayak, ICSL-Clinical Studies, Normal, IL; H.S. Nelson, National Jewish Medical & Research Center, Denver, CO; M. Noonan, Allergy Associates, Portland, OR; J.J. Oppenheimer, Pulmonary & Allergy Associates, Springfield, NJ; A.J. Pedinoff, Princeton Center for Clinical Research, Princeton, NJ; F.J. Picone, The Clinical Research Center of Asthma & Allergy Consultants, PA, Tinton Falls, NJ; J.D. Plitman, Cornerstone Research Care, High Point, NC; B.M. Prenner, Allergy Associates Medical Group, Inc, San Diego, CA; A. Razzetti, University Clinical Research-Deland, Deland, FL; A. Rooklin, Allergy Research Associates, Upland, PA; E.J. Schelbar, Healthcare Research Consultants, Tulsa, OK; E.J. Schenkel, Valley Clinical Research Center, Easton, PA; G.C. Scott, Charleston Pulmonary Associates, Charleston, SC; G.A. Settipane, Asthma, Nasal Disease, & Allergy Research Center of New England, Providence, RI; W.N. Sokol, Health Research Institute, Newport Beach, CA; S. Spangenthal, Nalle Clinic, Charlotte, NC; W.W. Storms, Asthma & Allergy Associates, PA, Colorado Springs, CO; M. Strek, University of Chicago, Chicago, IL; D.O. Sun, Orlando, FL; S.F. Weinstein, Allergy & Asthma Specialists Medical Group, Huntington Beach, CA; R. White, UC Davis General Medicine Research Group, Sacramento, CA; J. Wolfe, Allergy & Asthma Associates of Santa Clara Valley Research Center, San Jose, CA; R. Wolfe, Southern California Institute for Respiratory Diseases, Los Angeles, CA; all USA.
- 收到了2005年的10月28日。
- 接受2006年6月26日。
- ©人期刊有限公司