摘要gydF4y2Ba
本研究验证了慢性阻塞性肺疾病(COPD)患者肺泡巨噬细胞(AM)比正常肺功能吸烟者和不吸烟者释放更多的促炎和/或更少的抗炎介质的假设。gydF4y2Ba
采用流式细胞术对13例慢性阻塞性肺病患者的支气管肺泡灌洗液进行AM分选(平均±gydF4y2Ba扫描电镜gydF4y2Ba67±2年,一秒用力呼气量(FEV)gydF4y2Ba1gydF4y2Ba) 61±4%参考),16例吸烟者,肺功能正常(55±2年,FEVgydF4y2Ba1gydF4y2Ba97±4%参考文献)和7位不吸烟者(67±7年,FEVgydF4y2Ba1gydF4y2Ba94±4%的引用)。分选后,培养AM(有或无脂多糖刺激)4 h和24 h,白细胞三烯B浓度gydF4y2Ba4gydF4y2Ba(LTBgydF4y2Ba4gydF4y2Ba),转化生长因子(TGF)-βgydF4y2Ba1gydF4y2Ba通过ELISA在上清液中量化金属蛋白酶(TIMP)-1的组织抑制剂。通过流式细胞术确定新鲜分离的反应性氧中间体(ROI)的生产。gydF4y2Ba
LTBgydF4y2Ba4gydF4y2Ba各组间分泌和ROI无显著差异。相反,慢性阻塞性肺病患者AM释放TGF-β明显减少gydF4y2Ba1gydF4y2Ba与肺功能正常的吸烟者和不吸烟者相比,TIMP-1的表达水平更高。gydF4y2Ba
总之,这些观察结果与慢性阻塞性肺疾病的抗炎和抗弹性能力降低相一致,这可能与慢性阻塞性肺疾病的发病机制有关。gydF4y2Ba
对烟草吸烟的炎症反应是慢性阻塞性肺病(COPD)的基本致病因子gydF4y2Ba1gydF4y2Ba.多种炎症细胞,包括肺泡巨噬细胞(AM)、多形核(PMN)白细胞和淋巴细胞gydF4y2Ba2gydF4y2Ba和细胞因子,氧化剂和基质金属蛋白酶(MMPS)等介质参与这种反应gydF4y2Ba2gydF4y2Ba.鉴于烟草吸烟引发所有吸烟者的炎症反应gydF4y2Ba3.gydF4y2Ba,但他们中的一些人发展了COPDgydF4y2Ba4gydF4y2Ba,它的类型、强度、定位和/或戒烟后未能解决可能有助于疾病的发病机制gydF4y2Ba5gydF4y2Ba.gydF4y2Ba
AM非常适合控制吸烟引起的炎症反应的程度和持续时间,因为它们是人类下呼吸道的主要免疫活性细胞群,在那里它们充当哨兵细胞gydF4y2Ba6gydF4y2Ba.1)细胞因子,如白介素(IL)-8和肿瘤坏死因子-α,它们进一步招募pmn,进而释放更多的炎症介质gydF4y2Ba7gydF4y2Ba;2)白三烯BgydF4y2Ba4gydF4y2Ba(LTBgydF4y2Ba4gydF4y2Ba),一种对其他炎症细胞有效的化学引诱剂gydF4y2Ba7gydF4y2Ba;活性氧中间体gydF4y2Ba8gydF4y2Ba,gydF4y2Ba9gydF4y2Ba,有助于增强炎症反应;4) MMP-1、MMP-9,可降解间质基质,引起肺气肿gydF4y2Ba7gydF4y2Ba相反,AM也有助于炎症反应的解决,因为它们能够释放多种抗炎分子,如转化生长因子(TGF)-β和MMPs组织抑制剂(TIMPs)gydF4y2Ba6gydF4y2Ba,gydF4y2Ba7gydF4y2Ba.既往COPD研究报道了AM在这些患者中异常释放IL-8、MMP-1和MMP-9gydF4y2Ba9gydF4y2Ba- - - - - -gydF4y2Ba11.gydF4y2Ba.在目前的研究中,假设从COPD患者获得的AM释放更多的促炎介质(LTB)gydF4y2Ba4gydF4y2Ba或更少的抗炎分子(TGF-β)gydF4y2Ba1gydF4y2Ba测试,TIMP-1)测试了从保存肺功能的吸烟者获得的那些。gydF4y2Ba
方法gydF4y2Ba
主题和道德gydF4y2Ba
目前作者研究了13例COPD(四辆流和九次出吸烟者),如全球阻塞性肺病(金)标准所定义的gydF4y2Ba1gydF4y2Ba,16名无慢性支气管炎或呼吸困难且肺功能正常的积极吸烟者,7名从不吸烟者。所有患者均需经支气管镜检查,以确定是否有孤立性肺结节或咯血发作。所有COPD患者在纳入st研究。患者接受吸入性支气管扩张剂(沙美特罗和/或沙丁胺醇和/或异丙托溴铵)治疗,4名患者接受吸入性皮质类固醇(ICS)治疗,但没有一名患者接受口服类固醇。患有其他慢性肺部疾病的患者(gydF4y2Ba如。gydF4y2Ba哮喘、支气管扩张和肺间质疾病)和心脏、肝脏或肾脏衰竭除外。所有参与者都签署了知情同意书。该研究方案获得了西班牙帕尔马马洛卡市德赛巴尔耳委员会(Committee d’etica de les Illes Balears)伦理委员会批准。gydF4y2Ba
肺功能gydF4y2Ba
强迫肺活量测定法(GS;Warren E. Collins, Braintree, MA, USA)gydF4y2Ba12.gydF4y2Ba. 肺活量参考值为地中海人群的参考值gydF4y2Ba13.gydF4y2Ba.在支气管镜检查前记录呼出CO浓度(ToxCO;Bedfont,Rochester,UK),以排除主动吸烟。gydF4y2Ba
支气管镜检查gydF4y2Ba
用柔性纤维电镀支气管(Pentax 15V; Pentax,日本Pentax,日本)进行支气管镜检查。在支气管科检查之前,活性吸烟受试者避免吸烟至少12小时。这是通过呼出的Co浓度检查,在所有情况下<10 ppm。支气管肺泡灌洗(BAL)按照标准方法进行。将八个25ml等分试样在未含有任何结节的下肺裂片的一种肺区段中灌输了八个25ml的无菌盐水溶液。将等分试样置于塑料受体中,并立即以200×离心gydF4y2BaggydF4y2Ba4°C保存10分钟。细胞颗粒在不含钙和镁的汉克平衡盐溶液中洗涤一次(Gibco BRL, Eggenstein,德国),并在最低必需培养基中重悬(Gibco BRL)直到分选。用血球计计数细胞。台台蓝排除后的存活率为>95%。gydF4y2Ba
使用保护标本刷(PSB;Mill-Rose实验室,Mentor, OH, USA), BAL前无菌采集支气管分泌物gydF4y2Ba14.gydF4y2Ba。PSB样品的培养产生<10gydF4y2Ba3.gydF4y2Ba集落形成单位·毫升gydF4y2Ba−1gydF4y2Ba在所有参与者。gydF4y2Ba
肺泡巨噬细胞分选gydF4y2Ba
使用Coulter Epics Altra HyPerSortgydF4y2Ba商标gydF4y2Ba系统(Beckman Coulter, Izasa,西班牙)。光学系统的校准使用流量检查氟球(Beckman Coulter)。喷嘴口、流量和分选策略如前所述设置gydF4y2Ba15.gydF4y2Ba简单地说,使用直径为100µm的流动池尖端,并将流速调整为400–500事件·sgydF4y2Ba−1gydF4y2Ba.AM在前向散射(线性标度)上选通gydF4y2Ba与gydF4y2Ba绿色荧光(对数标度)区分,中性粒细胞和淋巴细胞有高度的自身荧光。细胞悬液,在分选前后,保存在聚丙烯管中并保存在冰上。分选后,用血球计计数细胞,用台班蓝排除法测定细胞活力。经巴氏染色制备细胞旋蛋白,用于BAL细胞的形态学分化。经流式细胞术和目视定量分析,分选AM的纯度始终为>96%。台台蓝排除后的细胞存活率始终为>95%。gydF4y2Ba
巨噬细胞培养gydF4y2Ba
分拣AM在5×10暂停gydF4y2Ba5gydF4y2Ba·毫升gydF4y2Ba−1gydF4y2Ba在无内毒素RPMI 1640/10%胎牛血清中添加2 mMgydF4y2BalgydF4y2Ba谷氨酰胺,25 U·毫升gydF4y2Ba−1gydF4y2Ba青霉素25µg·mLgydF4y2Ba−1gydF4y2Ba链霉素。将细胞分离成等分试样并在37℃和5%CO的24孔聚苯乙烯板(Nunc,Wiesbaden,德国)中培养gydF4y2Ba2gydF4y2Ba四 h和24 h、 含或不含脂多糖(LPS(O55:B5),100 ng·mLgydF4y2Ba−1gydF4y2Ba(最终浓度);gydF4y2Ba大肠杆菌gydF4y2Ba有限合伙人;Sigma Chemicals CO, St. Louis, MO, USA)。在这些时间点,收集上清,在−80°C下保存细胞游离,直到分析。gydF4y2Ba
测量TGF-β,TIMP和LTBgydF4y2Ba4gydF4y2Ba
细胞培养上清中TGF-β浓度gydF4y2Ba1gydF4y2Ba,timp-1和LTBgydF4y2Ba4gydF4y2Ba采用市售三明治酶联免疫吸附测定试剂盒(Amersham Pharmacia Biotech, Chalfont, UK)。生物活性TGF -βgydF4y2Ba1gydF4y2Ba(0.02 mL的1-M盐酸加入到100µL的样品中以达到pH 1-2)。LTBgydF4y2Ba4gydF4y2Ba根据制造商的指示,使用酶免疫分析系统(Amersham Pharmacia Biotech)进行测量。TGF-β的检测限gydF4y2Ba1gydF4y2Ba,timp-1和LTBgydF4y2Ba4gydF4y2Ba6 pg·mLgydF4y2Ba−1gydF4y2Ba15.6 pg·毫升gydF4y2Ba−1gydF4y2Ba和1.25 pg·毫升gydF4y2Ba−1gydF4y2Ba,分别。gydF4y2Ba
测量投资回报率gydF4y2Ba
通过流式细胞术通过流式细胞术通过从二氢隆红胺-123(DHR;分子探针,烯烯或美国)的荧光化合物Rhodamine-123形成荧光化合物罗丹明-123来产生ROI的生产。简而言之,两个200μl样品的巨噬细胞悬浮液(5×10gydF4y2Ba5gydF4y2Ba·毫升gydF4y2Ba−1gydF4y2Ba;猎鹰2052号;Beckton-Dickinson, Lincoln Park, NJ, USA)在聚丙烯管中孵育10µL DHR溶液(100µg·mL)gydF4y2Ba−1gydF4y2Ba)在37°C下放置10分钟。其中一个样品用于评估自发ROI的产生,另一个样品与20 μ L LPS (10 ng·mL)混合gydF4y2Ba−1gydF4y2Ba最终浓度)。两个样品均在37℃下孵育30分钟。在第二个孵育期结束时,将500µL的冷PBS加入到两个样品中,然后将其冷藏,直到在Coulter Epics Altra HyPerSort上进行流式细胞术分析gydF4y2Ba商标gydF4y2Ba系统(Beckman Coulter),具有向前和侧向散射的巨噬细胞门设置。总共分析了10000个细胞;测定绿色荧光,并使用LYSIS II软件计算平均细胞荧光强度。细胞悬浮液作为自体荧光的对照。计算特定荧光强度,并表示为相对线性平均荧光(RLMF),即特定与非特异性(自体荧光)线性荧光的比率。gydF4y2Ba
统计分析gydF4y2Ba
结果显示为平均值±gydF4y2Ba扫描电镜gydF4y2Ba.单因素方差分析(其次是gydF4y2Ba事后gydF4y2Ba对比(Scheffe),如果合适的话)被用来评估组间差异的统计学意义。为分析ICS对COPD患者的潜在影响,采用Mann-Whitney u检验。用Spearman秩检验探讨兴趣变量之间的相关性。p值<0.05被认为是显著的。gydF4y2Ba
结果gydF4y2Ba
人体测量和功能数据gydF4y2Ba
桌子 1gydF4y2Ba⇓gydF4y2Ba呈现所有分子的主要临床和肺功能数据。年龄在嗜烟和患者的患者中相似,但具有正常肺功能的吸烟者年轻。同样,后者比COPD的患者较小的吸烟暴露(表1gydF4y2Ba⇓gydF4y2Ba).根据GOLD标准,COPD患者表现为中度气流阻塞。根据定义,肺功能正常的吸烟者和不吸烟者的肺活量测定是正常的。gydF4y2Ba
所有参与者的临床和肺功能数据gydF4y2Ba
BAL细胞计数gydF4y2Ba
肺功能正常的吸烟者总细胞计数较高(3.6±0.6×10)gydF4y2Ba5gydF4y2Ba·毫升gydF4y2Ba−1gydF4y2Ba(0.9±0.5×10)gydF4y2Ba5gydF4y2Ba·毫升gydF4y2Ba−1gydF4y2Ba;p < 0.05)。COPD患者也有升高的趋势(2.1±0.5×10)gydF4y2Ba5gydF4y2Ba·毫升gydF4y2Ba−1gydF4y2Ba),但差异未达到统计学意义。各组间细胞计数差异相似(表2)gydF4y2Ba⇓gydF4y2Ba).而AM在肺功能正常的吸烟者中有增高的趋势,而在COPD患者中中性粒细胞增多。总的来说,这些观察结果与之前的研究一致gydF4y2Ba16.gydF4y2Ba.gydF4y2Ba
支气管肺泡灌洗液总细胞数和差异细胞数gydF4y2Ba
LTBgydF4y2Ba4gydF4y2Ba释放gydF4y2Ba
在培养4小时后,LTBgydF4y2Ba4gydF4y2Ba非吸烟者的水平相似(222±107) pg·mLgydF4y2Ba−1gydF4y2Ba)和肺功能正常吸烟者(244±107 pg·mL)gydF4y2Ba−1gydF4y2Ba).COPD患者呈下降趋势(137±61 pg·mL)gydF4y2Ba−1gydF4y2Ba),但差异未达到统计学意义。LPS刺激没有显著调节这些水平(非吸烟者:284±144 pg·mLgydF4y2Ba−1gydF4y2Ba;肺功能正常吸烟者:342±99 pg·mLgydF4y2Ba−1gydF4y2Ba;COPD患者:226±94 pg·mLgydF4y2Ba−1gydF4y2Ba).当前作者没有测量LTBgydF4y2Ba4gydF4y2Ba在培养24 h后释放,如以前的研究表明gydF4y2Ba4gydF4y2Ba在这个时候几乎完全代谢了吗gydF4y2Ba17.gydF4y2Ba.gydF4y2Ba
ROI生产gydF4y2Ba
ROI生产在非莫克斯(8.32±3.67 RLMF)中,吸烟者,具有正常的肺功能(5.03±1.47 RLMF)和COPD患者(6.32±1.68 RLMF)。LPS刺激没有显着修改这些值(非摩托车:8.26±4.07 RLMF;肺部肺功能的吸烟者:5.29±1.60 RLMF; COPD患者:6.37±1.69 RLMF)。gydF4y2Ba
TGF -βgydF4y2Ba1gydF4y2Ba释放gydF4y2Ba
培养4 h后,TGF-βgydF4y2Ba1gydF4y2Ba所有组的浓度均低于检测限。24岁 h、 转化生长因子-βgydF4y2Ba1gydF4y2Ba所有患者的水平均可检测到且相似(图。 1gydF4y2Ba⇓gydF4y2Ba).LPS的添加增加了TGF-βgydF4y2Ba1gydF4y2Ba但这一效应在COPD患者中明显减弱(67±13 ng·mL)gydF4y2Ba−1gydF4y2Ba),肺功能正常吸烟者(135±55 ng·mL)gydF4y2Ba−1gydF4y2Ba;p<0.01)或非吸烟者(110±10 ng·mL)gydF4y2Ba−1gydF4y2Ba;p < 0.05)。gydF4y2Ba
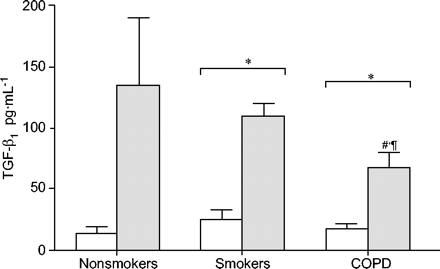
转化生长因子(TGF) βgydF4y2Ba1gydF4y2Ba每一组研究对象在培养24小时后释放,均用(gydF4y2Ba )而无(□)gydF4y2Ba大肠杆菌gydF4y2Ba脂多糖(100 ng·毫升gydF4y2Ba−1gydF4y2Ba)刺激。COPD:慢性阻塞性肺疾病。*: p < 0.05;**:P <0.01;gydF4y2Ba#gydF4y2Ba:p<0.05gydF4y2Ba与gydF4y2Ba不吸烟者;gydF4y2Ba¶gydF4y2Ba:p<0.05gydF4y2Ba与gydF4y2Ba肺功能正常的吸烟者。gydF4y2Ba
)而无(□)gydF4y2Ba大肠杆菌gydF4y2Ba脂多糖(100 ng·毫升gydF4y2Ba−1gydF4y2Ba)刺激。COPD:慢性阻塞性肺疾病。*: p < 0.05;**:P <0.01;gydF4y2Ba#gydF4y2Ba:p<0.05gydF4y2Ba与gydF4y2Ba不吸烟者;gydF4y2Ba¶gydF4y2Ba:p<0.05gydF4y2Ba与gydF4y2Ba肺功能正常的吸烟者。gydF4y2Ba
TIMP-1释放gydF4y2Ba
培养4 h后,无LPS刺激,肺功能正常的吸烟者AM释放的TIMP-1较少(6.2±2.1 ng·mL)gydF4y2Ba−1gydF4y2Ba)与不吸烟者相比(11.7±2.4 ng·mLgydF4y2Ba−1gydF4y2Ba;p < 0.05)。这一缺陷在COPD患者中进一步加重(1.7±0.4 ng·mL)gydF4y2Ba−1gydF4y2Ba;p < 0.05gydF4y2Ba与gydF4y2Ba肺功能正常的吸烟者;图2gydF4y2Ba⇓gydF4y2Ba).LPS刺激增加了非吸烟者TIMP-1的释放(16.7±4 ng·mL)gydF4y2Ba−1gydF4y2Ba;p < 0.05)。有趣的是,在肺功能正常的吸烟者中,这种效应明显降低(6.2±2.1 ng·mL)gydF4y2Ba−1gydF4y2Ba), COPD患者基本消除(2.4±0.8 ng·mL)gydF4y2Ba−1gydF4y2Ba).在24 h时,各组的TIMP-1释放量均显著增加(图2中注意y轴刻度的变化)gydF4y2Ba⇓gydF4y2Ba).LPS刺激在任何组中都没有进一步增强TIMP-1的释放,但在4 h时观察到的组间差异仍然存在。因此,TIMP-1释放在肺功能正常的吸烟者中显著降低,而在COPD患者中几乎不存在(图2)gydF4y2Ba⇓gydF4y2Ba).gydF4y2Ba
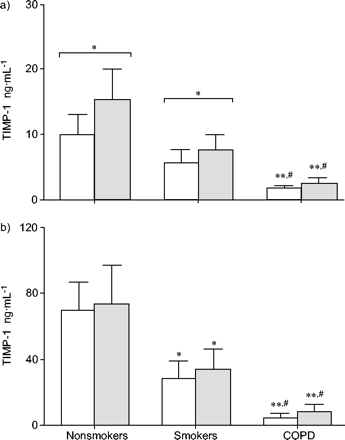
组织金属蛋白酶抑制剂(TIMP)-1的释放在a) 4 h和b) 24 h的每一组研究对象中,两者(gydF4y2Ba )而无(□)gydF4y2Ba大肠杆菌gydF4y2Ba脂多糖(100 ng·毫升gydF4y2Ba−1gydF4y2Ba)刺激。COPD:慢性阻塞性肺疾病。*: p < 0.05;* *: p < 0.01gydF4y2Ba与gydF4y2Ba不吸烟者;gydF4y2Ba#gydF4y2Ba:p<0.05gydF4y2Ba与gydF4y2Ba肺功能正常的吸烟者。gydF4y2Ba
)而无(□)gydF4y2Ba大肠杆菌gydF4y2Ba脂多糖(100 ng·毫升gydF4y2Ba−1gydF4y2Ba)刺激。COPD:慢性阻塞性肺疾病。*: p < 0.05;* *: p < 0.01gydF4y2Ba与gydF4y2Ba不吸烟者;gydF4y2Ba#gydF4y2Ba:p<0.05gydF4y2Ba与gydF4y2Ba肺功能正常的吸烟者。gydF4y2Ba
ICS的影响gydF4y2Ba
LTBgydF4y2Ba4gydF4y2BaTGF -βgydF4y2Ba1gydF4y2Ba,在治疗组(n = 4)和未治疗组(n = 9)的任何时间点上,TIMP-1和ROI产量没有差异。gydF4y2Ba
生理上的关联gydF4y2Ba
因为肺功能正常的吸烟者比COPD患者更年轻,吸烟次数更少(表1)gydF4y2Ba⇑gydF4y2Ba),为了研究这两个变量对所研究的不同介质的潜在混杂效应,我们探讨了前者和后者之间的生物学关系。然而,没有发现显著的关系。gydF4y2Ba
讨论gydF4y2Ba
吸烟是慢性阻塞性肺病的主要危险因素gydF4y2Ba1gydF4y2Ba.然而,只有一小部分吸烟者会患上这种疾病gydF4y2Ba2gydF4y2Ba.过度和持续的炎症反应似乎是这些后者的标志gydF4y2Ba5gydF4y2Ba.从理论上讲,这可能是由于吸烟引起的炎症反应增强,或者是刺激停止时炎症机制没有关闭gydF4y2Ba5gydF4y2Ba.AM是人类下呼吸道的主要免疫活性细胞群,因此,它们可能在吸烟后炎症的起始、调节和最终终止中发挥重要作用gydF4y2Ba7gydF4y2Ba.在本研究中,AM能分泌两种pro- (LTB)gydF4y2Ba4gydF4y2Ba,roi)和抗炎分子(tgf-βgydF4y2Ba1gydF4y2Ba研究慢性阻塞性肺病(COPD)患者中TIMP-1的表达。结果发现,这些患者的AM释放出相似数量的LTBgydF4y2Ba4gydF4y2Ba和ROI高于肺功能保持的吸烟者或非吸烟者。相反,释放TGF-βgydF4y2Ba1gydF4y2BaAM对TIMP-1有明显损害。gydF4y2Ba
LTBgydF4y2Ba4gydF4y2Ba在呼吸中增加冷凝gydF4y2Ba18.gydF4y2Ba、诱导痰gydF4y2Ba18.gydF4y2Ba和血清gydF4y2Ba19.gydF4y2Ba慢性阻塞性肺病患者。但是,AM发布了LTBgydF4y2Ba4gydF4y2Ba之前没有对这些患者进行过调查。LTB的异常释放gydF4y2Ba4gydF4y2Ba在慢性阻塞性肺病中,AM未观察到。这与Spencer报告的相似gydF4y2Baet al。gydF4y2Ba20.gydF4y2Ba在α-抗胰蛋白酶缺乏症患者的AM中,提示LTB的主要细胞来源gydF4y2Ba4gydF4y2Ba慢性阻塞性肺病是一种不同的细胞类型,可能是中性粒细胞gydF4y2Ba21.gydF4y2Ba.这并不是说AM不是COPD中其他炎症介质(如IL-8)的重要来源gydF4y2Ba9gydF4y2Ba.gydF4y2Ba
氧化应激是COPD发病的重要因素gydF4y2Ba22.gydF4y2Ba, AM可以产生ROIgydF4y2Ba6gydF4y2Ba.McLeod之前的一项研究gydF4y2Baet al。gydF4y2Ba23.gydF4y2Ba不能检测到从COPD吸烟者和非COPD吸烟者收集的AM中超氧阴离子释放的显著差异。本研究的结果支持先前的观察,因此,也提示AM在COPD的氧化应激发病机制中发挥边缘作用。gydF4y2Ba
TGF -βgydF4y2Ba1gydF4y2Ba是由几种细胞谱系产生的有效的抗炎细胞因子,包括AMgydF4y2Ba24gydF4y2Ba- - - - - -gydF4y2Ba29gydF4y2Ba.它还具有重要的抗弹性能,因为它减少了MMP的产量gydF4y2Ba30gydF4y2Ba,并刺激TIMP-1和基质蛋白gydF4y2Ba31gydF4y2Ba.目前的作者观察到慢性阻塞性肺病患者AM释放TGF-β的浓度显著降低gydF4y2Ba1gydF4y2Ba与肺功能保持的吸烟者和不吸烟者相比(图1)gydF4y2Ba⇑gydF4y2Ba).据目前作者所知,这之前没有报道过。既往研究报道TGF-β表达增加gydF4y2Ba1gydF4y2Ba在慢性支气管炎或COPD患者的气道上皮中gydF4y2Ba32gydF4y2Ba,gydF4y2Ba33gydF4y2Ba.然而,没有一家分析了AM发布的报告。目前的研究和以前的研究之间的差异可能与分析的不同细胞谱系和使用的技术有关。用于支气管上皮组织的研究gydF4y2Ba原位gydF4y2Ba杂交和/或免疫化学以确定细胞相关蛋白,这可能产生不同的结果gydF4y2Ba32gydF4y2Ba,gydF4y2Ba33gydF4y2Ba,而在目前的研究中,ELISA用于确定TGF-βgydF4y2Ba1gydF4y2Ba上清液中的浓度。此外,也可能是气道上皮和AM在TGF-β方面表现不同gydF4y2Ba1gydF4y2Ba在慢性阻塞性肺病发布。TGF-β表达增加gydF4y2Ba1gydF4y2Ba在上皮中,可以反映这种细胞因子在COPD中的气道重塑中的相关性gydF4y2Ba34gydF4y2Ba相反,TGF-β的释放减少gydF4y2Ba1gydF4y2BaAM可能反映了COPD患者中这些细胞的抗炎/修复能力不足。COPD患者气道上皮和AM的不同行为也有其他细胞因子的报道gydF4y2Ba35gydF4y2Ba.有趣的是,TGF-β的多态性gydF4y2Ba1gydF4y2Ba与低TGF-β相关的基因gydF4y2Ba1gydF4y2Ba水平在COPD患者中是常见的gydF4y2Ba36gydF4y2Ba这一观察结果与目前TGF-β降低的研究结果一致gydF4y2Ba1gydF4y2Ba慢性阻塞性肺病患者AM释放。gydF4y2Ba
同样,我们还观察到,COPD患者AM释放的TIMP-1比肺功能正常的吸烟者或非吸烟者要少(图2)gydF4y2Ba⇑gydF4y2Ba).作为TGF-βgydF4y2Ba1gydF4y2Ba刺激TIMP-1释放gydF4y2Ba31gydF4y2Ba,我们很容易推测,COPD中TIMP-1释放较低可能与TGF-β减少在机制上有关gydF4y2Ba1gydF4y2Ba先前讨论的释放。在任何情况下,考虑到TIMP-1是重要的抗弹性分子gydF4y2Ba10.gydF4y2Ba,其在COPD中的释放减少可能导致肺气肿的发展。然而,目前的结果与之前的一项研究相对照,该研究报道了AM在COPD患者和肺功能正常的吸烟者之间的TIMP-1释放没有差异gydF4y2Ba10.gydF4y2Ba.几个方法学方面可能有助于解释这一差异,因为与前一项研究不同gydF4y2Ba10.gydF4y2Ba,目前的作者非常小心地控制吸烟的急性影响已知会导致氧化应激和降低TIMP-1活性gydF4y2Ba37gydF4y2Ba.在被研究的个体中,活跃吸烟者的分布不均匀gydF4y2Ba10.gydF4y2Ba可能模糊了群体之间潜在的差异。同样,与之前的研究不同gydF4y2Ba10.gydF4y2Ba,gydF4y2Ba11.gydF4y2Ba,全身排除支气管感染,因为它会加重肺部炎症gydF4y2Ba38gydF4y2Ba.gydF4y2Ba
目前研究的其他方法学方面也值得评论。首先,COPD患者在年龄和吸烟史上与肺功能正常的吸烟者并不完全匹配。然而,这两个变量与本研究的任何生物介质之间没有任何显著的关系,这表明年龄和吸烟史之间相对较小的差异(尽管有统计学意义)并没有产生任何相关的混杂效应。其次,COPD患者与肺功能正常吸烟者之间的BAL细胞计数差异无统计学意义。这与之前的一些研究一致gydF4y2Ba16.gydF4y2Ba,并与他人形成对比gydF4y2Ba10.gydF4y2Ba,表明这些受试者的炎症细胞计数具有高度的可变性。第三,以往的研究对AM的粘附性质进行了分离gydF4y2Ba10.gydF4y2Ba,gydF4y2Ba11.gydF4y2Ba,而目前的作者使用的是流分类AM。该策略避免了不粘接AM的损失gydF4y2Ba39gydF4y2Ba,虽然它不能阻止粘附细胞的启动,因为在展示期间,细胞是在塑料孔板中培养的,可能也已经粘附到塑料表面。第四,以前的报告在刺激前24小时培养AMgydF4y2Ba9gydF4y2Ba,gydF4y2Ba10.gydF4y2Ba,gydF4y2Ba40gydF4y2Ba.如前所述,这可能会改变AM响应gydF4y2Ba39gydF4y2Ba.因此,本文作者决定在对早期(4小时)和晚期(24小时)不同炎症介质的浓度进行分类和量化后立即刺激AM。第五,使用的LPS浓度和选取的时间点与之前的研究相似gydF4y2Ba10.gydF4y2Ba,gydF4y2Ba41gydF4y2Ba,gydF4y2Ba42gydF4y2Ba.然而,不同的结果在LTBgydF4y2Ba4gydF4y2Ba如果使用不同的LPS浓度和/或不同的时间点,则可以找到和/或ROI释放gydF4y2Ba17.gydF4y2Ba,gydF4y2Ba41gydF4y2Ba.六,目前的作者没有分析可能在COPD中相关的其他炎症标记,例如IL-8和MMP-9。这是因为之前的研究已经这样做了gydF4y2Ba9gydF4y2Ba,gydF4y2Ba43gydF4y2Ba最后,目前的作者排除了ICS的潜在混杂效应,因为(n = 4) 不含ICS(n = 9) 这与许多研究表明COPD患者存在相对的类固醇抵抗相一致gydF4y2Ba44gydF4y2Ba- - - - - -gydF4y2Ba46gydF4y2Ba.gydF4y2Ba
综上所述,本研究表明慢性阻塞性肺疾病肺泡巨噬细胞释放转化生长因子-β明显减少gydF4y2Ba1gydF4y2Ba和金属蛋白酶组织抑制剂-1的含量高于肺功能保持的吸烟者和不吸烟者。这一观察结果表明,这些患者的抗炎和抗蛋白水解活性较低,这可能最终导致了该病的发病机制。gydF4y2Ba
致谢gydF4y2Ba
作者想要感谢参与研究的个人的合作,以及F. Bauzà, M. Bosch, A. Noguera和M. López,感谢他们在研究过程中的帮助。gydF4y2Ba
- 收到了gydF4y2Ba2004年3月17日。gydF4y2Ba
- 接受gydF4y2Ba2005年3月21日。gydF4y2Ba
- ©ERS期刊有限公司gydF4y2Ba
参考文献gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba














