摘要
在本研究中评估了轻度慢性阻塞性肺病的人们支气管扩张剂反应的长期变化。
一秒用力呼气量(FEV)的变化1.)对肺健康研究中4194名参与者的异丙肾上腺素反应进行了为期5年的每年测量,并在进入研究11年后再次测量。反应以mL(绝对值)、前支气管扩张剂值(相对值)的百分比和预测正常值的百分比(预测值)进行定量。
在基线,平均前支气管扩张剂FEV1.预测75.4%,响应很小。相对和百分比预测的反应在雄性和女性中类似;并与甲胆碱反应性正相关,对吸烟强度和年龄的负面相关。基线支气管扩张剂反应与FEV的后续下降不相关1..在研究的第一年,反应显著增加,很大程度上是由于戒烟,戒烟者的反应更大。在第一年之后,那些坚持戒烟的人的绝对反应变化不大,而那些不戒烟的人的绝对反应则有所增加。在整个研究中,所有参与者的平均相对反应和预测反应百分比都增加了。绝对反应的年变异性很大,个体参与者的重现性很差。
总之,戒烟增加了支气管扩张剂反应,并未预测强制呼气量的衰落率一秒钟。
大多数早期COPD指南推荐用肺活量学方法评估慢性阻塞性肺疾病(COPD)中支气管扩张剂的反应性1.,2.. 美国胸科会1.以及阻塞性肺病(金)准则的初始全球倡议2.>为200 mL, >为支气管扩张剂前值的12%。这两者都表明,由于可重复性差,在慢性阻塞性肺病中发生了这种情况,并且其患病率随着系列检测而增加1..最近的指导方针3.–5.不要将支气管扩张剂反应称为诊断标准或状态,除非“大”5..然而,最近的临床试验,特别是吸入类固醇,排除了患有显着的支气管扩张剂反应的患者6.,7.,可能是为了在不知情的情况下降低哮喘患者或哮喘特征的风险。
关于COPD中的支气管扩张剂反应的数据通常已经检查了严重或中度严重疾病的患者,很少有次数8.,9.在这方面,肺部健康研究(LHS)10.是一个唯一的数据集。它招募了近6,000名吸烟者,带有温和至温和的气道阻塞,并在支气管扩张剂施用之前和之后具有11岁的肌肉测量测量。这些数据允许在相对温和的COPD中表征支气管扩张剂反应,其可变性,随着时间和吸烟习惯的变化,以及其与肺功能下降率的关系。
方法
LHS10.–12.志愿者吸烟者的吸烟和支气管扩张剂(IPRATROPIUM)治疗是在35-59 YRS的志愿者障碍物(一秒钟内强迫呼气量(FEV1.)/强迫肺活量(FVC) <70%),且无其他疾病,并有FEV基线值1.预测正常值的55–90%13.. 在最初的5887名受试者中,超过90%的受试者在5个月内接受了年度肺活量测定 原始研究的年数10..在原始研究之后,随着大多数参与者维持电话联系,并重新审查注册4,194后的〜11 YRS,77%未知死亡11..最初的5年研究和11年随访都得到了所有参与机构伦理委员会的批准。
结果按照原LHS治疗组分组进行分析;常规护理(UC)和特殊干预(SI)。后者是一组被分配到异丙托品或安慰剂治疗的组合。他们都接受了戒烟计划,戒烟率相似,而且都没有接受任何进一步的研究相关干预。参与者还根据吸烟习惯分为三组。从第1年到第11年的每次随访中,持续戒烟者(SQ)都是经过生物化学验证的非吸烟者,他们在所有这些年中都有戒烟史。从第1年到第11年的所有随访中,持续吸烟者(CS)报告吸烟。间歇性戒烟者(IQ)在一些但不是所有的随访中报告吸烟。由于香烟剂量的不确定性,IQ组在一些分析中没有被考虑在内。
使用滚动密封肺活量计(Spirotech 500;Spirotech,亚特兰大,乔治亚州,美国),并有密集的质量控制方案14.. 在10年前和10年前进行了测量 从计量吸入器中吸入两次异丙肾上腺素(总剂量200μg)后的分钟。参与者停止使用支气管扩张剂12 h试验前。FEV的最大值1.报告了来自多项努力的FVC。支气管扩张剂反应来自FEV1.测量并没有影响研究进入。响应(预支气管扩张剂和后支气管扩张剂值之间的差异)以三种方式量化;作为绝对数(绝对值),作为前支气管扩张剂值(相对)的百分比,以及预测正常FEV的百分比1.(% 预料到的)。在基线测量甲胆碱反应性15..
原始队列的数据,随访5年 将yrs和随访11年的队列进行比较,以确保它们之间并没有差异。否则,报告11年队列的数据。
基于分类数据百分比、均值和标准差的标准描述性统计(SD.)使用定量变量。单变量分析采用Chi平方进行分类变量和未配对的T检验和用于定量变量的ANOVA。多变量分析用于评估基线协变量(年龄,性,治疗组,吸烟习惯和甲素反应性)对基线反应的影响。基线响应之间的关系和FEV的后续衰落1.考虑相同基线协变量的多元线性模型进行评估。为了测量从1年到5年的绝对响应的变异性,从一个纵向混合效应模型计算重复响应的残差。截距作为随机效应输入,吸烟状态和每日吸烟作为时间依赖的协变量输入。残差的平方,平方根,并报告为均方根误差(RSME)类似于SD.. 这种变化估计考虑了评估期间响应的系统性变化。所有多变量模型包括以下协变量:年龄、性别、治疗组、基线吸烟习惯、乙酰甲胆碱反应性和基线FEV1..
结果
Table 1⇓显示在11年以上检查的群组的原始基线特征。虽然该集团的基线特征与11年不审查的人不同,但差异因年龄和吸烟习惯的变化而占11..在基线时,所有三个响应通常分布。平均值SD.相对支气管扩张反应为4.32±5.01%,平均绝对反应为111±129 平均预测应答率为3.14±3.56%。这些数字与5年队列的数字没有差异。
表2.⇓显示与其他基线特征相关的多变量反应分析结果。虽然男性的绝对反应更大,但相对或百分比预测反应并不如此。反应与年龄和吸烟习惯呈负相关,表现为基线烟·天−1.和pack-yrs曝光。应答与甲胆碱反应性正相关。基线反应与治疗组或随后的吸烟习惯没有涉及。
基线支气管扩张剂反应与随后支气管扩张剂后FEV的下降无显著相关性1.当基线数据被排除在减少的评估之外,因此,从一年到11年起。
Figure 1⇓显示SI组和UC组的支气管扩张剂反应随时间的变化。
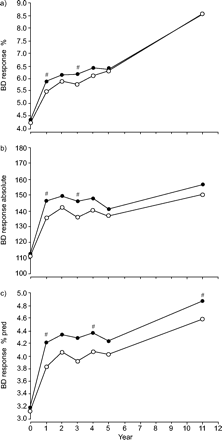
特殊干预(•)和常规护理中的支气管扩张剂(BD)反应(○) 11岁以上的群体 a)表示相对响应,b)表示绝对响应,c)表示预测响应的百分比。#:各组之间存在显著差异。
所有三项反应在研究的第一年显示出大幅度和显着增加。在第一年之后,相对反应在整个后续行动中逐渐和显着增加,而绝对反应在一年和五年之间升级,略微增加,而且显着增加,但在五年和11年之间。随着预测的额度倾向于趋于水平两组中的一年和五年,然后在五年和11年之间增加。在第一年的所有三项反应中的变化在SI组中明显大于UC集团(P = 0.02)。
图2.⇓显示与吸烟习惯相同的数据。在第一年,响应的增加在SQ集团中最大,CS集团中最小,并且在所有群体中都很重要。第一年后,SQ集团的绝对反应无重大变化,而在智商和CS组中,绝对反应在一年和五年之间没有变化,然后略有增加,但在五年和11之间大大增加。相对在所有三次吸烟组中,反应在所有三个吸烟组中逐渐增加,在SQ集团发生的第一年后,最少的变化。随着预测的估算,预测的响应表明了绝对反应的类似模式,除了在所有三个群体中增加五年和11之间的增加更加引人注目。在11-YR队列中的前5个YRS上的结果(图1⇑和2⇓)与较大的5年组基本相同。
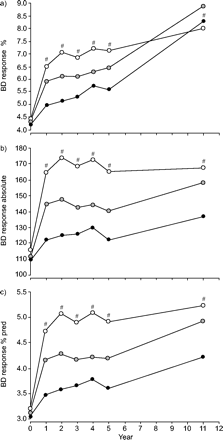
在持续戒烟者(〇)、间歇戒烟者(烧嘴)和持续吸烟者(•)中,支气管扩张剂(BD)的反应随时间变化。A)显示相对响应,b)显示绝对响应,c)显示预测响应的百分比。#:各组之间存在显著差异。
当考虑所有参与者时,反应的增加与每天吸烟的减少显著相关(p<0.001),但这种关系依赖于完全停止吸烟的参与者。在没有完全戒烟的参与者中,在研究的第一年结束时,支气管扩张剂反应和吸烟强度的变化之间没有显著的关系。在智商组中,目前的作者研究了吸烟习惯改变的反应年复一年的变化。在前一年戒烟的人比复发的人反应更大,但差异不显著。在SQ和IQ组中,第一年绝对和相对反应的增加与基线methacholine反应呈正相关(p<0.001),但在CS组中没有。
图3.⇓显示RMSE的频率分布,表示当数年一到五年的绝对响应的可变性,当平均反应为143毫升时。RMSE的平均值为77.1毫升,分布稍微偏向更高的值,中位数为69.5毫升(四分位数范围49.2-95.7ml)。随着年龄的增加,变异性显着(p = 0.017),并且对基线FEV也负面相关1.以预测正常值的百分比表示(p = 0.001)。变异性与基线烟龄和乙酰胆碱反应呈正相关(p<0.001)。在整个队列中,多变量回归分析显示,5 - 11岁间变异增加与肺功能损失更大相关(p<0.0001)。IQ (p = 0.0098)和CS (p = 0.0002)都是如此,但SQ (p = 0.0645)却不是这样。
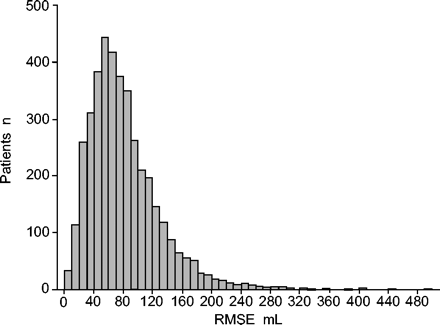
根均方误差(RMSE)的频率分布,标准偏差的模拟,绝对响应一到五年。
讨论
被检查的11岁队列是原始5岁队列的一个有偏见的样本。未参与11年随访的受试者更有可能是年轻人、男性,且不遵守戒烟和随访。然而,他们的基线肺功能与11岁的参与者没有差异,在症状和FEV下降率方面也没有差异1.在最初的5年期间,吸烟习惯的差异解释了11..最后,研究前5年的支气管扩张剂反应在11年组和5年组之间没有差异。
一般来说,支气管扩张剂的反应较小,平均而言,比早期COPD指南指定的显著反应更少1.,2.. 在4194名参与者中,∼20%的患者的初始反应>200 mL,但超过支气管扩张剂前值15%或预测正常值12%的反应不常见,分别发生在2.58%和1.17%的参与者中。个体内的反应差异很大(图。 3.⇑), RMSE平均为平均绝对响应的56%。由于这种可变性,反应的可重复性很差。在第一次年访时绝对反应<200毫升的参与者中,有20%的参与者在随后的年访试验中有更大的反应2-5,而在第一次年访时反应≥200毫升的参与者中,有45%的参与者在随后的年访试验中反应<200毫升。
相对和预测的基线反应百分比在雄性和女性中相似,但在雄性中绝对反应较大。据推测,当考虑身体规模时,应对响应相似。所有三个回应随着年龄的增长而下降;对于目前的作者,知识目前尚未报告。对吸烟的反应相关的反应,过去已被观察到8.. 这些反应与乙酰甲胆碱的反应性呈正相关,这一点以前也已注意到15..这种相关性可能已经预期,因为这两个响应都被认为反映气道平滑肌肉色调和/或兴奋性的差异。但是,有证据表明支气管扩张剂反应和甲素反应并不是非常相似的(表3⇓).在LHS中,methacholine的反应性有明显的性别差异,女性比男性有更大的反应性16..但支气管扩张剂反应却不是这样。基线的methacholine反应与年龄无关,而支气管扩张剂反应与年龄相关,而支气管扩张剂反应与吸烟习惯的相关性要比methacholine反应强得多15..戒烟对两种反应有相反的影响,增加支气管扩张剂反应,而倾向于减少甲基胆碱反应17..然而,由于CS组中的数据判断,疾病进展增加了甲胆碱反应性和支气管扩张剂反应。最后,甲素反应性的基线水平是随后肺功能丧失的强预测因子18.,不是支气管扩张剂反应的情况。
本研究中最引人注目的发现是在LHS的第一年观察到的支气管扩张剂反应的增加。这两种治疗组发生,但在Si组中比UC组更大(图1⇑),在那些戒烟的人中比没有那些没有的人(图2⇑).SI组和UC组之间的差异很大程度上是因为前者中SQ参与者的比例更大。因此,似乎戒烟与支气管扩张剂反应的增加有关。在目前和之前的研究中,基线反应与吸烟呈负相关,这一事实支持了这一观点8.. 值得注意的是,CS组中未戒烟的参与者在第一年的反应也有小幅增加,但本研究作者认为其中一些人可能在LHS开始时减少或戒烟,在进行测量的第一年年底,这些变化没有被记录下来。无法证明IQ参与者在研究期间戒烟和开始吸烟时的反应发生了变化;虽然变化方向正确,但并不显著。尽管有这些警告,目前的作者认为,对第一年反应增加的最好解释是,这是由于戒烟。完全停止比部分停止对反应的影响更大,因为后者与支气管扩张剂反应无关。
显然,作者不能确定上述支气管扩张剂反应变化背后的机制,但认为最好的解释是与日常吸烟相关的急性炎症过程的减少。这一论点被用于解释支气管扩张剂后FEV的小幅度增加1.与戒烟有关8..目前的数据表明,其中50%的增加因支气管扩张剂反应的增加而占了;也就是说,前支气管扩张剂FEV的增加1.随着吸烟停滞的比率远小于支气管扩张剂值的增加。
相对和百分比预测响应的相对和百分比之间的增加(图1⇑和2⇑)几乎与分母下降肯定有关,这是前支气管扩张剂FEV1.及其预测的正常价值。但是,绝对反应也从IQ和CS组中的五年到11增加。在CS组中,这些变化可能是由于疾病的进展,而在智商中,它们可能与疾病进展的组合有关,并进一步吸烟10..然而,预测11年的平均响应是4.79%(SD. = 这与间歇性正压呼吸(IPPB)研究中观察到的平均反应非常接近8.该研究的参与者与研究对象的年龄大致相同,但气道阻塞的情况要严重得多。因此,目前还不清楚,平均而言,这种反应指数随疾病进展变化很大。
然而,该研究没有发现支气管扩张剂反应,但表达了与随后的FEV下降相关1..由于基线测量用于评估响应,因此从第一次年度访问中使用数据作为估算率下降率的初始点。作者结果与阻塞性肺病中吸入类固醇的数据一致(Isolde)研究9,但与IPPB学习的研究发生冲突8.,该研究报告,有大量支气管扩张剂反应的COPD患者肺功能下降相对缓慢。在这两项研究中,用于评估初始反应的值没有用于计算下降率。目前的作者认为,目前的结果和来自ISOLDE研究的结果最有可能是正确的,IPPB结果可能与研究设计规定的支气管扩张剂治疗的残余效应有关,因此基线后FEV1.价值观受到同时治疗的影响。如果存在的话,这种效应在反应性更强的受试者中会更大,因此会降低下降率。
单个支气管扩张剂响应的变异性指数类似于SD.是根据第一至五年的绝对响应得出的,这一时期的平均响应变化相对较小。正如预期的那样,有相当大的可变性;RMSE平均为平均值的56%(图3)⇑).反应变异性与乙酰胆碱反应性之间的正相关关系,可以通过反映气道平滑肌张力的程度来解释。先前已经发现,反应的变异性与基线FEV呈负相关1.8.但是,变异性和年龄之间的关系,包装率和FEV率之间的关系1.吸烟者的减少并没有被注意到到作者的知识,也不容易解释。
总之,在一大批轻中度慢性阻塞性肺疾病患者中,发现大剂量支气管扩张剂反应不常见,但反应倾向于随着时间的推移而增加。停止吸烟的人比不吸烟的人反应更明显。支气管扩张剂反应与随后的肺功能下降率之间没有关系。
致谢
临床和协调中心的主要调查员和高级工作人员,全国心脏,肺和血液研究所以及数据监测委员会成员以及发病率和死亡率审查委员会的成员如下。案例西方储备大学,俄亥俄州克利夫兰:M.D.Allose(主要调查员),S. Redline(Co-Pi),C.D.deitz;亨利福特医院,底特律,MI,USA:M.S.Eichenhorn(主要调查员),W.A.Conway(Co-Pi),R.L. Jentons,K. Braden;Johns Hopkins大学医学院,巴尔的摩,MD,USA:R.A.Wise(主要调查员),S. Permutt(Co-PI),C.S.兰特(Co-PI),M. Daniel,V.Santopietro,K.A。席勒;Mayo Clinic,罗切斯特,MN,USA:P.D.Scanlon(主要调查员),J.P.Tuz(Co-Pi),G.M. Caron, K.S. Mieras, L. Walters; Oregon Health Sciences University, Portland, OR, USA: A.S. Buist (Principal Investigator), V.J. Bortz, D.J. Youtsey; University of Alabama at Birmingham, AL, USA: W.C. Bailey (Principal Investigator), C.M. Brooks (Co-PI), L.B. Gerald (Co-PI), S. Erwin, D. Gardner, M. Johnson, J. Mangan; University of California, Los Angeles, CA, USA: D.P. Tashkin (Principal Investigator), A.H. Coulson (Co-PI), E.C. Kleerup (Co-PI), I.P. Zuniga; University of Manitoba, Winnipeg, MB, Canada: N.R. Anthonisen (Principal Investigator), J. Manfreda (Co-PI), R.P. Murray (Co-PI), S.C. Rempel-Rossum; University of Minnesota Coordinating Center, Minneapolis, MN, USA: J.E. Connett (Principal Investigator), C.P. Irwin, P.G. Lindgren, M.A. Skeans, H.T. Voelker; University of Pittsburgh, Pittsburgh, PA, USA: R.M. Rogers (Principal Investigator), G.R. Owens (Co-PI), M.E. Pusateri; University of Utah, Salt Lake City, UT, USA: R.E. Kanner (Principal Investigator), G.M. Villegas, A. Sharp; Safety and Data Monitoring Board: C. Furberg, J.R. Landis, E. Mauger, J.R. Maurer, Y. Phillips, J.K. Stoller, I. Tager, A. Thomas Jr; Morbidity and Mortality Review Board: T. Cuddy, R. Fontana, R.E. Hyatt, C.T. Lambrew, B.A. Mason, D. Mintzer, R. Wray; National Heart, Lung, and Blood Institute, Bethesda, MD, USA: S.S. Hurd, (Former Director, Division of Lung Diseases), J.P. Kiley (Director, Division of Lung Diseases), G. Weinmann (Project Officer, Director, Airway Biology and Disease Program), T. Croxton (Project Officer), M.C. Wu (Div. of Epidemiology & Clinical Applications).
脚注
编辑意见见第6页。
- 已收到2004年9月1日。
- 认可的2005年3月17日。
- ©ERS期刊有限公司














