抽象的
我们评估了一种新型可溶性胍基环化酶刺激剂的Riociguat的治疗潜力,慢性血栓栓塞肺动脉高血压(CTEPH; N = 42)或世界卫生组织(WHO)功能级别的肺动脉高压(PAH; N = 33)/ III。
在这项为期12周、多中心、开放标签、不加控制的II期研究中,患者接受口服利ociguat 1.0-2.5 mgt.i.d。根据系统性收缩压(SBP)滴定。主要终点是安全性和耐受性;药效学变化是次要终点。
Riociguat通常耐受良好。在11名患者中发生无症状的低血压(SBP <90 mmHg),但血压归一化而不会在九个和剂量减少后进行剂量改变。中位数6分钟的步行距离增加了CTHEPH的患者(距离基线55.0米(390米); P <0.0001)和PAH(距离基线57.0米(337米); P <0.0001);患者II级或III级和博塞坦预处理的患者表现出类似的改善。肺血管抗性显着降低215··s·cm-5从基线(709 Dyn·S·CM-5;P <0.0001)。42例(56%)患者被认为经历了有关的药物相关的不良事件(AES; 96%温和或中等)。消化不良,头痛和低血压是最常见的AES。由于AES而停止停药是4%。
这些初步数据显示,Riociguat具有有利的安全性,并提高CTEPH和PAH的运动能力,症状和肺血管动力学。随机对照试验正在进行中。
肺动脉高压包括疾病亚型的不同收集。肺动脉高压(PAH)是这些最佳特征1,但其缓解学仍然不完全理解。几个介质参与了PAH的发病机制;降低了内源性血管抑制器的生物利用度,如一氧化氮和前列环素,并且增加了血管收缩剂如内皮素-I的产生2.磷酸二酯酶-5抑制剂,前列腺素和内皮素受体拮抗剂的引入,以靶向这些信号传导途径,提高了PAH患者的存活率3.而且,尽管他们的长期预后仍然非常差,大规模的登记报告显示1年生存率为~ 90%4.现在大约一半从初步诊断中存活5年5..
在另一种亚型肺动脉高压(慢性血栓栓塞性肺动脉高压(CTEPH))的患者中也发现了类似的生存趋势,这很可能是因为在专门的中心使用了肺动脉内膜切除术。CTEPH的特征是肺动脉内存在血栓。肺动脉内膜切除术是近端(大血管)CTEPH的治疗选择,可改善症状和生存率6.但是,大量的CTEPH患者不用于肺子宫切除术(具有远端CTEPH或严重伴随疾病)的候选者,或在肺下端切除术后遭受持续或复发性肺动脉高压的患者7.那8.. CTEPH和PAH之间的病理生理学相似性表明,针对PAH中异常信号的治疗也可能有益于CTEPH。然而,尽管对CTEPH患者进行的几种PAH治疗的非对照研究表明,在血流动力学和运动能力方面比基线检查时有所改善,但随机安慰剂对照试验得出了不确定的结果9.那10..
CTEPH和PAH的管理进一步进展可能是通过具有新的药物的可用性的可用性驱动。目前在开发中的一类新药直接靶向一氧化氮受体,可溶性胍基环化酶(SGC)。这种SGC刺激器显示了双向作用模式:它们增加了SGC对内源性生物可利用的一氧化氮的敏感性,并在不存在一氧化氮或稀缺时模仿这些效果11.那12..Riociguat (BAY 63-2521)是该类中第一个进入临床开发的成员。在肺动脉高压的大鼠和小鼠模型中,口服利ociguat对肺血流动力学、右心肥厚和肺血管重建有有益的作用11.. 对58名健康的白人男性志愿者(18-45岁)进行的一期研究表明,单次口服剂量(0.25-5毫克)的利奥雪卡很容易被吸收,并且耐受性良好13..不良事件(AES)均报告50%的受试者,所有这些受试者都是轻度或中度的。没有报告严重或威胁危及生命的事件,除了学习完成,也得到了一个案例。在19例CTEPH或PAH患者中进行了随后的概念研究。试验剂量滴定研究确定了Riociguat的剂量,其在不影响安全性和耐受性的情况下给出最大的临床效果。然后在过夜禁食期(≥8小时)后接受单个口服剂量(1或2.5mg)。在基线中评估药效学参数,以及在10分钟的一氧化氮中吸入期间和之后。当血液动力学参数恢复到基线时,施用Riociguat。概念证明研究的结果表明,Riociguat具有良好的安全性突细,并且在肺动脉高压患者中具有显着提高肺部血液动力学参数和心脏指数,以剂量依赖性方式,并且在更大程度上的程度越大而不是一氧化氮。平均肺动脉压(P̄.巴勒斯坦权力机构)减少≤40%14..概念证明研究的结果表明,与许多当前可用的PAH疗法一样,个性化剂量滴定可能是利用Riociguat潜在益处的最合适的方法。
我们报告二期研究的结果,用来评估口服riociguat治疗12周的治疗潜力滴定根据患者的收缩压(SBP) CTEPH或多环芳烃的功能,以及血液动力学的改善,并进一步描述这部小说疗法的安全性和耐受性。
方法
研究设计和患者
这种前景,开放标签,剂量滴定阶段II研究在15个专业中心进行,用于德国肺动脉高压;患者于2007年2月12日至2008年4月23日注册和治疗。年龄在世界卫生组织(WHO)功能二年级III或III中诊断为CTEPH或PAH的人工动态患者均注册,如果<4在研究开始前几周,诊断右心导管15.表示他们有P̄.巴勒斯坦权力机构平均肺血管阻力(PVR) >300 dyn·s·cm-5.CTEPH患者有资格包含在技术上不可操作(IE。远端)CTEPH,因伴发疾病或拒绝手术而被视为无法手术。此外,他们的诊断至少由以下两项确定:灌注-通气扫描、螺旋计算机断层扫描、磁共振血管造影或侵入性肺血管造影(向肺动脉注射造影剂)通过导管)。严重全身性动脉高压患者(SBP> 200 mmHg或舒张压> 120 mmHg),全身SBP <100 mmHg,急性或慢性留心力衰竭,肾功能不全(肌酐> 2 mg·DL-1(177μm)或蛋白尿> 1 g·日-1)或肝功能不全(胆红素> 2.5 mg·DL-1(43μM))被排除在外。允许服用内皮素受体拮抗剂的患者继续此治疗,但不包括服用磷酸二酯酶-5抑制剂或前列环素衍生物的患者。允许使用利尿剂、口服抗凝剂、洋地黄、钙通道阻滞剂和氧气补充。
当地的机构审查委员会和独立伦理委员会批准了研究议定书,并从所有患者获得书面知情同意书。
程序
该研究的主要终点是根据外周SBP的rIociguat的安全性,耐受性和可行性。患者接受了RIOCIGUAT的直接释放片剂(拜耳Schering Pharma Ag,Wuppertal,德国)t.i.d。12周,以0.5mg为0.5mg的间隔滴定,从1mg的起始剂量为2.5mgt.i.d。在服用早上剂量的利奥雪卡前1小时测量谷SBP。按照方案的规定,在休息20分钟后,采用非侵入性方法测量血压。用于测量血压的方法由医生决定,且未标准化(各研究中心之间一致)。如果外周血收缩压>100 mmHg,利奥雪卡的剂量增加;如果外周血收缩压为90-100 mmHg,利奥雪卡的剂量保持不变;如果外周血收缩压<90 mmHg,利奥雪卡的剂量减少,且无低血压症状(如头晕或晕厥);如果收缩压<90 mmHg并伴有低血压症状,则暂时停止治疗24小时,并以低剂量0.5 mg重新开始治疗。研究结束时,患者可以选择进入长期延长期。
研究者测量低血压(SBP<90 mmHg)时记录,如果患者自发报告或对开放、非定向询问作出反应,则记录其他不良事件。研究人员根据强度(轻度、中度或重度)以及与研究药物的可能关系对所有治疗引起的不良事件进行分级。任何致命或危及生命的事件,需要住院或延长现有住院时间,导致持续或严重残疾或丧失能力,或构成先天性异常或出生缺陷,均被视为严重AE。每2周评估一次生命体征、心电图检查结果和实验室参数。实验室参数包括血气、血液学、临床化学和自发尿液成分。
研究的次要终点(在每协定人口中评估)是从运动能力的基线(第0周)的变化(6分钟步行距离(6MWD)),修改的Borg Dyspnoea评分和世卫组织的职业阶级(在12之后评估周)。在同意第二个程序的患者12周后,还评估了心肺血管动力学的变化;在学习进入的4周内进行诊断右导管的结果被视为基线。包括直接测量P̄.巴勒斯坦权力机构,右心房压力,肺毛细血管楔压,平均动脉压和心输出(由使用热渗透装置进行和计算的三次测量)。计算的测量包括体表面积,肺血管抗性,全身血管抗性和心脏指数。
统计方法
在该探索性研究中,没有进行正式的统计样本量估计。安全分析基于所有接受至少一剂研究药物的患者。在完成研究的患者中进行疗效分析(每协定人口)。SAS®版本9.1统计软件(SAS Institute,Cary,NC,USA)用于数据分析。从成对数据计算连续药效变量中的基线的变化,并以中位数(四分位数范围)呈现。对这些变化进行威尔科克朗签名等级试验,P值为<0.05被接受为统计学意义。
结果
患者人口统计和吸毒给药
总共有75名患者(42例用CTHEPH和PAH)接受了至少一剂RIOCIGUAT,并对安全性分析有效。主体年龄为63.0(50-70)YRS,41(55%)是女性,所有人都是白色的。六(8%)患者在研究之前与内皮素受体拮抗剂吻合体的治疗稳定;没有持续或前后接触其他类别的药物。通过72名患者(96%; 41 CTHEPH和31 PAH)完成了12周的研究;它们的基线人口统计和临床特征如图所示表格1.可以预期,PAH患者似乎具有比CTEPH的那些更差的基线血液力学和运动能力。这也已在注册表数据中显示16.并且不太可能影响研究结果的解释。在基线上使用伴随药物,例如钙通道阻滞剂,利尿剂和氧气在很大程度上类似于CTEPH和PAH亚组(表2.).口服抗凝药物使用的发生率CTEPH组(92.7%)略高于PAH组(71.0%)。
在研究结束时,52名(72%)患者至少收到Riociguat的最大剂量(≥2.5mgt.i.d。)4(5%)在起始剂量(1毫克)t.i.d。);只有一名患者(1%)结束了0.5毫克的研究t.i.d。由于两名患者中的无症状低血压,Riociguat剂量减少0.5mg。剂量滴定在第12周的基线的120.0(110.0-130.0.0)mmHg中仅为120.0(110.0-130.0.0)mmHg的略微降低相关(p = 0.0067),这伴随着中位数的微小增加心率,从76.0(68.0-84.0)击败·min-1在基线到76.5(70.5-84.4)节拍·min-1第12周(P = 0.0406)。
安全
三(4%)患者由于AES停止了这项研究(一种患有肺部水肿而导致肺部静脉闭塞疾病的肺水肿;一个与研究药物无关的进步右心力衰竭;一个具有多种过敏史的历史有毒- 相关的exanthema)。通过65名(87%)的75名患者报道了AES,其中至少有一剂RIOCIGUAT(表3);42例患者(56%)被判定为药物相关。AEs的发生率与利ociguat的剂量无关。大多数药物相关的不良反应(96%)为轻度或中度严重,仅2例患者停用药物。报告的11例低血压发作中没有一例伴有导致永久停用研究药物的症状;其中9例恢复正常,无剂量变化,其余2例患者减少剂量耐受良好。有4例患者报告晕厥,但不认为与药物相关,因为可以确定独立的原因,如6分钟步行试验结束后咳嗽或用力发作。这些病例中没有一例需要降低利ociguat的剂量,并且在所有4例患者中继续上行滴定过程。最高剂量2.5 mg利西瓜特未发生晕厥t.i.d。11名患者经历过严重的AES,其中两个人停止了这项研究(一个与肺部水肿有关的肺静脉闭塞病,一个具有渐进式右心力衰竭的水肿)。在停止研究药物后,患有进步右心力衰竭的患者死亡。没有一个受试者在血清天冬氨酸氨基转移酶或丙氨酸氨基转移酶水平中经历过治疗的升高至正常上限的三倍以上,并且在其他实验室参数中没有药物诱导的异常的适应症。对博斯坦坦治疗的患者没有具体的安全性或耐受性问题。使用Bazett或Fridericia的公式(QTC Bazett和Frifericia)从最初的12周的研究期间从基线计算的正确QT间隔的中位变化在临床上微不足道:ΔQTCBazett和ΔQTCRifericia的中位数为2.4 ms和3.0MS分别在研究结束时(IE。在每位患者的最佳剂量下滴定rIociguat之后)。
锻炼能力
在Riociguat治疗过程中运动能力增加。在整个人口以及CTEPH和PAH亚组中观察到6MWD的显着增加(无花果。1).到本研究结束时,6MWD在86%的患者中改善了(50米,54%,均为29%> 100米)。
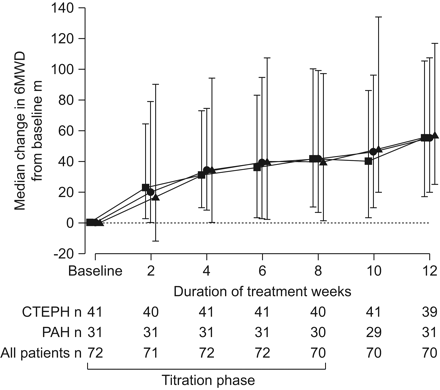
6分钟步行距离(6MWD)的中位数改善肺动脉高压亚型(n = 72)。在用Riociguat治疗12周后,在慢性血栓栓塞肺动脉高压(CTEPH)和肺动脉高压(PAH)患者组中观察到6MWD的显着改善(P <0.0001)。▪:CTEPH;▴:PAH;•:所有患者。误差栏显示间的间距。
在总人口中,基线的6MWD为359.0(300.0-420.0)。在治疗12周后,观察到55(20.0-107.0)m的显着中值改善(P <0.0001)。在基线上的官能二级的总人口中也观察到显着增加:基线423.5(396.0-511.0)m的改善71.5(40.0-133.0)m(p = 0.0001)。世卫组织职能III级患者的改善并不伟大:在基线的350.0(283.0-409.0)m中显着增加50.0(17.0-105.0)m(P <0.0001)。患有毛楸的患者中6MWD的改善(57.5(6.0-142.0)m; p = 0.0938)类似于单独服用Riociguat(55.0 m(22.5-106.5)m; p <0.0001)。
CTEPH子组
在CTEPH组中,6MWD为基线390.0(330.0-441.0)米。在治疗12周后,观察到55(17.0-105.0)米的显着改善(P <0.0001)。CTEPH的患者患者中也可以在基线上运作II级的患者(450.0(410.0-511.0)m以55.0(26.0-97.0)m(p = 0.0039)改善。世卫组织职能III级患者的改善相似:在基线的354.5(321.0-410.0)m中显着增加55.0(17.0-105.0)m(P <0.0001)。服用波丝菊酯的患者6MWD的改善(43.0m(-1.5-111.0)m; p = 0.3750)略小于单独服用Riociguat(55.0(20.0-105.0)m; p <0.0001)。
PAH亚群
与CTEPH的患者相比,PAH患者观察到6MWD的略微更大的改善。在PAH集团中,在基线的6MWD为337.0(215.0-406.0)米。在治疗12周后,观察到57.0(25.0-117.0)m的显着改善(P <0.0001)。在PAH患者中还可以看到患者在基线上运作II级的患者(305.0-407.0)M患者,基线患者的改善117.0(63.0-150.0)m(p = 0.0625)。世卫组织职能III类患者的改善不如基线的337.0(215.0-400.0)米的显着增加(20.0-79.0米)(p = 0.0002)。将Riociguat与波丝菊酯(90.0(35.0-145.0)m; p = 0.5000)的6MWd的改善大于单独服用rIociguat的人群(57.0(25.0-115.0)m; p <0.0001)。
其他探索结果
在为期12周的研究中,中位数修饰的Borg呼吸困难呼吸困难呼吸困难评分在10分尺度上得到一个点。总共有22例患者中的22例(31%)表现出世卫组织功能阶级的改善,只有一名患者劣化(无花果。2).
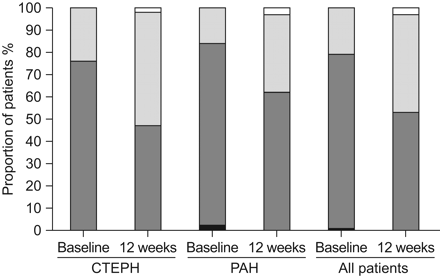
世界卫生组织(WHO)基线的功能阶级和第12周的肺动脉高压(n = 72)。世卫组织职业阶级在72名患者中有22例改善,只有一名患者恶化。CTEPH:慢性血栓栓塞肺动脉高压;PAH:肺动脉高压。□:I类;░:II级;▒:III类;▪:IV类。
在接受右心导管患者的患者的亚组(n = 50),P̄.巴勒斯坦权力机构已显着下降。我们观察到基线的-4.5(-8.0-1.0)mmHg的改善(45.0(37.0-53.0)mmhg; p <0.0001)。减少P̄.巴勒斯坦权力机构CTEPH(n = 30)的患者中也显着。在该亚组中,来自基线的-4.5(-7.0-1.0)mmHg(P <0.0001)的中位数改善(42.5(37.0-52.0)mmHg)。在PAH(n = 20)的患者中,来自基线的-4.0(-15.5-1.0)mmHg的中位数改善(47.5(39.0-55.5)mmHg)。PVR,全身血管抗性和PVR与全身血管阻力的比例也降低,而心脏指数增加(表4.).PVR的降低伴随着大多数患者6MWD的增加(无花果。3.).
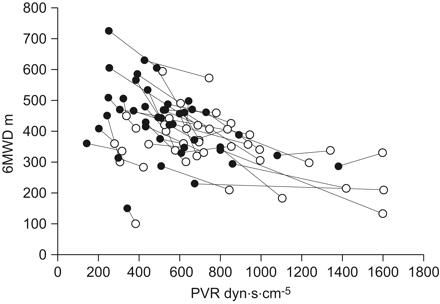
48例利ociguat治疗12周后患者6分钟步行距离(6MWD)和肺血管阻力(PVR)的变化。大多数患者PVR的改善伴随着6MWD的增加。每例患者显示配对基线(〇)和第12周(•)值。
讨论
CTEPH和PAH都是衰弱性与低生存率相关的疾病。虽然现在存在几种经批准的药理治疗方法,但生存率和与健康相关的生活质量仍然很差3.那17..重要的是,患有CTEPH的患者尚未获得批准的药理学疗法9..Riociguat是进入临床发展的第一个SGC刺激器。在这12周的12周中,HycleDRE,CTEPH和PAH患者的II期试验,RIOCIGUAT良好,表现出有利的安全性,并且在两种患者亚组中的运动能力和肺部血管动力学引起了强烈且临床上有意义的改善。
口服riociguat施用t.i.d。在大多数患者中成功地从起始剂量1mg滴定到最大目标剂量2.5 mg。个体化给药是可行和直接的。按计划测量收缩压,观察到全身血管舒张被心输出量增加所补偿。尽管在药物相关紧急治疗的AE患者中观察到系统性血压下降,但在大多数病例中,它与临床无关,只有2例患者需要调整剂量。目前还不清楚心率的轻微增加是否与临床有关。根据研究人员的判断,晕厥事件与药物无关,但需要仔细评估晕厥是否为CTEPH或PAH患者的潜在AE。
Riociguat没有导致天冬氨酸氨基转移酶或丙氨酸氨基转移酶水平的增加,在目前的研究中的上限的3倍以上。这些结果需要更大,长期试验的确认。来自随机,双盲,安慰剂控制,交叉,30个健康男性志愿者的相互作用研究的结果表明,Riociguat与抗凝血的华法林的组合不会影响华法林药代动力学和药效学18..Riociguat(2.5毫克t.i.d。)没有影响因子VII凝血活性或凝血酶原时间并具有有利的安全性。因此,伴随着具有现有抗凝血疗法的Riociguat的用途是没有预期代表风险。
血流动力学提供有关肺循环状态的客观和强大的直接信息。减少P̄.巴勒斯坦权力机构(CTH11%; PAH 8%)和PVR(CTH 29%; PAH 33%),本研究中观察到的心脏指数(CTEPH 19%; PAH 20%)在临床上是有意义的以前的PAH疗法研究。RIOCIGUAT的血液动力学效应在随机对照试验中进一步调查。
在研究结束时,6MWD在大多数患者中有所改善,重要的是,在CTEPH(55米)的患者中显示6MWD的大量和显着改善,以及PAH(57米)的患者。同样,这些数据必须在随机,受控研究中确认。有趣的是,世卫组织职业课程II和III的患者表现出6MWD的类似改善,表明RIOCIGUAT即使在具有相对轻微症状的患者中也可以提供显着的功能性改善。PAH疗法主要是在III类或IV类的患者中进行研究,但观察研究表明,可能存在在疾病早期阶段开始PAH治疗的临床优势19.那20..
本研究是第一个评估肺动脉高压下SGC刺激治疗潜力的研究。本II期研究设计的局限性包括其大小,缺乏盲目和不存在安慰剂控制。在未来的研究中应考虑在研究结束时接受第二次右心导管术(67%)的相对较少的患者进行患者。此外,患有持续或复发性肺动脉高血压后肺下气肌切除术的患者不包括在目前的研究中。这些患者应考虑在riociguat的未来研究中纳入患有Inoced CTEP的患者。在20分钟的休息时间后,使用非侵入装置记录血压。学习调查员决定了确切的方法。标准化的协议将用于III期研究,以确保学习中心之间的一致性。在未来的研究中,特定PAH Aetiologies的较大试验规模和分组可能允许Pah亚型之间有效的疗效比较。最后,本研究获得了从德国的独立伦理委员会获得批准,涉及新诊断的患者以批准的PAH疗法治疗,以便用调查药物治疗。 The ethics of such studies must always be carefully considered when designing the protocol, bearing in mind the potential risks in relation to the research value of the study. The delaying of treatment with approved PAH therapies is the subject of ongoing debate, particularly in the context of placebo-controlled studies21..
尽管存在这些局限性,但6MWD和血流动力学参数相对于基线检查的中位数改善幅度使研究结果充满希望。利奥雪卡的良好耐受性及其对血流动力学、6MWD、WHO功能分级和呼吸困难评分的积极影响有可能转化为患者健康相关生活质量的改善,因此有必要对利奥雪卡在CTEPH和PAH中进行进一步的随机对照研究。来自少量服用波生坦患者的数据首次提示,内皮素受体拮抗剂和利奥雪卡的联合治疗可能是可行的。在未来的临床研究中,还应研究利奥雪卡与现有PAH疗法的联合使用。
该第二阶段研究的结果表明1.0-2.5毫克t.i.d。Riociguat可能具有有利的安全性,可以改善CTEPH和PAH患者的运动能力,症状和血液力学。最近在CTEPH和PAH中进行了两个全球性,第II期临床研究,并正在进行临床研究,评估RIOCIGUAT在其他几种肺动脉和心血管适应症中的作用。
致谢
我们要感谢学习调查人员:B.卡拉达斯(德国Giessen大学);H. WIRTZ和H.-J.Seyfarth(莱比锡大学,德国莱比锡);G. Hoeffken(德国德累斯顿德累斯顿大学);H. GOLPON(汉诺威大学,德国汉诺威大学);V. Mitrovic和B. Swidnicki(Kerckhoff-Clinic Bad Nauheim,Bad Nauheim,德国);M. Buerke和M. Russ(哈勒大学,德国哈雷);C.F.Opitz(柏林德克医院,德国柏林);H. Leuchte(慕尼黑大学,德国慕尼黑); H. Klose and M. Karjalainen (University of Hamburg and CTC Hamburg, respectively; Hamburg, Germany); H. Wilkens (University of Saarland, Homburg, Germany); S. Rosenkranz (University of Cologne, Cologne, Germany); M. Pfeifer and T. Lange (University of Regensburg, Regensburg, Germany); S. Glaeser (University of Greifswald, Greifswald, Germany). We would also like to thank S. Unger (Bayer Schering Pharma AG, Wuppertal, Germany) for statistical analysis of the data. C. Mulligan (Oxford PharmaGenesis Ltd, Oxford, UK) provided editorial assistance, supported by Bayer Schering Pharma AG.
脚注
支持声明
该研究得到了德国柏林拜耳先灵制药公司的支持。
临床试验
这项研究在ClinicalTrials.gov上注册NCT00454558..
兴趣表
所有作者的利益陈述都可以找到www.www.qdcxjkg.com/misc/statements.dtl.
- 收到了2009年11月17日。
- 公认2010年4月21日。
- ©2010 ers.















