摘要
我们评估了一种新型可溶性鸟苷酸环化酶刺激剂riociguat对慢性血栓栓塞性肺动脉高压(CTEPH;n = 42)或肺动脉高压(PAH;n = 33)。
在这项为期12周、多中心、开放标签、不加控制的II期研究中,患者接受口服利ociguat 1.0-2.5 mgt.i.d。根据全身收缩压(SBP)滴定。主要终点是安全性和耐受性;药效学变化是次要终点。
Riociguat的耐受性一般良好。11例患者出现无症状低血压(收缩压< 90mmhg), 9例患者血压恢复正常,无剂量变化,2例患者减量后血压恢复正常。CTEPH患者中位6分钟步行距离增加(从基线(390 m)增加55.0 m;p<0.0001)和PAH (57.0 m from baseline (337 m);p < 0.0001);功能II或III类患者和波生坦治疗前的患者表现出类似的改善。肺血管阻力降低215 dyn·s·cm−5.从基线(709 dyn·s·cm)开始−5.;p < 0.0001)。42例(56%)患者被认为经历了药物相关不良事件(AEs;96%轻度或中度)。消化不良、头痛和低血压是最常见的AEs。因AEs而中止研究的比例为4%。
这些初步数据表明,利ociguat具有良好的安全性,可改善CTEPH和PAH患者的运动能力、症状和肺血流动力学。随机对照试验正在进行中。
肺动脉高压包括一系列不同的疾病亚型。肺动脉高压(PAH)是最好的特征1.,但其病因尚不完全清楚。几种介质参与了PAH的发病机制;内源性血管舒张剂(如一氧化氮和前列环素)的生物利用度降低,血管收缩剂(如内皮素- i)的产生增加2.通过引入磷酸二酯酶-5抑制剂、前列环素和内皮素受体拮抗剂来靶向这些信号通路,提高了PAH患者的生存率3.而且,尽管他们的长期预后仍然非常差,大规模的登记报告显示1年生存率为~ 90%4.大约一半的患者在最初诊断后存活了5年5..
在另一种亚型肺动脉高压(慢性血栓栓塞性肺动脉高压(CTEPH))的患者中也发现了类似的生存趋势,这很可能是因为在专门的中心使用了肺动脉内膜切除术。CTEPH的特征是肺动脉内存在血栓。肺动脉内膜切除术是近端(大血管)CTEPH的治疗选择,可改善症状和生存率6.,但大量CTEPH患者不适合进行肺动脉内膜切除术(远端CTEPH或严重伴发疾病),或肺动脉内膜切除术后持续或复发性肺动脉高压7.,8..CTEPH和PAH的病理生理学相似性表明,针对PAH中异常信号的治疗也可能对CTEPH有益。然而,尽管对CTEPH患者的几种PAH治疗进行的非对照研究显示,血流动力学和运动能力较基线有所改善,但随机安慰剂对照试验却没有得出结论性结果9,10.
CTEPH和PAH管理的进一步进展可能是由具有新作用模式的药物的可用性推动的。目前正在开发的一类新药物直接靶向一氧化氮受体可溶性鸟苷酸环化酶(sGC)这种sGC刺激剂表现出双重作用模式:它们增加了sGC对内源性生物可利用一氧化氮的敏感性,并在一氧化氮缺乏或缺乏时模拟这些效应11,12.Riociguat (BAY 63-2521)是该类中第一个进入临床开发的成员。在肺动脉高压的大鼠和小鼠模型中,口服利ociguat对肺血流动力学、右心肥厚和肺血管重建有有益的作用11.一项对58名健康白人男性志愿者(18-45岁)的I期研究显示,单次口服利ociguat (0.25 - 5mg)易于吸收,耐受性良好13.50%的受试者报告了不良事件(AEs),均为轻度或中度。未报告严重或危及生命的事件,除1例病例外,所有病例均在研究完成后得到解决。随后对19例CTEPH或PAH患者进行了概念验证研究。一项初步剂量滴定研究确定了在不影响安全性和耐受性的情况下,能产生最大临床效果的利西瓜特剂量。然后,患者在一夜禁食(≥8小时)后接受单次口服剂量(1或2.5 mg)。药效学参数在基线、10分钟一氧化氮吸入期间和之后进行评估。当血流动力学参数恢复到基线时给予利西瓜特。概念验证研究的结果显示,利西瓜特具有良好的安全性,显著改善肺动脉高压患者的肺血流动力学参数和心脏指数,且呈剂量依赖性,且改善程度大于一氧化氮。平均肺动脉压(P̄巴勒斯坦权力机构)减少≤40%14.概念验证研究的结果表明,与目前许多可用的PAH疗法一样,个体化剂量滴定可能是利用利ociguat潜在益处的最合适方法。
我们报告二期研究的结果,用来评估口服riociguat治疗12周的治疗潜力滴定根据患者的收缩压(SBP) CTEPH或多环芳烃的功能,以及血液动力学的改善,并进一步描述这部小说疗法的安全性和耐受性。
方法
研究设计与患者
这项前瞻性、开放标签、剂量滴定II期研究在德国15个肺动脉高压管理专家中心进行;患者于2007年2月12日至2008年4月23日登记和治疗。世界卫生组织(who)诊断为CTEPH或PAH的18-75岁非卧床患者如果在研究开始前4周内,右心导管插入术诊断为右心导管插入术,则登记为功能性II级或III级15表明他们已经P̄巴勒斯坦权力机构平均肺血管阻力(PVR) >300 dyn·s·cm−5..如果CTEPH患者在技术上不能手术,则符合纳入条件(即(远端)CTEPH,因伴随疾病不能手术或拒绝手术。此外,他们的诊断是通过以下至少两种方法确定的:灌注通气扫描、螺旋计算机断层扫描、磁共振血管造影术或侵入性肺血管造影术(肺动脉注射造影剂)通过导管)。严重全身性动脉高压(收缩压> 200mmhg或舒张压> 120mmhg),全身性收缩压< 100mmhg,急性或慢性左心衰,肾功能明显不全(肌酐> 2mg·dL)−1.(177μM)或蛋白尿>1g·d−1.)或肝功能不全(胆红素>2.5 mg·dL−1.(43 μM))。服用内皮素受体拮抗剂的患者被允许继续治疗,但服用磷酸二酯酶-5抑制剂或前列环素衍生物的患者被排除在外。允许使用利尿剂、口服抗凝剂、洋地黄、钙通道阻滞剂和补充氧气。
当地机构审查委员会和独立伦理委员会批准了研究方案,并获得了所有患者的书面知情同意。
程序
研究的主要终点是根据外周收缩压单独滴定利西胍的安全性、耐受性和可行性。患者接受利ociguat立即释放片(拜耳先灵制药公司,伍珀塔尔,德国)t.i.d。连续12周,从起始剂量1毫克到最大剂量2.5毫克,每隔2周以0.5毫克的剂量递增t.i.d。在给药前1小时测定空腹收缩压。按照该方案的规定,在休息20分钟后使用无创方法测量血压。测量血压的方法由医生自行决定,没有标准化(各研究中心之间一致)。当收缩压<90 mmHg且无低血压症状(如头晕或晕厥)时,利西胍的剂量增加;当收缩压为90 - 100 mmHg时,利西胍的剂量维持不变;如果收缩压< 90mmhg,伴有低血压症状,则暂时停止治疗24小时,并以较低0.5 mg的剂量重新开始治疗。在研究结束时,患者可以选择进入长期延长阶段。
研究者记录低血压(收缩压< 90mmhg),如果患者自发报告或回答公开的、非直接的询问,则记录其他AEs。所有紧急治疗的ae都由研究者按强度(轻度、中度或重度)和可能与研究药物的关系进行分级。任何致命或危及生命的事件,需要住院或延长现有住院时间,导致持续或重大残疾或丧失能力,或构成先天性异常或出生缺陷,都被认为是严重的AE。每2周评估一次生命体征、心电图和实验室参数。实验室参数包括血气、血液学、临床化学和尿液自发成分。
该研究的次要终点(在每个方案人群中评估)是从基线(第0周)到运动能力(6分钟步行距离(6MWD))、改良Borg呼吸困难评分和WHO功能分级(12周后评估)的变化。同意接受第二次手术的患者在12周后也评估了心肺血流动力学的变化;研究开始前4周的诊断性右置管结果作为基线。直接测量包括P̄巴勒斯坦权力机构,右心房压力,肺毛细血管楔压,平均动脉压和心输出量(用热调节装置测量并计算得出的平均值)。计算测量包括体表面积、肺血管阻力、全身血管阻力和心脏指数。
统计方法
在这个探索性研究中没有进行正式的统计样本量估计。安全性分析基于所有接受至少一剂研究药物的患者。对完成研究的患者进行疗效分析(按方案人群)。采用SAS®9.1版统计软件(SAS Institute, Cary, NC, USA)进行数据分析。连续药效学变量的变化由配对数据计算,并以中位数(四分位数范围)表示。对这些变化进行Wilcoxon符号秩和检验,p值<0.05为具有统计学意义。
结果
患者的人口特征和药物剂量
总共有75例患者(42例CTEPH患者和33例PAH患者)接受了至少一剂利ociguat,并对安全性进行了有效分析。受试者年龄为63.0岁(50-70岁),41名女性(55%),均为白人。6例(8%)患者在研究前使用内皮素受体拮抗剂波生坦治疗后病情稳定;没有持续或先前接触其他类别的药物。这项为期12周的研究共有72名患者完成(96%;41 CTEPH和31 PAH);他们的基线人口统计和临床特征显示在表1.可以预料,肺动脉高压患者的基线血流动力学和运动能力似乎比CTEPH患者差。注册表数据也显示了这一点16CTEPH亚组和PAH亚组在基线检查时联合用药,如钙通道阻滞剂、利尿剂和氧气的使用基本相似(表2).口服抗凝药物使用的发生率CTEPH组(92.7%)略高于PAH组(71.0%)。
在研究结束时,52例(72%)患者接受了至少最大剂量的利ociguat(≥2.5 mg)t.i.d。)和4例(5%)在起始剂量(1mg)t.i.d。);只有1例(1%)患者结束了0.5 mg的研究t.i.d。2例患者由于无症状低血压,利西加剂量减少了0.5 mg。剂量滴定仅与中位收缩压轻微下降有关,从基线时的120.0 (110.0-130.0)mmHg降至第12周时的110.5 (106.0-126.0)mmHg (p = 0.0067),同时伴随中位心率从76.0(68.0-84.0)次·分钟增加−1.在基线检查时达到76.5(70.5–84.4)次·分钟−1.第12周(p = 0.0406)。
安全
三(4%)名患者因不良事件而停止研究(一名患者因药物相关的肺静脉闭塞性疾病暴露而出现肺水肿;一名患者出现与研究药物无关的进行性右心衰;一名患者有多次过敏史,且出现药物相关疹)。75名至少服用一剂利奥雪卡的患者中有65名(87%)报告了不良事件(表3);42例患者(56%)被判定为药物相关。AEs的发生率与利ociguat的剂量无关。大多数药物相关的不良反应(96%)为轻度或中度严重,仅2例患者停用药物。报告的11例低血压发作中没有一例伴有导致永久停用研究药物的症状;其中9例恢复正常,无剂量变化,其余2例患者减少剂量耐受良好。有4例患者报告晕厥,但不认为与药物相关,因为可以确定独立的原因,如6分钟步行试验结束后咳嗽或用力发作。这些病例中没有一例需要降低利ociguat的剂量,并且在所有4例患者中继续上行滴定过程。最高剂量2.5 mg利西瓜特未发生晕厥t.i.d。11例患者出现严重的AEs,其中2例终止了研究(1例肺静脉闭塞性疾病相关肺水肿,1例进行性右心衰)。该患者在停止研究药物治疗后50天死亡。没有一个受试者在治疗后出现血清天门冬氨酸转氨酶或丙氨酸转氨酶水平升高到正常上限的三倍以上,其他实验室参数也没有药物引起异常的指征。在接受波生坦治疗的患者中没有特别的安全性或耐受性问题。中值的变化正确QT间隔计算Bazett或Fridericia公式Bazett(高职院校学前教育专业和Fridericia)从基线到任何访问最初12周的研究期间临床无关紧要:Fridericia Bazett和δδ高职院校学前教育专业高职院校学前教育专业的中位数是2.4和3.0女士,女士分别的研究(即在每个病人滴定至最佳剂量后)。
运动能力
治疗后运动能力增加。在整个人群以及CTEPH和PAH亚组中,6MWD显著增加(图1).到研究结束时,86%的患者6MWD得到改善(>50 m为54%,>100 m为29%)。
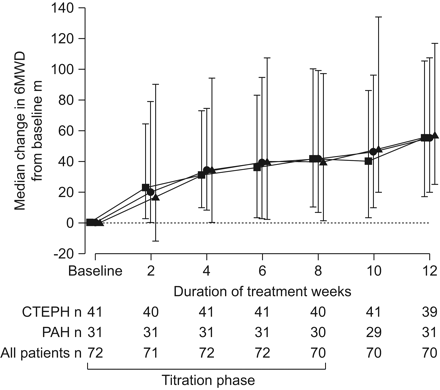
不同类型肺动脉高压6分钟步行距离(6MWD)的中位数改善(n = 72)。治疗12周后,慢性血栓栓塞性肺动脉高压(CTEPH)和肺动脉高压(PAH)患者组6MWD均有显著改善(p<0.0001)。▪:CTEPH;▴:多环芳烃;•:所有患者。误差条显示四分位数范围。
在所有人群中,6MWD基线值为359.0 (300.0-420.0)m。12周治疗后,观察到显著的中位改善55 (20.0-107.0)m (p<0.0001)。在基线时具有II类功能的总人群中也可以看到显著增加:从基线时的423.5 (396.0-511.0)m增加了71.5 (40.0-133.0)m (p = 0.0001)。WHO功能III级患者的改善并不显著:从基线时的350.0 (283.0-409.0)m显著增加了50.0 (17.0-105.0)m (p<0.0001)。利ociguat联合波生坦(57.5 (6.0-142.0)m;P = 0.0938)与单独服利鼠嗪组(55.0 m (22.5 ~ 106.5 m);p < 0.0001)。
CTEPH子群
在CTEPH组中,6MWD在基线检查时为390.0(330.0–441.0)m。在治疗12周后,观察到55(17.0–105.0)m的显著改善(p<0.0001)。在基线检查时功能等级为II级的CTEPH患者中也观察到增加:从基线检查时的450.0(410.0–511.0)m改善了55.0(26.0–97.0)m(p=0.0039)。WHO功能III级患者的改善情况相似:从基线检查时的354.5(321.0-410.0)m显著增加了55.0(17.0-105.0)m(p<0.0001)。服用利奥雪卡和波生坦的患者的6MWD改善情况(43.0 m(-1.5-111.0)m;p=0.3750)略低于单独服用利奥雪卡的人群(55.0(20.0–105.0)m;p<0.0001)。
多环芳烃组
与CTEPH患者相比,PAH患者6MWD的改善略大。在肺动脉高压组,6MWD为337.0 (215.0-406.0)m。12周治疗后,观察到显著改善57.0 (25.0-117.0)m (p<0.0001)。基线时who功能II级PAH患者也出现了增加:从基线时的393.0 (305.0-407.0)m增加了117.0 (63.0-150.0)m (p = 0.0625)。WHO功能III级患者的改善并不显著:从基线时的337.0 (215.0-400.0)m显著增加了50.0 m (20.0-79.0) m (p = 0.0002)。利ociguat联合波生坦(90.0 (35.0-145.0)m;P = 0.5000)大于单独服利鼠鼬组(57.0 (25.0-115.0)m;p < 0.0001)。
其他勘探结果
在12周的研究中,10分制中改良Borg呼吸困难评分的中位数提高了1分。在72例患者中,22例(31%)显示世卫组织功能等级改善,只有1例患者病情恶化(图2).
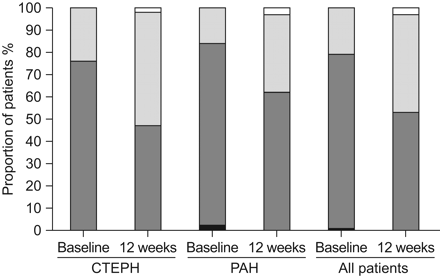
世界卫生组织(WHO)根据肺动脉高压类型在基线检查时和第12周时的功能分级(n=72)。WHO功能分级在72名患者中有22名患者改善,只有一名患者恶化。CTEPH:慢性血栓栓塞性肺动脉高压;PAH:肺动脉高压。□: 第一类;░: 第二类;▒: 第三类;▪: 第四类。
在接受两次右心导管置管的亚组患者中(n = 50),P̄巴勒斯坦权力机构有显著下降。我们观察到-4.5 (-8.0-1.0)mmHg较基线(45.0 (37.0-53.0)mmHg;p < 0.0001)。的减少P̄巴勒斯坦权力机构在CTEPH患者中也有显著性差异(n = 30)。在这个亚组中,与基线(42.5 (37.0-52.0)mmHg相比,中位改善为-4.5 (-7.0-1.0)mmHg (p<0.0001)。在PAH患者中(n = 20),与基线(47.5 (39.0-55.5)mmHg相比,中位改善为-4.0 (-15.5-1.0)mmHg。PVR、全身血管阻力及PVR /全身血管阻力比值降低,心脏指数升高(表4).在大多数患者中,PVR的降低伴随着6MWD的增加(图3).
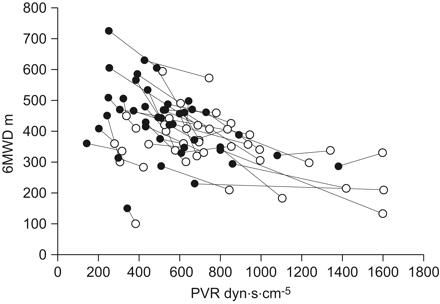
48例利ociguat治疗12周后患者6分钟步行距离(6MWD)和肺血管阻力(PVR)的变化。大多数患者PVR的改善伴随着6MWD的增加。每例患者显示配对基线(〇)和第12周(•)值。
讨论
CTEPH和PAH都是与低生存率相关的衰弱性疾病。尽管目前已有几种经批准的PAH药物治疗方法,但生存率和与健康相关的生活质量仍然很差3.,17重要的是,CTEPH患者尚未获得批准的药物治疗9.Riociguat是第一款进入临床研发的sGC刺激器。在这项为期12周的多中心II期临床试验中,75名CTEPH和PAH患者对Riociguat耐受性良好,安全性良好,并在两个患者亚组的运动能力和肺血流动力学方面都有显著的临床意义的改善。
口服利奥雪卡t.i.d。在大多数患者中成功地从起始剂量1mg滴定到最大目标剂量2.5 mg。个体化给药是可行和直接的。按计划测量收缩压,观察到全身血管舒张被心输出量增加所补偿。尽管在药物相关紧急治疗的AE患者中观察到系统性血压下降,但在大多数病例中,它与临床无关,只有2例患者需要调整剂量。目前还不清楚心率的轻微增加是否与临床有关。根据研究人员的判断,晕厥事件与药物无关,但需要仔细评估晕厥是否为CTEPH或PAH患者的潜在AE。
在目前的研究中,利西瓜特并没有引起天冬氨酸转氨酶或丙氨酸转氨酶水平升高到正常上限的三倍以上。这些结果需要在更大、更长期的试验中得到证实。一项对30名健康男性志愿者进行的随机、双盲、安慰剂对照、交叉、相互作用的研究结果表明,利ociguat与抗凝剂华法林联合用药不会影响华法林的药动学和药效学18.Riociguat(2.5毫克t.i.d)不影响因子VII的凝血活性或凝血酶原时间,且具有良好的安全性。因此,利ociguat与现有的抗凝治疗同时使用不存在风险。
血流动力学提供了有关肺循环状态的客观和可靠的直接信息P̄巴勒斯坦权力机构(CTEPH 11%;PVR (CTEPH 29%;心脏指数升高(CTEPH 19%;鉴于既往PAH治疗研究中观察到的结果,本研究中发现的PAH 20%具有临床意义。利ociguat对血液动力学的影响需要在随机对照试验中进行进一步的研究。
在研究结束时,大多数患者的6MWD都得到了改善,重要的是,CTEPH患者(55 m)和PAH患者(57 m)的6MWD都有实质性和显著的改善。有趣的是,WHO功能分级II和III的患者在6MWD中表现出类似的改善,提示即使在症状相对较轻的患者中,利ociguat也能提供明显的功能改善。多环芳烃治疗主要在功能III或IV类患者中进行研究,但观察性研究表明,在疾病早期开始多环芳烃治疗可能具有临床优势19,20..
目前的研究是第一个评估sGC刺激治疗肺动脉高压的潜力。本II期研究设计的局限性包括其规模、缺乏致盲和没有安慰剂对照。在研究结束时选择进行第二次右心导管置入术的患者比例相对较小(67%),应在未来的研究中予以考虑。此外,肺动脉内膜切除术后持续或复发性肺动脉高压的患者不包括在本研究中。在未来的利ociguat研究中,应考虑将这些患者与不能手术的CTEPH患者一起纳入研究。静息20分钟后,使用无创装置记录血压。具体方法由研究人员决定。III期研究将采用标准化方案,以确保研究中心之间的一致性。在未来的研究中,更大的试验规模和对特定PAH病因的分组可能允许对PAH亚型之间的疗效进行有用的比较。最后,这项研究获得了德国独立伦理委员会的批准,涉及了新诊断的患者,他们放弃了已批准的PAH治疗,以接受一种研究药物治疗。在设计方案时,必须始终仔细考虑此类研究的伦理问题,并考虑到与研究价值相关的潜在风险。 The delaying of treatment with approved PAH therapies is the subject of ongoing debate, particularly in the context of placebo-controlled studies21.
尽管存在这些局限性,但6MWD中位数和血流动力学参数较基线的改善幅度使研究结果充满希望。利ociguat良好的耐受性及其对血流动力学、6MWD、WHO功能分级和呼吸困难评分的积极影响可能转化为患者健康相关生活质量的改善,进一步的随机对照研究利ociguat在CTEPH和PAH中的应用是有必要的。少数服用波生坦患者的数据首次提示内皮素受体拮抗剂和利西瓜特联合治疗可能是可行的。在未来的临床研究中,利ociguat与现有PAH疗法的联合使用也应该进行研究。
II期研究的结果表明,1.0-2.5 mgt.i.d。利ociguat可能具有良好的安全性,并可能改善CTEPH和PAH患者的运动能力、症状和血流动力学。两项针对CTEPH和PAH的全球III期临床研究最近已经启动,评估利ociguat在其他几个肺部和心血管适应症中的作用的临床研究正在进行中。
致谢
我们要感谢研究人员:B. Karadas(吉森大学,吉森,德国);h。Wirtz和h。j。Seyfarth(莱比锡大学,莱比锡,德国);G. Hoeffken(德累斯顿大学医院,德国德累斯顿);H. Golpon(汉诺威大学,汉诺威,德国);V. Mitrovic和B. Swidnicki (Kerckhoff-Clinic Bad Nauheim, Bad Nauheim, Germany);M. Buerke和M. Russ(哈雷大学,哈雷,德国);C.F. Opitz(柏林DRK医院,柏林,德国);l . Leuchte(慕尼黑大学,德国慕尼黑);H. Klose和M. Karjalainen(分别为汉堡大学和汉堡反恐中心; Hamburg, Germany); H. Wilkens (University of Saarland, Homburg, Germany); S. Rosenkranz (University of Cologne, Cologne, Germany); M. Pfeifer and T. Lange (University of Regensburg, Regensburg, Germany); S. Glaeser (University of Greifswald, Greifswald, Germany). We would also like to thank S. Unger (Bayer Schering Pharma AG, Wuppertal, Germany) for statistical analysis of the data. C. Mulligan (Oxford PharmaGenesis Ltd, Oxford, UK) provided editorial assistance, supported by Bayer Schering Pharma AG.
脚注
支持声明
该研究得到了德国柏林拜耳先灵制药公司的支持。
临床试验
这项研究在ClinicalTrials.gov上注册NCT00454558.
感兴趣的语句
所有作者的兴趣声明可以在www.www.qdcxjkg.com/misc/statements.dtl
- 收到了2009年11月17日。
- 认可的2010年4月21日。
- ©2010人队















