摘要
浆细胞样树突状细胞是具有抗病毒和致耐受性的专业抗原提呈细胞。病毒感染和自身免疫是慢性阻塞性肺疾病(COPD)的重要发病机制。
本研究旨在通过免疫组化和流式细胞术量化有无COPD受试者肺部血液树突状细胞抗原2阳性pDCs,并结合香烟烟雾提取物(CSE)对pDCs功能的影响进行研究在体外.
pDCs主要位于淋巴滤泡,这一发现与它们的淋巴归巢趋化因子受体CXCR3和CXCR4的表达相一致。与未受气流限制的吸烟者和COPD全球慢性阻塞性肺疾病(GOLD) III-IV期患者相比,轻至中度COPD患者的淋巴滤泡和肺消化系统中积累pDC。将健康受试者的成熟pDC暴露于CSE中在体外显示共刺激分子的表达减弱和干扰素-α的产生受损。与健康受试者相比,COPD患者成熟的pDC产生更高水平的肿瘤坏死因子(TNF)-α和白细胞介素(IL)-8。
CSE会严重损害pDCs的抗病毒功能。在COPD中,pDC在淋巴滤泡中存在GOLD阶段依赖的积累,并伴随着成熟的pDC增加TNF-α和IL-8的产生。
慢性阻塞性肺疾病(COPD)是一种影响气道和肺实质的慢性炎症性疾病,在世界范围内引起大量发病率和死亡率1.炎症过程导致小气道狭窄(阻塞性毛细支气管炎),导致气流受限,不能完全可逆。此外,肺泡实质被破坏(肺气肿),导致气体交换受损,肺弹性反冲减弱。在西方国家,吸烟是迄今为止发展为慢性阻塞性肺病的最重要的危险因素2.尽管戒烟,导致持续炎症的确切致病机制仍有待阐明。在这方面,已经提出了一些致病因素,如低级别细菌和病毒感染、对改变的表位和遗传易感性的自身免疫反应3..
COPD中的炎症过程包括先天免疫反应(上皮细胞激活和中性粒细胞和巨噬细胞浸润)和适应性免疫反应(细胞毒性CD8+ t细胞、CD4+ t辅助细胞和b细胞的流入)。此外,COPD患者肺部淋巴滤泡数量增多4,5.
树突状细胞(DCs)是造血源的专业抗原提呈细胞,连接这些先天性和适应性免疫反应。树突状细胞利用特定的受体感知危险信号,同时对周围环境进行抗原取样。树突状细胞处理抗原,将其呈现在主要组织相容性II类和I类分子上,并通过上调共刺激分子和产生特定的细胞因子将这些信息与感知到的危险信号整合在一起。然后,树突状细胞通过与naïve淋巴细胞相遇形成免疫突触,引导抗原特异性t细胞的增殖,从而协调适应性免疫反应6.
一般来说,树突状细胞有两大不同的亚群:髓系树突状细胞(mDCs)和浆细胞样树突状细胞(pDCs)。7.pDCs代表一个独特的人口专业的抗原递呈细胞浆细胞样的形态和独特的表面受体表型,能够产生大量的I型干扰素对病毒和核酸acid-containing复合物从主机,感觉到通过toll样受体(通常7和98,9.除了这种与生俱来的抗病毒防御功能,pdc还通过表达吲哚胺2,3双加氧酶在维持耐药性方面发挥着至关重要的作用,该酶通过消耗氨基酸色氨酸诱导t细胞死亡10.此外,通过上调诱导型t细胞共刺激配体,pDCs能够产生调节性t细胞11.综上所述,有证据表明pDCs在外周耐受性和抗病毒防御机制中发挥重要作用。
我们和其他人使用流式细胞术对消化的人肺组织的单细胞悬液和支气管肺泡灌洗液(BAL)描述了人肺中存在的mDCs和pDCs12- - - - - -15.最近,越来越多的证据表明,不同亚群的mDCs及其在COPD等呼吸系统疾病发病机制中的功能和作用16- - - - - -19.然而,到目前为止,pDCs在人类肺中的确切位置尚不清楚。在这项研究中,我们感兴趣的是确定小气道中的pDCs。此外,考虑到pDCs的重要免疫学作用,我们假设,在吸烟者和慢性阻塞性肺病患者中,pDCs的数量和功能可能发生改变,从而导致抗病毒防御受损和/或耐受性丧失,这两者都是COPD发病机制中的机制概念20..
本研究首次描述了pDCs在人肺小气道中的分布,突出了pDCs在淋巴滤泡中的浓度。此外,与不受气流限制的吸烟者相比,轻至中度COPD患者的淋巴滤泡中有显著的pDCs积累。最后,我们发现了香烟烟雾提取物(CSE)的重要影响。在体外pDC的先天和适应性功能。
材料和方法
肺组织
组织取自比利时根特大学医院诊断为孤立性肺病变的患者的手术肺切除术标本。病理学家收集离肺病变最大距离的肺组织,且无后梗阻性肺炎或肿瘤侵袭迹象。恶性肿瘤手术患者均未接受新辅助化疗。终末期COPD肺组织取自肺移植(比利时鲁汶大学Gasthuisberg医院)或肺减容手术(荷兰马斯特里赫特大学医学中心)患者的移植肺。所有患者均在手术前签署知情同意书,并对其吸烟习惯和用药情况进行采访。COPD的诊断和严重程度是根据全球慢性阻塞性肺疾病倡议(GOLD)的分类,采用术前肺活量测定法确定的2.这项研究得到了根特大学医院、加斯修斯堡鲁汶大学医院和马斯特里赫特大学医学中心的医学伦理委员会的批准。
组织学
冰冻切片与抗血树突状细胞抗原2 (BDCA-2;CD303)单克隆抗体(克隆AC141, Miltenyi Biotec, Bergisch Gladbach, Germany)。如前所述进行Langerin (CD207)免疫组化染色16.免疫组化染色的详细信息请参见在线补充材料。
图像分析
使用计算机图像分析系统(Axiocam, Axioskop II mot + KS400;蔡司、从、德国)。选择基底膜周长< 6000 μm的无软骨气道进行分析21.在苏木精染色的切片中,靠近小气道的淋巴滤泡在100倍放大倍数下被鉴定为相邻单核细胞的集合22.在相邻切片中,通过CD3/CD20双染色识别出带有b细胞带的滤泡。通过追踪毛囊的周长来划定毛囊边界,并使用Image J软件(National Institutes of Health, Bethesda, MD, USA)计算面积。计数这些滤泡内bdca -2阳性细胞的数量。观察人员(G.R. Van Pottelberge和S. Van den Broeck)的临床数据是盲法。更多信息可在在线补充材料中找到。
流式细胞术
切除标本如前所述处理以获得肺单核细胞的单细胞悬液12.单克隆抗体和使用的设备在在线补充材料中介绍。
在体外pDC文化
CSE的准备过程如前所述23.从健康不吸烟志愿者和COPD患者的新鲜血液中分离出pDCs。所有COPD患者均为戒烟者,肺测量符合GOLD II期。所有患者均未使用全身皮质类固醇。受试者在研究前2个月没有恶化或感染。所有参与者在研究前签署知情同意书。使用Plasmacytoid Dendritic Cell Isolation Kit MicroBeads (Miltenyi Biotec)通过阴性选择分离pDCs。
3 μg·mL孵育pDCs−1cpg -寡脱氧核苷酸(2216 CpG-type A)或10 μg·mL−1imiquimod-R837 (invvivogen, San Diego, CA, USA),在含或不含CSE的37°C、5% CO的湿化气氛下保存18小时2.
采用夹心ELISA法(PBL干扰素源,Piscataway, NJ, USA)测定上清液中的干扰素-α浓度。其他细胞因子用细胞计数珠阵列人炎症反应试剂盒测定。采用流式细胞术分析pDC中成熟标记物的表达情况。所使用的抗体在在线补充材料中有描述。
统计分析
免疫组化研究采用SPSS 16.0 (SPSS Inc.)进行统计学分析。美国芝加哥,IL)。在评估多个独立组间的连续变量差异时,采用Kruskal-Wallis检验。当概率值<0.05时,选取对组进行Mann-Whitney u检验。相关性采用Spearman秩检验。p-值<0.05被认为是显著的。为在体外研究时,在Graph Pad Prism (Graph Pad software Inc.)中进行统计分析。美国加州圣地亚哥)。成熟标记的相对表达采用单样本t检验。其他比较采用配对和非配对t检验。
结果
人肺小气道中pDCs的鉴定
使用免疫组化染色的特异性标记物BDCA-2,在人肺小气道中检测到低数量的pDCs (图1).对人的呼吸道和扁桃体进行适当的同型对照染色,以确保特异性(如图在线补充材料中的图E1所示)。pDCs主要分布于小气道外膜,也有部分分布于固有层和上皮细胞。有趣的是,小气道中的pDCs通常位于淋巴滤泡(图1b).在相邻切片中通过CD3/CD20双染色检查这些淋巴滤泡中pDCs的定位(在线补充材料中的图E2)。定量分析显示平均值±sd淋巴滤泡中72.1±33.1%的pdc位于T细胞区。
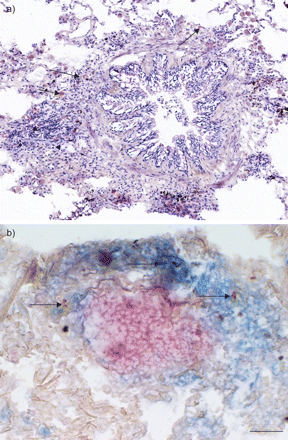
小气道浆细胞样树突状细胞的鉴定。a)冰冻切片的人肺(不受空气流动限制的吸烟者)与抗bdca -2抗体孵育,用新的品红(红色)染色,苏木精反染色。pDCs位于外膜(黑色箭头),集中在淋巴滤泡(箭头)(原始放大100倍)。b)对人肺组织冷冻切片进行CD3(蓝色表示t细胞区)、CD20(红粉色表示b细胞区)和BDCA-2(棕色表示pDCs)的三联染色。pDCs(箭头)主要存在于淋巴滤泡的t细胞区。比例尺= 50 μM。
肺pDCs表达CXCR3和CXCR4
为了研究肺pDCs的淋巴归巢潜能,我们用流式细胞术检测淋巴归巢趋化因子受体CXCR3、CXCR4和CCR7在消化的人肺组织标记单细胞悬液(图2),使用前面描述的控制策略12.肺pDCs呈CXCR3和CXCR4高表达。重要的是,CCR7在这些pDCs中表达非常低。比较未受气流限制的吸烟者(n = 3)和COPD患者(n = 2)中这些趋化因子受体的表达,可以发现CXCR3在COPD患者中呈高表达趋势(图2 f).
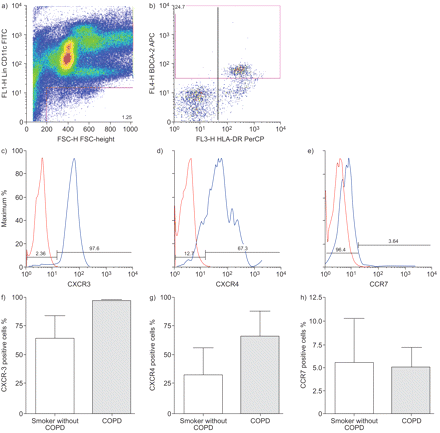
肺浆细胞样树突状细胞(pDCs)趋化因子受体的表达。用流式细胞术检测经酶解的人肺组织的单细胞悬液中的肺pDCs。)和b)控制策略识别pDCs:首先,血统负,CD11c消极和低autofluorescent细胞被选中(a),然后浇注关注HLA-DR BDCA-2双阳性细胞(b),在这些pDCs,淋巴归航的表达趋化因子受体CXCR3 c), d)趋化因子受体CXCR4和e) CCR7评估(蓝色柱状图)。红色直方图表示同型对照染色。数据来自一名慢性阻塞性肺疾病(COPD)患者。f-h非COPD吸烟者(n = 3)和COPD患者(n = 2)肺pDC趋化因子受体表达的比较。数据以平均值±表示扫描电镜.f) pDC上CXCR3的表达;g) pDC上CXCR4的表达;h) pDC上CCR7的表达。
COPD患者和非COPD受试者小气道pDCs的量化
研究人群的特征显示在表1.共调查74名受试者。该人群包括从不吸烟者(n = 10)、非COPD吸烟者(n = 22)、COPD GOLD I-II期受试者(n = 28)和COPD GOLD III-IV期受试者(n = 14)。轻至中度COPD患者未使用吸入或全身皮质类固醇。
对小气道的总气道壁、上皮细胞、固有层或外膜(不包括淋巴滤泡区域)中pDCs的数量进行定量分析,结果显示各组间无显著差异(图3以及在线补充资料中的图E3)。此外,无论是有气流限制还是没有气流限制(数据未显示),目前和已戒烟的受试者之间没有差异。
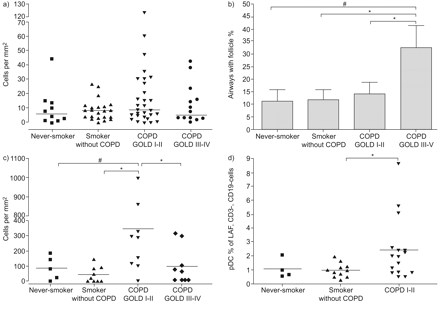
a)通过免疫组化染色确定bdca -2阳性的pDCs,在从不吸烟者的小气道壁上(不包括淋巴滤泡区域)进行量化。无慢性阻塞性肺疾病(COPD)吸烟者、COPD全球慢性阻塞性肺疾病倡议(GOLD) I-II期和COPD GOLD III-IV期。水平线表示每一组的中值。b)淋巴滤泡定量。均值±扫描电镜每组显示含有淋巴滤泡的小气道百分比。*:组间差异显著(p<0.05);#: p = 0.09。c)通过免疫组化染色确定的BDCA-2阳性pDCs在不吸烟者、非COPD吸烟者、COPD GOLD I-II期和COPD GOLD III-IV期的淋巴滤泡中进行量化。*:组间差异显著(p<0.05);#: p = 0.08。d)采用流式细胞术对独立研究人群消化的人肺组织的单核单细胞悬液中的pDCs进行量化。pDC为BDCA-2阳性细胞。定量表达为低自荧光(LAF)、cd3阴性、cd19阴性人群的百分比。水平线表示平均值。*:显著p值(p<0.05)。
总气道壁上pDCs的数量与langerin阳性mDCs的数量无显著相关性。然而,当根据GOLD分期将受试者细分为不同研究组时,总气道壁上的pDCs数量与朗叶素阳性mDCs数量之间出现了显著的正相关(r年代= 0.64, p = 0.004)。有趣的是,这种正相关在COPD GOLD III-IV期患者中消失了(在线补充材料中的图E4)。
淋巴滤泡中pDCs的定量分析
在同一研究人群中,发现了带有淋巴滤泡的小气道。COPD GOLD III-IV期患者中有淋巴滤泡的气道比例明显高于COPD GOLD I-II期患者(p = 0.02),且与从不吸烟者相比,COPD GOLD III-IV期患者中有更高的比例(p = 0.06) (图3 b).
轻至中度COPD患者淋巴滤泡中pDCs数量显著高于不受气流限制的吸烟者和重度至极重度COPD患者(p = 0.004和p = 0.04) (图3 c).在不吸烟者和非COPD吸烟者之间没有显著差异。重要的是,当在相邻切片中确定b细胞带(占所有滤泡的30%)定量滤泡中的pDCs时,在轻至中度COPD患者中观察到类似的pDCs积累趋势(在线补充材料中的图E5)。不同研究小组的代表性冷冻切片见图4.
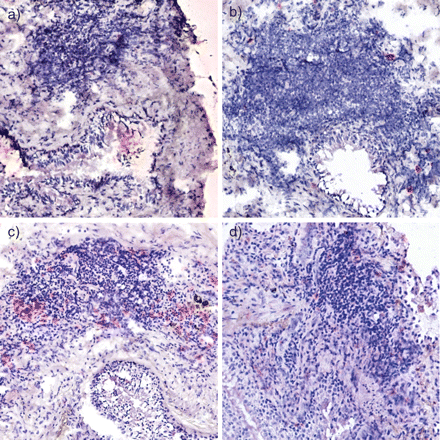
淋巴滤泡中的浆细胞样树突状细胞。人肺冰冻切片血树突状细胞抗原2免疫组化染色,以淋巴滤泡为重点。a)从不吸烟者,b)无慢性阻塞性肺病(COPD)吸烟者,c) COPD慢性阻塞性肺病全球倡议(GOLD) I期,d) COPD GOLD IV期。原始放大倍数200x。
肺消化物中pDCs的定量分析
在第二个独立研究人群中,用流式细胞术对pDCs进行了定量。在人肺消化酶的单核单细胞悬液中,pDCs被鉴定为低自荧光、cd3阴性、cd19阴性门内的BDCA-2阳性细胞。研究人群的特征显示在表2.
COPD患者(GOLD I-II期)单细胞悬液中pDCs的数量明显高于不受气流限制的吸烟者(p = 0.02) (图3 d).
CSE抑制成熟相关pDC的共刺激分子表达在体外
将人类血液中“未接触”的pDCs暴露于不同浓度的CSE中,以确定其对细胞活力的影响。2%的CSE浓度对细胞活力有不利影响,如图在线补充材料中的图E6所示。
在CSE(0.5或1%)存在或不存在的情况下,通过添加咪喹莫特(TLR-7激动剂)或CpG寡核苷酸(TLR-9激动剂),血液衍生pDCs成熟。TLR-7和-9刺激用于诱导cse暴露的pdc的成熟反应。吸烟暴露pDCs的成熟反应减弱,CpG/ cse刺激pDCs的CD83表达显著受损,imiquimod/ cse刺激的健康非吸烟受试者pDCs的CD80、CD83和CD86表达显著受损。在COPD患者的pDCs中也观察到由于CSE导致的成熟反应降低(图5以及在线补充资料中的图E7)。
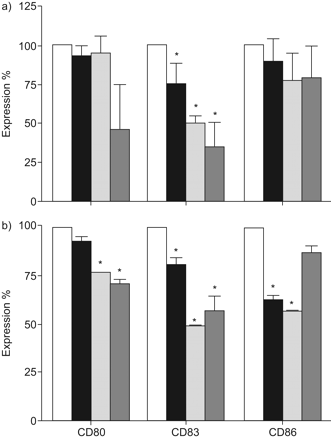
香烟烟雾提取物(CSE)损害浆细胞样树突状细胞(pDC)成熟。血液来源的pdc暴露于CSE和成熟刺激18小时。流式细胞术检测成熟标志物在活pDCs上的表达情况。均值±扫描电镜在0.5% CSE(▪)和1% CSE(代码)环境中,相对于没有CSE的成熟反应,成熟标记的上调被描述。▒:在1% CSE环境下,CpG或IMQ刺激慢性阻塞性肺疾病患者pDC的相对成熟;□:CSE控制为0%。a)以CpG寡核苷酸为成熟刺激;b)以IMQ作为成熟刺激。*: p < 0.05。这些数据分别适用于6个和5个独立实验。
CSE改变cpg诱导的由pDCs产生的细胞因子在体外
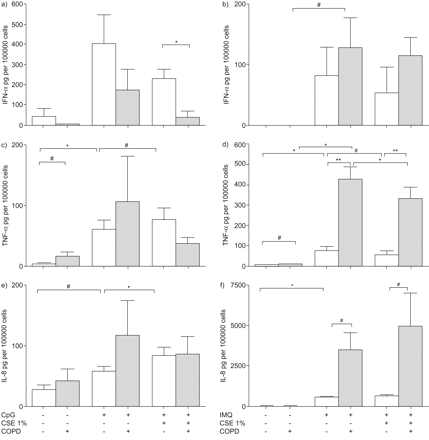
在CSE存在或不存在的情况下,CpG寡核苷酸刺激pDCs (1%) (图6a, c, e).在健康受试者和慢性阻塞性肺病患者中,CSE降低了CpG产生的干扰素-α。值得注意的是,与健康受试者的pDC相比,COPD患者经cse暴露的pDC产生的干扰素-α显著降低。在COPD患者的pDCs中,肿瘤坏死因子(TNF)-α和白细胞介素(IL)-8的生成在基线时已经趋于较高。在健康受试者中,CSE增加了cpg诱导的IL-8和TNF-α的生成,但在COPD患者中,CSE没有显著改变。
香烟烟雾提取物(CSE)在响应CpG寡核苷酸或imquimod (IMQ)时改变浆细胞样树突状细胞(pDCs)的细胞因子生产。健康受试者和慢性阻塞性肺疾病(COPD)患者的血液pDCs在CSE存在或不存在CpG寡核苷酸或IMQ的情况下(1%)孵育18小时。a, b)干扰素(IFN)-α, c, d)肿瘤坏死因子(TNF)-α和e, f)白细胞介素(IL)-8浓度。数据以平均值±表示扫描电镜.*: p < 0.05;* *: p < 0.01;#: p-值在0.05-0.08之间。数据代表6个(CpG)和5个(IMQ)独立实验。
CSE改变了吡喹莫特诱导的pdc细胞因子的产生在体外
在咪喹莫特刺激的pDCs中,CSE诱导健康受试者pDCs和COPD患者pDCs中TNF-α产量显著下降(图6b d f).我们观察到COPD患者的pDCs产生的TNF-α和IL-8水平显著高于健康受试者的pDCs。
在1% CSE的影响下,CpG或咪喹莫特处理的pDCs中IL-6、IL-10、IL-12或IL-1β的产生没有差异(数据未显示)。
讨论
本研究首次确认了人肺小气道中存在pDCs,并强调了它们在淋巴滤泡中的存在,这一发现与淋巴归巢趋化因子受体CXCR3和CXCR4在这些细胞上的表达一致。此外,我们发现在轻至中度COPD患者的淋巴滤泡和肺消化系统中有显著的pDCs积累。我们还证明了CSE对pDC功能的显著影响在体外表明COPD患者的pDCs能够产生更高水平的TNF-α和IL-8。
虽然通过使用消化肺组织的单细胞悬液或分析BAL液的研究已经很好地确定了人肺中存在pDCs,但pDCs在小气道中的确切分布和定位迄今尚不清楚。过去的,马斯顿et al。13使用免疫组化方法对人肺组织的CD123进行染色,以识别pDCs,但该标记物不具有特异性,因为它也被其他细胞表达,如mDCs、巨噬细胞和粒细胞。使用特异性标记物BDCA-2,在小气道粘膜表面发现少量pDCs,常在淋巴滤泡中发现。这种主要的淋巴样定位与所描述的pDCs在其他周围组织(如鼻黏膜和滑膜)的分布平行24- - - - - -26.事实上,众所周知,血液中的pdc直接从血液循环回到这些淋巴组织通过CXCR3和CXCR4配体影响下的高内皮小静脉。有趣的是,无论是COPD患者还是非COPD患者,在这些黏膜相关淋巴组织结构之外都发现了少量的pDCs,这表明pDCs也可以迁移到周围非淋巴组织。
肺bdca -2阳性的pDCs主要被认为是不成熟的,正如之前对消化的人肺组织的单细胞悬液的流式细胞分析所示12.成熟后,pDCs下调BDCA-2,但保留CD123的表达27.此外,我们的数据显示,趋化因子受体CCR7低表达,通常在DC的成熟过程中上调。弗里曼et al。17最近显示,bdca -2阳性的pDCs可以表达更高水平的成熟标志物,特别是在COPD中。这表明BDCA-2阳性细胞群由未成熟和成熟的pDCs组成,而成熟的pDCs可能变成BDCA-2阴性。
当量化COPD患者和没有气流限制的受试者小气道中pDCs的数量时,我们发现,与非COPD吸烟者相比,轻度和中度COPD患者的淋巴滤泡中这些细胞有显著的聚集。重要的是,流式细胞术对独立研究人群的人肺消化液中pDCs的定量证实了这些发现。由于淋巴滤泡中含有肺中大部分的pDCs,可以想象,肺消化液的流式细胞术研究结果反映了淋巴滤泡中pDCs的定量。淋巴滤泡中pDCs的积累与本研究中观察到的COPD患者肺pDCs中CXCR3表达增加以及最近发表的COPD患者中CXCR3滤泡表达增加的观察结果是一致的22.
相比之下,我们发现从不吸烟者和不受气流限制的吸烟者之间的pDC数没有差异。这些结果与急性烟雾暴露后BAL液的结果一致28并指出吸烟本身并不影响呼吸道和淋巴滤泡中pDCs的数量。
由于未成熟的pDCs存在于肺粘膜区域,它们可以直接受到香烟烟雾的影响。因此,我们将pDCs与CSE一起孵育,模拟主蒸汽烟雾暴露。当使用TLR-9激动剂CpG寡核苷酸或TLR-7激动剂咪喹莫特模仿病毒感染时,这导致了这些细胞钝化成熟反应。这些发现与之前发表的cse暴露的mdc成熟受损的观察结果一致23.
此外,我们发现,在成熟过程中,CSE降低了TLR-9刺激的pDCs的干扰素-α反应,从而改变了细胞因子的产生。这种迟钝的干扰素-α反应既存在于健康受试者的pDCs中,也存在于COPD患者的pDCs中。这一发现很重要,因为干扰素-α的产生是pDCs的基本固有特征,也是早期抗病毒防御的基石。i型干扰素反应迟钝,再加上吸烟导致的pDCs成熟能力受损,可能会增加吸烟者对病毒感染的易感性29以及COPD患者低级别感染的发展,刺激持续的致病性炎症过程30..此外,CSE诱导健康受试者成熟pDCs中IL-8的产生增加,这可能导致吸烟者中性粒细胞流入增加。与健康受试者相比,COPD患者成熟pDCs中IL-8和TNF-α的产生显著增加。在IL-8的情况下,CSE不能进一步增加IL-8的产生,而CSE降低了COPD患者pDC中TNF-α的产生。随着COPD中pDCs成熟状态的增加17,这种由pDCs促进TNF-α和IL-8的产生也可能存在在活的有机体内,参与COPD的炎症过程。
重要的是,我们的在体外数据证实并扩展了最近公布的数据在体外研究Mortazet al。31在CpG刺激的CSE暴露健康受试者的pDC中,显示了受损的干扰素-α反应和增加的IL-8产生。
轻、中度COPD患者淋巴滤泡中pdc积累的确切作用尚不清楚。人们可以推测,这种pDCs数量的增加反映了这些细胞作为一种补偿机制的涌入,试图抑制COPD中增强的免疫反应,因为pDCs以其致耐受性特性而闻名。因此,最近发表的一篇文章显示,与吸烟者和非吸烟者相比,中度COPD患者的淋巴滤泡中存在调节性CD4+Foxp3+ t细胞的积累32.pDCs还可能在淋巴样新生和肺三级淋巴样结构的稳态中发挥重要作用33,34.Tsoumakidou认为,除了pDCs流入增加外,COPD中DC成熟过程减少et al。19,可能导致COPD患者淋巴滤泡中未成熟bdca -2阳性DCs的积累。
重要的是,在COPD最严重的阶段,bdca -2阳性DCs的数量与没有气流限制的个体相同。这可能反映了在慢性低级别病毒感染中常见的pDCs的相对耗竭35.Freeman建议,重症COPD中pDCs的成熟反应增加et al。17,也可以解释bdca -2阳性pDCs数量较低的原因。最后,在本研究中,重度和非常重度COPD患者使用吸入性和全身性糖皮质激素可能有助于减少pDCs的数量,因为这些药物已知会诱导循环和组织驻留pDCs的凋亡36- - - - - -39.使用吸入性类固醇治疗的非常严重的COPD患者淋巴滤泡中pDCs的减少可能与观察到的COPD患者肺炎风险增加和吸入性皮质类固醇使用之间的关联有关40.
pDC数量的减少可能导致一种“耐受性丧失”的状态,这可能与调节性t细胞数量的下降和COPD最严重阶段的自身免疫过程的发生有关41.此外,肺部中mdc和pdc之间的失衡可能会导致炎症控制脱轨。事实上,在COPD GOLD I期,我们观察到在整个气道壁上朗格蛋白阳性的mDCs数量和pDCs数量之间存在显著的正相关。然而,这种正相关在COPD GOLD III-IV期完全消失。这表明langrin阳性的mDCs(积聚在COPD患者的小气道并刺激T-helper 1和T-helper 17反应)在致耐受性pDC中占主导20..
有几个方面加强了本研究。免疫组化研究首次使用特定的pDC标记物研究了大人群肺中pDC的数量,涵盖了COPD的不同严重程度,并将其与没有气流限制的个体进行了比较。描述性的定量体外数据补充了在体外功能测试,突出CSE对pDC功能的影响。
然而,有几个限制需要解决。首先,用于免疫组化和流式细胞术研究的组织样本主要来自于肺肿瘤手术患者。理论上,这种肿瘤可以影响pDCs的数量和表型。然而,组织样本是在距离病变最大的地方获得的,这将其影响降到最低。
其次,小气道和滤泡中pDCs的免疫组化染色显示这些细胞数量相当低。这可能会对检测研究组间pDC数量差异的敏感性产生影响。然而,免疫组化研究的数据是通过流式细胞术对独立人群中的pDCs进行定量证实的。此外,我们的数据与Freeman最近对肺消化物的流式细胞术研究一致等17,在中度COPD患者中显示出较高的pDC数量的趋势。
最后,在体外CSE实验只研究了烟雾对pDC的直接影响。然而,香烟烟雾的间接作用(通过暴露在烟雾中的上皮细胞、炎症细胞和结构细胞释放的介质)可以极大地影响这些抗原提呈细胞的功能。
结论
吸烟不会影响人体肺部的pDCs数量。然而,CSE改变了pDCs的功能,导致抗病毒防御机制受损。这一观察结果直接将pDC功能与吸烟者对病毒感染的易感性增加联系起来。
健康受试者和COPD患者的小气道中存在pDCs。在COPD中,成熟的pDCs可产生更高水平的TNF-α和IL-8,有助于增强中性粒细胞内流和COPD患者肺部巨噬细胞的激活。
最后,肺pDCs通过淋巴归巢趋化因子受体CXCR3的增强表达,在轻、中度COPD患者的淋巴滤泡中显著积累。然而,在COPD最严重的阶段,pDCs的数量会减少,这可能与COPD终末期适应性免疫反应控制受损和耐受能力丧失相一致。
致谢
作者感谢A. Neesen(根特大学医院呼吸内科,根特,比利时),I. De Borle(根特大学医院呼吸内科),K. De Saedeleer(根特大学医院呼吸内科),E. Castrique(根特大学医院呼吸内科),A. Goethals(根特大学医院呼吸内科),E.J.J. Vulto-De Groot(阿姆斯特丹学术医学中心耳鼻咽喉科),E.J. van der Toom(学术医学中心耳鼻咽喉科),D. van Egmond(学术医学中心耳鼻咽喉科),S. Verschraegen(根特大学医院呼吸内科)和L. Raman(根特大学医院呼吸内科)对这项工作的技术贡献。作者还想感谢M. Hamels(根特大学医院内科)仔细阅读了手稿,D. Testelmans(比利时鲁汶加斯修斯堡大学医院呼吸内科),J Vernooy(营养,马斯特里赫特大学呼吸内科,马斯特里赫特,马斯特里赫特,比利时)M Dentener (Nutrim, department of Respiratory Medicine, University of Maastricht, Maastricht, Netherlands)提供GOLD IV期患者的患者特征。作者要感谢根特大学医院呼吸内科H. Middendorp、F. Vandewalle和T. Verstraete在数据管理方面的支持。
脚注
这篇文章有补充资料可从www.www.qdcxjkg.com
支持声明
本研究得到了佛兰德斯科学研究基金(FWO Vlaanderen,研究项目G.0011.03和G0343.01N)、根特大学协同研究计划项目(01G01009)和比利时大学间吸引极项目(IUAP) -比利时科学政策P6/35的资助。范波特尔伯格(G.R. Van Pottelberge)是弗兰德斯科学研究基金的博士研究员。k·r·布拉克是弗兰德斯科学研究基金的博士后研究员。
感兴趣的语句
凡·波特尔伯格和布鲁塞尔感兴趣的声明可在www.www.qdcxjkg.com/misc/statements.dtl
- 收到了2009年9月4日。
- 接受2010年3月3日。
- ©2010人队