文摘
内皮细胞功能障碍和microcirculatory功能受损明显COVID-19威胁生命的并发症,如静脉血栓栓塞疾病和多种器官参与https://bit.ly/3cZMjKV
冠状病毒疾病2019 (COVID-19)代表一个带有普遍性的公共卫生危机。造成的严重急性呼吸系统综合症冠状病毒2 (SARS-CoV-2),报告的最常见的症状包括咳嗽、发烧和呼吸短促,但肺外症状也可能存在,神经系统和胃肠病等表现。
疾病的发病机理主要取决于冠状病毒的进入和行动的机制。直到2003年,两种类型的冠状病毒表面受体是已知的。我组冠状病毒,例如人类冠状病毒229 e和病毒引起传染性胃肠炎和猫传染性腹膜炎,需要锌metallo-protease氨基肽酶N (APN CD13)进入他们的靶细胞1,2]。第二组冠状病毒鼠肝炎病毒(MHV)使用受体的免疫球蛋白超家族的成员,如鼠癌胚antigen-related细胞粘附分子(CEACAMs) [3]。l我et al。(4)发现了一个不同的冠状病毒的病原学的代理2003严重急性呼吸系统综合症(SARS),使用表面糖蛋白的SARS-CoV-1称为峰值(S)访问宿主细胞。有趣的是,SARS-CoV-2 SARS-CoV-1密切相关,这是表明,蛋白质的冠状病毒需要与细胞受体结合调解感染的靶细胞(5]。李和同事能够表明metallopeptidase(血管紧张素转换酶2;ACE-2) [6),隔绝SARS-CoV-permissive州立E6细胞(非洲绿猴肾细胞线),可以有效地结合冠年代S1域蛋白质和功能性受体为冠状病毒条目。最近,ACE-2已经证明人类干扰素刺激基因,这表明SARS-CoV-2可能利用特有的interferon-driven upregulation ACE-2, tissue-protective中介在肺损伤,提高感染(7]。
疾病的发病机理也取决于冠状病毒受体作为应变的本地化。如图所示,H我et al。(8],ACE-2大量出现在人类的肺和小肠上皮细胞,细胞接触外部环境,这可能提供了可能的途径SARS-CoV-2条目。这个上皮表达提供了一个理解的第一步主要SARS疾病的发病机理表现,特别是在肺(咳嗽、肺炎和严重急性呼吸系统综合症)。I型和II型pneumocytes ACE-2明显阳性,表明肺泡pneumocytes是冠的可能的入口网站。病毒进入可能会导致cytopathological变化在上皮alveolo-capillary界面,最初导致诱导II型肺泡细胞作为首次尝试修复。在非典,丰富表达ACE-2 II型肺泡细胞可能导致病毒迅速扩张和地方肺泡壁破坏,导致迅速进步的严重的弥漫性肺泡损伤和hyperinflammation称为细胞因子风暴综合症(9]。此外,它已经表明,氧化应激引起SARS-CoV-2会加剧DNA甲基化缺陷,可能导致进一步的ACE2脱甲基作用和增强病毒血症(10]。肺部氧化应激时的抗氧化能力是不知所措或耗尽外部风险,如改变氧张力或空气污染,或内部居民细胞和炎症细胞的活化招募曝光,受伤或感染(11,12]。有趣的是,bouhashemet al。(13]最近表明,通过单个细胞RNA序列数据的人类肺,抗氧化防御系统的特定组件的肺泡II型细胞,如超氧化物歧化酶3和激活转录因子4,内质网压力传感器,削弱在应对老龄化老年捐助者。这些结果可以在一定程度上有助于COVID-19观察到严重的老人。
冠的其他目标免疫器官和全身小血管,导致系统性血管炎和免疫功能下降。其他受体/主持人在人类细胞的表面已经提出调解SARS-CoV-2的条目,包括跨膜丝氨酸蛋白酶2 (14),唾液酸(15)和细胞外基质金属蛋白酶诱导物(CD147,也称为遗传性)(16]。
ACE-2,有趣的是,还有其他三个主持人,存在于动脉和静脉的内皮细胞和动脉平滑肌细胞8]。ACE-2是这些受体的研究最多/协调员和使用最近质疑肾素血管紧张素醛固酮系统抑制剂,如血管紧张素ⅱ受体拮抗剂(ARB)和血管紧张素转换酶抑制剂,为COVID-19高血压患者(17- - - - - -23]。特别是,一个潜在的数据之间的联系使用血管紧张素转换酶抑制剂或arb和发展中SARS-CoV-2冲突的风险。最近,两个截然不同的研究已经证明,在大群病人,没有证据表明风险增加的COVID-19由于ACE抑制剂或ARB治疗(23,24]。感兴趣的,它也表明,在细胞因子白细胞介素- 6产生风暴综合症也可以通过盐皮质激素引起的血管紧张素ⅱreceptor-dependent机制(25,26]。
ACE-2的表达于内皮细胞,平滑肌细胞和血管周的周几乎所有器官SARS-CoV-2表明,一旦出现在循环,可以很容易通过人体传播(8]。有趣的是,在最近的一份工作比较事后剖析从病人死于COVID-19肺组织,急性呼吸窘迫综合征由于甲型流感(H1N1)感染和年龄,肺部感染控制,作者发现更多的ACE-2-positive内皮细胞内皮形态学和重大变化与细胞间连接的破坏,细胞肿胀,失去与基底膜(27]。
增加临床证据显示COVID-19患者最常见的并发症观察,与预后差相关死亡的和更高的利率,是系统性高血压、糖尿病和肥胖,内皮功能障碍(28是一个关键因素。在这个问题的欧洲呼吸杂志,两个研究快报强调深静脉血栓形成的风险和急性肺栓塞在COVID-19 [29日,30.]。这些数据确认和扩展以前的观测支持底层SARS-CoV-2-related内皮功能障碍与静脉血栓栓塞疾病的风险增加,系统性血管炎,血管内皮细胞凋亡和炎症在不同器官(31日- - - - - -34]。它也知道,像其他传染性微生物,SARS-CoV-2可以通过炎症反应激活凝血障碍。发现血小板致密颗粒含有聚磷酸盐和分泌在激活导致识别广泛的免疫系统之间的联系和凝血级联(35]。聚磷酸盐释放激活血小板加速因子V活化,抑制组织因子途径抑制剂的抗凝活性,促进系数ξ由凝血酶活化,导致合成抗纤维蛋白溶解的厚纤维蛋白链(36]。炎性细胞因子的影响也导致与合成凝血激活血管内皮细胞和内皮损伤特性。血管内皮损伤引起的血小板减少,也减少天然抗凝血剂,止血剂激活血栓性弥漫性血管内凝血的表型表达。在COVID-19-associated凝血病(37),激活凝血机制SARS-CoV-2感染仍未知但似乎与炎症反应而不是特定属性的病毒(38]。
K洛克et al。(39)最近公布COVID-19血栓性并发症的发生率31%患者在重症监护室。G小河et al。(40)发现,23%的COVID-19肺炎有急性肺栓塞患者检测到计算tomography-pulmonary血管造影术。此外,急性肺部水肿可以观察到在关键COVID-19闭塞患者和micro-thrombosis肺小血管的41]。其他研究人员提出,血栓会直接和重要作用气体交换异常和多系统器官功能障碍在COVID-19肺炎42]。此外,一些作者指出假定antiphospholipid抗体在[COVID-19-related血栓事件中的作用43- - - - - -45]。到目前为止,它仍然是有争议的这些抗体的存在是否应该被用作证据COVID-19患者的早期抗凝,知道antiphospholipid抗体在普通人群中很常见,尤其是在感染(46]。
Gattinoniet al。(47)强调,COVID-19急性呼吸窘迫综合征患者的特点是相对保存完好的肺力学之间的分离和严重的低氧血。这些作者提出这样的严重低氧血发生在兼容的肺可能是由于肺灌注监管和缺氧性血管收缩的损失。这让人想起减毒缺氧性肺血管收缩导致肺动脉内皮细胞功能障碍引起的线粒体氧化应激增加dasatinib-exposed啮齿动物(48]。最后,它已经表明,SARS-CoV-2元素可以检测到COVID-19患者内皮细胞,炎症细胞的积累和内皮细胞和炎症细胞死亡的证据(49]。这表明可以促进endotheliitis SARS-CoV-2感染和诱导在不同器官的直接后果病毒感染和宿主炎性反应。与此一致的是,ckermannet al。(27]发现,除了弥漫性肺泡损伤血管周的t细胞浸润和广泛血栓形成微血管病,独特的血管功能COVID-19患者由严重的内皮损伤与细胞内病毒的存在和破坏细胞膜,以及血管血管生成。
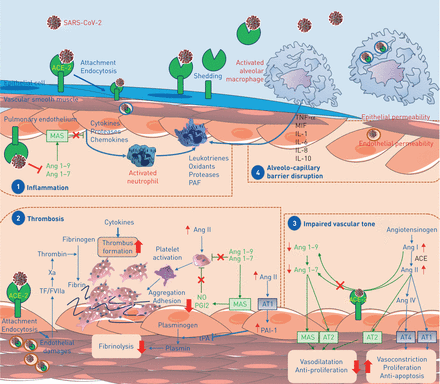
总之,SARS-CoV-2病毒在内皮细胞的存在表明直接病毒影响,以及血管周围炎症,可能导致内皮细胞损伤。很可能endotheliitis、血管内皮损伤、血管内皮细胞功能障碍和microcirculatory功能受损在不同血管床明显有助于COVID-19威胁生命的并发症,如静脉血栓栓塞疾病和多种器官参与(图1)。
小说示意图表示的假设机制严重急性呼吸系统综合症冠状病毒2 (SARS-CoV-2)导致内皮功能障碍和肺血管的变化。分裂后的蛋白质,SARS-CoV-2报道进入人类细胞通过绑定到血管紧张素转换酶2 (ACE-2)。这个跨膜ACE-2受体广泛表达于各种肺细胞包括II型肺泡细胞,巨噬细胞、内皮细胞、平滑肌细胞和血管周的周。这将导致控制炎症(1),伴随着micro-thrombosis和肺小血管闭塞(2)和内皮血管张力调节受损(3),导致alveolo-capillary屏障破坏(4)。Ang:血管紧张素;在:血管紧张素受体;IL:白介素;MAS:巨噬细胞活化综合征;MIF:巨噬细胞迁移抑制因子;没有:一氧化氮;改善:血小板激活因子;PAI-1:纤溶酶原激活物inhibitor-1;PGI2:前列腺素I2; TF: tissue factor; TNF: tumour necrosis factor; tPA: tissue plasminogen activator.
可共享的PDF
脚注
利益冲突:a .韦尔塔没有披露。
利益冲突:d . Montani报告赠款和个人费用从Actelion股价和拜耳,葛兰素史克的个人费用,辉瑞,基耶西和勃林格,资助,个人费用和非金融默沙东公司的支持,从Acceleron非金融支持,在提交工作。
利益冲突:l . Savale报告个人费用和非金融支持Actelion股价和拜耳,赠款和葛兰素史克的个人费用,提交的工作。
利益冲突:j . Pichon没有披露。
利益冲突:l .你没有披露。
利益冲突:f .家长报告从拜耳赠款,CSL贝林和赛诺菲安万特,外提交的工作。
利益冲突:c . Guignabert没有披露。
利益冲突:m·亨伯特报告赠款和个人费用从Actelion股价,拜耳,葛兰素史克和Acceleron,个人费用从默克公司和联合疗法,外提交的工作。
- 收到了2020年5月6日。
- 接受2020年6月8日。
- 版权©2020人队
这个版本分布在创作共用署名非商业性许可证的条款4.0。