文摘
背景COVID-19与特异表达的免疫反应,但目前尚不清楚如何免疫功能紊乱导致的慢性病的发病率持续许多COVID-19患者在康复期(长COVID)。
方法我们评估了单核细胞的表型和功能变化COVID-19病人在住院期间和COVID-19后9个月的恢复期,呼吸道合胞体病毒或流感a进步fibrosing间质性肺病患者作为一个积极的控制严重,持续的肺损伤。
结果单核细胞的改变在急性COVID-19病人包括白细胞游走分子的异常表达,一直持续到恢复期(n = 142)和相应的与特定的长COVID的症状。长COVID悬而未决的肺损伤患者,表示持续的呼吸短促和胸部放射学异常,被定义为高C-X-C图案的单核细胞表达趋化因子受体6 (CXCR6) (p < 0.0001)和粘附分子P-selectin糖蛋白配体1 (p < 0.01),与优惠向CXCR6单核细胞迁移趋化因子配体配位体C-X-C图案16 (CXCL16) (p < 0.05),肺中大量表达。单核细胞CXCR6和肺CXCL16高度进步fibrosing间质性肺疾病患者(p < 0.001),确认CXCR6-CXCL16轴的肺损伤的作用。相反,从长COVID持续疲劳患者单核细胞表现出持续减少prostaglandin-generating酶环氧酶2 (p < 0.01)和CXCR2表达(p < 0.05)。这些单核细胞的变化并不存在于呼吸道合胞体病毒或流感康复期。
结论我们的数据定义独特的长COVID单核细胞签名定义子组病人,表明单核细胞迁移的关键作用COVID-19病理生理学。针对这些途径可以提供小说在COVID-19持续发病率患者治疗的机会。
文摘
免疫功能紊乱是一个关键因素在急性COVID-19病理生理学,单核细胞异常持续在恢复期至少9个月后出院,对应于特定的长COVID症状https://bit.ly/3xEIY0H
介绍
COVID-19大流行导致了全球超过7.62亿人感染,680万人死亡,到目前为止(1]。COVID-19表现各种各样的症状,从轻微的流感样症状,急性呼吸窘迫综合征的致命后果严重疾病(2 gydF4y2Ba]。有显著改善我们的理解COVID-19病理学的研究工作详细的变化在SARS-CoV-2感染宿主免疫力,与关键改变髓细胞的先天免疫系统的疾病严重程度、重症监护住院和死亡的发生率[3- - - - - -9]。
单核细胞从骨髓中释放到循环和招募肺呼吸道感染期间,按照我们以前的工作证明系统性水平升高monocyte-chemoattractant蛋白1 (MCP-1) COVID-19病人和增强Ki67从骨髓单核细胞的快速释放3]。其他早期的研究在第一波COVID-19证明增强单核细胞浸润在肺部,肾脏,心脏,脾脏和肌肉从已故COVID-19病人10- - - - - -12),支持角色COVID-19异常单核细胞迁移到周围组织。事实上,后来的研究表明严重COVID-19-associated变异都与单核细胞和巨噬细胞趋化因子受体基因控制13]。单核细胞的迁移特性的详细了解COVID-19以及他们如何与疾病严重程度和重症监护承认将支持更好的发展,有针对性的临床干预措施。
现在有大量的证据表明慢性病发病率持续在许多COVID-19患者在康复期,与常见的持久的症状包括极度疲乏、气短、肌痛、脑雾、抑郁、纤维化肺病和肺血管疾病(长COVID) [14- - - - - -18]。最近的证据表明系统性炎症持续COVID-19恢复期,剩下长COVID症状在1年随访17)和长期的激活先天免疫系统在康复期患者即使在不重的疾病(19]。目前治疗方法有限长COVID因为靶向治疗策略的发展需要一个深入了解潜在的免疫病理生理学。
我们试图解决单核细胞迁徙的签名是否与急性COVID-19疾病严重程度和是否持久免疫档案在康复期的变化与长COVID相关症状。我们收集血液样本作为冠状病毒的免疫反应和临床结果的一部分(圆环)研究[3英国大曼彻斯特)在四医院,和识别关键单核细胞迁徙签名在急性疾病,坚持为康复期出院后9个月。独特的单核细胞概要杰出长COVID气短和解决患者的肺损伤与持续疲劳,和从无症状患者。我们的数据显示持续的单核细胞功能障碍的急性和长期COVID作为一个关键特性。
方法
研究设计
2020年7月至2021年1月,两群COVID-19患者(急性和康复的)是从四医院招募两个信托:曼彻斯特大学NHS信托基金会(MFT)和索尔福德皇家NHS信托基金会(SRFT)。样本收集通过曼彻斯特过敏、呼吸和胸手术(ManARTS)生物(研究号码m2020 - 88;MFT)或保健北部联盟研究集合(NCARC)组织生物(研究号码nca - 009;SRFT)。伦理批准由国家研究伦理提供了服务(REC ManARTS参考15 /西北/ 0409;NCARC 18 / WA / 0368)。知情同意是由所有参与者提供。
病人纳入和排除标准是一样的在我们之前的研究3];人口统计学和临床信息提供的补充材料(补充数据S1和S3)。外周血样本收集7天内急性住院的病人,并在门诊复诊3 - 9个月出院后康复的病人。健康血液样本来自曼彻斯特大学的一线工人和管辖,并检查与患者样本。所有健康对照组anti-Spike 1受体结合域抗体检测呈阴性(年龄35 - 71岁,平均年龄50.9岁,52%的男性)。
定量计算机断层扫描分析
胸腔计算机断层扫描(CT)扫描图像从症状康复的COVID-19病人(上气不接下气和/或疲劳)建议在后续任命(ManARTS研究数量m2022 - 119)进行了分析使用肺密度分析和肺纹理分析程序(Imbio Inc .,明尼阿波利斯,美国)生成定量CT报告。这个生成量化扫描报告所示补充图S5。进一步的信息在这个技术可以找到Imbio LDA +用户手册版本4.1.0和肺纹理分析用户手册版本2.2.0 (https://www.imbio.com/support-documentation/)。
分离外周血单核细胞和血清
外周血单核细胞(PBMCs)从全血和血清样本孤立如前所述[3]。PBMCs染色流式细胞术,建立微生物刺激化验,或者存储在DMSO溶液10%胎牛血清(的边后卫)−150°C。
细胞培养
新鲜PBMCs刺激100 ng·毫升−1脂多糖(LPS)(σ)的蛋白质运输抑制剂鸡尾酒(eBioscience) RPMI包含10%的边后卫,谷酰胺,不必要的氨基酸,玫瑰,链霉素和青霉素(完整的媒体)对3 h在37°C。刺激后,细胞被洗和彩色流仪分析来确定细胞内浓度的过氧化氢酶环氧酶2 (cox - 2)和细胞因子肿瘤坏死因子α(TNF-α)和白介素- 1β(IL-1β)。
Transwell迁移分析
冷冻PBMCs健康对照组和气喘吁吁,non-breathless恢复期的COVID-19患者解冻,洗和resuspended完整的媒体。PBMCs孵化在37°C 18 h。PBMCs (2×105细胞)被镀上井的98孔细胞迁移/趋化性板Boyden室(5µm膜;Abcam)。较低的井中C-X-C主题趋化因子配体16 (CXCL16)(0.1、0.5或1µg·毫升−1)或媒体只有(负控制)。PBMCs离开迁移4 h在37°C。使用一个血球计手动迁移的细胞数。
流式细胞术
表面污渍(迁移标记),样本固定与BD Cytofix (BD生物科学)抗体染色后,之前的收购。细胞内的污渍(TNF-αIL-1β,cox - 2), FoxP3 /转录因子染色缓冲区设置(eBioscience)使用。列出使用的抗体补充表S1。所有样品都获得一个LSRFortessa流式细胞分析仪(BD生物科学)和分析使用FlowJo恒星(树)。
Luminex化验
白细胞游走标记测定血清中使用Luminex化验(研发系统)根据制造商的指示。
统计数据
正常测试进行所有的数据集,并使用棱镜进行统计分析软件(Graphpad软件Inc .) 9。统计测试详细信息如图传说。在所有情况下,假定值≤0.05被认为是显著的。无统计差异显示在图表,没有显著差异。
结果
在急性COVID-19临床特点
7月6日至2020年11月5日,71例急性疾病患者住院期间招募停留7天内COVID-19入学。所有患者分层最大疾病严重程度的基础上补充氧气需求(吸入氧气分数< 28% (FiO2 gydF4y2Ba)轻微的疾病,28 - 60%FiO2 gydF4y2Ba温和的疾病和> 60%FiO2 gydF4y2Ba严重疾病或非侵入式/机械通风)。此外,急性无创通气的使用在非慢性阻塞性肺病(COPD)患者中,入侵通风和进入重症监护自动导致严重疾病的一个分类。最常见的并发症是高血压、缺血性心脏病、糖尿病、哮喘和其他慢性肺病,尽管只有糖尿病与疾病严重程度(严重COVID-19是糖尿病患者的55%)。严重病例的45% COVID-19导致30天内死亡,30天死亡率、c反应蛋白和住院时间与COVID-19疾病严重程度呈正相关(补充图S1)。
迁徙的签名在急性单核细胞异常COVID-19定义疾病严重程度
招聘网站后炎症,单核细胞对炎性疾病直接或作出了重大贡献通过分化成巨噬细胞和树突细胞在外围组织20.,21]。Monocyte-derived巨噬细胞主要集中在支气管肺泡灌洗(BAL)患者的严重COVID-19 [8 gydF4y2Ba),导致炎症的环境。我们检查了循环单核细胞表达改变的一系列分子参与白细胞游走,根据他们的能力和功能产生炎症介质(总结补充图S2a)。
通过结合这些微分分析,我们生成的概述severity-specific单核细胞签名(图1)。严重COVID-19被减少比例的CD14的特征+古典单核细胞(控制策略:补充图开通cox - 2)表达prostaglandin-generating酶和趋化因子受体C-X-C主题趋化因子受体2 (CXCR2) (图1和2、b)与增强表达粘附分子CD62L (图1和2摄氏度)和gut-homing整合素β7 (Itg-β7)(图1和二维)。轻微的疾病,患者更快康复COVID-19显示一个独特的签名和TNF-α的特点是提高生产(图1和2 e)和增强的趋化因子受体的表达主题趋化因子受体8 (CCR8)单核细胞(图1和2 f)。趋化因子受体CXCR6,粘附分子P-selectin糖蛋白ligand-1 (PSGL-1)和趋化因子主题趋化因子配体2 (CCL2)对单核细胞异常增加COVID-19患者整体但没有分层与疾病严重程度(图1和2 g,补充图S2c)。
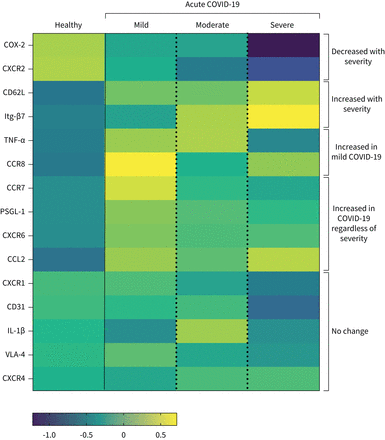
总结不同的单核细胞在急性COVID-19患者。热图显示免疫参数的行。每一列表示平均(平均)z得分为每个参数计算从单核细胞表达个人价值观的健康个体或轻度患者,中度或重度COVID-19作为单独的组。热图生成视觉引导,用个人的一个子集从每组每组包括所有个人为每个免疫参数分析结果(即。个人在样本用于所有迁移分子表面染色,和微生物刺激细胞因子和cox - 2读数的分析)。健康个体,n = 25;轻度COVID-19, n = 13;温和COVID-19 n = 14;严重的COVID-19, n = 7。
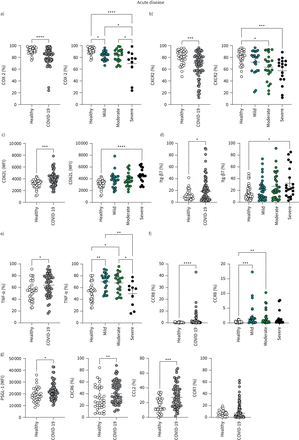
单核细胞急性COVID-19患者的资料。总结图表显示数据从健康的个人和所有COVID-19患者。患者COVID-19也分为轻微、中等和严重疾病组。CD14的)频率+单核细胞表达cox - 2在脂多糖(LPS)刺激,从健康人(n = 32),所有患者急性COVID-19 (n = 56)。疾病分层:轻度(n = 23)、中度(n = 20)和严重(n = 10)。b) CD14的频率+单核细胞表达CXCR2从健康人(n = 34),所有患者急性COVID-19 (n = 66)。疾病分层:轻度(n = 22)、中度(n = 23)和严重(n = 17)。c) CD14+单核细胞L-selectin (CD62L)表达水平取决于平均荧光强度(MFI)在健康个体(n = 33),所有患者急性COVID-19 (n = 65)。疾病分层:轻度(n = 22)、中度(n = 22)和严重(n = 17)。d) CD14的频率+单核细胞整合素表达β7 (Itg-β7)健康人(n = 35),所有患者急性COVID-19 (n = 67)。疾病分层:轻度(n = 23)、中度(n = 23)和严重(n = 16)。e) CD14的频率+单核细胞生产TNF-αLPS刺激后,从健康人(n = 34),所有患者急性COVID-19 (n = 55)。疾病分层:轻度(n = 23)、中度(n = 20)和严重(n = 10)。f) CD14的频率+单核细胞表达CCR8从健康人(n = 33),所有患者急性COVID-19 (n = 66)。疾病分层:轻度(n = 22)、中度(n = 23)和严重(n = 17)。g) CD14+单核细胞表达水平PSGL-1和频率的单核细胞表达CXCR6 CCL2, CCR7在健康个体(PSGL-1: n = 35;CXCR6: n = 35;CCL2: n = 33;CCR7: n = 31),所有患者急性COVID-19 (PSGL-1: n = 66;CXCR6: n = 60;CCL2: n = 57;CCR7: n = 66)。图表显示个别病人数据栏代表的意思是±扫描电镜(a, c, e)或中位数±四分位范围(b, d, f, g)。使用未配对t组进行了比较- - - - - -测试(a, c, e:健康与COVID-19), Mann-Whitney测试(b, d, f, g:健康与与Holm-Sidak COVID-19)、单向方差分析事后测试(a, c, e: COVID-19严重程度)或与Dunn的克鲁斯卡尔-沃利斯事后测试(b, d, f: COVID-19严重性)。*:p≤0.05;* *:p≤0.01;* * *:p≤0.001;* * * *:p≤0.0001。
有一个趋势的比例增加单核细胞趋化因子受体表达与淋巴结归航,CCR7在急性COVID-19但这尚不具备统计学意义(图2 g)。单核细胞趋化因子受体的表达没有改变CXCR1或整合素很晚antigen-4 (VLA-4)(用于粘附激活内皮(22,23COVID-19患者和健康对照组之间的])(补充图S2d)。CD31水平(用于通过内皮细胞迁移24])和单核细胞趋化因子受体CXCR4比例进行评估,而不是由于循环单核细胞表达这些分子的100%;COVID-19患者和健康对照组之间没有差异。也没有区别IL-1β单核细胞生产(补充图S2d)。
这些数据显示异常单核细胞迁移COVID-19病理生理学作为一个关键因素。
定义可溶性介质参与白细胞游走在急性COVID-19特异表达
我们和其他人以前观察到的异常表达可溶从急性COVID-19患者血清中炎症介质,特别是细胞因子il - 6和il - 10和趋化因子MCP-1 CXCL10,占主导地位的严重COVID-19 [2 gydF4y2Ba,3,25- - - - - -27]。这里,我们扩展我们的血清蛋白质的分析使用一系列Luminex珠针对白细胞迁移。
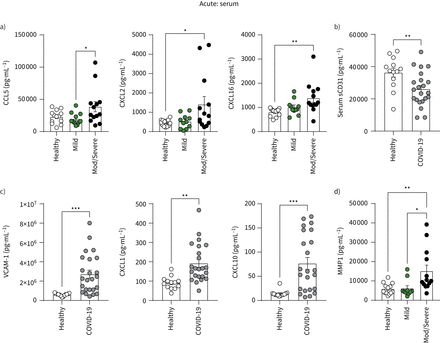
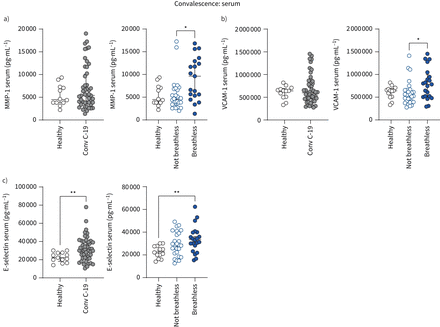
血清趋化因子CCL5水平(招募白细胞炎症的网站),CXCL2(骨髓细胞化学引诱物)和CXCL16(绑定伙伴CXCR6 COVID-19单核细胞的增加图2 g)增加患者急性中度/重度COVID-19 (图3一)。可溶性CD31,抑制CD31-mediated transendothelial迁移(28],减少COVID-19患者,进一步支持作用提高白细胞游走在COVID-19周组织(图3 b)。粘附分子血管粘附分子1 (VCAM-1)和趋化因子处于受控和CXCL10也升高(图3 c),但并没有与疾病严重程度分层(数据没有显示)。血清水平的矩阵metalloprotease(金属蛋白酶- 1)介导单核细胞和血管内皮细胞之间的相互作用(29日),也加剧了中度/重度患者COVID-19 (图3 d)。
血清急性COVID-19患者的资料。水平的系统性CCL5, CXCL2, CXCL16;b)可溶性CD31 (sCD31);c) VCAM-1,处于受控,CXCL10;和d)测量金属蛋白酶- 1在健康人的血清(n = 13)和COVID-19患者使用Luminex化验(n = 24)。a, d)患者COVID-19也分为轻度(n = 11)和中度/重度疾病(n = 13)。图表显示数据与酒吧代表的意思是±个别病人扫描电镜。使用未配对t组进行了比较- - - - - -测试(b, c:健康与与Holm-Sidak COVID-19)或单向方差分析事后测试(a, d: COVID-19严重性)。*:p≤0.05;* *:p≤0.01;* * *:p≤0.001。
这些数据进一步支持作用异常白细胞游走在COVID-19外围组织,显示不正常的血管内皮细胞与单核细胞的相互作用,。
在COVID-19康复临床特点
与招募患者急性COVID-19, 7月14日至2020年12月3日,142名患者参加住院病人入院后门诊随访COVID-19被招募为康复的COVID-19病人(后续的意思是:151天;范围:放电后63 - 246天)。在门诊复查患者问他们是否出现呼吸困难或疲劳,以及是否这是SARS-CoV-2以来新的感染。如果已存在的症状,病人被要求如果是更好的,稳定的或者更糟因为SARS-CoV-2(量化使用医学研究理事会呼吸急促呼吸困难量表)。进一步的临床试验,如。睡眠研究和血板,超声心动图是由评审专家呼吸医师表示,气短和疲劳排除其他疾病。如果在评估病人的症状被认为是由于其他疾病,他们被排除在分析之外。
在门诊随访,31%的患者继续在胸部放射学归因于COVID-19(显示异常补充图S3)。气短长COVID是最常见的症状,指出解决肺损伤(48%的康复的病人;补充图S3)。在这里,我们使用的组合异常胸部放射学与气短确认未解决的肺损伤,实际上这两个参数之间有显著关系(补充图S3)。长期的疲劳也是一个主要症状COVID(44%的康复的病人;补充图S3)。批判性、气短和疲劳恢复期并不对应于最初的急性住院期间疾病严重程度;因此,在这一群人,COVID-19严重程度没有解释坚持在恢复期症状。这个信息是非常重要的考虑的长COVID剩下的世界范围的一个主要公共卫生问题在刚出版的时候,尽管温和SARS-CoV-2和疫苗接种菌株的出现导致严重疾病和住院治疗的风险降低。
有一般所有肺功能参数以减少康复的COVID-19患者总体而言,与预测值(30.健康人群的)(补充图S4)。减少用力肺活量(FVC)、用力呼气量在1 s (FEV1)和扩散能力的肺一氧化碳(DLCO)相比,健康人群(%)预测预计由于COVID-19与住院治疗相关并发症。例如,高体重指数可能减少肺容积(FVC)和哮喘可能影响气流(FEV1),而慢性阻塞性肺病和肺气肿会影响肺泡毛细血管膜和肺泡体积(DLCO)。
FEV气喘吁吁恢复期的患者低1比non-breathless恢复期的病人,这可能表明患者在这个集团正在经历更大的气流阻塞继发于炎症后SARS-CoV-2感染(补充图S4)。小的减少DLCO病人在恢复期的COVID-19表明能力降低运输氧气从肺部进入血液循环。有一个强大的趋势更大的减少DLCO(%)预测患者的持续异常的放射学在随访(补充图S4),这可能是由于持续肺损伤的贡献。本研究没有足够的动力去探索肺功能指标之间的关系。因此,未知是否FEV1和DLCO结果代表的是单一的或独立的呼吸困难的机制。气喘吁吁的高放射性异常患病率(44.4%)和疲劳(38.2%)相比,无症状(25.2%)患者(补充图S3)也暗示正在进行的肺损伤或不完整导致长COVID修复。实际上,最近的证据表明炎症介质的组织损伤和修复在等离子体与长COVID症状的严重程度(17]。
其他的研究也表明增强检测肺异常COVID-19使用非标准的成像技术,如。hyperpolarised氙- 129核磁共振成像(31日]。评估是否我们可能错过了使用传统放射学方法进行肺部异常,我们进行了定量CT分析使用肺密度分析和肺纹理分析程序(Imbio Inc .)生成定量CT报告症状的一个子集的肺康复的COVID-19患者显示正在进行的呼吸困难和/或疲劳的症状在随访(补充图S5)。在矢状面CT扫描生成和评估,日冕和横向飞机之前满意的扫描质量分割和肺的映射(补充图S5a)。这个自动化的计算机分析肺纹理的提供详细的信息关于不同类型的肺损伤,如hyperlucency磨砂玻璃变化,网状和蜂窝(补充图S5b)。这个分析也提供了详细的信息关于肺损伤肺密度的分析,与高密度代表炎症和磨砂玻璃和非常高的密度变化代表致密区域的炎症或感染(补充图S5c)。
这种方法虽然是以前未在COVID-19恢复期,它有预测价值的严重程度和结果在急性COVID-19 [32]。只有62.5%的COVID-19恢复期的病人表现出异常放射性的发现使用标准测试(补充图S6a),但定量CT分析发现肺部异常在所有这些评估患者症状,最常见的异常是磨砂玻璃的变化和网状物(补充图S6b),它通常与炎症过程有关。这些结果表明,持续的肺损伤可能发生在大多数症状COVID-19病人在恢复期。我们下一个评估先天免疫功能障碍是否与持续的肺损伤和长COVID的症状。
异常的单核细胞迁徙概要坚持COVID-19长COVID恢复期和对应的症状
单核细胞的机制可能参与恶化与解决肺损伤尚不清楚,尽管发展的关键作用的单核细胞肺纤维化引起的肺损伤的失败的决议(33]。的确,pro-fibrotic monocyte-derived巨噬细胞积聚在患者的肺部严重COVID-19具有相同特征的特发性肺纤维化患者(34]。在这里,我们专注于呼吸急促和胸部放射学异常表明解决肺损伤并调查是否持续单核细胞失调对应解决肺损伤,COVID长。
已经表明,单核细胞趋化因子受体的表达CXCR6和粘附分子在急性COVID-19 PSGL-1增加,我们在这里展示,这些变化是持续进入康复期,特别是在患者进行呼吸困难的症状。此外,这些分子的表达也异常患者胸部放射学最高(传统评估方法;图4一f)。因此,提高CXCR6和PSGL-1单核细胞在气喘吁吁恢复期的患者可能是由于活跃的单核细胞招聘持续的炎症反应和损伤的肺。的确,CXCR6引向迁移趋化因子CXCL16,表达在肺35),PSGL-1调停拘束和滚动激活内皮促进迁移到组织从血液中36]。
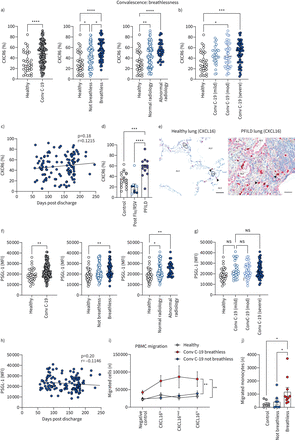
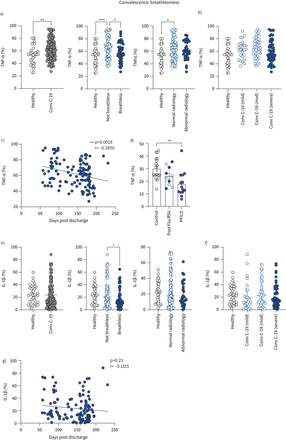
单核细胞迁移的长COVID解决肺损伤患者。CD14的)频率+单核细胞表达CXCR6从健康人(n = 35)和恢复期的COVID-19病人(Conv C-19) (n = 127)。患者康复的COVID-19也分层到了令人窒息的(n = 52),不上气不接下气(n = 71),正常的放射学(n = 91)和放射学异常(n = 33)。b)患者恢复期的COVID-19也分为轻度(n = 28),中等(n = 43)或严重疾病(n = 56)指的是他们之前的住院期间急性COVID-19严重性。c)的相关性CXCR6(单核细胞百分比表达CXCR6)天数自出院康复的所有COVID-19病人(n = 122)。d) CD14的频率+单核细胞表达CXCR6在不同的健康个体(n = 19),恢复期的甲型流感(猪流感)/呼吸道合胞体病毒(RSV)患者(n = 10)和所有进步fibrosing间质性肺病(PFILD)患者(n = 14)。患者恢复期的流感/ RSV分层到喘不过气来的(n = 5,圆圈),而不是气喘吁吁(n = 5,开放圈)在同一组。e)人类肺组织部分。健康的人类肺(左):肺泡与偶尔可以看到CXCL16-expressing免疫细胞(黑色箭头)近端毛细血管(虚线)。正确显示人类特发性肺纤维化肺,细胞外基质代替正常的肺结构。CXCL16-expressing免疫细胞内存在血管(黑色箭头)。CXCL16也是在破坏肺泡上皮细胞和基质细胞。用甲苯胺蓝复染色。酒吧规模:50µm。ALV:肺泡; CAP: capillary. f) CD14+单核细胞表达水平的PSGL-1由平均荧光强度(MFI)健康人(n = 35)和恢复期的COVID-19病人(n = 130)。患者康复的COVID-19也分层到了令人窒息的(n = 54),不上气不接下气(n = 74),正常的放射学(n = 95)和放射学异常(n = 32)。g)患者恢复期的COVID-19也分为轻度(n = 30),中等(n = 43)或严重疾病(n = 57),指的是他们之前的住院期间急性COVID-19严重性。h)的相关性PSGL-1(水平的表达式由MFI)天数自出院康复的所有COVID-19病人(n = 130)。i)的外周血单核细胞迁移(PBMCs)计入Boyden只在媒体室的底部(负控制),0.1µg·毫升−1CXCL16 (CXCL16罗),0.5µg·毫升−1CXCL16 (CXCL16地中海)和1µg·毫升−1CXCL16 (CXCL16嗨)4 h孵化后,从2×105细胞在前室在所有情况下(健康对照组:n = 10;喘不过气来的恢复期的COVID-19: n = 10;没有扣人心弦的疗养COVID-19: n = 10)。图表显示病人数据与均值±相结合扫描电镜每组,每个条件下。j)单核细胞迁移的数量被CD45流式细胞术+住CD19−CD3−CD66b−HLA-DR+CD64+CD14+从迁移的细胞在CXCL16 Boyden室的底部嗨条件(1µg·毫升−1CXCL16)(健康对照组:n = 7;喘不过气来的恢复期的COVID-19: n = 10;没有扣人心弦的疗养COVID-19: n = 8)。以外的所有图c和我展示个别病人数据与酒吧代表值±四分位范围。使用Mann-Whitney测试组进行了比较(a、f:健康与康复的COVID-19),克鲁斯卡尔-沃利斯与邓恩事后测试(a, b, d, f, g, j),斯皮尔曼等级相关系数测试(c、h)或与重复措施和Holm-Sidak单向方差分析事后测试(我)。*:p≤0.05;* *:p≤0.01;* * *:p≤0.001;* * * *:p≤0.0001。
CXCR6表达单核细胞在COVID-19恢复期仍高,特别是在患者急性住院期间严重COVID-19图4 b),但最初的急性疾病严重程度没有影响PSGL-1表达COVID-19恢复期(图4 g)。线性回归分析比较CXCR6和PSGL-1表达与时间(天出院后)透露,康复的COVID-19病人没有减少单核细胞CXCR6表达式回到健康的控制水平在出院后的最长时间研究(9个月;图4 c)。然而,有一个趋势非常PSGL-1水平随时间逐渐下降(图4 h)。
确定增强单核细胞CXCR6表达式出现在恢复期后与其他呼吸道病毒住院治疗,我们评估CXCR6表情单核细胞分离后门诊随访患者住院承认与呼吸道合胞体病毒(RSV)或甲型流感(猪流感)与相应的平均随访时间(COVID-19: 151天;RSV /流感:155天)。所有RSV和流感患者肺炎住院和五10(50%)仍然气喘吁吁在随访(补充图S7,临床特点及肺功能)。年龄组相比,没有明显的差异post-RSV CXCR6 /流感病人单核细胞表达,也有加剧的迹象CXCR6那些仍在后续呼吸急促(图4 d)。作为一个积极的控制未解决的肺损伤,我们评估CXCR6表情从进步fibrosing间质性肺病患者单核细胞(PFILD)有严重持续的肺部炎症和损伤补充图S7)。从PFILD患者单核细胞表达高水平的CXCR6 (图4 d),类似于恢复期的患者COVID-19悬而未决的肺损伤。然而,PSGL-1对单核细胞水平持平后流感/ RSV病人和PFILD患者(补充图S8a)。
进一步审问CXCR6-CXCL16轴在持续的肺损伤,我们CXCR6配体的特征表达CXCL16 PFILD患者的肺组织部分。与结构性破坏和混乱的明确证据,CXCL16水平明显提高PFILD部分相比健康的肺组织,与表达局部PFILD-damaged肺泡上皮细胞和免疫细胞浸润(图4 e)。因此,增强单核细胞CXCR6功能正在进行的肺损伤CXCR6-CXCL16信号特异表达的明确证据。尽管如此,增加单核细胞CXCR6表达式上下文中的呼吸道感染只是COVID-19患者中发现。
接下来,我们确定是否增加单核细胞上表达CXCR6恢复期的患者COVID-19解决肺损伤是功能相关的白细胞迁移能力。为此,我们进行了transwell迁移试验,揭示了迁徙的潜力PBMCs向CXCR6配体CXCL16(表示在肺高水平)。PBMCs从康复的气喘吁吁COVID-19患者演示了一个增强的能力迁移对CXCL16 non-breathless康复的同行相比,健康对照组(图4我)。在流仪分析迁移细胞中的细胞组件CXCL16浓度最高,有增强单核细胞迁移从康复的COVID-19病人喘不过气来的(图4 j)。
这些数据异常强烈暗示单核细胞迁移在长COVID病理,尤其是在那些尚未解决的肺损伤和长COVID最常见的症状,即。呼吸短促。
定义可溶性介质参与白细胞游走在养病的COVID-19特异表达
已经表明,一些可溶性的血清炎症介质增加患者急性COVID-19,我们现在显示两种血清蛋白质,金属蛋白酶- 1(这是参与monocyte-endothelial细胞相互作用)和粘附分子VCAM-1,居高不下的COVID-19恢复期的患者呼吸困难(图5一个b)。此外,在证明PSGL-1增加单核细胞在气喘吁吁恢复期的患者未解决的肺损伤(图4 d),我们发现血清水平的伙伴E-selectin PSGL-1绑定,绑定的PSGL-1促进leukocyte-endothelial交互,增强在气喘吁吁COVID-19恢复期的患者(图5 c)。
患者血清的长COVID悬而未决的肺损伤。水平的系统性金属蛋白酶- 1,b) VCAM-1和c) E-selectin测定血清从健康人(n = 12)和恢复期的COVID-19 (Conv C-19)患者使用Luminex化验(n = 48)。患者康复的COVID-19也分层到喘不过气来的(金属蛋白酶- 1:n = 19;VCAM-1: n = 21;E-selectin: n = 21),而不是气喘吁吁(金属蛋白酶- 1:n = 26;VCAM-1: n = 28;E-selectin: n = 26)。图表显示数据与酒吧代表的意思是±个别病人扫描电镜(c)或中位数±四分位范围(a, b)。使用未配对t组进行了比较- - - - - -测试(c:健康与康复的COVID-19), Mann-Whitney测试(a, b:健康与康复的COVID-19),与Holm-Sidak单向方差分析事后测试(c:呼吸困难)或与Dunn的克鲁斯卡尔-沃利斯事后测试(a, b:呼吸困难)。*:p≤0.05;* *:p≤0.01。
这些数据表明,血清特异表达特定的介质参与白细胞游走在急性COVID-19居高不下COVID-19恢复期长COVID突出他们的角色,特别是在呼吸短促。在一起,到目前为止,这些数据表明,针对白细胞游走和monocyte-endothelial交互可能长COVID的治疗价值。
TNF-α生产由单核细胞坚持COVID-19恢复期和对应解决肺损伤
我们在先前的研究已经证明了第一波COVID-19 TNF-α加剧生产住院期间突出在轻度COVID-19患者康复的很快2 gydF4y2Ba]。复制这个发现在这项研究中(样本期间COVID-19在英国的第二波),我们现在证明提高单核细胞生产TNF-α持续到COVID-19恢复期,又对应于肺损伤方面的好的结果。康复的COVID-19患者持续产生高水平的细胞因子TNF-α异常,尤其是患者没有气短的症状(图6)。符合TNF-α生产解决患者的肺损伤,增加TNF-α显著增加患者的正常胸部放射学在COVID-19恢复期(图6)。TNF-α生产在恢复期单核细胞在急性承认没有最初与疾病严重程度(图6 b),随着时间的推移显著下降,表明一个返回到健康控制水平(图6 c)。
单核细胞因子的患者长COVID-19悬而未决的肺损伤。CD14的)频率+单核细胞生产TNF-α从健康人(n = 33)和恢复期的(Conv C-19) COVID-19病人(n = 122)。患者康复的COVID-19也分层到了令人窒息的(n = 49),不上气不接下气(n = 67),正常的放射学(n = 87)和放射学异常(n = 35)。b)患者恢复期的COVID-19也分为轻度(n = 26),中等(n = 44)或严重的疾病(n = 52),指的是他们之前的住院期间急性COVID-19严重性。c)的相关性TNF-α(单核细胞比例生产TNF-α)天数自出院康复的所有COVID-19病人(n = 117)。d) CD14的频率+单核细胞在不同人群的健康个体生产TNF-α(n = 19),恢复期的甲型流感(猪流感)/呼吸道合胞体病毒(RSV)患者(n = 10)和所有进步fibrosing间质性肺病(PFILD)患者(n = 14)。患者恢复期的流感/ RSV分层到喘不过气来的(n = 5,圆圈),而不是气喘吁吁(n = 5,开放圈)在同一组。e) CD14的频率+单核细胞生产IL-1β从健康人(n = 34)和恢复期的COVID-19病人(n = 122)。患者康复的COVID-19也分层到了令人窒息的(n = 49),不上气不接下气(n = 68),正常的放射学(n = 87)和放射学异常(n = 34)。f)患者恢复期的COVID-19也分为轻度(n = 26),中等(n = 44)或严重疾病(n = 52),指的是他们之前的住院期间急性COVID-19严重性。g)的相关性IL-1β(单核细胞比例生产IL-1β)天数自出院康复的所有COVID-19病人(n = 118)。所有的图表显示数据与酒吧代表的意思是±个别病人扫描电镜(a, b)或中位数±四分位范围(e, f)。使用未配对t组进行了比较- - - - - -测试(健康与康复的COVID-19), Mann-Whitney测试(e:健康与康复的COVID-19),与Holm-Sidak单向方差分析事后测试(a、b),克鲁斯卡尔-沃利斯邓恩事后测试(d, e, f)、皮尔森相关系数测试(c)和斯皮尔曼等级相关系数测试(g) . *: p≤0.05;* *:p≤0.01;* * *:p≤0.001。
是否改变TNF-α生产由单核细胞在恢复期后与其他呼吸道病毒住院治疗,我们评估TNF-α生产由单核细胞隔离恢复期的流感和RSV的病人。没有明显差异控制和post-RSV /流感患者单核细胞生产TNF-α(图6 d)。确定TNF-α水平差异的一般特性解决/未解决的肺损伤,我们评估TNF-α生产从单核细胞PFILD严重持续的肺部炎症和损伤患者。符合TNF-α解决肺损伤的作用,从PFILD患者单核细胞产生显著降低TNF-α(图6 d)。
单核细胞产生细胞因子的能力IL-1β也明显高于non-breathless COVID-19期间气喘患者康复期相比,虽然健康对照组相比没有变化,没有IL-1β生产和胸部放射学结果(之间的关联图6 e)。之间没有相关性IL-1β生产从单核细胞和急性疾病严重程度图6 f),有一个逐步减少IL-1β生产从单核细胞在COVID-19康复时间(图6克)。
这些数据表明,单核细胞产生细胞因子的能力TNF-α对应好结果的解决肺损伤(正常的胸部放射学和没有呼吸急促)。这个信息突出考虑细胞因子单独使用的重要性在COVID-19 anti-cytokine-targeted疗法,因为不是所有与炎症相关细胞因子通常可能有助于病理。
不同的单核细胞签名在COVID-19恢复期长COVID慢性疲劳患者有别于那些尚未解决的肺损伤
气短和疲劳是最常报道的症状长COVID长COVID清晰的两组患者出现呼吸道症状在另一集群和疲劳37]。我们这里,康复的COVID-19持续疲劳患者不同于那些呼吸短促,显示一个不同的免疫签名。定义一个fatigue-specific免疫签名,我们删除长COVID重叠症状患者的呼吸急促,从这些分析疲劳。因此,我们比较无症状患者长COVID病人出现呼吸短促只有(没有疲劳),患者持续COVID-19-induced疲劳(没有呼吸急促)产生单核细胞的概述签名长COVID(对应于特定的特性图7)。
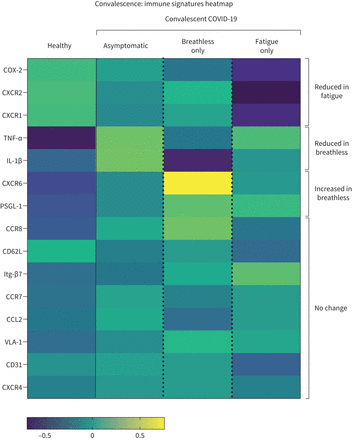
总结不同的单核细胞在患者长COVID子集。热图显示免疫参数的行。每一列表示平均(平均)z得分为每个参数计算从个人价值观的表达单核细胞从健康人或康复的COVID-19患者没有呼吸困难或疲劳(无症状),与呼吸困难但不是疲劳(气喘吁吁)和疲劳但不是呼吸困难(疲劳)作为单独的组。热图生成视觉引导,用个人的一个子集从每组每组包括所有个人为每个免疫参数分析结果(即。个人在样本用于所有迁移分子表面染色,和微生物刺激细胞因子和cox - 2读数的分析)。健康人(n = 25),无症状(n = 29),上气不接下气(n = 13),疲劳(n = 16)。
prostaglandin-generating的早些时候,有表明减少单核细胞表达cox - 2酶和趋化因子受体CXCR2的特性严重COVID-19在急性疾病,这些最低要求强化治疗单位护理,我们这里显示这些单核细胞功能异常患者持续进入恢复期,但具体持续疲劳(图7和8- d)。有趣的是,没有CXCR2或cox - 2表达的相关性与最初的急性疾病严重程度(恢复期图8- d)。cox - 2的表达在单核细胞随时间逐渐增加(图8 b)以缓慢的速度同时CXCR2水平还未恢复到正常水平(图8 d),建议长期单核细胞功能障碍患者长COVID疲劳。尽管迹象显示单核细胞趋化因子受体的表达减少的趋势CXCR1疲劳患者(图7),没有明显差异在单核细胞表达CXCR1之间健康控制和康复的COVID-19病人(疲劳或不疲劳;补充图S8b)。
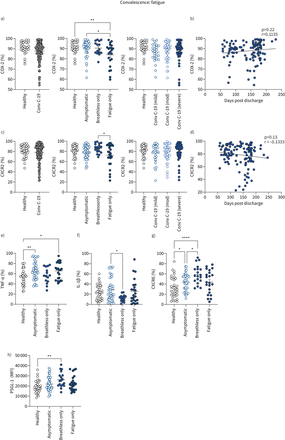
单核细胞的患者长COVID疲劳。总结图表显示数据从健康的个人和康复的COVID-19病人。CD14的)频率+从健康个体单核细胞表达cox - 2 (n = 32)和恢复期的COVID-19 (Conv C-19)患者(n = 121)。患者康复的COVID-19也分为无症状(呼吸困难或疲劳:n = 45),喘不过气来的只有(喘不过气来的但不是疲劳:n = 15)或疲劳(疲劳但不是气喘吁吁:n = 22)和轻度(n = 26),中等(n = 44)或严重疾病(n = 52),指急性COVID-19严重性前住院期间(所有康复的患者)。b) cox - 2的相关性(单核细胞百分比表达cox - 2)与天数自出院,在恢复期的COVID-19病人(n = 122)。c) CD14的频率+单核细胞表达CXCR2从健康人(n = 34)和恢复期的COVID-19病人(n = 133)。患者康复的COVID-19也分为无症状(n = 51),喘不过气来的只有(n = 18)或疲劳(n = 25)和轻度(n = 30),中等(n = 44)或严重疾病(n = 59),指急性COVID-19严重性前住院期间(所有康复的患者)。d) CXCR2的相关性(单核细胞表达CXCR2的百分比)天数自出院康复的所有COVID-19病人(n = 128)。e) CD14的频率+单核细胞在健康个体生产TNF-α(n = 33)和恢复期的COVID-19患者分为无症状(n = 45),喘不过气来的只有(n = 15)或疲劳(n = 23)。f) CD14的频率+单核细胞在健康个体生产IL-1β(n = 34)和恢复期的COVID-19患者分为无症状(n = 45),喘不过气来的只有(n = 15)或疲劳(n = 23)。g) CD14的频率+单核细胞表达CXCR6在健康个体(n = 35)和恢复期的COVID-19患者分为无症状(n = 45),喘不过气来的只有(n = 19)或疲劳(n = 22)。h) CD14+单核细胞的表达水平PSGL-1由平均荧光强度(MFI)在健康个体(n = 35)和恢复期的COVID-19患者分为无症状(n = 50),喘不过气来的只有(n = 18)或疲劳(n = 24)。所有的图表显示数据与酒吧代表的意思是±个别病人扫描电镜。使用未配对t组进行了比较- - - - - -测试(a, c:健康与康复的COVID-19),与Holm-Sidak单向方差分析事后测试(a、c、超高频:长COVID症状,原始严重程度)或皮尔逊相关系数测试(b, d)。*: p≤0.05;* *:p≤0.01;* * *:p≤0.001;* * * *:p≤0.0001。
这个微分分析更少的病人仅基于特定的呼吸困难的症状与疲劳只有再次证实,加剧TNF-α生产由单核细胞在恢复期患者仅限于解决肺损伤(即。不喘不过气来;图8 e)。单核细胞生产IL-1β比那些更高的无症状患者喘不过气来的(没有疲劳;图8 f)。这些数据支持数据包括所有病人康复的早些时候,展示由单核细胞细胞因子的生产(特别是TNF-α)与好结果的分辨率的肺损伤(图6)。然而,值得注意的是增强单核细胞生产TNF-α解决患者肺损伤包括那些持续的疲劳(图8 e),提高的可能性,提高TNF-α可以参与病理长COVID患者持续的疲劳。这些数据也清楚地阐明,加剧CXCR6和PSGL-1恢复期的患者COVID-19解决肺损伤(图4一f)是特定于呼吸困难而不是疲劳(图7和8 g,h)。
总之,我们首次展示,单核细胞迁移对应COVID-19严重性特异表达,在急性期和恢复期。在急性COVID-19单核细胞功能障碍的特点是持续进入康复期,与不同的单核细胞签名对应两个长COVID最常报道的症状,呼吸急促和疲劳(总结补充图S8c)。
讨论
COVID-19流行继续造成毁灭性的全球疾病的炎症病理结果急性疾病和持久的免疫功能紊乱在恢复期,导致长COVID,这仍然是一个世界性的公共卫生问题。现在普遍建立,许多病人发展长期慢性SARS-CoV-2感染后的症状。我们的数据表明在COVID-19病理生理学单核细胞迁移,我们表明,特异表达单核细胞功能障碍甚至持续到康复出院后9个月,与微分单核细胞签名对应的特定方面长COVID(气短和疲劳)。
我们展示一个广泛的分子参与白细胞游走异常表达在急性单核细胞和康复的COVID-19,其中一些与transendothelial迁移允许出口从血管周围组织。我们展示增加VCAM-1和E-selectin水平在长COVID呼吸困难患者,血清中其他的趋化因子,进一步暗示参与肺内皮和支持先前的研究显示VCAM-1水平上升和E-selectin急性COVID-19 [38]。
通过恢复期的高度表达单核细胞CXCR6功能相关,与单核细胞从气喘吁吁的恢复期的病人优先向CXCR6配体CXCL16迁移在体外和CXCL16表达高水平的肺35]。增强表达CXCR6 PFILD患者单核细胞和明确证据CXCL16参与这些病人是支持CXCR6-CXCL16轴的关键作用的持续的肺损伤。缺乏高度的单核细胞CXCR6表达RSV或流感恢复期可能反映了不同免疫反应产生的不同的呼吸道病毒或疾病病因学和严重程度不同的患者为急性COVID-19承认,RSV和流感。与更大的群组研究中进行后续的进一步研究流感和RSV病人必须完全定义了这些不同的病毒产生的免疫应答的差异。
我们的数据显示,两个截然不同的免疫特征对应于特定功能的长COVID-19:呼吸困难和疲劳。同时增强单核细胞CXCR6和PSGL-1表达式定义的喘不过气来的病人,减少cox - 2的表达和CXCR2定义那些持续的疲劳。我们的数据符合研究识别两个截然不同的集群长COVID病人在英国一大群500 000,与疲劳主在另一和呼吸道症状(37]。重要的是,前列腺素E2水平变化(从花生四烯酸转化生成的cox - 2)与慢性疲劳综合症(有关39),针对这类二十烷酸通路可能治疗中获益。相关数据显示低水平的CXCR2在急性严重疾病COVID-19和持续的疲劳在恢复期支持保护作用CXCR2的炎症,符合CXCR2缺乏诱导夸张与增加巨噬细胞炎症反应相关积累在发炎的网站(40]。
单核细胞的高度生产TNF-α轻度急性肺损伤疾病和解决患者在康复期支持TNF-α指示作用的研究结果在一个好的结果在小鼠模型中,它被认为是解决肺损伤,加速解决肺纤维化(41]。事实上,我们在这里展示TNF-α生产减少PFILD患者严重,持续,持续的肺损伤。此外,增加响应toll样受体结扎在单核细胞和随后的炎性细胞因子的生产是患者的功能恢复COVID-19 [42]。高度TNF-α生产在恢复期出现特定COVID-19,没有康复的RSV的变化或流感病人。高度TNF-α生产长COVID解决患者肺损伤,然而,包括那些持续的疲劳。虽然目前还不清楚如何TNF-α可能导致疲劳病理学,我们的数据支持最近的研究暗示作用TNF-α在COVID-19-associated疲劳恢复期(43]。
总之,我们已经确定了在COVID-19循环单核细胞的异常特征对我们理解长COVID意义深远。我们的数据支持的研究证明长期变化在先天免疫COVID-19恢复期(19,42,44,45)和显示异常单核细胞迁移COVID-19病理生理学作为一个关键因素在急性疾病和康复期。其中的一些分子,如。CXCR6,表示没有返回到健康的控制水平。这些发现已经直接关系到买卖时代由于长COVID的持久性,尽管全球经济温和的感染和疫苗接种规划的引入。同时新变异可能会导致不同程度的抗体中和和记忆t细胞反应由于不同的抗原表位,我们描述先天而非适应性免疫的变化对应于持续长COVID的症状。本质上与底层病理生理学改变,我们的数据是高度可能相关的买卖和任何未来的变异和subvariants。此外,我们PFILD数据显示更改CXCR6-CXCL16轴作为一个广泛适用的持续的肺损伤的病理生理学机制重要的仍然是一个特征长COVID今天患者呼吸困难。这些数据提供了新的机会在COVID-19持续发病率患者治疗目标。
补充材料
可共享的PDF
确认
我们感谢所有的参与者和他们的家庭他们的贡献,而本研究将不可能。这份报告是英国支持的独立研究冠状病毒免疫学协会(UK-CIC),西北肺中心慈善和NIHR曼彻斯特Wythenshawe医院临床研究机构。我们感谢曼彻斯特过敏、呼吸道和胸外科生物,我们感谢Post-Hospitalisation COVID-19研究(PHOSP-COVID)合作组,和北方护理联盟研究收集组织银行支持这个项目。我们感谢Imbio Inc .(明尼阿波利斯,美国)肺密度分析和肺纹理分析项目定量CT用于生成报告。中表达的观点不一定是作者和出版的英国国民健康保险制度,国家卫生研究所或卫生部。a·辛普森·a·霍斯利,t·费尔顿,p .黑暗和t . Hussell受到NIHR曼彻斯特生物医学研究中心的支持。支持c Brightling NIHR莱斯特生物医学研究中心。此外,我们要感谢免疫学社区内丽迪雅贝克研究所免疫学和炎症,流式细胞术的核心设施在曼彻斯特大学,曼彻斯特COVID-19快速反应组和研究参与者对他们的贡献。
脚注
圆环调查员:r·艾哈迈德·m·艾弗里k .伯彻尔r·凯恩斯e . Charsley a . Chenery c .咀嚼,r·克拉克·e·康诺利,k·o .角落,道森,l . Durrans h .杜灵顿j·伊根,c·福克斯,h·弗朗西斯·s·格拉斯哥,n . Godfre kj灰色、心胸狭窄的人,j . Guerin m·伊克巴尔·c·海耶斯,e·哈迪·j·哈里斯,a . John b .快活、克里希,他,n .马吉德·j·米切尔,k .摩尔摩斯,美国Murtuza贝克,r·奥利弗·g . Padden c .帕金森m . Phuycharoen m . Rattray a·萨哈Salcman,沙玛,j . Shaw T.N.肖,e . Shepley斯蒂芬,r·斯蒂芬斯g . Tavernier r . Tudge乌列,l .沃宁r·沃伦·l·威尔莫r·威尔特郡m . Younas和Zriba。
利益冲突:g . Lindergard联合创始人和科学顾问委员会成员,粗砂岩生物有限公司,这是一家上市公司,开发治疗性疫苗用于治疗癌症和传染病,包括COVID-19。其他作者宣称他们没有利益冲突。
支持声明:这项工作是支持的威康信托基金会/皇家学会(雌激素受体曼206206 / Z / 17 / Z);肯尼迪信任风湿病学研究,提供了一个快速反应奖与实验室相关的成本分析COVID-19病人jr固安捷的免疫反应;医学研究委员会(l .红苹果先生/ R00191X / 1;k . Piper汉利先生/ P023541/1);威康信托基金会(t . Hussell 202865 / Z / 16 / Z;106898 / / 15 / Z,这有助于支持一些圆环成员),李斯特研究所(J.E. Konkel);不明白(J.E. Konkel, BB / M025977/1);英国和创新(k . Piper汉利,40896)。资金信息,本文已沉积的Crossref资助者注册表。
- 收到了2022年5月19日。
- 接受2023年2月16日。
- 版权©2023年作者。
这个版本分布在创作共用署名非商业性许可证的条款4.0。商业生殖权利和权限接触权限在}{ersnet.org