文摘
背景次优公开接触的(抗结核)药物与不利的治疗结果有关。我们旨在调查评估和决定因素的一线抗结核药物药物动力学在儿童和青少年在全球层面。
方法我们系统地搜索MEDLINE、Embase和网络科学的药代动力学研究(1990 - 2021)一线抗结核药物的儿童和青少年。个体患者数据取自作者的符合条件的研究。总结估计下/推断总面积的血浆浓度时间曲线从0到24 h post-dose (AUC0-24)和血浆浓度峰值(C马克斯与随机模型)进行了评估,与当前世界卫生组织推荐的儿科剂量正常化。AUC的决定因素0-24和C马克斯与线性mixed-effects模型进行评估。
结果55资格研究,个别病人数据可供39(71%),包括来自12个国家的1628名参与者。几何稳态AUC的手段0-24总结了异烟肼(18.7 (95% CI 15.5 - -22.6) h·L·毫克−1)、利福平(34.4 (95% CI 29.4 - -40.3) mg·h·L−1)、吡嗪酰胺(375.0 (95% CI 339.9 - -413.7) mg·h·L−1)、乙胺丁醇(8.0 (95% CI 6.4 - -10.0) mg·h·L−1)。多变量模型表明,年轻的年龄(特别是< 2年)和艾滋病毒阳性状态AUC较低有关0-24所有一线抗结核药物,严重营养不良AUC较低有关0-24异烟肼和吡嗪酰胺。N乙酰转移酶2快速乙酰化器异烟肼AUC较低0-24异烟肼AUC和慢乙酰化器高0-24比中间乙酰化器。的决定因素C马克斯通常是类似AUC吗0-24。
结论这项研究提供了最全面的估计的等离子体接触一线抗结核药物在儿童和青少年。确定了药物暴露的关键决定因素。这些可能是相关的特定人群剂量调整或个性化治疗药物监测。
文摘
摘要估计和抗结核药物在儿童和青少年药物动力学的关键决定因素从全球可用的数据进行评估,提倡剂量调整或治疗药物监测在某些组织不佳的风险敞口https://bit.ly/3Vzw4f0
介绍
结核病仍然是一个主要的全球卫生挑战。直到2019年冠状病毒病(COVID-19)大流行,结核病是死亡的主要原因从一个传染病,排名高于艾滋病(1]。对于15岁以下的儿童,世界卫生组织(世卫组织)估计,有110万新的结核病例和226 000 2020年全球结核相关死亡1]。青少年也遭受重大的疾病负担,估计有727 000结核病例其中10 - 19岁2012年(2]。足够的获得治疗和最佳剂量策略是至关重要的组件的全球战略结束童年和青少年结核病(3]。
理想接触抗结核药物与治疗结果差,包括获得性耐药治疗失败和死亡4,5]。目标抗结核药物在儿童和青少年暴露在很大程度上是基于药代动力学资料近似成人暴露(6),尽管药物动力学和药效学在幼儿和成人可能不同的成熟因素(7]。此外,抗结核药物的药代动力学的可变性来源儿童和青少年尚未系统地综述。这可能是由于不同的研究包括研究人口、研究设计和方法,药物和剂量的特点,共包含在分析和药代动力学评估和参数用于解释结果。
为了克服这些挑战,我们旨在总结药代动力学的估计一线抗结核药物(即。异烟肼、利福平、吡嗪酰胺和乙胺丁醇)在儿童和青少年,学习水平分层的特点。此外,我们旨在评估患者的立场特点和关键的亚种群的平均观察到的药代动力学资料可能不同于儿童结核病。这将确定潜在的剂量调整的必要性在特定团体或个人理想药物暴露的风险目前使用世卫组织建议的剂量策略。
方法
搜索策略和选择标准
这项研究是在注册普洛斯彼罗CRD42018110807数量与标识符。普洛斯彼罗协议进行分析的主要结果登记在这个研究。我们跟着PRISMA-IPD(首选项报告个人参与者的系统回顾和荟萃分析数据)的指导方针,报告结果(8]。
所有一线抗结核药物的药代动力学研究0-18岁儿童和青少年治疗药物敏感肺和/或肺外结核病资格进入这个系统回顾和个体患者数据的荟萃分析。研究在健康志愿者和那些接受一线药物适应症以外的结核病(如。结核感染和葡萄球菌菌血症)被排除在外,因为pathology-mediated药代动力学变化可能发生在不同的疾病状态(9]。此外,评论文章、评论、社论和案例系列少于五个患者被排除在外。
相关研究发表在1990年1月1日和2021年2月2日在MEDLINE搜索(通过PubMed)、Embase和Web的科学;搜索更新于2021年12月31日。这段时间被选中,是因为预期的原始数据的可用性。没有对语言运用的限制。以下的组合网格(医学主题词)条款和使用关键字:(肺结核或结核)和一线抗结核药物(或异烟肼、利福平、吡嗪酰胺和乙胺丁醇)和(药物动力学和药物浓度)和(儿童和青少年)(补充附录1)。
所有检索到的文章上传到Rayyan搜索策略,系统评价一个web应用程序(www.rayyan.ai)[10]。删除重复后,所有标题和摘要筛选资格及相关综述了全文研究的两个独立的评论者(F.G.和R.E.W.)。原因排除研究指出。寻找额外的研究不是检索的搜索策略,执行手动搜索的参考列表包括了两个独立的研究和相关评论文章评论者(F.G.和R.E.W.)。
在缺乏有效的工具来评估质量的药代动力学研究中,我们开发了一个检查表(补充附录2),包括相关标准根据ROBINS-I工具non-randomised干预的研究(11),辅以必要的组件所需的关键评估临床药代动力学研究[12]。一个专家小组(D.J.T.,M.G.G.S.,J。年代。和J-W.C.A.) evaluated and approved the components to be included in the checklist. Each study was graded as low, moderate or high quality by two independent reviewers (F.G. and R.E.W.).
第一次和第二次之间的所有差异评论者(F.G.和R.E.W.)在研究包括研究的选择和质量评估是通过共识来解决;第三个审稿人不需要没有持续两个审稿人之间的分歧。
数据管理
合格的研究的作者被要求提供匿名患者的立场人口统计信息(年龄、性别、体重和身高),临床和实验室特征(类型的结核病感染艾滋病毒,血清肌酐和白蛋白,芳基胺N乙酰转移酶2 (NAT2)基因型和溶质载体有机阴离子转运蛋白家族成员1 b1 (SLCO1B1)基因型)、药物特征(药物剂量,药物配方和管理、计量时间和剂量间隔)和药代动力学特征(观察血浆浓度和采样时间)(补充附录3)。
道德是由独立的伦理委员会批准,格罗宁根大学医学中心,荷兰格罗宁根(M21.278329)。数据收集是通过当地伦理委员会参与最初的研究。从父母或法定监护人的书面知情同意并书面/口头同意从老参与者得到的包容。
研究的定义
儿童和青少年与药物敏感结核病包括culture-confirmed情况下容易至少异烟肼和利福平,和临床诊断的结核病例和一线抗结核药物治疗。人体测量的测量转换为z分数值基于标准参考人群zscorer包在R(0.3.1版)。营养不良是定义为一个体重或身高z分数小于2−但≥−3(温和的)或<−3(严重)5岁以下的病人和一个身高和/或身体质量index-for-age z分数< 2−但≥<−−3(温和的)或3(严重)的患者年龄≥5年(13]。参与者的表型遗传型的,分为快速、中间和慢乙酰化器NAT2遗传多态性(可用)和异烟肼消除半衰期,分别为(补充附录4)。
数据分析
我们的主要药代动力学措施/推断总面积在血浆浓度时间曲线从0到24 h post-dose (AUC0-24)和血浆浓度峰值(C马克斯)[14]。AUC0-24估计是基于linear-up /注销梯形法则和C马克斯是直接源自浓度时间曲线。(药代动力学评估补充附件5)患者的密集抽样进行non-compartmentally PKNCA包R(0.9.4版);稀疏采样数据被排除在外。
学习水平总结统计AUC的几何方法0-24和C马克斯,几何平均数的95%置信区间估计与随机荟萃分析中使用metafor包R(版本测试盒框)。异质性是评估使用I²统计(I2);任何级别的异质性获准强调之间的差异的重要性。允许不同剂量之间的比较,AUC0-24和C马克斯是dose-normalised除以个人AUC0-24和C马克斯值由mg·公斤−1剂量,然后乘以当前世卫组织建议的儿科剂量异烟肼(10 mg·公斤−1)、利福平(15毫克公斤−1)、吡嗪酰胺(35毫克公斤−1)、乙胺丁醇(20毫克公斤−1)[15];高剂量的利福平数据> 35毫克公斤−1被排除在这一特定分析这种药物表现出非线性动力学与等离子体接触由于肝脏清除率(饱和16]。报道,AUC0-24和C马克斯估计是由几组分层的,包括剂量间隔(日常和间歇(如。三次每周),抽样计划(稳态(即。≥14天后第一剂量)和non-steady-state)和世卫组织区域。
在对数转换AUC患者的立场的影响特征0-24和C马克斯与线性mixed-effects分析评估使用lme4包R(1.1.28版),与学习水平随机效应估计通过限制最大似然。对于这些mixed-effects分析,AUC0-24和C马克斯没有dose-normalised允许模型的调整药物剂量,在其他变量。找出最相关的变量,基础模型(仅调整药物剂量)为每个病人开发特点;在每个模型中,观察错过某些变量被排除在外。接下来,我们调整我们的多元模型药物剂量,年龄、性别、营养不良的严重程度和艾滋病毒状况,完成与变量显示趋势协会基础模型(p < 0.1)。mixed-effects模型的方差分量估计,包括剩余方差,随机拦截方差,随机斜率方差药物剂量,随机斜截相关性和组内相关系数。最后的多元选择模型都是基于最高的总方差解释说,最低Akaike或贝叶斯信息准则值和最大数量的观察包括在模型中。固定后果回归系数(β)被用来评估对数转换AUC的程度变化0-24和C马克斯每一个单位预测变量的变化。接受了统计学意义,p < 0.05。
子群分析儿童年龄< 5 < 2年,那些体重≥25公斤,与稳态浓度,与稳态和每日剂量,以及考虑到地区作为第三级聚类变量。
结果
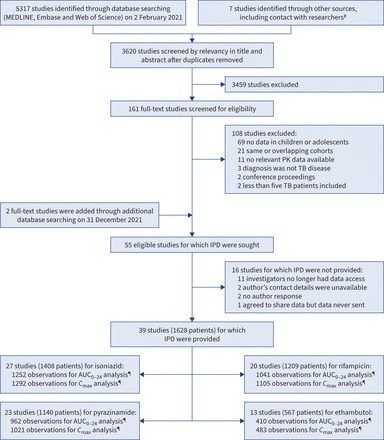
从3620个人文章发现在我们的搜索2021年2月2日,我们读标题和摘要,随后筛选163年全文的研究,包括两个全文研究增加通过更新搜索2021年12月31日(图1)。这导致了包含55个符合条件的研究,排除108研究,其中21个有相同或重叠群合格的研究(补充表E1)。个别病人数据提供39(71%)的55合格的研究(补充表E2)[16- - - - - -53Mlotha-Mitole],包括未发表的数据从一个研究et al。马拉维布兰太尔()。这些39包括研究,26(67%)高质量的和13(33%)温和的质量(补充表E3)。的16个研究个体患者数据没有提供,13(81%)进行了/在1990年代之前,当大多数的调查人员不再有访问数据(补充表E4)。
研究选择。#:包括未发表的研究或提交的手稿确认通过接触调查人员(提供进一步的细节补充表E2);¶药代动力学:重复测量的病人在不同的日子(不同的采样情况下)。AUC0-24:血浆浓度时间曲线下的面积从0到24小时post-dose;C马克斯:血浆浓度峰值;IPD:个体患者数据;PK:药代动力学;结核病:肺结核。
1628名患者中有来自12个国家和3个地区,738年(45.4%)< 5岁,875(53.7%)男孩,931年(57.2%)有肺结核,847营养不良(52.0%)和324(19.9%)呈阳性(表1)。AUC0-24值评估从1252年(78.6%)的1593个观测(即。异烟肼日常场合)1408例,1041例(70.8%)1470年1209例观察利福平,962(73.8%)1304年1140例观察吡嗪酰胺和410年(72.3%)的567个观察567例患者乙胺丁醇(图1)。利福平的一个子集的数据研究Dentiet al。(49)(n = 60/184观测)是所有AUC排除在外0-24和C马克斯分析基于使用劣质药物产品,据报道导致降低61%利福平生物利用度(49),在早先的研究也证实了Mc我lleronet al。(54]。AUC的细节观察0-24和C马克斯价值不能可靠地评估了补充表E5。
异烟肼,总结了AUC dose-normalised估计0-24(几何平均数18.7 (95% CI 15.5 - -22.6) mg·h·L−1)(图2一个),C马克斯(几何平均数4.9 (95% CI 4.1 - -5.8) mg·L−1)(图3一)患者的稳态浓度,和其他学习水平组(表2,E1和E2补充数据)。在多元mixed-effects分析(表3日志AUC),低0-24值与年轻有关< 2年(β−0.28 (95% CI 0.40 - 0.16−−)),中度营养不良(β−0.10 (95% CI 0.19 - 0.01−−)),严重营养不良(β−0.15 (95% CI 0.24 - 0.06−−)), hiv阳性(β−0.15 (95% CI 0.25 - 0.04−−))和半衰期快速乙酰化器表型(β−0.39 (95% CI 0.50 - 0.28−−)),而日志AUC更高0-24价值观与更高的mg·kg−1剂量(β0.42 (95% CI 0.34 - -0.51))和半衰期慢乙酰化器表型(β0.70 (95% CI 0.62 - -0.77))。基于NAT2基因分型、快速乙酰化器日志AUC较低0-24值(β−0.30 (95% CI 0.46 - 0.15−−)),而慢乙酰化器日志AUC有更高0-24值(β0.71 (95% CI 0.58 - -0.83))与中间乙酰化器(补充表E6)。异烟肼的决定因素C马克斯AUC是相似的吗0-24,除了中度营养不良,没有显著的影响C马克斯(表4)。
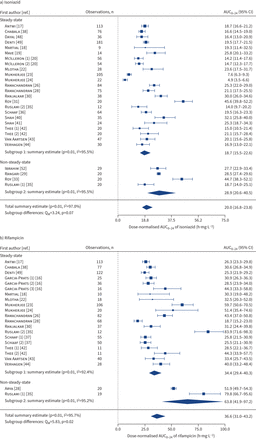
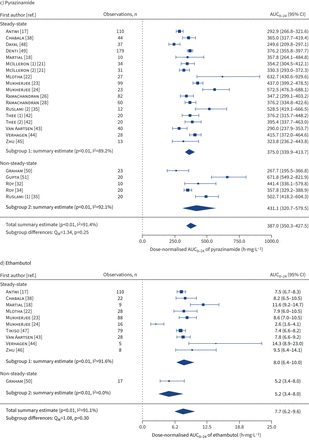
总结森林情节估计(几何平均数(95% CI))的血浆浓度时间曲线下dose-normalised面积从0到24 h post-dose (AUC0-24))异烟肼,利福平,c)吡嗪酰胺和d)乙胺丁醇与结核病的儿童和青少年,通过抽样计划(稳态和non-steady-state)。AUC0-24价值观对异烟肼dose-normalised 10 mg·公斤−1在15 mg·公斤利福平−1,吡嗪酰胺35毫克公斤−1和乙胺丁醇在20 mg·公斤−1。数量在圆括号中作者的名字表示不同的采样情况下的研究。我2:研究中的变量比例是由于异质性;问米:综合测试的模型系数。
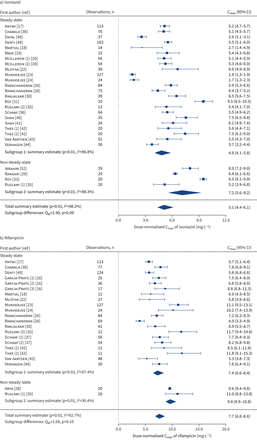
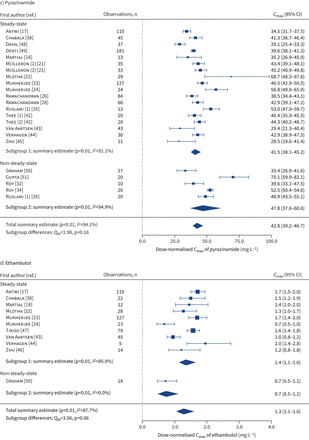
摘要森林情节估计(几何平均数(95% CI)) dose-normalised血浆浓度峰值(C马克斯))异烟肼,利福平,c)吡嗪酰胺和d)乙胺丁醇与结核病的儿童和青少年,通过抽样计划(稳态和non-steady-state)。C马克斯价值观对异烟肼dose-normalised 10 mg·公斤−1在15 mg·公斤利福平−1,吡嗪酰胺35毫克公斤−1和乙胺丁醇在20 mg·公斤−1。数量在圆括号中作者的名字表示不同的采样情况下的研究。我2:研究中的变量比例是由于异质性;问米:综合测试的模型系数。
总结下dose-normalised面积血浆浓度时间曲线的估计从0到24 h post-dose (AUC0-24)和血浆浓度峰值(C马克斯)值对公开一线药物在儿童和青少年肺结核、给药间隔、抽样计划和世界卫生组织的地区
多元线性mixed-effects回归分析的因素影响下对数转换面积血浆浓度时间曲线从0到24 h post-dose (AUC0-24)值对公开一线药物在儿童和青少年
利福平,总结了AUC dose-normalised估计0-24(几何平均数34.4 (95% CI 29.4 - -40.3) mg·h·L−1)(图2 b),C马克斯(几何平均数7.4 (95% CI 6.6 - -8.4) mg·L−1)(图3 b)患者的稳态浓度,和其他学习水平组(表2,补充图E3和E4)。在多元mixed-effects分析(表3日志AUC),低0-24值与年轻有关,包括年龄< 2年(β−0.48 (95% CI 0.64 - 0.33−−))和2 - 4年(β−0.35 (95% CI 0.50 - 0.21−−))。此外,日志AUC低0-24价值观与艾滋病毒阳性状态(β−0.25 (95% CI 0.39 - 0.11−−)),而日志AUC更高0-24价值观与更高的mg·kg−1剂量(β0.65 (95% CI 0.44−0.85))。利福平的决定因素C马克斯AUC是相似的吗0-24,除了严重营养不良降低日志C马克斯值(β−0.12 (95% CI 0.24 - 0.01−−)) (表4)。
吡嗪酰胺,总结了AUC dose-normalised估计0-24(几何平均数375.0 (95% CI 339.9 - -413.7) mg·h·L−1)(图2 c),C马克斯(几何平均数41.5 (95% CI 38.1 - -45.2) mg·L−1)(图3 c)患者的稳态浓度,和其他学习水平组(表2,补充图E5和E6)。在多元mixed-effects分析(表3日志AUC),低0-24值与年轻有关,包括年龄< 2年(β−0.28 (95% CI 0.38 - 0.17−−)), 2 - 4年(β−0.24 (95% CI 0.34 - 0.14−−))和5 - 9年(β−0.12 (95% CI 0.21 - 0.03−−))。此外,日志AUC低0-24值与男性有关(β−0.08 (95% CI 0.14 - 0.02−−)),严重营养不良(β−0.08 (95% CI 0.16 - 0.005−−))和艾滋病毒阳性状态(β−0.19 (95% CI 0.29 - 0.10−−)),而日志AUC更高0-24价值观与更高的mg·kg−1剂量(β0.17 (95% CI 0.10 - -0.23))。吡嗪酰胺的决定因素C马克斯AUC是相似的吗0-24,除了男性性没有显著的影响C马克斯(表4)。
乙胺丁醇,总结了AUC dose-normalised估计0-24(几何平均数8.0 (95% CI 6.4 - -10.0) mg·h·L−1)(图2 d),C马克斯(几何平均数1.4 (95% CI 1.1 - -1.6) mg·L−1)(图3 d)患者的稳态浓度,和其他学习水平组(表2,补充图E7和E8)。在多元mixed-effects分析(表3日志AUC),低0-24值与年轻有关,包括年龄< 2年(β−0.55 (95% CI 0.76 - 0.33−−)), 2 - 4年(β−0.35 (95% CI 0.55 - 0.14−−))和5 - 9年(β−0.19 (95% CI 0.37 - 0.001−−))。此外,日志AUC低0-24价值观与艾滋病毒阳性状态(β−0.39 (95% CI 0.56 - 0.21−−)),而日志AUC更高0-24价值观与更高的mg·kg−1剂量(β0.15 (95% CI 0.05 - -0.24))。乙胺丁醇的决定因素C马克斯AUC是相似的吗0-24,除了5 - 9岁没有显著的影响C马克斯(表4)。
在dose-adjusted mixed-effects分析,我们确定了低日志AUC的附加因素0-24值,包括严重发育不良(即。身高z分数<−3)对异烟肼(β−0.13 (95% CI 0.24 - 0.02−−))、利福平(β−0.13 (95% CI 0.25 - 0.01−−))、吡嗪酰胺(β−0.16 (95% CI 0.24 - 0.07−−))、乙胺丁醇(β−0.19 (95% CI 0.37 - 0.02−−));中等发育不良(即。身高z分数≥−3但<−2)吡嗪酰胺(β−0.09 (95% CI 0.17 - 0.02−−));严重体重不足(即。体重z分数小于−3)吡嗪酰胺(β−0.10 (95% CI 0.19 - 0.01−−));和SLCO1B1利福平(rs4149032) TT基因型(β−0.34 (95% CI 0.61 - 0.08−−))。详细的AUC dose-adjusted分析的结果0-24和C马克斯介绍了补充表E7-E14。
AUC的决定因素0-24和C马克斯在很大程度上保持一致的和不变几个子群分析5岁以下儿童(补充表E15和E16天稳态浓度(患者),补充表E19和E20),稳态浓度和患者每日剂量(补充表E21和E22),并考虑世卫组织区域作为第三级聚类变量(补充表E23和E24)。此外,成人剂量≥25公斤为儿童推荐日志AUC较低有关0-24值异烟肼(4 - 6毫克公斤−1;β−1.01 (95% CI 1.27 - 0.76−−))和利福平(8 - 10毫克公斤−1;β−0.35 (95% CI 0.63 - 0.07−−))与儿科剂量(补充表E25和E26)。额外的药代动力学预估时间C马克斯,消除半衰期和消除速率常数补充表E27。
讨论
在这个个体患者数据的荟萃分析中,我们总结了等离子AUC0-24和C马克斯估计几个学习水平组织一线抗结核药物的儿童和青少年与结核病全球代表研究。我们还发现了等离子体接触一线抗结核药物的患者的立场决定因素在这些儿童和青少年。
与成人的数据相比,我们总结为稳态AUC估计0-24比较了异烟肼(几何平均数18.7 (95% CI 15.5 - -22.6)与值范围11.6 - -26.3 mg·h·L−1)[55)、吡嗪酰胺(几何平均数375.0 (95% CI 339.9 - -413.7)与值范围233 - 429 mg·h·L−1)[55)和利福平(几何平均数34.4 (95% CI 29.4−40.3)与意思是38.7 (95% CI 34.4 - -43.0) mg·h·L−1)[56),但降低了乙胺丁醇(几何平均数8.0 (95% CI 6.4 - -10.0)与值范围16-28 mg·h·L−1)[55),无论重要方法论之间的异构性问题的研究包括在两个系统评价评估这些估计成人结核病患者(55,56]。理想情况下,目标AUC0-24和C马克斯价值观是建立基于药代动力学/药效学知识、服用药物疗效、安全性和耐受性考虑(14]。成年人,然而,与药代动力学研究大多数儿科临床和细菌学的研究缺乏数据对结核病治疗的反应,可能由于paucibacillary疾病和困难获得微生物标本。这导致了一个重大的挑战在建立目标AUC0-24和C马克斯基于药代动力学/药效学分析值。直到这些药代动力学/药效学指标可用,我们总结AUC0-24和C马克斯估计可以作为真实的临床医生和研究人员引用值剂量一线抗结核药物的儿童和青少年。
一般来说,15岁以下儿童结核病治疗成功率高(88 - 96%)1,57,58),虽然那些与结核脑膜炎等严重疾病,死亡率很高(10 - 30%)59- - - - - -61年]。在目前的研究中,药物动力学和治疗结果之间的关系并不是重点,和结果数据不可用包括多数的研究(n = 34/39 (87%))。应该注意的是,抗结核药物的药代动力学研究的儿科患者通常有一个较小的样本量,因此没有动力分析药物在治疗结果的影响。因此重要的药代动力学数据包括在大型结果研究[14,62年]。
儿童最容易受到严重形式的疾病,包括粟粒状的结核和结核脑膜炎。降低药物在儿童接触,尤其是< 2岁,很可能归因于体重间隙的非线性效应,由于异速生长的比例,从而减少风险敞口较小的儿童服用后在同一mg·公斤−1作为更大的儿童和青少年63年]。此外,这些可能是由于低生物利用度的异烟肼和利福平在< 2 - 3岁的儿童49]。结核脑膜炎,这些低血浆暴露可能导致极低的接触感染部位的脑膜,尤其是对利福平、乙胺丁醇脑脊液渗透差(25,35]。可以考虑更高剂量的利福平儿科结核脑膜炎(64年),一般小儿结核病(16),具有良好的安全性配置文件(16]。然而,乙胺丁醇高剂量可能增加眼部毒性的风险(65年),强调探索的重要性乙胺丁醇的替代品,如乙硫异烟胺或氟喹诺酮类原料药(如。左氧氟沙星)。
重要的是,儿童和青少年体重≥25公斤接受世卫组织建议的成人剂量较低比世卫组织建议的儿科异烟肼和利福平曝光剂量。成人固定剂量组合的使用剂量也导致次优的暴露在南非和赞比亚儿童体重≥25公斤(38]。进一步调查儿科制定和修订重量乐队需要优化剂量的一线抗结核药物(49),包括儿童体重≥25公斤。
不同程度的低接触一线抗结核药物在儿童和成人艾滋病毒感染者最近报告了两个系统评价,但是估计没有混杂因素调整后,无法获得一致的结果由于方法和统计包括之间的异构性问题研究[55,66年]。艾滋病毒的影响在减少接触一线抗结核药物被提出是由于药物的吸收不良患者先进艾滋病毒合并感染(67年]。然而,随着抗逆转录病毒数据不可用在我们的数据集,这还需要进一步的研究来评估的潜在影响的抗逆转录病毒治疗抗结核药物在儿童和青少年感染艾滋病毒药物动力学。
严重营养不良被发现有小但对异烟肼和吡嗪酰胺曝光严重的负面影响。对于高度蛋白结合的利福平(68年],protein-unbound分数严重蛋白质能量营养不良患者可能更高,这可能导致患者类似的等离子体之间的接触protein-unbound利福平,没有营养不良,由一个成年人研究[69年]。在我们dose-adjusted模型,降低暴露所有一线药物严重发育不良患者的观察,但我们的研究结果不同病人体重不足和浪费。同样重要的是,导致发育不良enteropathogens最近被证明对负面影响一线抗结核药物药物动力学在营养不良的儿童43]。综上所述,我们怀疑不同程度和营养不良倾向可能有不同的影响生理变化影响抗结核药物药物动力学(70年]。
的潜在好处NAT2genotype-guided异烟肼剂量减少毒性和治疗失败已报告在成人患者(71年]。基因分型结果在资源有限的环境中,很少使用,自动测定GeneXpert平台检测可以作为一个替代选择NAT2多态性和指导异烟肼剂量(72年]。接下来,我们的研究结果表明SLCO1B1多态性对利福平曝光适度的负面影响,虽然这些结果只获得两项研究在非洲儿童(17,49]。SLCO1B1多态性降低利福平曝光已报告在非洲成人患者中更常见(73年),这些可能部分解释了利福平低暴露在我们的病人来自非洲与非洲以外的地区。
越来越有兴趣使用较短的结核治疗方案。最近的临床试验表明,4个月的抗结核治疗rifapentine-based方案包含莫西沙星在成人肺结核(74年),和一个标准的一线抗结核药物疗法在儿童不重的结核病患者(58),非劣标准6个月疗程,显示出良好的治疗结果。高收益机会的分层和个性化的医学方法,包括微分剂量关键的亚种群,应该探索作为潜在的替代传统的放之四海而皆准的策略75年]。虽然编程结核病治疗可能适合大多数病人,分层的治疗和某些群体更以人为本的方法是必要的,以确保高质量的护理,如患者理想的风险暴露于抗结核药物,病人的风险与毒品有关的毒性和患者可能受益于治疗药物监测62年]。此外,微创治疗药物监测方法使用唾液,头发和干血现货样本进一步研究应该探索减少静脉血液采样在这个人口的负担(14,62年,76年]。
这项研究有一定的局限性,应该承认。首先,总结学习水平组药代动力学估计显示高异构性问题,虽然我们可以纠正这些协变量个体层面和方差估计在mixed-effects模型组件。第二,尽管dose-normalised曝光高剂量的利福平> 35毫克公斤−1没有估计由于饱和肝间隙(4%的观察)16),不能排除对标准剂量的影响(49),因此利福平估计应该仔细解释。第三,我们无法可靠地评估AUC0-24和C马克斯从三个已发表的研究(稀疏采样数据25,39,53)和未发表的一项研究(Mlotha-Mitoleet al。马拉维布兰太尔,)。进一步的研究使用药代动力学/药效学模型和蒙特卡罗模拟需要更好的描述与药代动力学参数(生理上明智的协变量的关系如。药物间隙分布和体积)和设计更优的计量策略14),包括密集和稀疏采样数据。此外,考虑到只有protein-unbound浓度通常被认为具有药理作用,蛋白质绑定参数的包含在未来的药代动力学/药效学模型可能是重要的,尤其是对利福平,因为只有∼10 - 20%的总药物浓度可以自由渗透感染的网站(68年,77年]。第四,没有一个来自欧洲国家,包括研究和缺乏数据< 3个月岁儿童和青少年15—18岁。后者可能是因为历史上分散的方法只有分类的人年龄< 15年作为孩子,排除那些15—18岁的儿科和成人研究[78年]。尽管有这些限制,我们的研究结果提供了最全面的学习水平估计的等离子体接触一线抗结核药物包括∼30年的全球可用数据,因此结果可以全面的全球人口> 3个月至14岁儿童。此外,mixed-effects模型包括一个广泛的变量和各子群分析我们的结果是一致的。
总之,我们的系统回顾和个体患者数据分析总结了药代动力学的估计一线抗结核药物在儿童和青少年中使用大量的全球可用的数据。尽管儿童和青少年与结核病通常有很好的治疗结果与标准治疗方法在之前的报道,某些子组药物暴露不佳的风险,尤其是儿童< 2岁和严重营养不良或艾滋病毒,可能需要特定人群剂量调整或个性化治疗药物监测。设计更优的计量策略使用药代动力学/药效学在这些弱势群体建模和仿真是十分必要的。这是重要的政策制定者和结核病规划,以确保最好的治疗效果与结核病的儿童和青少年。
补充材料
可共享的PDF
确认
本文是对已故的鲍勃Wilffert(格罗宁根的格罗宁根大学、荷兰),谁导致了本研究的构思和设计,但不幸的是在2021年7月去世了。我们感谢Sjoukje van der Werf(格罗宁根大学医学中心,格罗宁根,荷兰)帮助发展中最初的搜索策略和太极Ochi(格罗宁根的格罗宁根大学、荷兰)帮助基因数据的解释。我们也感谢所有特约机构、调查人员、父母或法定监护人和病人参与最初的研究。
脚注
作者的贡献:f . Gafar Wilffert__和J-W.C。Alffenaar设计研究和协议。f . Gafar右眼Wasmann莫莱森McIlleron,右眼Aarnoutse, H.S. Schaaf d·阿加瓦尔和队友,北达科他州,a . Bekker D.J.贝尔c . Chabala l . Choo广义相对论戴维斯J.N.天,r .新德里p . Denti公关唐纳德,e . Engidawork A.J. Garcia-Prats, d·吉布克里·格雷厄姆,交流塞尔,”栏目Heysell, M.I.伊德里斯,,a . Kinikar Kabra A.K.H. Kumar a . Kwara r . Lodha c . Magis-Escurra n .马丁内斯B.S.马修诉Mave e . Mduma r . Mlotha-Mitole密度Mpagama, a·慕克吉Nataprawira, c.a Peloquin, t . Pouplin g .拉马钱德兰j . Ranjalkar罗伊诉,r . Ruslami沙,y辛格E.M. Svensson, s . Swaminathan Thatte, s .你又托马斯,t . Tikiso a . Turkova t . Velpandian L.M. Verhagen, J.L. Winckler h·杨和诉Yunivita贡献个体患者数据。f . Gafar分析数据和创建的表和数据的监督下j·史蒂文斯和J-W.C。Alffenaar。f . Gafar写了初稿的手稿k的监督下出租车,j·史蒂文斯和J-W.C。Alffenaar。右眼Wasmann莫莱森McIlleron,右眼Aarnoutse, H.S. Schaaf和B.J. Marais说编写委员会的成员,并帮助修改起草手稿之前和之后的循环所有合作者。所有作者提供了重要的输入和修改的草稿和批准前的最后一个版本的手稿提交出版。
利益冲突:H.S. Schaaf赠款从美国国立卫生研究院/ IMPAACT报告;和谢礼安湖出版物(由强生(Johnson & Johnson)教育出版管理耐多药结核病的儿童。答:Bekker报告从IMPAACT赠款,国际药品采购机制;讲座从Sandoz谢礼;对参加五PIM会议的支持;并得到了通用LPV / r, 3 tc和ABC娇小的研究。D.J.贝尔从欢悦药品支持参加一个会议报告;和一个顾问委员会会议出席费用从药品欢悦。l . Choo报道赠款UKRI MRC DFID Wellcome NIHR联合全球卫生试验,结核联盟支持试验药品采购和UKRI COVID-19格兰特扩展分配奖。p . Denti报告授权为儿童结核病药物世卫组织专家评审。 S.M. Graham reports participation on a data safety monitoring board for the TB CHAMP trial; and leadership roles as a co-chair for the Guidelines Development Committee of the WHO updated recommendations and consolidated guidelines on child and adolescent TB, and as a core member for the WHO Child and Adolescent TB Working Group. S.K. Heysell reports grants from the NIH, DANIDA and EDTCP; royalties or licences from UpToDate; and honoraria for lectures from Henry Stewart Talks. A. Kwara reports a grant from the NIH/NICHD. V. Mave reports grants from the NIH and CDC. C.A. Peloquin reports a grant from the NIH. V. Roy reports a grant from the Delhi State TB Association; and leadership roles as a member of the Delhi State TB Association and the MAMC TB Committee. E.M. Svensson reports grants from the NWO personal Veni, IMI UNITE4TB consortium, TB Alliance, UNITAID BenefitKids consortium, WHO expert review, NIH support for IMPAACT studies, Blueprint, Probex, ACTG study Clo-FAST, Janssen Pharmaceuticals, EDCTP support PanTB-HM and Legochem; and leadership or fiduciary roles in the ISOP DI&E committee and BenNeLux PMX organising committee. U. Thatte reports participation on a data safety monitoring board for an ICMR TB trial. T.A. Thomas reports grants from the NIH and the University of Virginia. D.J. Touw reports a grant from Chiesi; consulting fees from Pure IMS and Sanguin; and participation on a data safety monitoring board for the FORMAT trial. A. Turkova reports grants from the UKRI MRC DFID Wellcome NIHR Joint Global Health Trials and MRC Grants for core funding of the Medical Research Council Clinical Trials Unit at the UCL; and TB Alliance Support for SHINE trial drug purchase. All of this work was declared by the authors to be outside the submitted work. All other authors declare no competing interests.
支持声明:系统回顾和个人赞助病人数据荟萃分析受到了印尼教育捐赠基金(LPDP;201711220412046)通过格罗宁根大学评为f . Gafar博士奖学金。这个资助机构没有参与这项研究概念和设计,数据收集和分析、写作和出版审查的手稿或决定。最初的研究包括在这个个体患者数据的荟萃分析,金融支持收到尤尼斯肯尼迪施莱佛国立儿童健康和人类发展研究所美国国立卫生研究院(HD071779和R01HD069175),英国医学研究理事会(MRC)和国际发展部(DFID)康NIHR联合全球卫生试验(先生/ L004445/1),结核联盟通过UNITAID-funded STEP-TB项目,英国威康信托基金会,Armauer汉森研究所国家过敏症和传染病研究所的美国国立卫生研究院(K23AI097197和U01AI115594),美国临床药理学的格罗宁根大学医学中心通过左Suppletiefonds Sonnevanck,临床药理学单位部门基金和机构流体研究资助基督教的医学院和医院Vellore,百时美施贵宝的“安全未来”基础上,印度医学研究理事会,德里Tapedic Unmulan Samiti,新德里国家结核病协会的学术领导授予意大利Padjadjaran,印尼教育捐赠基金,一般临床研究中心授予的美国国立卫生研究院(M01RR00051和1 ro1ai37845)。调查结果和结论的系统回顾和个体患者数据的荟萃分析是作者的观点,并不代表这些格兰特提供者。资金信息,本文已沉积的Crossref资助者注册表。
- 收到了2022年8月12日。
- 接受2022年10月10日。
- 版权©2023年作者。
这个版本分布在创作共用署名非商业性许可证的条款4.0。商业生殖权利和权限接触权限在}{ersnet.org