文摘
背景治疗方法不实用的慢性血栓栓塞肺动脉高压(CTEPH)仍然有限。Selexipag,口服选择性IP环前列腺素受体激动剂批准肺动脉高血压,CTEPH是一个潜在的治疗选择。
方法在这个多中心、随机、双盲、安慰剂对照研究中,78名日本瘫痪CTEPH或持久/复发患者肺部动脉内膜切除术和/或气球后肺动脉高压肺血管成形术被随机分配接受安慰剂或selexipag。主要终点是肺血管阻力(PVR)的变化从基线到20周。二级终端其他血流动力学参数的变化:6分钟步行距离(6随钻测量),Borg呼吸困难量表得分,世界卫生组织(世卫组织)功能类,EuroQol显示五级工具和n端pro-brain利钠肽。
结果PVR−98.2±111.3的变化动力学·s·厘米−5和−4.6±163.6达因·s·厘米−5分别selexipag和安慰剂组(平均差−93.5达因·s·厘米−5;95%可信区间156.8−−30.3;p = 0.006)。心脏指数的变化(p < 0.001)和Borg呼吸困难量表得分(p = 0.036),也显著提高了安慰剂。6随钻测量和功能类没有显著改善。selexipag组中常见的不良事件与那些通常观察后环前列腺素类似物的管理。
结论Selexipag显著提高PVR和其他CTEPH患者的血流动力学变量,虽然运动能力保持不变。进一步的大规模的调查是必要的证明在CTEPH selexipag所扮演的角色。
文摘
Selexipag显著提高肺血管阻力和其他慢性血栓栓塞肺动脉高压患者的血液动力学,虽然运动能力保持不变https://bit.ly/3HfPA9s
介绍
慢性血栓栓塞肺动脉高压(CTEPH)是一种危及生命的疾病的特点是肺动脉梗阻由于未解决的有组织的血栓,导致肺动脉高压(PH)恶化,如果不及时治疗(右心衰和死亡1]。
肺部动脉内膜切除术(豌豆)是一线,只有治疗治疗CTEPH [1- - - - - -4]。然而,并发症的患者,或拒绝治疗,不符合豌豆5- - - - - -8]。即使豌豆执行成功,患者可能有残留或复发PH值(2,4]。同时,气球肺血管成形术(BPA)是一个新兴的治疗的患者没有得到豌豆(4]。然而,一些CTEPH病人是BPA的资格。此外,部分患者症状残余PH值后BPA (9]。因此,需要存在实施新的有效治疗瘫痪CTEPH或豌豆/双酚a后剩余的PH值。
CTEPH病理研究显示小血管血管病变类似于观察肺动脉高血压(PAH) [2]。因此,肺血管舒张药针对小血管血管病变的治疗选择瘫痪CTEPH或豌豆后剩余的PH值和双酚a。例如,riociguat CHEST-1结果研究表明,可溶性鸟苷酸环化酶刺激器,提高了6分钟步行距离(由39±79 6随钻测量)和肺血管阻力(PVR)−226±248达因·s·厘米−5从瘫痪CTEPH或剩余的PH值(基线值10]。
Selexipag是一种口服选择性环前列腺素受体(IP)受体激动剂nonprostanoid结构。其代谢物,绝笔- 269 IP的高选择性受体(11,12]。Selexipag增加阵营,导致松弛血管平滑肌(12]。PAH患者的一项早期研究证明的有利影响selexipag发病率和死亡率的风险事件在国际三期安慰剂对照双盲研究[13),导致其批准的治疗多环芳烃在许多国家,包括美国,欧盟和日本。
CTEPH的上下文中,前一个概念验证selexipag日本患者的临床试验提出一个可能的信号与selexipag改善血液动力学(14]。在这里,我们报告的结果安慰剂对照、双盲研究检查的有效性和安全性selexipag (NS304C-P3-1)在日本瘫痪CTEPH或持久的PH值/复发后患者豌豆和/或双酚a。
方法
研究对象
我们选择CTEPH患者(20 - 85岁)证实了肺通气/灌注扫描,肺血管造影术和胸部电脑断层扫描,两个或更多的反应了肺血流量不足的地方。静止的肺血流动力学变量,由心脏catheterisation被设置为基线。平均肺动脉压(肺动脉平均)被设定为≥25毫米汞柱;肺动脉楔压(PAWP)被设定为≤15毫米汞柱;和PVR被设定为> 360达因·s·厘米−5。人口由患者无法接受豌豆由于血栓外围组织的存在。这项研究还包括患者无法接受豌豆由于其高风险(如。并发症或年龄),或其他原因(如。拒绝接受手术)。这些疾病分类评估每个调查员在他们自己的机构。人口也包括一些患者持续或复发性PH值在豌豆或双酚a。
那些收到环前列腺素和/或其衍生品被排除在外。伴随使用riociguat,内皮素受体拮抗剂(时代),phosphodiesterase-5抑制剂或钙拮抗剂被允许如果剂量稳定≥90天前基线对心脏catheterisation和维持到这个双盲研究。而患者经历了豌豆和/或包括双酚a,豌豆和BPA研究中不允许的。包含和排除标准的细节中提供补充材料。
本研究按照道德原则出发进行的人类机构伦理委员会参与设施或地区和《赫尔辛基宣言》。研究设计是在每一个研究机构审查委员会批准的网站,包括国家脑和心血管中心(参考号# 924)。所有科目提供书面知情同意参与这项研究。
的评估结果
主要终点是休息PVR的变化从基线到20周。二级终端在PVR指数变化(PVRI)、肺动脉平均,心脏指数、平均右心房压力(mRAP),肺总阻力(TPR),混合静脉氧饱和度(年代签证官2)和EuroQol显示五级(EQ-5D-5L)治疗20周后;6随钻测量的变化,Borg呼吸困难量表评分和n端pro-brain利钠肽(中位数水平以上病人)在每个访问;和世界卫生组织(世卫组织)的变化随着时间的推移,每一次访问太阳系时功能类。探索性的疗效终点的时候从随机临床恶化事件(如。死亡,住院由于恶化或并发症的PH值或使用任何额外的干预治疗CTEPH的恶化,并满足以下两个要求:纽约心脏协会/功能恶化类和6随钻测量)> 15%下降到20周。肺血液动力学使用Swan-Ganz导管方法进行评估,而病人平卧。热稀释法方法或间接菲克的方法被用来计算心输出量。
端点安全药品不良反应(adr),实验室测试值、生命体征和心电图在每个访问。
统计分析
目标样本容量被设定为72例,随机接受selexipag或安慰剂在1:1的比例由最小化。双盲,安慰剂对照,第二阶段的研究在日本CTEPH selexipag患者(14)发现了一个变化意味着±sd在PVR) selexipag群−104±191达因·s·厘米−5和改变PVR的安慰剂组±180达因·s·26厘米−5。使用这些结果和假设80%的力量和一个双边显著性水平为5%,检测所需的样本规模的显著差异Wilcoxon等级测试和计算是34每组对象,或68。假设∼5%将被排除在全分析集。提供的随机方法补充材料。
数据意味着±sd、中值(范围)或百分比。的主要分析疗效端点进行全分析集。PVR的变化,PVRI,年代签证官2,Borg呼吸困难量表评分和中位数水平以上病人水平selexipag和安慰剂组之间比较使用Wilcoxon等级和测试。肺动脉平均、心脏指数、mRAP TPR 6随钻测量和EQ-5D-5L使用未配对t检验进行比较。进行亚组分析PVR的性别、年龄、疾病分类、存在/之前没有豌豆/双酚a和/没有伴随riociguat或时代和基线PVR和手段的差异和95%置信区间所示图4。所有子组预先确定的统计分析计划。那些功能类的变化随着时间的推移,每一次访问太阳系时使用确切概率法进行了比较。如果数据失踪20周的治疗,主要是与病人发生过早退出研究,丢失的数据估算了基线观测结转,最后观察结转或最差值(PH值恶化的情况下)和数据包括估算值作为数据的研究。时间第一临床恶化,生存曲线使用生存率较组之间的比较。主要药效变量进行灵敏度分析PVR (补充材料)。安全分析的安全评价变量进行分析。一个显著差异是定义为p < 0.05(双尾检验)。没有统计调整多重性。所有分析使用SAS(版本9.4;美国NC SAS研究所,卡里)。
第三阶段研究的主要终点包括CTEPH病人是6随钻测量。然而,由于这个研究只在日本和CTEPH是一种罕见的疾病,病例数有限。因此,讨论后的药品和医疗器械代理在日本,PVR是这第三阶段研究的主要终点。然而,PH值目前的临床试验,本研究可能会被认为是第二阶段的研究。
结果
病人
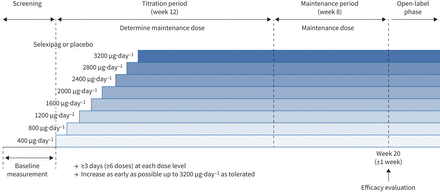
2016年至2019年间,78名受试者被来自42个机构。全面分析组78例(39个受试者被分配给selexipag和39安慰剂)是主要用于分析。患者在基线人口统计学特征提出了表1。患者无法接受豌豆,因为远端组织观察血栓在整个群体占主导地位。组的患者无法接受豌豆由于高风险或其他原因,患者近端分布的慢性纤维化的凝块被录取。大约有60%的患者接受riociguat。维持剂量的分布所示表2。维持剂量的33.3%(39)13日的患者是1600μg,最大容许剂量在这项研究。比较的基线数据从这个研究和其他随机对照试验的使用医学疗法CTEPH病人所示补充表S1。
selexipag组39例,5个中断研究(三个发达的不良事件,和两个撤回了他们的同意),而安慰剂组患者39的,四个停止研究(因为不良事件)(图2)。规则的缺失数据的归责,请统计分析部分。
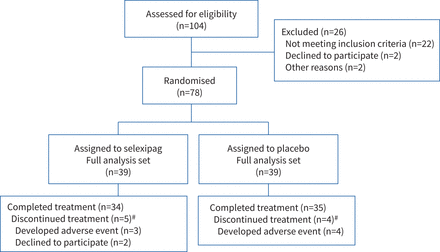
耐心的性格。#在20周的治疗:如果数据丢失,丢失的数据估算了基线观测结转,最后观察结转,或最值(肺动脉高压的情况恶化)和数据,包括估算数据作为数据的研究。
功效
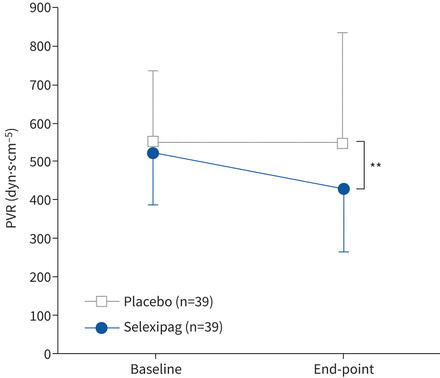
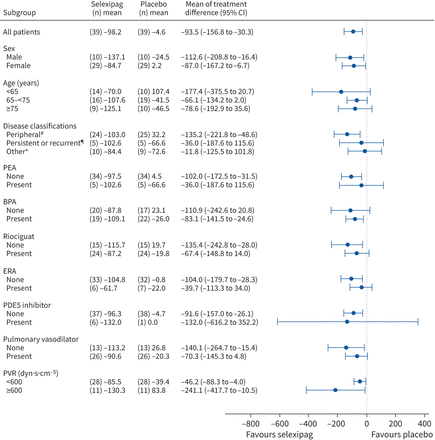
PVR的变化从基线到星期20所示图3,轮廓的变化提出了肺血流动力学变量和其他疗效端点表3。PVR的变化从基线到20周selexipag组−98.2±111.3达因·s·厘米−5,而在安慰剂组−4.6±163.6达因·s·厘米−5。平均差(95% CI)在PVR组治疗20周后−93.5(156.8−−30.3)达因·s·厘米−5,表明显著减少PVR selexipag组与安慰剂组相比(p = 0.006)。这个结果证实在敏感性分析(补充表S2)。所有子群分析PVR selexipag表示一致的有益效应(图4)。在病人无法接受豌豆因为远端组织血栓,均值差异(95% CI)在PVR组治疗20周后−135.2(221.8−−48.6)达因·s·厘米−5,表明显著减少PVR相比,这些病人豌豆后持续或复发患者的PH值,或有高风险(如。并发症或年龄),或因其他原因不接受豌豆(如。拒绝手术)。在病人经历了BPA,平均差(95% CI)在PVR组治疗20周后−83.1(141.5−−24.6)达因·s·厘米−5。selexipag组中,没有与此同时接受肺血管舒张药(n = 13),治疗效果(平均差(95% CI))治疗20周后−140.1(264.7−−15.4)达因·s·厘米−5。PVR显示更大的减少患者selexipag不如患者selexipag与肺血管舒张。selexipag维持剂量的分析表明,更高的维持剂量与更大的减少在PVR (补充图S1)。
改变肺血管阻力(PVR)从基线到20周。数据意味着±sd。均值变化从基线到20周的治疗是达因·s·厘米−98.2−562.1 (95% CI 134.2−−达因·s·厘米−5selexipag组)和−4.6达因·s·厘米−5(95% CI 57.7−48.4达因·s·厘米−5在安慰剂组)。selexipag显著的治疗效果与观察安慰剂组(治疗效果−93.5,95% CI 156.8−−30.3;p = 0.006使用Wilcoxon等级和测试)。* *:p < 0.01。
肺血流动力学变量的变化,6分钟步行距离(6随钻测量),Borg呼吸困难量表得分,氨基端pro-brain利钠肽(中位数水平以上病人),EuroQol显示五级工具(EQ-5D-5L)和世界卫生组织(世卫组织)功能类(全分析集)
改变基线的肺血管阻力(PVR)的基线特征子群。#:肺部动脉内膜切除术(豌豆)并不表示因为远端组织血栓;¶豌豆后:持续或复发性肺动脉高压;+:高风险情况下(如。并发症和老年)或豌豆因为其他原因无法执行。双酚a:气球肺血管成形术;时代:内皮素受体拮抗剂;PDE5: 5型磷酸二酯酶。
至于PVRI,心脏指数、TPR、年代签证官2和Borg呼吸困难量表评分,均值差异(95% CI) 20周的治疗后两组之间−154.4(−255.3−53.4)达因·s·m2·厘米−5(p = 0.004), 0.487 (0.262 - 0.711) L·分钟−1·米−2(p < 0.001),−116.8(189.3−−44.2)达因·s·厘米−5(p = 0.002), 2.58%(0.30%对4.87%)(p = 0.029)和0.85−1.58 (−−0.11)(p = 0.036),分别指示显著改善selexipag组与安慰剂组相比。相比之下,两组之间没有显著差异对于肺动脉平均变化观察,mRAP、6随钻测量,中位数水平以上病人或EQ-5D-5L从基线到20周。在大多数患者中,世卫组织功能类保持不变在20周的治疗。作为参考,PAWP没有显著改变从基线到20周selexipag组或安慰剂组。在一个病人临床观察恶化selexipag组和安慰剂组的一个病人。
安全
adr(不包括那些与selexipag)发生的速度selexipag≥10%和安慰剂组所示表4。药物不良反应发生在35 (89.7%)39 selexipag组的患者。的药物不良反应发生的速度selexipag≥10%组头痛(53.8%)、腹泻(41.0%)、恶心(33.3%)、不适(23.1%),疼痛的下巴和食欲下降(20.5%)、肌痛和呕吐(15.4%)和关节痛(10.3%)。这些反应通常是一样的那些观察到当环前列腺素类似物管理。大多数药物不良反应发生在早期阶段的治疗和在低剂量。大多数病人症状改善或恢复与不停用研究药物治疗。
selexipag组39例,三个停止这项研究由于不良事件(n = 1,腹泻、恶心和眩晕恶心n = 1, n = 1)头痛,而安慰剂组患者39的,四个停止这项研究由于不良事件(腹部不适n = 1,白细胞计数减少n = 1,头痛n = 1、心肺衰竭n = 1)。
严重不良事件的研究包括心房心动过速和右心室衰竭,每在一个(2.6%)病人selexipag组和心肺衰竭,结肠癌和咯血,每在一个(2.6%)病人安慰剂组。selexipag集团的心房心动过速发生的因果关系不能排除,是温和的。右心室衰竭也温和,排除因果关系。
两组、血压或脉搏率没有改变(补充表S3),没有异常的实验室测试值或心电描记法的结果可能被认为是一个临床问题发生在整个研究期间。
讨论
Selexipag改善血液动力学在日本瘫痪CTEPH或持久的PH值/复发后患者豌豆和/或双酚a与安慰剂相比,但没有改善运动能力。这是良好的耐受性和安全。
与安慰剂相比,selexipag PVR的改善,本研究的主要终点。PVR反映了作家的基本条件,血液动力学的PH值和与多环芳烃的长期预后15]。减少PVR豌豆CTEPH病人后与改善预后相关(16]。因此,PVR临床相关,被用来作为衡量治疗效果的PH值(17]。PVR的改善本研究观察到的是一致的,在以前的研究的肺血管舒张药CTEPH [10,18- - - - - -20.]。此外,前一个概念验证临床试验在日本CTEPH病人建议一个可能的信号与selexipag改善血液动力学(14]。PVR改进不是其他的改善血液动力学的特征(如。PVRI、心脏指数、TPR、年代签证官2)。
PVR selexipag引起变化的程度本研究相对温和(−98达因·s·厘米−5)相比,在先前的研究(116 - 239−−达因·s·厘米−5)[10,18- - - - - -20.]。这可能是由于相对较低的基线PVR在我们的研究中(523.4±132.8达因·s·厘米−5)在前面的国际研究(778 - 984达因·s·厘米−5)(补充表S1)[10,21,22)和以前的日本CTEPH研究(700 - 756达因·s·厘米−5)[14]。我们的研究包括CTEPH患者接受相对高比例的背景治疗riociguat(61.5%)和双酚a (52.6%)。上市后监测的riociguat日本CTEPH人口表明riociguat BPA PVR减少了280达因·s·厘米−5(23]。因此,本研究的背景治疗可能减少了基线PVR,因此衰减selexipag的治疗效果。这个假设可能支持的亚组分析,显示更大的PVR减少患者selexipag不如患者selexipag接受背景肺血管舒张。虽然PVR减少本研究中观察到的是温和的,在以前的研究相比,20周的几何平均数PVR下降到78.7%和94.1%的基线selexipag和安慰剂组,分别。selexipag:安慰剂比几何方法(95% CI),这是作为主要终点MERIT-1研究,为83.6%(74.9 - -93.3%),这是类似于其他临床研究获得的比率10,21,22]。
双酚a,获得广泛的一致好评(CTEPH患者的临床治疗(4]。selexipag治疗后残留的PH值BPA的好处还不清楚。与post-BPA患者亚组分析,PVR显著降低selexipag组与安慰剂组相比(p = 0.009),这表明selexipag治疗的角色BPA后剩余的PH值。考虑到小样本应用于亚组分析,这些结果应该被视为探索。
然而,在目前的研究中,两个次要的端点,6随钻测量功能类,没有显著改善selexipag组与安慰剂组相比。差异的一个潜在原因的结果,血液动力学的运动能力是样本容量。我们的样本大小,使观察PVR的显著差异,其他参数,如6随钻测量和功能类。进一步的大规模的调查是必要的证明selexipag在运动能力的功效。另一个假设是,基线血流动力学和其他参数,包括6个随钻测量,更接近正常的比之前的研究(补充表S1)[10,21,22),可能由于存在背景BPA和PH值等药物治疗。占主导地位的基本功能类是谁还在当下研究低于CHEST-1研究(II类(59%)和III类(67%),分别)(10]。轻度血液动力学的障碍和相对保存完好的运动公差基准可能减6日治疗效果随钻测量功能的类,以及其他血流动力学参数(肺动脉平均和mRAP)和临床参数(中位数水平以上病人和EQ-5D-5L)。此外,天花板6随钻测量的影响可能在温和的面膜功效PH患者症状高基线6随钻测量[24]。然而,在目前的研究中,Borg 6随钻测量后呼吸困难量表评分明显下降。
selexipag,环前列腺素药物不良事件的发生率特点是高,安全性在这项研究是类似于在其他selexipag在多环芳烃的研究13,25,26]。严重不良事件是有限的,大部分的不良事件是轻度或中度。不良事件的发生率最高剂量范围在400 - 800年间µg·−1,大多数发生在剂量滴定。没有显示不良事件发生率的增加与增加剂量。hypotension-related不良事件的发生率是7.7% selexipag组;然而,事件是温和和解决selexipag治疗没有任何变化。没有观察到不良事件与甲状腺功能障碍。这些发现表明selexipag每剂1600μg每天两次被CTEPH患者安全和耐受性良好。
这项研究有一些局限性。这项研究有一个更短的治疗周期比通常在临床的设置和报道有一个小样本大小。此外,这项研究是在日本进行的。因此,疗效端点除了肺血液动力学的结果需要进一步调查全球更多的患者。我们排除了严重阻塞性肺疾病患者,限制性肺病,中度或严重的肾脏或肝脏疾病和妊娠或可能干扰6随钻测量测试的条件,比如那些并发症如心绞痛或间歇性跛行。
这项研究的结果表明,selexipag耐受性良好,安全,而且提高了肺血液动力学CTEPH病人不能接受豌豆或豌豆后持续或复发性PH值和/或双酚a。没有观察到的运动能力提高。进一步的大规模的调查是必要的证明在CTEPH selexipag所扮演的角色。
补充材料
可共享的PDF
确认
这项研究是由日本Shinyaku有限公司有限公司和詹森制药株式会社研究赞助商参与研究设计、数据收集、统计分析、数据解释和医学写作。作者要感谢学习小组,subinvestigators、研究人员和病人。
脚注
试验注册:日本药品信息中心临床试验信息(JapicCTI: 163279)。去除了识别信息的参与者数据和研究协议将不会被共享。
作者的贡献:k辰:田边,n . Shiota田中s和c山本参与研究设计、数据收集、数据分析和解释。t . Ogo h . Shimokawahara h .木下光男,s . Sakao k .安倍s Matoba h .题材的n . Takama j .赤穗池田y s .约翰h . Maki t的火箭,t . Sugano i Tsujino吉冈k .参与数据收集。所有作者参与开发的手稿,最终批准提交的手稿,并同意负责工作的完整性。
利益冲突:日本Shinyaku有限公司,这个研究小组提供的赠款。t Ogo报告个人费用从日本Shinyaku有限公司有限公司在进行研究;詹森制药株式会社个人费用,Bayer Yakuhin, Ltd, Nippon Shinyaku Co., Ltd, GlaxoSmithKline K.K., Pfizer Japan Inc., and Mochida Pharmaceutical Co., Ltd, outside the submitted work. H. Shimokawahara reports grants from Kaneka Corporation, Bayer Taiwan Co., Ltd, Bayer Yakuhin, Ltd, Daiichi Sankyo Company, Ltd, Japan Lifeline Co., Ltd, Actelion Pharmaceuticals Ltd, Pfizer Inc., and Mochida Pharmaceutical Co., Ltd, outside the submitted work. H. Kinoshita reports grants and personal fees from Nippon Shinyaku Co., Ltd, during the conduct of the study; personal fees from Janssen Pharmaceutical K.K., Nippon Shinyaku Co., Ltd, and Bayer Yakuhin, Ltd, outside the submitted work. S. Sakao reports personal fees from Actelion Pharmaceuticals Ltd, Bayer Yakuhin, Ltd, Daiichi Sankyo Company, Ltd, and Pfizer Japan Inc., grants from the Ministry of Health, Labour, and Welfare of Japan (number 27280401), and Grant-in-Aid for Scientific Research B from the Japan Society for the Promotion of Science (JSPS) (number JP18H03664), outside the submitted work. K. Abe reports grants from Mochida Pharmaceutical Co., Ltd, and Daiichi Sankyo Healthcare Co., Ltd, outside the submitted work. H. Maki reports grants from Bayer Yakuhin, Ltd, and Mochida Pharmaceutical Co., Ltd, outside the submitted work. T. Sugano reports personal fees from Janssen Pharmaceutical K.K., Bayer Holding Ltd, Mochida Pharmaceutical Co., Ltd, Daiichi Sankyo Company, Ltd, Takeda Pharmaceutical Company Ltd, Amgen Inc., Otsuka Pharmaceutical Co., Ltd, Novartis Pharma K.K., and Nippon Shinyaku Co., Ltd, outside the submitted work. I. Tsujino reports grants from Actelion Pharmaceuticals Japan Ltd, Mochida Pharmaceutical Co., Ltd, and Nippon Boehringer Ingelheim Co., Ltd, personal fees from Bayer Yakuhin, Ltd, Janssen Pharmaceutical K.K., Pfizer Japan Inc., and Nippon Shinyaku Co., Ltd, outside the submitted work. N. Tanabe reports personal fees from Nippon Shinyaku Co., Ltd, during the conduct of the study; personal fees from Nippon Shinyaku Co., Ltd, Bayer AG, and Janssen Pharmaceutical K.K., outside the submitted work. K. Tatsumi reports personal fees from Nippon Shinyaku Co., Ltd, Janssen Pharmaceutical K.K., and Actelion Pharmaceuticals Ltd, during the conduct of the study. S. Matoba, H. Motoki, N. Takama, J. Ako, Y. Ikeda, S. Joho, T. Saeki and K. Yoshioka, have no conflicts of interest outside the submitted work. N. Shiota, S. Tanaka and C. Yamamoto are employees of Nippon Shinyaku Co., Ltd.
支持声明:本研究是由日本Shinyaku有限公司有限公司和詹森制药株式会社临床实验的产品是由日本提供Shinyaku有限公司有限公司融资信息本文已沉积的Crossref资助者注册表。
- 收到了2021年6月15日。
- 接受2021年11月4日。
- 版权©2022年作者。
这个版本分布在创作共用署名非商业性许可证的条款4.0。商业生殖权利和权限接触权限在}{ersnet.org