文摘
背景血液生物标志物已广泛描述为潜在的预后标志物特发性肺纤维化(IPF),但研究一直受到使用视阈值分析,调整了混杂因素不一致和一组端点,因此常常屈服ungeneralisable结果。荟萃分析的个体参与者数据(IPD)是一个强大的工具来克服这些限制。通过系统回顾血液生物标志物,充分研究与测量基质金属蛋白酶7 (MMP)被确定促进标准化分析在IPF的预后的潜在生物标志物。
方法电子数据库是2020年11月12日搜索识别前瞻性研究报告未经处理的IPF患者预后,分层根据至少一个预先确定的生物标志物,以基线,或改变超过3个月。IPD是寻求研究调查MMP-7预后因子。主要结果是总体死亡率根据标准化MMP-7 z得分,二级结果的疾病进展在12个月内,所有调整年龄、性别、吸烟和基线用力肺活量。
结果IPD可供九12研究发现,从1664年参与者报告结果。基线MMP-7水平与死亡率增加有关风险(调整风险比为1.23,95%可信区间1.03 - -1.48;我2= 64.3%)和疾病进展(调整或1.27,95%可信区间1.11 - -1.46;我2= 5.9%)。在有限的研究中,三个月改变MMP-7与结果无关。
结论IPD荟萃分析表明,更大的独立基线MMP-7水平与风险增加有关的未经处理的IPF患者预后差,虽然短期变化没有反映疾病进展。
文摘
健壮的方法使用个人参与者的数据分析表明,基线MMP-7水平预测总体死亡率和未经处理的IPF患者疾病进展独立于年龄、性别、吸烟状态和肺功能https://bit.ly/2WlPudQ
介绍
特发性肺纤维化(IPF)是一种原因不明的慢性进行性纤维化肺病影响全世界∼300万人,发病率上升,生存中值诊断∼3年(1- - - - - -5]。疾病轨迹是变量,从缓慢发展到迅速流失,肺功能和死亡(6]。最认可的生物标志物IPF的疾病进展的变化用力肺活量(FVC)在12个月7,8]。然而,肺功能测量的局限性,包括测试的变化与患者的努力有关,干扰的并发症如肺气肿(9]。
血液生物标志物已广泛描述为潜在的预后标志物,反映疾病的严重程度,虽然没有被实现成常规临床实践。生物标志物的研究一直受到小样本大小,不一致的方法包括混杂变量不一致的调整,各种终端使用视生物标志物阈值和分析的结果,因此,往往产生不一致和ungeneralisable结果(10,11]。
个别病人数据(IPD)荟萃分析被认为是黄金标准收集和合成证据,提供优于传统聚合方法,通过支持标准化的分析和结果,一致的调整了潜在的干扰因素和健壮的子群分析根据患者特点(12,13]。没有发表的研究利用IPD系统合成血液生物标志物在IPF的证据。通过系统回顾血液生物标志物,充分研究与测量基质金属蛋白酶7 (MMP)被确定促进标准化分析在IPF的预后的潜在生物标志物。因此,我们探索MMP-7以基线之间的联系和变化超过3个月,和临床终端包括死亡率和疾病进展在成人未经处理的IPF患者。
方法
系统进行了审查按照预先确定的协议(普洛斯彼罗注册号:CRD42019120402),据报道使用PRISMA-IPD(首选项报告个人参与者的系统回顾和荟萃分析数据)指南(14]。
选择搜索策略和研究
电子数据库的搜索进行了MEDLINE(1946最新),Embase(1974最新),谷歌学者,对照试验和ClinicalTrials.gov Cochrane中央登记,最后搜索2020年11月12日进行。关键字和受控词汇表术语“特发性肺纤维化”和“生物标记”,与预后研究搜索过滤器被应用(补充图S1)[15]。手搜索文章进行检索的参考列表来确定进一步的研究。未发表的和正在进行的研究发现通过搜索预印本服务器包括medRxiv bioRxiv和威康开放研究。搜索后,前两个评论者独立筛选通过标题和摘要全文回顾。有分歧的共识解决第三个审稿人。
审查包括所有原始前瞻性观察性研究报道结果稳定或加剧antifibrotic天真IPF患者> 18岁,诊断根据同期共识指南(16- - - - - -18根据至少一个突变),分层血液生物标志物。会议摘要报告为包括足够的细节都有资格。回顾性研究、病例报告、动物实验和研究调查non-IPF间质性肺病(ILD)被排除在外。语言或一年出版的限制并不适用。没有为包含指定最小样本量的研究。
研究报告以下生物标记测量基准和/或趋势/ 3个月资格审查:生物标记上皮功能障碍(MMP-7克雷布斯·冯·窝Lungen-6,表面活性剂蛋白质a - d,金属蛋白酶- 1、癌抗原125 (ca - 125),碳水化合物抗原胜负,血管内皮生长因子和胰岛素样生长因子结合蛋白2);生物标记的细胞外基质造型(胶原蛋白合成肽、neoepitopes lysyl oxidase-like 2, periostin和骨桥蛋白);和生物标记物的免疫失调(主题趋化因子ligand-18,趋化因子配体13日interleukin-8,热休克蛋白70,chitinase-3-like蛋白1 (YKL40)和胞内粘附molecule-1)。
数据提取和risk-of-bias评估
IPD是寻求相应的作者研究调查MMP-7预后因子,使用安全,加密的电子邮件通信。至少三个提醒发送,每4周。赞助的临床研究的数据要求通过各种门户网站(www.clinicalstudydatarequest.com,www.vivli.org,https://yoda.yale.edu)。请求的数据包括参与者人口结构(年龄、性别、吸烟状态和肺功能基线),基线和3个月MMP-7水平和成果包括12个月的肺功能和总体死亡率(补充图S2)。
IPD并不可用,聚合数据提取研究出版物使用形式发票,并验证了第二个审稿人。数据包括研究设计、参与者和生物标志物特征和结果数据包括样本大小,平均值和标准偏差的生物标志物在个人,没有事件。比较数据收集使用调整风险比率(人力资源)报道。
Risk-of-bias评估是由两个独立评论员在预后研究(讽刺)使用质量工具(19]。俏皮话工具评估偏差的风险在六个领域:研究参与,研究磨损,预后因子的测量,测量结果,研究混杂和统计分析和报告。所有研究都包括在审查无论偏见的风险评级。年级(分级的建议,评估,开发和评估)框架应用于利率的总体质量证据为每个结果(20.]。
统计分析
识别的研究都是包含在数据合成、汇总表的研究特点。多个组在相同的研究被视为个人军团。主要结果是总体死亡率。二次结果措施包括改变比例预测FVC在12个月内从基线及疾病进展定义为10%的相对衰落FVC或死亡在12个月内的基线。MMP-7水平在预测死亡率风险比率,优势比预测疾病进展与随机效应估计使用两级IPD荟萃分析和提出了森林的阴谋。估计被调整的先天的混杂因素包括年龄、性别、吸烟史和基线FVC。未经调整的分析介绍补充材料(补充图S10)。研究随访时间> 3年被审查的生存分析。标准化在研究生物标记值,z得分特定于每个研究计算和分析了风险变量。MMP-7超过3个月的变化进行了计算,使用相对百分比变化从基线。参与者使用listwise删除与缺失的数据被排除在外。我的2数据被用来评估统计研究之间的异质性。多元回归进行了充分的研究包括探索可变性在异质性根据研究设计(队列与同行评议的手稿,随机试验),只有研究测定(ELISA方法与non-ELISA)和使用的血液样本类型(血清与等离子体)。发表偏倚评估使用漏斗图分析和食叶蛾的测试21]。所有统计分析使用占据16(美国StataCorp、大学城、TX)。由于方法论上的异质性,明显不同的结果为IPD措施和研究不足,生物标志物MMP-7以外的其它故事体地描述在表。
结果
2020年11月12日电子数据库的搜索了4930篇文章,69年进一步研究确定通过预印本服务器。删除重复后,筛选和全文审查,29日发表的研究包括2007年和2020年之间,全球报告结果从3950年IPF参与者(图1)。12项研究报告结果与MMP-7, IPD是用于9(75%)的研究,从11个人组和1664个参与者报告数据(表1)。没有发现问题IPD的完整性。15血液生物标志物进行评估纳入研究的特征,与一些生物标记物的研究评估组合(补充表S1)。
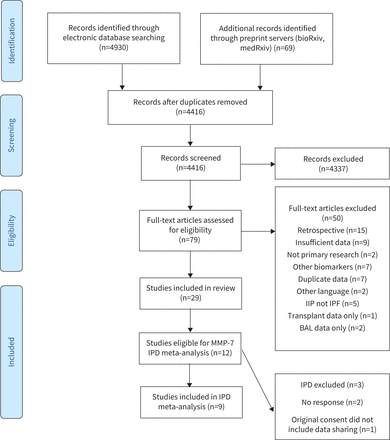
流程图说明系统的搜索和筛选策略,包括数量的研究会议合格标准和数字排除在外。MMP:基质金属蛋白酶;IPD:个人参与者的数据;国际信息局:特发性间质性肺炎;IPF:特发性肺纤维化;拜尔港:支气管肺泡灌洗。
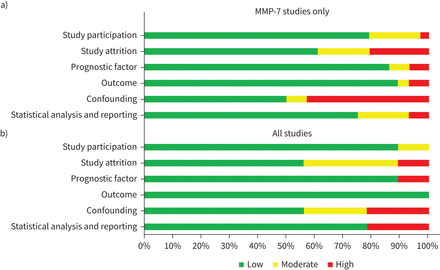
Risk-of-bias评估检索研究确定的局限性和一些可能的偏见(图2,补充表S2)。研究包括在MMP-7荟萃分析,发表偏倚没有发现统计学,但目测烟囱的情节暗示发表偏倚在场的一些结果评估(补充数据S3和S4)。大多数MMP-7研究定义了研究人口特别清楚包含/排除标准。生物标记物测定一直使用相同的示例矩阵(血浆或血清)包括参与者在每个研究中,尽管试验平台用于测量分析物的细节经常被报道。结果数据客观地测量和应用到所有参与者。研究评估MMP-7以外的生物标记物有类似的局限性和风险的偏见。血液生物标志物,受年龄和性别的影响,以及可能的生活方式因素,如吸烟,而随着基线肺功能都是混杂因素在疾病的结果(22]。在大约一半的包括研究中,可能的混杂因素没有测量,有不一致的测量调整在接受了混杂因素的估计。此外,在许多研究中,分析使用数据相关生物标志物在研究阈值是不一致的。
偏见的风险评估的)基质金属蛋白酶7 (MMP)的研究;b)包括所有研究项目。偏见的风险在研究被评为低,中等或高六个类别使用预后研究质量工具。
血液生物标志物和临床结果之间的联系
基线血液生物标志物预测死亡率
10个研究评估死亡率和MMP-7之间的关系,与IPD可供8个研究总计1492名参与者。荟萃分析表明,大基线MMP-7价值观总体死亡率的风险增加23%(每标准偏差1.23 (a)人力资源调整增加,95%可信区间1.03 - -1.48;我2= 64.3%)(图3一),尽管有大量的统计学异质性无法解释的可变性因素评估(补充表S3)。死亡率在12个月检查时,基线MMP-7水平非决定性地和死亡联系在一起(1.33标准差气道高反应性的增加,95%可信区间0.99 - -1.78;我2= 59.6%)(图3 b)。应用级的框架,我们的信心死亡率估计中确定(补充表S4)。在IPD用时,MMP-7值> 5.7 ng·毫升−1与死亡率增加有关(aHR 2.18, 95% CI 1.1 - -4.32)的平均随访19个月接受研究的438名参与者(23]。57参与者的进一步研究发现,MMP-7水平并未预测死亡(24)(补充表S5)。
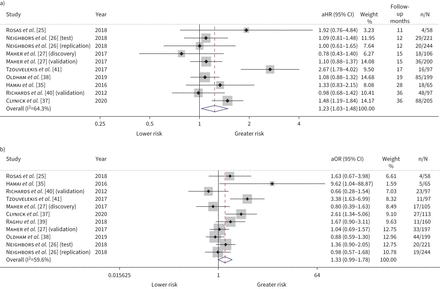
死亡森林的阴谋。一)总体死亡率;b)在12个月内死亡率。调整效应大小每标准偏差95%置信区间增加metalloproteinase-7基准矩阵。aHR:调整风险比;优势:调整后的优势比。估计都是调整年龄、性别、吸烟状况和基线用力肺活量。从随机影响模型权重。
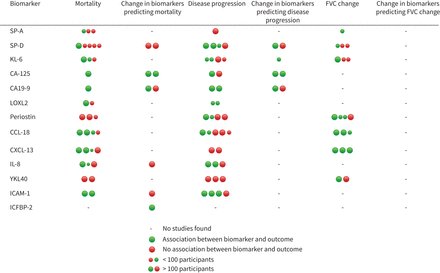
死亡率的主要结果评估进一步14生物标记共有17项研究没有在IPD荟萃分析评估,不一致和不确定的结果(图4和补充表S5)。研究随访时间不一致,与广泛的置信区间效应大小不同,估计通常是未经重要的协变量。
研究结果的总结。每个点代表一项研究(或单独的队列研究的多个队列)。FVC:用力肺活量;SP:表面活性剂蛋白质;吉隆坡:克雷布斯·冯·窝这;ca - 125:癌抗原125;CA19-9:碳水化合物抗原胜负;LOXL: lysyl oxidase-like;三地:主题趋化因子配体;CXCL:趋化因子配体; IL: interleukin; YKL40: chitinase-3-like protein 1; ICAM: intracellular adhesion molecule; IGFBP: insulin-like growth factor binding protein.
生物标记物预测死亡率的变化
三项研究总计498名参与者探讨MMP-7随3个月变化和死亡率之间的关系(25,26]。IPD荟萃分析显示没有与死亡率(aHR 1.00, 95%可信区间0.99 - -1.02;我2= 53.3%),也不是死亡率审查时12个月(优势比为1.00,95%可信区间0.99 - -1.01;我2= 37.4%)(补充图S5和S6)。
三个出版物从同一队列评估纵向测量生物标志物和死亡率之间的关系(27- - - - - -29日]。发现和验证军团,ca - 125 / 3个月上升,死亡的风险增加了一倍,但其余的生物标志物没有预测死亡率(图4和补充表S6)。验证的145名参与者演示复制上升neoepitopes退化的基质金属蛋白酶(C1M、C3M C6M和CRPM),但胶原蛋白合成肽的变化率与死亡率[无关29日]。
基线预测疾病进展和变化FVC的生物标志物
10个研究测量MMP-7水平作为疾病进展的标记,与八个研究总计1383名参与者包括在IPD荟萃分析。荟萃分析表明,基线MMP-7与疾病进展(优势比1.27标准差增加,95%可信区间1.11 - -1.46;我2= 5.9%)(图5)。异质性低时,多元回归确定样本(ELISA检测技术与其他)是一种异质性的来源。在亚组分析根据分析,疾病进展的优势比是估计每标准差增加1.56 (95% CI 1.26 - -1.82;我2= 0%)当仅限于研究使用ELISA (补充图S7)。当基线MMP-7之间的关系和相对变化FVC在12个月检查尤其是6研究的891名参与者,荟萃分析表明,1sd大基线MMP-7有关−0.85%在12个月的比例相对变化预测FVC (95% CI 1.65−−0.05%;我2= 0%)(图6)。我们评估发现疾病进展和变化FVC确定性高的结果(补充表S4)。研究不包括在IPD荟萃分析,基线MMP-7值> 3.8 ng·毫升−1气道高反应性疾病进展的风险增加了一倍(2.2,95% CI 1.4 - -3.7)在19个月的中位随访211名参与者(30.]。57岁的进一步研究参与者,MMP-7没有预测疾病进展(补充表S7)。
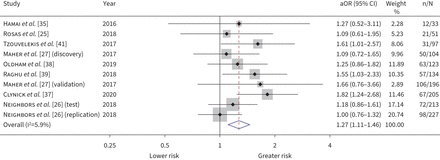
疾病进展森林阴谋。集中调整优势比(aOR)为95%的置信区间为疾病进展的风险,每metalloproteinase-7标准差增加基准矩阵。估计都是调整年龄、性别、吸烟状况和基线用力肺活量。从随机影响模型权重。
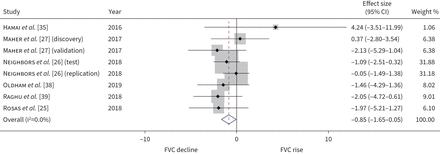
相对百分比变化预测用力肺活量(FVC)森林的阴谋。混合效应的大小和95%置信区间FVC % pred相对变化在12个月里,每metalloproteinase-7标准差增加基准矩阵。估计都是调整年龄、性别、吸烟状态和基线FVC。从随机影响模型权重。
疾病进展评估的其他生物标志物在19研究并不包括在IPD荟萃分析。没有一致的预测疾病进展,尽管采用的定义有显著的异质性疾病进展,与肺功能指标、死亡率、移植和急性加重包括在各种组合nonunified时间点(图4和补充表S7和S8)。
生物标记物预测疾病进展的变化
三项研究共计481人参加调查MMP-7变化超过3个月和疾病之间的关系发展是包括在IPD荟萃分析。改变MMP-7超过3个月没有与疾病进展相关(aOR每增减百分比1.00,95%可信区间0.99 - -1.01;我2= 22.5%)(补充图S8),也不改变FVC超过12个月(效果增加MMP-7比例每增加0.01%,95% CI 0.07−-0.08;我2= 60.8%)(补充图S9)。211年一项研究的参与者不包括在IPD荟萃分析,改变了1/2 MMP-7 / 4个月与疾病进展的风险翻倍(30.]。
在一项研究中,参与者与进步疾病ca - 125浓度上升了3个月相比,那些有稳定的疾病,但没有复制其他生物标志物的关系(27)(图4,补充表S9)。
讨论
这个系统的未经处理的IPF患者的前瞻性研究确定了16种血液生物标志物和评估六个结果变量,但只有充分研究进行一个MMP-7 IPD荟萃分析。IPD荟萃分析表明,基线MMP-7水平预测全因死亡率和疾病进展和相关比例预测FVC变化超过12个月。有23%的更大风险的总体死亡率和27%每标准偏差大的疾病进展风险增加基线MMP-7值。无果协会观察12个月死亡率的风险。值得注意的是,MMP-7水平似乎没有改变纵向超过3个月,观察到任何没有联系的测量结果。然而,不包括在定量合成的一项研究表明,在那些MMP-7确实上升,可能会有一个相关的进展的风险(30.]。死亡率与温和的确定性和疾病进展和成果被评为改变FVC确定性高的结果(补充表S4)。
我们IPD荟萃分析代表第一次有可能合成在IPF血液生物标志物的发现。荟萃分析是集中在MMP-7有足够可用的研究;然而,这些已经产生了不一致的结果,单独报道视阈值,通常没有调整了混杂因素。IPD启用分析MMP-7水平连续变量转换为z分数来克服试验可变性和支持标准化的定义和一致的结果调整重要的协变量,使健壮和可靠的结论。我们进行两级IPD荟萃分析,不评估研究估计,同时影响,虽然它被认为是产生无偏估计(31日),使造型IPD从1492名参与者在单独的安全服务器和门户。分析异质性在IPD荟萃分析表明,试验类型是异质性的重要因素,特别是在疾病进展的估计。
有限制审查。虽然没有语言限制应用,两篇文章在日本被排除在外,因为他们无法评估入选标准翻译成英语。我们只包括那些研究参与者被诊断根据国际共识指南,支持我们的研究结果的鲁棒性和generalisability。我们排除了研究特发性间质性肺炎不是特定于IPF,这限制了解释在non-IPF ILDs,尽管正在进行研究探索共享机械化的途径将提供进一步的见解32]。此外,通过专注于未经处理的IPF患者,我们的结果不解决theranostic MMP-7与antifibrotic治疗的价值。有显著统计学异质性的一些结果,因此这些进行解释时应特别谨慎。我们无法解释所有剩余异质性使用我们评估的因素。IPD并非来自有限数量的合适的研究,因此我们必须报告这些发现故事体地。
生物标志物的疾病活动有可能促进临床管理和转换早期阶段临床试验作为代理端点。不正常的上皮细胞分泌导致纤维发生的profibrotic介质包括基质金属蛋白酶(33),负责降解细胞外基质的多个组件,激活生物介质和促进epithelial-mesenchymal过渡(34]。进一步的研究可以阐明IPF药物治疗和MMP-7之间的关系,尤其是确定MMP-7水平变化可能代表治疗反应的生物标记。从临床的角度来看,MMP-7实施应考虑作为预后的诊断工具,特别是在肺功能测试是笨重的或不可用。
由于非均质性研究设计和报告结果,non-MMP-7有足够的数据进行定量分析研究。虽然许多生物标志物显示死亡率在单一的研究有一定的联系,复制的影响研究是薄弱。我们强调的来源相当大的偏差和可变性。通常是观察性研究,相对温和的大小与缺乏预先确定的功率计算。许多不同的实验室技术应用于测量生物标志物水平的研究,很少有研究报告详细的试验信息,特别是关于精度的措施,和阈值定义积极和消极的生物标志物有不一致的结果。生物标志物浓度超过3个月的短期变化往往与指定的临床结果,表明需要进一步的研究这些生物标志物可以采用临床。进一步的生物标志物研究应该关注严格设计纵向研究与发现和验证组,使用验证生物标志物检测和标准化的端点。此外,生物标记的组合可能会增加粒度对我们理解IPF发病和预后,需要进一步研究评估他们的效用。作为进一步的研究发表,IPD荟萃分析应该考虑和支持generalisability产生更可靠的结果。
总之,而其他一些血液生物标志物研究了预测预后,目前不足的复制,使进入临床试验,采用MMP-7可能是个例外。我们健壮的方法和IPD荟萃分析应用于演示基线MMP-7水平预测总体死亡率和未经处理的IPF患者疾病进展独立于年龄、性别、吸烟状况和肺生理。然而,MMP-7超过3个月的短期变化提供有限的预后价值缺乏实证的阈值。
补充材料
可共享的PDF
确认
这份出版物是基于研究使用数据从数据贡献者勃林格殷格翰集团和Genentech公司已经通过Vivli, Inc . Vivli没有导致或批准,并没有以任何方式负责,这个刊物的内容。勃林格殷格翰集团是有机会审查的抽象医学和科学的准确性,以及知识产权方面的考虑。这从赛诺菲通过出版还使用数据ClinicalStudyDataRequest.com。研究使用这些数据的解释和报告是完全的责任作者,不一定代表ClinicalStudyDataRequest.com或赛诺菲的官方观点。作者还要感谢以下个人的宝贵的支持提供个别病人数据:Hiroshi Ivamoto(广岛大学、日本),Naftali来说卡明斯基(美国耶鲁大学医学院),玛格丽特的邻居(美国Inc . Genentech),贾斯汀·奥尔德姆(美国加州大学),Ganesh拉(美国华盛顿大学医学中心),伊凡罗(美国布莱根妇女医院),Argyrios Tzouvelekis(亚历山大·弗莱明生物医学科学研究中心、希腊)和张迎泽(美国匹兹堡大学)。
脚注
普洛斯彼罗注册号:CRD42019120402
利益冲突:粮农组织的汗没有披露。
利益冲突:即斯图尔特没有披露。
利益冲突:g·赛没有披露。
利益冲突:·罗宾逊没有披露。
利益冲突:R.G.詹金斯报告个人费用从生原体,加拉帕戈斯群岛,葛兰素史克,Heptares,落实勃林格殷格翰的发言,顺从,罗氏/ InterMune,落实PharmAkea,百时美施贵宝公司,基耶西,罗氏/ Promedior Veracyte;从生原体和研究经费支付给他们的机构,Galecto,葛兰素史克和落实;从RedX和北欧的生物科学合作奖;是NuMedii的顾问委员会成员,所有外提交工作;还支持由国家卫生研究所的教授(NIHR裁判:rp - 2017 - 08 - st2 - 014),是肺纤维化的受托人采取行动。
支持声明:粮农组织支持的汗和i . Stewart诺丁汉国家卫生研究所(NIHR)生物医学研究中心。R.G.詹金斯支持NIHR研究教授(rp - 2017 - 08 - st2 - 014)。资金信息,本文已沉积的Crossref资助者注册表。
- 收到了2021年6月7日。
- 接受2021年8月21日。
- 版权©2022年作者。
这个版本分布在Creative Commons归因执照的条款4.0。