摘要
在COVID-19患者中,呼吸衰竭与全身血压升高有关,这可能是由于SARS-CoV-2感染对肾素-血管紧张素-醛固酮系统的调节https://bit.ly/3cINsHB
致编辑:
2019冠状病毒(COVID-19)是由严重急性呼吸综合征-冠状病毒-2 (SARS-CoV-2)引起的疾病,从中国扩展到世界各地。COVID-19主要表现为低氧正常-低碳酸血症伴保留肺顺应性[1]。在缺乏靶向治疗的情况下,亚重症临床医生支持患者使用无创通气和抗炎/抗病毒药物等待病情改善。血管紧张素转换酶(ACE)2是SARS-CoV-2刺突蛋白的结合位点,在肺、心脏、肾脏和胃肠道细胞外膜上高度表达[2]。ACE2被认为是肾素-血管紧张素-醛固酮系统(RAAS)的对应物,将血管紧张素(Ang) II转化为Ang-(1-7)和Ang I转化为Ang-(1-9)。ACE2活性诱导血管扩张,减少细胞生长和炎症反应。在模拟病毒性急性呼吸窘迫综合征的实验模型中,缺乏Ace2导致炎症、血管通透性和肺损伤通过Ang II通路的激活[3.,4]。SARS-CoV-2导致ACE2活性下降,可通过加剧ACE产物作用的不平衡来释放一系列有害影响与ACE2。转到临床环境,ACE2下调可能是维持动脉高血压的途径之一[5]及肺动脉高压[6]。因此,可以想象,在COVID-19中,膜ACE2的切割及其循环水平可能会影响疾病进展和临床恶化[7]。因此,为了支持ACE2的病理生理作用,本报告分享了一项观察性研究的临床数据,该研究对40名确诊为COVID-19的患者进行了研究,这些患者在意大利米兰的Fondazione IRCCS Ca' Granda Policlinico医院的心肺亚重症COVID-19病房住院。
连续招募了40名COVID-19患者。当时,标准化治疗是羟氯喹和洛匹那韦/利托那韦。血压、动脉氧张力/吸气氧分数(PaO2/FIO2)和肺泡-动脉氧张力差(P一个——一个O2)根据标准临床方案每天测量2 - 4次。血浆钾浓度中位数([K+]等离子体)也进行了评估。在任何情况下,补充钾,或管理矿物皮质受体拮抗剂或利尿剂,[K+]等离子体我们认为是在药物干预前转介的。呼吸和血液动力学变量之间的关系,即P。一个——一个O2与平均BP由Poon的分析评估,这使我们能够标准化个体间的变异性[8]。在住院28天后评估死亡和有创通气的综合情况。
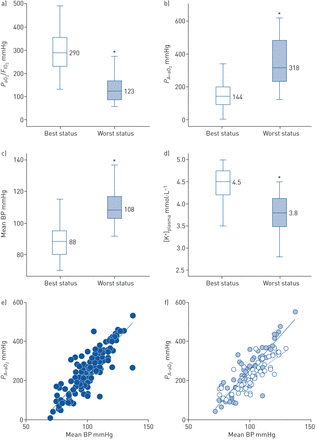
平均年龄64±11岁,40例患者中29例男性。所有患者心功能正常,但1例心衰稳定,射血分数降低。尽管只有23例患者存在高血压病史(preHT),但所有患者,尽管在优化的无创通气治疗(最佳FIO2和正呼吸终末压),显示退化PaO2/FIO2和P一个——一个O2同时伴有血压升高和[K+]平均下降等离子体(图1一个- d)。中位数(K +)等离子体为3.8 mmol·L−1。导致临床影像阴性的中位时间为4.25天。根据血流动力学和呼吸变化,将患者分为1组(8/40例,preHT组4/8例)和2组(32/40例,preHT组15/32例)。第1组表现为暂时性向高血压方向波动,肺功能发生相反变化(最佳)与糟糕的状态:PaO2/FIO2= 311与130毫米汞柱;P一个——一个O2= 107与312毫米汞柱;意味着英国石油(BP) = 83与89毫米汞柱)。28天后,这些患者表现出更好的结果,即。即使在需要有创通气支持后(2例),也无死亡和临床改善。2组患者病情危重(最佳状态:PaO2/FIO2= 286毫米汞柱;P一个——一个O2= 158毫米汞柱;平均血压=88 mmHg)。患者临床状况迅速恶化,血压呈线性升高,换气进行性恶化(最糟糕状态:PaO2/FIO2= 122毫米汞柱;P一个——一个O2= 364毫米汞柱;平均血压=111 mmHg)。图1 e之间的正相关P一个——一个O2平均BP(斜率=6.666,R2= 0.757;p < 0.0001)。根据我们的假设,[K+]等离子体被认为是RAAS激活的标志,在第2组中,3.8 mmol·L−1用于对患者进行分层。的斜率P一个——一个O2[K+]组/平均BP值关系显著(U-test p<0.001)陡峭。等离子体< 3.8更易·L−1(图1 f).28天后,与第1组相比,第2组的患者在很短的时间内(6.1天)有更高的重症监护需求(32人中有6人)和更高的死亡率(32人中有16人)。截至2020年4月12日,其余10例患者仍存活或出院。
a)氧和吸气含氧比例,b)肺泡-动脉含氧梯度,c)平均血压(BP)和d)血浆钾水平([K+]等离子体).通过Mann-Whitney U-test比较最佳状态和最差状态,结果有统计学意义。*: p < 0.001。e) Poon对P一个——一个O2/mean BP: n=137,斜率=6.666,R2= 0.757;p < 0.0001。f) Poon对P一个——一个O2/根据[K+]的平均BP等离子体地层。(f)中淡蓝色圆点表示[K+]的组等离子体≤3.8更易·L−1(n = 78;斜率= 6.686,R2= 0.774;p<0.0001),白点表示[K+]等离子体> 3.8更易·L−1(n = 59;斜率= 4.491,R2= 0.670;p < 0.0001)。PaO2:动脉血氧张力;FIO2:吸气氧分数;P一个——一个O2:肺泡-动脉氧张力差。
我们的研究结果表明,在COVID-19中,肺功能的退化可能与血压升高有关。虽然COVID-19主要被称为呼吸系统疾病,但它似乎逐渐演变为导致血流动力学不稳定的血管疾病。有证据表明,SARS-CoV-2破坏了ACE2驱动的血管舒张调节[7,9],我们间接记录了RAAS激活监测[K+]等离子体的变化。事实上,由于SARS-CoV-2与RAAS相互作用,COVID-19的低钾血症尤其令人担忧[10]。根据[K]+]等离子体而血压变异性,醛固酮上调可能是导致预后不良的致命机制之一。醛固酮是一种有效的小动脉血管收缩剂,直接作用于盐和水的潴留,以及炎症[6]。考虑到血压升高反映了ACE2耗竭引起的全身血管收缩,通气死区(P一个——一个O2)可能是肺血管张力改变导致血流重新分配的表现。的确,在稳定的情况下,缺氧肺血管收缩具有生理保护作用,允许灌注引导血液流向功能保存的肺区域[11]。当COVID-19达到一定阶段时,会出现不成比例的内皮损伤,破坏肺血管调节,促进通气-灌注不匹配(初始低氧血症的主要原因),并促进血栓形成[12]。总的来说,有待进一步验证的证据表明,COVID-19患者抵抗RAAS渐进式激活的能力较差。一旦COVID-19进展和ACE2减少,AngII/ATR1平衡失衡可能对心血管系统有效。在第1组中,某种生理或药理平衡恢复了最佳状态。在第2组中,疾病的极端严重程度导致了最坏的结果。血流动力学变化越快,COVID-19综合征的严重程度越高。重组人- ace2的试验结果仍在等待中(clinicaltrials.gov标识符NCT04335136), COVID-19患者可能受益于已知的内皮活性药物,即。ace抑制剂,血管紧张素II -i型受体阻滞剂或矿物皮质激素受体拮抗剂。
可共享的PDF
脚注
利益冲突:M. Vicenzi报告来自Janssen-Cilag SpA和MSD Italia的个人费用,在提交的工作之外。
利益冲突:R. Di Cosola没有什么可透露的。
利益冲突:M. Ruscica没有什么可透露的。
利益冲突:A.拉蒂没有什么可透露的。
利益冲突:一、罗塔没有什么可透露的。
利益冲突:F.罗塔没有什么可透露的。
利益冲突:V. Bollati没有什么可透露的。
利益冲突:S. Aliberti报告了来自拜耳医疗保健、Aradigm公司、Grifols、INSMED和Chiesi的资助和个人费用,以及来自阿斯利康、巴西利亚、Zambon、诺华、Raptor、Actavis UK Ltd和Horizon的个人费用。
利益冲突:F. Blasi报告了来自阿斯利康、基耶西、GSK、Insmed和辉瑞的资助和个人费用,来自拜耳的资助,来自Guidotti、Grifols、Menarini、Mundipharma、Novartis和Zambon的个人费用,在提交的工作之外。
- 收到了2020年4月13日。
- 接受2020年5月13日。
- 版权所有©ERS 2020
本版本根据知识共享署名非商业许可4.0的条款发布。