亲爱的编辑,
慢性阻塞性肺疾病(COPD)患者有更高的患严重疾病和死亡的风险后严重急性呼吸道冠状病毒2 (SARS-COV-2)感染[1]。疫苗接种预防冠状病毒疾病2019 (COVID-19)通过系统性的发展和气道免疫反应。COPD患者显示改变体液免疫,降低抗体反应与健康对照组相比(HC) [2,3]。我们研究SARS-COV-2疫苗特异性免疫反应在慢性阻塞性肺病患者与HC,使用系统性,鼻和痰液样本。
从3主题组织样本进行了分析;27日接种对象(慢性阻塞性肺病11和16个HC),使用疫苗前43个科目(24慢性阻塞性肺病和19个HC)和9 HC COVID-19感染史。接种对象捐赠样本> 2周后完成两个剂量的Vaxzevria (Oxford-AstraZeneca;5 COPD患者和9 HC)或Comirnaty(辉瑞公司;6 COPD患者和7 HC)样品;所有受试者提供血液和鼻样本,而10 COPD患者和9 HC也提供了痰。所有受试者年龄> 40年,慢性阻塞性肺病患者年龄超过HC(平均年:66.1与58.8,p = 0.04),类似的性别混合(意思是%男:55与50)。慢性阻塞性肺病患者黄金2级(n = 9)或三年级(n = 2), 10人。所有的受试者没有COVID-19的历史,由一个等离子体抗体阴性结果SARS-COV-2核衣壳蛋白(4]。Pre-vaccination样本来自两个人群:1)慢性阻塞性肺病患者痰(n = 22)和HC (n = 10)和等离子体慢性阻塞性肺病患者(n = 13)和HC (n = 12),有一些科目捐赠两样品。这些收集和冷冻前流行;2)血液和鼻样本收集的流感大流行期间从六个未接种疫苗的受试者(慢性阻塞性肺病:n = 2;HC: n = 4)细胞免疫和免疫球蛋白的分析。HC (n = 9) PCR-proven之前COVID-19疫苗接种史捐献的血液(n = 6)和鼻样本(n = 9);在抽样,8收到一剂疫苗(4 Vaxzevria和4 Comirnaty)。主题报道在2周内没有急性呼吸道疾病的样本集合。慢性阻塞性肺病患者吸烟史> 10包年,FEV1< 80%预测,FEV1/ FVC比< 0.7。HC肺功能正常,没有呼吸系统疾病,吸烟史< 1包,不吸烟者。
Heparinised血液收集细胞免疫评估和等离子体的免疫球蛋白的评估。吸鼻,鼻上皮衬里流体(NELF),收集和处理(如前所述)来测量免疫球蛋白后COVID-19 [5]。痰液浮在表面的处理没有二硫苏糖醇,如前所述[6]。Anti-SARS-COV-2飙升IgA在等离子体和免疫球蛋白水平,NELF和痰上层清液定量衡量ELISA (AESKU, Wendelsheim,德国)。等离子体,提供的标准,准备在plasma-like矩阵,使用,而重组anti-spike IgA和免疫球蛋白抗体(本地抗原公司,牛津大学,英国)准备在PBS包含1%牛血清白蛋白和0.05% Tween-20 (Sigma-Aldridge,普尔,英国)是用于NELF和痰上层清液。anti-SARS-COV-2核衣壳蛋白抗体的存在在等离子体被罗氏Elecsys定性分析检查,报告为积极或消极的(医生实验室,英国伦敦)。高峰protein-induced IFNγ血t细胞(细胞免疫)评估使用Euroimmun Quan-T-Cell化验(德国吕贝克)。结果分析利用Mann-Whitney和斯皮尔曼等级测试,使用GraphPad 9.2.0棱镜版本。
接种疫苗的COPD患者和HC anti-spike IgA和免疫球蛋白水平较高在等离子体和anti-spike痰COPD患者比未接种疫苗和免疫球蛋白水平HC (图1一个和b)。痰anti-spike疫苗接种后IgA水平并不高。
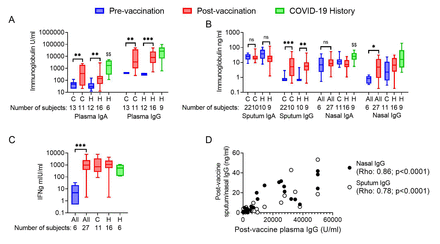
免疫反应在慢性阻塞性肺病患者和健康对照组SARS-COV-2疫苗接种或COVID-19感染。Anti-spike IgA和免疫球蛋白水平测量等离子体(a)和(b)由ELISA痰和鼻样本。(c)在血液细胞免疫是评估通过测量峰值protein-induced IFNγELISA。Pre-vaccination结果颜色蓝色,接种后在红色和科目COVID-19绿色的历史。预处理和接种后水平比较Mann-Whitney测试:* p < 0.05;* * p < 0.01;* * * p < 0.001;ns:非标准。比较接种后,由Mann-Whitney Covid-19感染水平测试:$ $p < 0.01。(d)之间的相关性post-vaccine等离子anti-spike免疫球蛋白水平post-vaccine痰和鼻腔免疫球蛋白水平被斯皮尔曼等级测试评估ρ并假定值报告。缩写:C:慢性阻塞性肺病样本;H:健康对照组样本;:合并慢性阻塞性肺病和健康的样本。
对细胞免疫和鼻分析,我们使用疫苗前合并慢性阻塞性肺病和HC结果由于有限的样本(n = 6);接种疫苗的受试者高血液细胞免疫突起蛋白反应和鼻anti-spike免疫球蛋白水平,但不是鼻anti-spike IgA的水平,比未接种疫苗的受试者(图1 b和c)。类似的诱发的免疫反应相比,慢性阻塞性肺病患者观察HC。合并慢性阻塞性肺病和HC的结果,等离子体(27 530与2391 U ml−111.0,p = 0.005)和鼻与2.6 ng毫升−1后,p = 0.03)免疫球蛋白水平高接种Comirnaty Vaxzevria相比,具有相似的趋势(与)等离子体IgA (231.5与73.4 U ml−1,p = 0.056)和痰液免疫球蛋白(17.9与3.6 ng毫升−1,p = 0.052)。疫苗接种和样本收集相似之间的时间Comirnaty和Vaxzevria(意味着分别为97和100天,p = 0.9)。免疫反应之间的类似慢性阻塞性肺病和HC疫苗,当独立分析。
Post-vaccine鼻和痰anti-spike免疫球蛋白水平与血浆免疫球蛋白水平(图1 d)。Induced-IgG和细胞免疫水平负相关疫苗接种和样本收集之间数量的天(范围:17 - 168天)(ρ:等离子体免疫球蛋白:−0.58;鼻腔免疫球蛋白:−0.50;痰液免疫球蛋白:−0.60和细胞免疫:−0.52,所有p≤0.01)。也出现了类似的趋势(与)对等离子体IgA(ρ:−0.34,p = 0.08)。任何免疫反应之间没有明显的相关性,年龄对慢性阻塞性肺病患者或HC。
在HC COVID-19的历史,和一个疫苗接种剂量,anti-spike IgA在等离子体(1719水平更高与138.6 U ml−1(25.5,p = 0.006)和鼻样本与7.2 ng毫升−1HC接种后相比,p = 0.003),而等离子体和鼻anti-spike免疫球蛋白水平和细胞免疫反应是相同的。
我们提供新颖的结果关于肺免疫反应COVID-19接种疫苗,包括慢性阻塞性肺病患者的反应。疫苗接种引起肺免疫球蛋白与系统性免疫球蛋白相关反应的反应。慢性阻塞性肺病体液和细胞免疫反应是类似于HC,提供保证当前疫苗导致所需的免疫反应在慢性阻塞性肺病,尽管存在免疫失调(7]。
我们报告之间的强相关性系统性鼻和痰液接种疫苗后免疫球蛋白水平。这表明,气道免疫球蛋白来源于等离子转导后,也为系统性报道流感疫苗诱发鼻免疫球蛋白(8]。虽然系统性anti-spike IgA水平高接种疫苗样本,肺部和鼻子没有水平,表明转导的缺失。Comirnaty诱发鼻anti-spike IgA [915天内的第二次疫苗接种,水平耗尽(3个月内9]。我们的样品收集在一段时期内,或许解释缺乏鼻IgA反应观察。早期鼻IgA也依赖疫苗的反应,Corona-vac不诱导响应9]。诱发粘膜免疫球蛋白持续时间比IgA [10),这反映了我们的鼻和痰液免疫球蛋白的结果。
Comirnaty被诱导系统性anti-spike免疫球蛋白高于Vaxzevria [11),我们也观察到等离子体和呼吸道样本。类似比例的慢性阻塞性肺病和HC收到了两种疫苗。
气道anti-spike IgA SARS-COV-2感染后当地生产的水平,与anti-SARS-COV-2 IgA COVID-19患者在支气管发现吸入物(12]。我们观察到更高水平的NELF anti-spike IgA在HC SARS-COV-2感染+接种疫苗相比,疫苗接种史。与系统性流感疫苗接种,活性疫苗引起持续粘膜IgA反应(13]。活性SARS-COV-2疫苗在发展可能引起类似IgA反应(14]。分泌IgA水平减少航空公司的严重慢性阻塞性肺病患者,IgA应对鼻疫苗应评估在这些慢性阻塞性肺病患者。吸烟会损害呼吸道IgA生产(15),但这不会影响我们的疫苗接种结果91%的慢性阻塞性肺病患者曾经抽过烟。
系统性免疫反应COVID-19疫苗(随着年龄增长而减少9]。我们观察到没有年龄和免疫反应之间的关系,虽然我们缺乏主题< 40岁完全评估。
我们的研究结果表明,慢性阻塞性肺病患者开发COVID-19疫苗的免疫反应,类似于HC。未来疫苗诱导持续anti-SARS-COV-2 IgA上呼吸道的反应可能对慢性阻塞性肺病患者和HC提供额外的保护。
脚注
利益冲突:托马斯Southworth没有披露。
利益冲突:娜塔莉·杰克逊没有披露。
利益冲突:戴夫·辛格报告个人从Aerogen咨询费,阿斯利康,勃林格殷格翰的发言,基耶西,Cipla公司,CSL贝林,Epiendo,基因泰克,葛兰素史克,Glenmark, Gossamerbio, Kinaset, Menarini, Novarti, Pulmatrix,赛诺菲,Synairgen Teva,治疗先锋和维罗纳。
- 收到了2022年3月14日。
- 接受2022年6月6日。
- 版权©2022年作者。
这个版本分布在Creative Commons归因执照的条款4.0。