背景
随机对照试验(相关的)被普遍认为是黄金标准来评估治疗的疗效。他们的主要优势在于,通过随机,他们避免任何重大失衡而组:因此,观察组的最后试验结果差异最可能相关的治疗效果。因为它们本质上是未来的设计,他们还允许稳定仍在整个研究,以确保所有条件最优测试感兴趣的假说。这些包括高质量的后续,钢筋的依从性,等。因此,这些研究可以达到最高水平的内部效度,提供所有遵循质量标准,如配偶所定义的指导方针(1]。
然而,这个不应该导致一个概括的结果的适用性,即。信贷与高水平的外部有效性研究:通过设计,一个随机对照试验招募一个特定的、定义良好的人口。自人类在生理上异构,他们不均匀药理代理人等刺激的反应。因此,观察到的结果在一个给定的人口应该仅适用于在这个人口而不是外推到其他没有互补测试(2]。
一个主要的困难是,在本质上,受试者参与一个随机试验可能是明显不同于那些拒绝参与或将不会被邀请基于研究者的决定(选择偏见)。出于这个原因,一个务实的声明可能是人口和/或上下文/设置一个随机对照试验往往不能完全代表在现实生活中会发生什么。
这个限制使得其他(补充)的设计很重要,有可能确定结果中观察到相关的可以应用到更广泛的人群,或其他假说是否应该考虑和测试(3]。这是真实的(或实际的)研究贡献(RLR)可以通过观察治疗效果在未经选择的病人。因此,RLR有潜力1)检查的可能性推断的结果相关的不同的患者群体,证实或反驳有效性,2)检查没有人群的干预的影响。但存在的偏见可能导致误导性的结论;比较有效的设计,最常见的类型的偏见是群体或多或少的存在明显差异,这可能很难检测(4]。
充分获益RLR可以提供什么,高质量协议需要开发和结果解释的需要谨慎。至于相关,提出了质量标准和工作在这个领域正在进行解决和完善至关重要的方法论问题。
RLR是与广泛的利益相关者参与相关使用行为,审查和/或质量评估治疗研究:病人,临床医生、研究人员、审核人员、决策者、机构,指导开发人员,等。(5]。
呼吸有效性集团(REG)成立于2013年,促进高质量的现实生活中的呼吸研究。REG参与建立和沟通RLR质量标准,促进RLR项目,提供领导和RLR卓越的例子,为RLR提供伦理审查项目,兴趣在内的各利益相关方参与RLR和促进协作网络。
我们定义
RLR是研究,包括病人尽可能广泛的目标人口,照顾在自然条件下,后续强度不超过提供的日常保健是什么(2]。
提出的研究框架内注册(图1),RLR对应图的右上角(病人诊断为(条件),开放的设计,自然的设置)与“真实”字符减少向左下角(高度选择病人,随机盲法设计,严格控制的设置)。
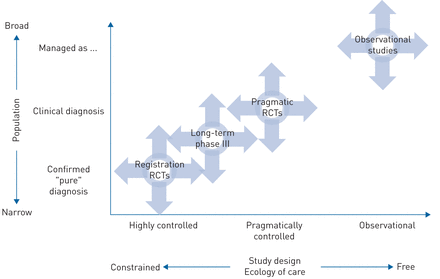
有效性的研究框架。出版商的许可(复制2]。
工具除了REG框架提出了确定的程度是在高度控制的研究与完全自然的研究,即。它坐落在efficacy-to-effectiveness连续体(6]。
我们知道
当适当地执行(1),传统相关的高度可靠的来源的证据治疗效果,内部效度高。
然而,尤其当进行登记的目的,他们依靠人口选择最大化展示效果的机会。调查人员倾向于避免招聘太多的并发症或伴随治疗患者,符合纳入和排除标准,控制变量和限制代表一个重要的不利影响的风险负担的病人,临床和研究资源。因此,可能的治疗效果不能修饰词的研究,限制了研究结果的generalisability(有限的外部效度)。例如,许多哮喘相关的不包括吸烟者或肥胖患者,这两个条件称为修改治疗效果(7,8]。在这种相关,患者接受的详细说明,并密切关注,以确保适当的吸入器使用和依从性。他们受益于更容易和更快的获得医疗,并且经常形成更强的与医疗服务提供者之间的关系。
,几项研究发现,哮喘或慢性阻塞性肺病治疗人群招募试验是代表这些病人中只有一个很小的少数人群,在许多研究[不超过15%9- - - - - -17]。
RLR可以观察(前瞻性或回顾性,如。使用medico-administrative数据库)或介入(务实试验)。重要的是,这些选项的严格质量标准已经开发出来,让读者决定的力量产生的证据。这些包括务实的CONSORT声明扩展试验(18],闪光灯声明在流行病学观察研究[19药物和药物警戒研究],EMA-ENCePP清单(20.],解锁项目质量标准和最小数据集要求观察性研究[21),棱镜的荟萃分析(22)实施和斯塔标准试验(23]。最近,REG已开发,测试和发布了现实生活的证据评估工具(相关)来评估质量的现实比较有效性研究(24,25]。这个工具依赖于先前建立REG和其他人提出的质量标准(4,26,27),预计将促进研究设计和评价。
因此,年级(分级的建议评估、开发和评价)系统承认的可能性升级一项观察性研究提供的证据级别,当满足所有相关质量标准,和被认为是“压倒性”证据。相反,未能满足这些标准会导致降低[提供的证据28]。
RLR不能取代传统相关的但很有用,甚至重要补充:RLR足够的质量(高外部效度)的研究可以帮助验证和扩展的适用性个随机对照试验结果(29日]。虽然确切的结论通常不能从观察性研究的结果(由于残余混杂的可能性),它们可以确认和/或存活率存在有关,例如,在感兴趣的子组治疗效果,安全范围广泛的人口和各医疗体系的成本效益。在可能的情况下,务实的试验可以提供更强的研究设计。
因此,RLR需要执行和占所有利益相关者参与相关问题的治疗,包括患者、临床医生、研究人员、审核人员、决策者、机构和指导开发人员。事实上,这种要求是承认在一些指导方针文档,比如一个由全球倡议对慢性阻塞性肺疾病慢性阻塞性肺病管理,这凸显了一个事实:缺乏外部有效性可能会影响试验结果的适用性更广泛的人口(30.];同样,欧洲呼吸协会最近强调了需188bet官网地址要使用超出相关证据时详细说明指南(31日]。
我们提倡
高质量的鉴定与包容现实研究临床实践指南的发展。
o虽然理论上任何研究可以用来通知指南,真实的研究经常被排除;这可能会导致非常低的使用的研究/数量和顺向不可知论者的位置,不帮助在临床实践中,潜在的破坏准则的适用性建议付诸实践。
oRLR可能改善的相关性临床医生的指导。
oRLR可能造成明显的识别最好的治疗方法通过识别响应人群,和增加价值和知识相关的提供的证据。
使用实现现实生活在不同的国家干预和设置的研究来评估其影响在不同的人口,环境和卫生保健系统。
使用真实的研究补充相关的注册的新治疗方法。
o监管机构现在开始理解不同类型的现实研究治疗方法补充证据,特别是对于在实践中如何优化使用。这些真实的研究应该用于支持决策有关登记的新治疗方法。真实的应用研究在这种情况下需要更好的建立和利用。
建立正式的调查计划/项目的研究开发和批准过程/上市后监测包括现实生活中的研究。
o在产品的生命周期,现实生活中的研究提供附加值,可以有帮助,尤其是在post-authorisation阶段。长期临床实验的计划包括现实生活中的研究为所有利益相关者产生附加值。
增加教育和意识的范围、作用和要求高质量的现实研究呼吸系统的研究。
o有一些困惑在RLR和变量方法中使用的术语。不同方法的限制和机会应该成为教育的一部分研究人员,研究管理人员和从业人员。
持续的方法论的研究,扩大和改善的质量和可解释性现实研究向临床实践。
o真实的极限方法尚未达到和创新是欢迎向我们提供新的证据类型的知识库。
建立设计良好的全球注册中心周围常见的呼吸道条件前瞻性收集关键疾病信息。
o注册中心目前提供一个具有成本效益的方法纵向流行病学与潜力在未来更大的作用。
RLR到技术进步的加速整合数字结果的形式,电子健康和移动医疗的研究/注册/指导过程中,并行分析工具的进步对大数据进行评估。
o技术进步的速度似乎比我们的能力更快速评估和调节的影响;机会,然而,通过小说获得(和使用)的知识技术形式有无限的可能性,需要探索高质量和结构化RLR框架内。
我们得出这样的结论
RLR现在清楚地定位治疗的研究框架内建立的,例如,注册。
RLR(高外部效度)是必要的补充传统相关的结果(高内部效度)对治疗效果。
RLR可能确认,发放结果相关的更广泛的人群和设置,并生成假设在特定的子组或感兴趣的情况。
RLR还可以提供证据,无法进行相关的原因与可行性、伦理和负担能力。
因此,RLR应该被认为是一个潜在的重要贡献者填补知识空白。
优质RLR可以而且应该被整合,通过病人,医疗专业人员,指导开发人员和决策者,指导决策过程。
等工具,以严格的质量评估RLR相关(REG开发的)现在可以使用和系统应该使用。
最后,研究人员应该确定最适当的研究设计回答一个定义良好的研究问题,无论是古典相关的、务实的相关,观察性研究或实施研究设计。
可共享的PDF
确认
这个文档已经被国际认可初级护理呼吸组和世界过敏组织。作者要感谢呼吸组团队有效性(首席执行官迈克尔·沃克和支持者联络,内奥米的废人,高级科学研究人员和莎拉•卢卡斯研究员)和监督委员会(特雷弗朗伯基思•艾伦和尼克可能)。
脚注
呼吸效果组的同事谁支持这个宣言是:Ioanna Agache,布拉索夫,罗马尼亚;彼得·巴恩斯,伦敦,英国;埃里克·贝特曼开普敦,南非;尤尔根•贝赫,慕尼黑,德国;列夫Bjermer、隆德、瑞典;英国利物浦约翰•布莱奇;德摩斯梯尼Bouros,雅典,希腊。法国蒙彼利埃Jean Bousquet;凯文·布朗,丹佛,美国;家伙Brusselle,根特,比利时; Moises Calderon, London, UK; Jon Campbell, Aurora, USA; Lars Olaf Cardell, Stockholm, Sweden; Jose A. Castro-Rodriguez, Santiago, Chile; Nazia Chaudhuri, Manchester, UK; Niels Chavannes, Leiden, The Netherlands; Tamera Corte, Sydney, Australia; Richard Costello, Dublin, Ireland; Vincent Cottin, Lyon, France; Adnan Custovic, London, UK; Ronald Dandurand, Montreal, Canada; Zuzana Diamant, Lund, Sweden; Pascal Demoly, Montpellier, France; Francine Ducharme, Montreal, Canada; Wojciech Feleszko, Warsaw, Poland; Mark Fitzgerald, Vancounver, Canada; Wytske Fokkens, Amsterdam, The Netherlands; Daryl Freeman, Cambridge, UK; Mina Gaga, Athens, Greece; Thomas Geiser, Barcelona, Spain; Ian Glaspole, Melbourne, Australia; Caroline Gouder, Valetta, Malta; John Haughney, Aberdeen, UK; Liam Heaney, Belfast, UK; Gunilla Hedlin, Stockholm, Sweden; Peter Hellings, Leuven, Belgium; Teoh Oon Hoe, Singapore, Singapore; Elliot Israel, Boston, USA; Tuomas Jartti, Turku, Finland; Mark Jones, Southampton, UK; Rupert Jones, Southampton, UK; Lynn Josephs, Southampton, UK; Omer Kalayci, Ankara, Turkey; Michael Keane, Dublin, Ireland; Janwillem Kocks, Groningen, The Netherlands; Robert Lemanske, Madison, USA; Helgo Magnussen, Grosshansdorf, Germany; Mika Makela, Helsinki, Finland; Mariano Mazzei, Sienna, Italy; Paolo Matricardi, Berlin, Germany; Andrew McIvor, Hamilton, CanadA; Maria Molina, Barcelona, Spain; Mario Morais-Almeida, Lisbon, Portugal; Ferran Morell, Barcelona, Spain; Ralph Mosges, Köln, Germany; Joaquim Mullol, Barcelona, Spain; Clare Murray, Manchester, UK; Steven Nathan, Falls Church, USA; Bernardino Alcazar Navarrete, Granada, Spain; Alberto Pappi, Ferrara, Italy; James Y Paton, Glasgow, UK; Wanda Phipatanakul, Boston, USA; David Price, Aberdeen, UK; Jennifer Quint, London, UK; Chin Kook Rhee, Seoul, South Korea; Pilar Rivera Ortega, Manchester, UK; Graham Roberts, Southampton, UK; Mohsen Sadatsafavi, Vancouver, Canada; Joaquim Sastre, Madrid, Spain; Glenis Scadding, London, UK; Moises Selman, Mexico City, Dave Singh, Manchester, UK; Mexico; Pawel Sliwinski, Warsaw, Poland; Iain Small, Peterhead, UK; Pete Smith, Southport, Australia; Mike Thomas, Southampton, UK; Ioanna Tsiligianni, Heraklion, Greece; Willem van Aalderen, Amsterdam, The Netherlands; Job van Bowen, Groningen, The Netherlands; Maarten van den Berge, Groningen, The Netherlands; Eric van Ganse, Lyon, France; Jorgen Vetsbo, Manchester, UK; Claus Vogelmeier, Marburg, Germany; Simon Walsh, London, UK; Vicky Xepapadaki, Athens, Greece; Heather Zar, Cape Town, South Africa.
利益冲突:n罗氏报告赠款从勃林格殷格翰集团和个人费用,诺华制药和辉瑞,个人费用从Teva,葛兰素史克公司,阿斯利康,基耶西,Mundipharma,赛诺菲,山德士,3 m, Zambon Trudell,外提交的工作。
利益冲突:a . Anzueto报告个人费用咨询公司葛兰素史克、阿斯利康和勃林格殷格翰的发言,在提交工作。
利益冲突:美国Bosnic Anticevich TEVA个人费用咨询委员会工作报告,个人费用咨询公司葛兰素史克和梅达赠款TEVA,个人费用从TEVA讲座,葛兰素史克和阿斯利康,个人费用从梅达手稿准备,个人费用从葛兰素史克教育活动,在提交工作。
利益冲突:a。卡普兰报告赠款和阿斯利康的个人费用,勃林格殷格翰集团和辉瑞,个人费用从Covis,葛兰素史克,赛诺菲,默克Frosst,诺华,普渡,Teva, Trudel,诺和诺德和Griffols,在进行这项研究的。
利益冲突:m . Miravitlles报告个人费用从阿斯利康讲座,勃林格殷格翰的发言,基耶西,Cipla Menarini, Rovi,比亚尔,Zambon, CSL贝林,Grifols和诺华公司,阿斯利康的个人费用咨询,勃林格殷格翰的发言,基耶西,葛兰素史克,比亚尔,Gebro制药,CSL贝林,laboratorio Esteve费雷尔,Mereo生物制药,维罗纳制药,TEVA, pH制药公司,诺华和Grifols,葛兰素史克和Grifols赠款,在提交工作。
利益冲突:d·瑞安报告个人费用咨询委员会工作从葛兰素史克,BI和诺华,个人费用从阿兹讲座和咨询委员会的工作,个人费用从梅达出席讲座和会议,在提交工作;REG的前总统,现任副总裁REG和顾问战略医疗顾问,最佳的病人护理。
利益冲突:J.B.索里亚诺参加演讲活动,咨询委员会和咨询公司2014 - 2019年期间由:Almirall,阿斯利康,勃林格殷格翰的发言,胸部,基耶西,人,GEBRO, Grifols,葛兰素史克公司,林德,Lipopharma, Mundipharma,诺华,辉瑞公司RiRL, Rovi,新兴SEPAR和武田。
利益冲突:o . Usmani报告赠款和阿斯利康的个人费用,勃林格殷格翰集团和基耶西,从葛兰素史克和埃德蒙医药拨款,个人费用从Aerocrine Napp, Mundipharma,新兴武田,Zentiva Cipla公司,在提交工作。
帕帕多普洛斯的利益冲突:n个人费用咨询委员会工作报告和讲座从诺华,纽迪希亚,哈尔,MENARINI /西班牙FARMA和MYLAN /梅达,个人费用从赛诺菲讲座,BIOMAY,默沙东公司,生物技术和勃林格殷格翰的发言,个人费用咨询委员会工作从阿斯利康、葛兰素史克、赠款Gerolymatos国际SA和Capricare外提交的工作。
利益冲突:G.W. Canonica没有披露。
- 收到了2019年7月30日。
- 接受2019年7月31日。
- 版权©2019人队
本文是开放和分布式根据创作共用署188滚球软件名非商业性4.0许可证。















