摘要
来自睾丸挑战的新证据和P2X抑制剂GeFapixant加强ATP作为慢性咳嗽的驾驶员。咳嗽对其他刺激物的反应可能涉及单独的外周激活途径。超敏反期可能是由于再次不同的过程。http://bit.ly/2yr6muz.
在许多情况下,咳嗽仍然是一个棘手的临床问题。尽管已发现了诱发因素和相关诊断,但患者因持续咳嗽就诊时仍未得到满意的治疗是常见的[1].慢性咳嗽是常见的,与大量的身体和心理发病有关[2].
近年来,人们提出了一种新的思考慢性咳嗽的模式,即咳嗽过敏综合征[3.].由于基本上未指明的机制,周围和中央神经途径对咳嗽反射的一体化被认为是上调到导致触发咳嗽的无害刺激的程度[4].沉淀因子,如哮喘下的较低的气道炎症,慢性鼻窦炎的上气道刺激,吸烟或胃肠食管反流可以明显咳嗽,但主要问题是患有咳嗽超敏反应。这个范式可能会解释为什么只有一部分具有这些二级因素的个人抱怨慢性咳嗽,以及为什么在许多情况下持续咳嗽似乎根本没有驾驶二级事业[5].
然而,尽管通过临床观察非常良好地支持,但咳嗽超敏反综合征主要是一个理论概念。潜在的机制更清楚,它是当前咳嗽研究的关键领域之一。潜在的解剖部位促使咳嗽超敏率的潜在解剖部位包括气道的外周围传入神经末端,迷走神经的颈颈部和牙龈神经节,脑干中的感觉整合位点以及更高的脑途径,每个脑途径都具有适应性的过兴奋剂或抑制不良的影响咳嗽反射[6].中枢神经途径的作用的证据可能是目前最强的,并且包括来自功能磁共振成像的数据。与健康的志愿者相比,长期耐火咳嗽的患者在中脑的特定区域中显示出增加的活性,并且在咳嗽时咳嗽时,在吸入的辣椒素咳嗽时,在特定的前脑位置的不起作用[7].最近的观察还建议缺乏自愿或半自愿抑制控制作为难治性慢性咳嗽的重要因素[8,9].此外,迄今为止已经证明有效的大多数治疗方法很可能都有一个中心作用点,包括由专业理疗师和语言治疗师提供的行为训练[10.]、抗癫痫药物加巴喷丁[11.和普瑞巴林[12.,抗抑郁药阿米替林[13.[吗?14.].中央影响对咳嗽的重要性显然是在睡眠期间健康和疾病中的咳嗽频率显着降低[15.].
到目前为止,关于更多的外周部位在咳嗽过敏机制中的作用的证据是非常有限的。虽然一些气道传入受体已被证明在咳嗽反射中起作用,但它们对慢性难治性咳嗽的病理生理学的贡献仍不清楚。例如,这种受体TRPV1可能在该疾病患者的气道中表达增加[16.),现在似乎没有以前认为的那么重要。尽管观察特定TRPV1拮抗剂可以成功地废除吸入辣椒素引起的咳嗽反射,缺乏任何改变在日常的慢性咳嗽患者咳嗽频率测试相同的代理违背任何重大贡献的TRPV1过敏性咳嗽综合症的机制(17.].非常相似的观察结果涉及受体TRPA1 [18.].
然而,最近通过对另一种受体P2X3的研究,人们对咳嗽的神经通路有了进一步的了解。P2X是一个进化上保守的atp门控离子通道家族,存在于许多生物和组织类型中[19.];p2x3是在感觉神经末端的气道中存在的亚型[20.].2005年,在豚鼠身上的研究表明吸入ATP会引起咳嗽,而P2X抑制剂会减弱这种反应[21.].ATP介导的刺激离体来自豚鼠肺部的迷走神经传入感觉c纤维被P2X3拮抗剂阻断[22.].在慢性难治性咳嗽的人类受试者中,一项2期研究显示P2X3/P2X2受体拮抗剂吉法吡嗪(以前的AF-219)显著减少了每日咳嗽频率[23.].这代表了一种新型药物在治疗难治性慢性咳嗽方面的潜在重大突破。gefaapixant和其他P2X3拮抗剂的3期临床试验目前正在进行中[24.,这类治疗可能会彻底改变治疗不足患者的方式。
从豚鼠模型推断,吉法吡嗪在人体内的作用方式可能是通过作用于atp介导的气道传入神经的激活。直到现在这个假设还没有被探索,但在当前的问题188bet体育备用网址欧洲呼吸杂志米马上订货et al。[25.]解决我们知识的这种不足。作者报告了第2期随机安慰剂对照研究的结果,了解GeFapixant对吸入辣椒素,柠檬酸,ATP和蒸馏水中的睾丸反应,在24例慢性耐火咳嗽和12例健康对照中的毒性反应。GeFapixant对辣椒素和柠檬酸显着适中咳嗽反应,但对提高患者预先指定数量的咳嗽的ATP剂量具有显着影响,并在健康受试者中逐渐提高。在咳嗽反应的患者中观察到类似但不太明显的药物对吸入蒸馏水的影响。
这是一项小剂量单次研究,短时间内多次暴露于不同吸入性咳嗽药物后,咳嗽反应的快速耐受性和相互作用是一个潜在的方法关注。然而,每个受试者的用药顺序是随机和固定的,在双盲交叉研究设计中,使用安慰剂和活性药物各进行了三次。因此,参与者作为自己的对照,任何快速耐受性可能潜在地减少而不是增强吉法吡嗪的明显止咳效果。
本论文的发现对我们理解咳嗽的病理生理学是一个可喜的贡献。这是第一个在人类中直接支持gefaapixant的作用机制涉及ATP受体靶的参与的研究。它也支持至少有两种不同的咳嗽激活传入途径的存在(图1).
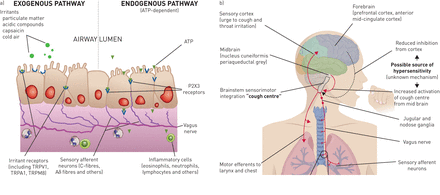
慢性难治性咳嗽和咳嗽过敏综合征的外周和中枢神经通路。外围。迷走神经受到气道传入神经末梢的刺激通过两个主要的互补途径。1)外源途径。主要通过源于肺部外部的物理和化学刺激引发,例如空气中的微粒和吸入的食物碎片,冷空气,酸。涉及受体,包括TRPV1, TRPA1和TRPM8,但可能不会,至少在很大程度上,P2X3。2)内源途径。由来自肺内部的ATP触发(可能是对炎症或其他组织应激原因的反应)。ATP与P2X3以及其他P2X受体相互作用。通过该模型,吸入型咳嗽主要通过外源性途径引起咳嗽,而ATP是内源性途径的直接诱因。P2X3拮抗剂吉法吡嗪减少吸入ATP的咳嗽反应,但不减少吸入柠檬酸或辣椒素的咳嗽反应[25.].TRPV1拮抗剂减少吸入辣椒素后的咳嗽反应[17.].对于慢性难治性咳嗽,内源性途径可能更重要;gefaapixant,而不是TRPV1或TRPA1拮抗剂,减少每日咳嗽频率[17.,18.,23.].这两种途径(未显示)可能与低渗溶液有重叠,例如,直接刺激周围神经和ATP释放。除ATP外的外周介质也可能参与内源性途径(未显示)。b)中枢咳嗽途径。迷走神经突触与脊髓“咳嗽中枢”内的神经元在孤束核内。这反过来又会引发咳嗽通过电动机型试验者到喉,隔膜和肋间肌。咳嗽中心受到较高中心的慢性耐火咳嗽的刺激,包括中脑的核楔形状和Periaqueyedal灰色[7].同时,正常的皮质抑制影响(例如从前额叶皮质和前部中间连杆皮质[7])减少。这些途径可能负责咳嗽超敏反应。因此,只有低水平的外源刺激通过外周Nociceptor,甚至是ATP的生理浓度通过内源性外周途径可引起咳嗽。迷走神经节水平的感觉加工调节也可能与此高度相关(未显示)。皮层通路也包括咳嗽的冲动和咳嗽的意识感觉。
刺激性药物辣椒素和柠檬酸似乎通过刺激c纤维和可能的a纤维引起咳嗽,涉及TRPV1和酸感应离子通道[26.],并且根据目前的研究,它独立于ATP/P2X途径。虽然慢性咳嗽患者对辣椒素和柠檬酸的咳嗽反射敏感性一般增加[27.[这可能代表咳嗽过敏综合征的一般特征,以及对外源有害刺激的提高反应,而不是慢性耐火咳嗽发病机制中的特定机制本身,正如之前所认为的那样。gefaapixant在该病中的深刻的止咳作用,以及现在对其对atp诱导的咳嗽的具体作用的证明,强烈地表明在人类中有一个独特的ATP-P2X通路,这可能与难治性慢性咳嗽的机制高度相关。
因此,我们可以从最近关于格法吡嗪和ATP治疗咳嗽的研究中得出什么结论?现在压倒性的证据是ATP驱动慢性难治性咳嗽,起作用通过P2X频道。虽然仍然不清楚,但仍然符合ATP / P2X3依赖性进程。ATP可以负责或直接参与咳嗽超敏反应的机制吗?在我们看来,可能没有。对于ATP的一个独特的超敏反应似乎不太可能,因为最近对A.H. Morice和同事的另一个观察是对吸入ATP的咳嗽反应没有比对其他吸入刺激物的难治性慢性咳嗽更夸张[28.].此外,考虑到吉法吡嗪对ATP/P2X的阻断不能改变对柠檬酸和辣椒素的反应,ATP似乎不能作为神经的一般增敏剂[25.].
因此,这导致我们得出结论,慢性咳嗽的P2X相关的增加的咳嗽频率可涉及释放的增加或降低ATP在气道的细胞外液中的衰退,而不是直接敏感。慢性耐火咳嗽中假设升高的ATP水平的原因,但目前未指明,但至少在某些情况下,涉及炎症或上皮损伤[20.].
最近在一个意识豚鼠模型上的研究表明,TRPV4和pannexin通道在ATP释放、气道a δ-纤维激活、迷走神经刺激和咳嗽中发挥作用,这些作用由应用于气道和TRPV4配体的低渗溶液触发,并被P2X3抑制剂阻断[25.].这可能是一个类似的过程,观察涉及吸入蒸馏水在当前的研究,起作用通过ATP-dependent机制(25.].然而,TRPV4似乎不需要人类难治性慢性咳嗽,因为来自临床试验的初步数据表明阻断该受体对咳嗽频率没有影响[29.].ATP在航空公司外部的可能性也是相关的;P2X通道是讽刺地普遍的,并且GeFapixant的味觉副作用清楚地表明药物的作用不限于人肺[23.].
基于目前的纸张和现有知识,增加慢性耐火咳嗽的咳嗽可能与三种方法的组合有关:1)响应于吸入物理或化学刺激物而增加传入神经元的激活通过“外源性”外周通路,不依赖于P2X3/ATP,但涉及TRPV1、TRPA1、TRPM8和其他受体;2)感觉传入被ATP激活,ATP来源于肺部本身由于炎症和其他未确定的过程,起作用通过P2X受体在“内源性”外周途径中导致不受直接外部刺激的基础咳嗽频率增加;3)咳嗽过敏,其原因尚未确定,但可能涉及其他外周和/或中枢过程,这降低了对传入刺激的咳嗽反射的激活阈值。这种想法在书中得到了说明图1.
该模型将解释为什么少数少数少数耐火咳嗽患者似乎不响应P2x封锁,特别是那些日常咳频的患者[30.].也许这些人的咳嗽主要是由于过敏和持续接触吸入刺激物,例如空气污染或胃食管反流,而不是内源性atp依赖机制。类似地,增加咳嗽的不止一种途径的存在可以解释为什么格法吡嗪似乎不能完全消除过度咳嗽[31.].
因此,目前的研究进一步加深了我们对慢性咳嗽中atp介导的通路的理解,即使过敏的来源仍有待确定。越来越清楚的是,慢性难治性咳嗽患者之间存在实质性的异质性[32.,33.].结合持续的临床和临床前研究,通过精确测量临床变量的准确表型,是更好地欣赏这种异质性的关键,预测各个潜在的外围或中央作用治疗中的哪些潜在的潜在潜力可能在每种情况下具有最高效果,并进一步推进对慢性耐火咳嗽的理解[34.,35.].
确认
作者非常感谢Stuart Mazzone,墨尔本斯图尔特Mazzone的评论。
脚注
利益冲突:R.D. Turner没有什么可透露的。
兴趣冲突:S.S.蒙克的报告报告来自Merck,咨询委员会的个人费用来自Merck,Bayer,GSK,Menlo和Sanofi,来自Boehringer Ingelheim的旅行费用,在提交的工作之外。
- 收到了2019年5月3日。
- 接受2019年5月7日。
- 版权©2019人队