文摘
慢性气道疾病的炎症反应导致肺气肿不是完全定义。有助于我们提出肺嗜酸细胞增多症领空扩大在小鼠模型和肺气肿患者的慢性阻塞性肺疾病(COPD)。
2型肺慢性炎症的转基因小鼠模型(I5 /合)是用于检查eosinophil-dependent机制导致空域扩大。人类唾液样本收集转化研究嗜酸性粒细胞和矩阵metalloprotease (MMP) -12年的水平在慢性呼吸道疾病患者。
空域扩大被确认在I5 /何老鼠和依赖于嗜酸性粒细胞。检查I5 /何支气管肺泡灌洗确定MMP-12升高,肺气肿的中介。我们表明,在体外,eosinophil-derived白介素(IL) -13促进肺泡巨噬细胞MMP-12生产。空域扩大在I5 /何老鼠依赖MMP-12和eosinophil-derived IL-4/13。与此一致的是,MMP-12是升高患者的痰液嗜酸性粒细胞和计算机断层扫描肺气肿的证据,并在1 s用力呼气量呈负相关。
2型肺慢性炎症的小鼠模型展出领空扩大依赖MMP-12和eosinophil-derived IL-4/13。慢性呼吸道疾病患者,肺嗜酸性粒细胞与MMP-12水平升高有关,这是一个预测的肺气肿。这些发现说明了机制嗜酸性粒细胞为病态与哮喘和慢性阻塞性肺病。
文摘
这项研究表明,嗜酸性粒细胞可能导致肺气肿观察慢性呼吸道疾病患者的一个子集http://ow.ly/mBsz30nvDaG
介绍
慢性阻塞性肺疾病(COPD)是一种慢性呼吸道疾病与吸烟有关,特点是不可逆气流阻塞。它往往伴随着气道炎症和肺气肿的存在。慢性阻塞性肺病是全世界死亡的主要原因之一,是越来越流行1]。没有治疗慢性阻塞性肺病,但更好的理解疾病亚型导致了更多的治疗选择(2- - - - - -4]。肺部炎性细胞浸润在慢性阻塞性肺病疾病发病机制的关键。肺泡巨噬细胞和浸润的中性粒细胞调解破坏性活动的体系结构和功能肺部分通过蛋白酶和炎性细胞因子的释放5]。尽管慢性阻塞性肺病的规范化分类作为一个中性疾病,血液和气道嗜酸性粒细胞在大约三分之一的COPD患者(6- - - - - -8]。临床研究表明,嗜酸性粒细胞和恶化的风险增加之间的关联(9,10]。SPIROMICS群的分析,痰嗜酸性粒细胞水平,尤其是与增加恶化,恶化固定气流阻塞和贫穷的生活质量得分在慢性阻塞性肺病患者(11]。SPIROMICS队列,明显高于肺气肿指数(以定量衡量计算机断层扫描(CT)是指出分层患者痰eosinophil-high集团(11]。
嗜酸性粒细胞产生广泛的介质,包括有毒颗粒蛋白(如。嗜伊红的过氧化物酶(EPX)),有效的脂质衍生品(如。白细胞三烯),和大量的细胞因子和趋化因子12]。在小鼠模型的慢性肺部炎症,嗜酸性粒细胞介质已被证明有助于病理观察到病人,包括支气管狭窄、纤维化和粘液生产(13,14]。Eosinophil-derived白介素(IL) -13是特别感兴趣的,因为它已被证明导致所有这些症状(15,16]。IL-13协调这些活动通过无数的细胞类型,包括肺肺泡巨噬细胞发挥关键作用的改造与严重的哮喘和慢性阻塞性肺病。
肺泡巨噬细胞蛋白酶的生产,包括矩阵metalloproteases(基质金属蛋白酶),导致肺泡毁灭在慢性阻塞性肺病17]。基质金属蛋白酶是细胞外基质降解酶。尤其是MMP-12,已被证明是一个关键的中介肺泡破坏小鼠模型的慢性阻塞性肺病(18)和COPD患者的证据指向它的重要性17]。IL-13信号可以极化巨噬细胞M2(或者激活)表型、功能中发现慢性哮喘和慢性阻塞性肺病(19),诱导MMP-12生产。值得注意的是,IL-13-stimulated小鼠肺泡巨噬细胞产生MMP-12在体外(20.,生产过剩的IL-13转基因小鼠的肺是足以引起MMP-12生产和破坏肺泡空间(21]。
我们提出,嗜酸性粒细胞IL-13慢性肺部疾病的一个重要来源,从而改造的航空公司导致肺气肿。探讨这个问题,我们利用小鼠模型慢性辅助(Th) 2型肺部炎症,也分析了哮喘或慢性阻塞性肺病患者的痰样本。识别肺气肿的途径发展/进步可能提供新的治疗靶点和策略来防止或稳定这个慢性呼吸道疾病的特性。
方法
老鼠
老鼠采用包括C57BL / 6 j野生型菌株(WT)(杰克逊实验室,巴尔港,我,美国),eoCRE [22],NJ.1638 [23],I5 / hE2 [14),菲尔13),MMP-12−−/(B6.129X -Mmp12tm1Sds/ J;杰克逊实验室),液氧IL-4/13 (C.129P2 (Cg)Il4 /使用Il13tm1.1Lky/ J;杰克逊实验室)和IL-13−−/安德鲁·麦肯齐(礼物MRC实验室分子生物学,剑桥,英国(24])。老鼠分析2到3个月的年龄。老鼠在亚利桑那州梅奥诊所小动物设施维护(一个特定的无菌设施)的梅奥诊所亚利桑那州(美国亚利桑那州斯科茨代尔)。
研究涉及老鼠按照美国国立卫生研究院的执行和梅奥诊所的机构动物保健和使用委员会的指导方针。
细胞隔离和文化
看到补充材料全部细节。
总之,嗜酸性粒细胞是孤立如前所述25从NJ.1638或IL-13]−−//新泽西。1638mice [23,24]。IL-33 (Peprotech落基山,新泽西,美国)被添加到激活嗜酸性粒细胞ng 50毫升−1实验组(IL-33省略休息的嗜酸性粒细胞)。细胞在37°C和5%孵化有限公司2,24 h后洗3次删除添加细胞因子。巨噬细胞从C57BL / 6 j或MMP-12被孤立−−/老鼠被描述为Lasburyet al。(26]。细胞被镀在150 000细胞/ 24-well文化板块(美国纽约康宁,康宁)和培养48 h的嗜酸性粒细胞(750 000个细胞)或媒体仅500年μL总量。评估接触依赖性、文化表现在transwell板(0.4μm孔隙)(康宁)。
ELISA和多路复用
MMP-12是由鼠标MMP-12 PicoKine ELISA(美国博士德生物技术,而往常,CA)。EPX测量如前所述[29日]。其他老鼠和人类细胞因子评估bead-based多路复用技术(夏娃技术,卡尔加里,AB,加拿大)。
评估临床痰
我们用痰上层清液(无细胞的分数)从43诊断为哮喘或慢性阻塞性肺病患者以前存储基于观察协议批准的当地医院研究伦理委员会在圣约瑟夫医院(汉密尔顿,加拿大)。这些痰样本诱导和加工如前所述33]。哮喘受试者被随机选择样本从临床上患者痰液测试在2017年1月至11月之间。哮喘的诊断是基于支气管扩张剂可逆性和/或挑衅剂量导致用力呼气量下降了20%在1 s (FEV1)< 8 mg·毫升−1醋甲胆碱挑战测试。COPD患者的痰收集以前的地方观察研究临床稳定的时期(从2016年11月到2017年11月)。入选标准包括固定气流阻塞(FEV1/ FVC < 0.7)和/或肺气肿的证据在成像≥10 pack-year吸烟史。那些先前诊断哮喘或显著改善post-bronchodilator肺量测定法被排除在外。慢性阻塞性肺病的评估是基于全球倡议对慢性阻塞性肺疾病的标准34]。胸部CT扫描,在常规的临床检查,因此有丰富的应用协议。最常见的CT扫描可以是正常的分辨率没有对比。证实了肺气肿分组分为三个步骤:1)推断从临床放射学家的总结报告,2)应用定量CT指标(低衰减区< 950胡(% LAA−950胡),使用开源胸部成像平台所提供的3 d切片机:https / /: chestimagingplatform.org)和3)确认存在的肺气肿蒙蔽放射科医生。嗜酸性的病人被定义为那些存在痰嗜酸性粒细胞> 3%和/或血液嗜酸性粒细胞> 300μL的证据−1,以及那些有历史证据的嗜酸性粒细胞现在抑制由于大剂量吸入或口服皮质类固醇治疗。
统计分析
数据分析与棱镜version 7(美国GraphPad拉霍亚,CA)。统计比较小鼠模型和细胞培养的数据进行t检验。结果被表示为±扫描电镜。人类学科组进行统计比较方差分析/克鲁斯卡尔-沃利斯非参数测试和协会是由斯皮尔曼等级/皮尔森相关测试基于各自的数据集的分布(D 'Agostino-Pearson综合正常测试)。SPSS 23.0版(美国、IBM、纽约Armonk)是用于多元回归分析。假定值≤0.05被认为是重要的。
结果
I5 /何老鼠展览eosinophil-dependent领空扩大
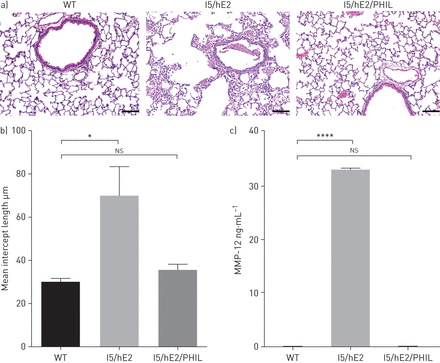
探讨在慢性炎症肺嗜酸性粒细胞的作用,我们采用I5 /何2型肺慢性炎症的小鼠模型。I5 /何鼠标已经证明发展标志着气道重构[依赖肺嗜酸细胞增多症14,27]。检查I5 /合与WT苏木精和eosin-stained肺部分显示领空肿大的肺实质I5 /何老鼠(图1一个)。我们穿过I5 /何鼠标eosinophil-deficient菲尔鼠标(13)检查eosinophil-dependent肺结构的变化。I5 / hE2的十字架与菲尔透露,这些病变是完全依赖嗜酸性粒细胞。量化的平均截距长度之间的肺泡隔显示增加(∼30倍与70嗯)在I5 /何老鼠大小与I5 /何/ PHIL老鼠(图1 b)。
Eosinophil-dependent肺泡的破坏和调制矩阵metalloprotease (MMP) -12。)苏木精和eosin-stained肺部分展示增加在I5 / hE2的肺部肺泡空间相对于野生型(WT)和eosinophil-deficient同行I5 / /菲尔。肺实质;酒吧规模:50µm。b)量化的平均肺泡空间显示长度增加2倍的意思是拦截I5 /何肺。n = 5老鼠。c)支气管肺泡灌洗液被MMP-12 ELISA,收集和评估肺改造中介I5 /何肺大幅度增加的表达式。n = 6小鼠。*:p < 0.05;* * * *:p < 0.0001;ns:不重要的。
我们之前调查eosinophil-dependent基因表达变化在I5 /何肺集中关注MMP-12作为中介的候选人I5 / hE2的领空放大观察。MMP-12已被证明导致肺泡隔emphysema-associated崩溃的COPD模型(18),我们发现MMP12是最调节eosinophil-dependent基因在I5 /何肺27]。符合这一观察,MMP-12球液中的蛋白质含量的升高在I5 /何老鼠,几乎检测不到I5 /何/ PHIL老鼠(图1 c)。总的来说,这些结果表明,嗜酸性粒细胞促进MMP-12生产和空域肿大。
MMP-12是中介在I5 /何小鼠肺泡杀伤性
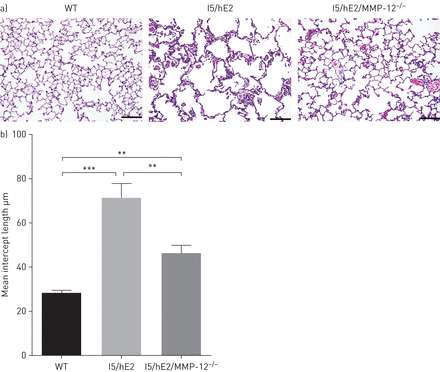
探索的意义MMP-12中观测到的领空扩大I5 /何我们比较I5 /何老鼠与MMP-12-deficient同行I5 / / MMP-12−−/。肺组织学检查显示减少病变在缺乏MMP-12 (图2一个)。量化的平均截距长度之间的肺泡隔显示显著减少I5 / / MMP-12−−/老鼠(图2 b)。然而,I5 / / MMP-12−−/老鼠的意思是增加拦截长度相对于WT老鼠,建议其他eosinophil-dependent介质导致这些病变。例如,其他基质金属蛋白酶(MMP-2和9)与肺气肿(35,36),我们发现这些在I5 /何肺也升高(补充图S1)。BAL细胞结构(I5 /何(46.85±6.45×105细胞·毫升−1)和I5 / / MMP-12−−/(35.23±4.25×105细胞·毫升−1))和嗜酸性粒细胞数量(I5 /何(43.79±5.53×105细胞·毫升−1)和I5 / / MMP-12−−/(34.6±4.85×105细胞·毫升−1)没有受到的损失MMP-12在这个模型。
矩阵metalloprotease (MMP) -12介导肺泡破坏I5 /合模型。)苏木精和eosin-stained肺部分展示扩大空域在I5 /何相对于野生型小鼠(WT)和MMP-12−−/老鼠。肺实质;酒吧规模:50µm。b)苏木精和eosin-stained肺部分评估意味着拦截长度显示在I5 /何小鼠肺泡空间相对增加MMP-12-deficient同行I5 / / MMP-12−−/。n≥3老鼠。* *:p < 0.01;* * *:p < 0.001。
Eosinophil-derived IL-13促进肺泡巨噬细胞MMP-12生产在体外
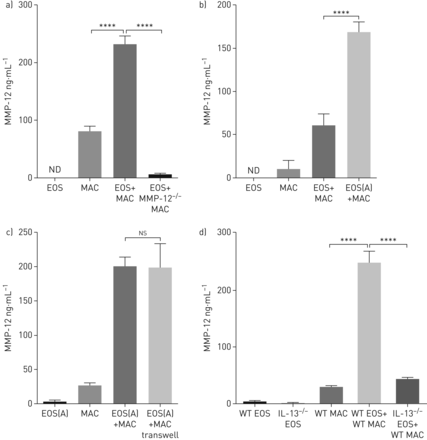
研究嗜酸性粒细胞和MMP-12生产我们表现之间的关系在体外实验与嗜酸性粒细胞和已知的气道MMP-12-producing细胞,肺泡巨噬细胞(37,38]。在体外实验表明,MMP-12不是嗜酸性粒细胞可检测的文化上层清液,而MMP-12肺泡巨噬细胞检测到上层的文化。嗜酸性粒细胞和巨噬细胞共培养导致显著增加MMP-12水平仅与巨噬细胞文化(图3一)。培养与MMP-12 WT嗜酸性粒细胞−−/肺泡巨噬细胞在这些文化的实验表明,MMP-12来自巨噬细胞(图3一)。
嗜酸性粒细胞直接调节肺泡巨噬细胞生产矩阵metalloprotease (MMP) -12年到白介素(IL) 13-dependent机制:MMP-12的ELISA测定细胞培养上清液在体外48 h文化的嗜酸性粒细胞和/或肺泡巨噬细胞。ND:没有发现;EOS:嗜酸性粒细胞;麦克:巨噬细胞;EOS (A):激活嗜酸性粒细胞;WT:野生型。嗜酸性粒细胞单独培养,巨噬细胞单独培养和培养(嗜酸性粒细胞+巨噬细胞)。WT嗜酸性粒细胞被激活(IL-33 24小时然后洗)和培养与WT巨噬细胞或MMP-12−−/巨噬细胞显示MMP-12来自巨噬细胞。b)评估的培养上清液嗜酸性粒细胞与嗜酸性粒细胞激活嗜酸性粒细胞和巨噬细胞表明pre-activation (IL-33 24 h然后洗)增强巨噬细胞MMP-12生产。c) Transwell激活嗜酸性粒细胞和巨噬细胞共培养表明,接触不需要增强巨噬细胞MMP-12生产。d) ELISA测定IL-13共培养上清液−−/与WT与WT嗜酸性粒细胞巨噬细胞表明eosinophil-derived IL-13促进巨噬细胞MMP-12生产。* * * *:p < 0.0001;ns:不重要的。
探索eosinophil-mediated巨噬细胞机制MMP-12生产我们第一次评估与IL-33嗜酸性粒细胞活化的作用,一个与慢性肺疾病相关的细胞因子和高架I5 /何鼠肺(27,39]。嗜酸性粒细胞激活IL-33已被证实能增加释放的可溶性介质可能会影响生产MMP-12从巨噬细胞40,41]。嗜酸性粒细胞的活化与IL-33之前与肺泡巨噬细胞共培养增强巨噬细胞MMP-12生产相对于培养与未激活的嗜酸性粒细胞(图3 b)。我们接下来检查接触依赖性transwell嗜酸性粒细胞与肺泡巨噬细胞的共培养。我们表明,增加MMP-12从巨噬细胞不依赖联系(图3 c),这表明巨噬细胞产生MMP-12 eosinophil-secreted中介作为回应。
先前的研究已经证明IL-13促进MMP-12生产由巨噬细胞(20.,36已知)和IL-33诱导IL-13从嗜酸性粒细胞15,42]。我们评估的角色eosinophil-derived IL-13 WT肺泡巨噬细胞和嗜酸性粒细胞的培养足够的或为IL-13不足。我们发现eosinophil-derived IL-13促进肺泡巨噬细胞MMP-12生产(图3 d)。
I5 /何老鼠表现出空域扩大依赖eosinophil-derived IL-13 MMP-12
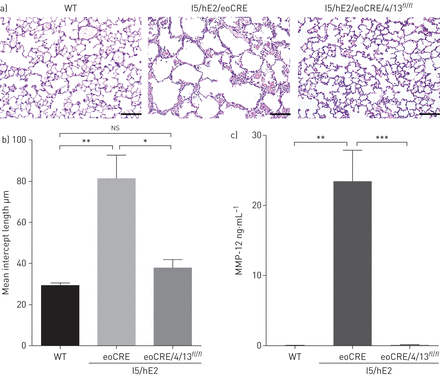
在我们检查,如果肺嗜酸细胞增多症2型肺慢性炎症诱发的小鼠模型肺泡的破坏通过IL-13-mediated MMP-12生产我们生成条件基因敲除小鼠(43)跨越eosinophil-specific Cre重组酶鼠标,eoCRE,可用液氧IL-4/13鼠标(44),导致eosinophil-specific IL-13损失表达式(il - 4) (补充图S2)。然后我们穿过这些老鼠与I5 /何创建I5 /何/ eoCRE / 4/13fl/fl,这是与I5 / / eoCRE作为控制。组织学检查肺部再次显示领空扩大在I5 /何/ eoCRE依赖eosinophil-derived IL-4/13 (图4一)。值得注意的是,肺泡空间在I5 /何/ eoCRE / 4/13fl/fl相当于WT的老鼠,这表明扩大在I5 /何小鼠肺泡空间完全依赖于eosinophil-derived IL-4/13 (图4 b)。BAL细胞结构(I5 /何/ eoCRE (39.1±8.74×105细胞·毫升−1)和I5 /何/ eoCRE / 4/13fl/fl(22.98±4.31×105细胞·毫升−1))和嗜酸性粒细胞数量(I5 /何/ eoCRE (26.1±4.04×105细胞·毫升−1)和I5 /何/ eoCRE / 4/13fl/fl(41.53±8.28×105细胞·毫升−1)没有受到的损失eosinophil-derived IL-4/13在这个模型。值得注意的是,BAL MMP-12水平完全取决于eosinophil-derived IL-4/13 (图4 c)。综上所述,我们的数据表明eosinophil-derived IL-13是肺泡巨噬细胞的关键中介MMP-12生产和肺泡破坏这慢性肺部炎症模型。
Eosinophil-derived白介素(IL) -4/13诱发矩阵metalloprotease (MMP) -12生产和肺泡破坏I5 /何老鼠。WT:野生型。)遗传交叉的I5 / hE2 eosinophil-specific Cre鼠标(eoCRE),然后可用液氧IL-4/13鼠标(I5 /何/ eoCRE / 4/13fl/fl)透露,扩大在I5 /何小鼠肺泡空间依赖eosinophil-derived IL-4/13。肺实质;酒吧规模:50µm。b)苏木精和eosin-stained肺部分演示扩大空域I5 /何老鼠相对于eosinophil-derived IL-4/13-deficient老鼠。c) ELISA测定的MMP-12支气管肺泡灌洗显示MMP-12 I5 /何老鼠取决于eosinophil-derived IL-4/13。n≥3老鼠。*:p < 0.05;* *:p < 0.01;* * *:p < 0.001;ns:不重要的。
嗜酸性粒细胞升高MMP-12与人类受试者肺气肿和肺功能下降
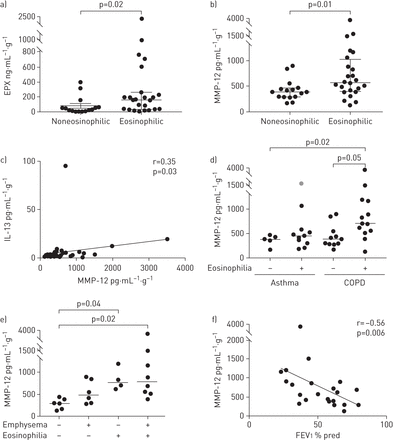
接下来,我们研究MMP-12之间的关系,在人类嗜酸性粒细胞,肺气肿和肺功能。的44个病人痰随机选择,五个被拒绝(三个拒绝并发症/其他炎症性异常,一个拒绝不符合标准哮喘或慢性阻塞性肺病和一个拒绝年龄< 18岁)。剩下的科目,16 23哮喘和慢性阻塞性肺病;在他们的临床特征表1和2。痰EPX水平高嗜酸性组(p = 0.002) (图5一个)和与痰IL-13水平显著相关(r = 0.536;斯皮尔曼等级,p = 0.0004)。无论诊断、MMP-12水平检测痰中嗜酸性组高(p = 0.01) (图5 b)和与痰IL-13水平适度相关(r = 0.35;p = 0.03) (图5 c)。MMP-12气道IL-13水平的显著相关,而不是EPX (r = 0.05;p = 0.7)建议的可能性MMP-12并未直接与嗜伊红血球过多有关本身,而是与eosinophil-derived有关,和潜在的其他来源,IL-13炎症。
矩阵metalloprotease (MMP) -12表达嗜酸性气肿航空公司。EPX:嗜酸性粒细胞过氧化物酶;IL:白介素;FEV1:在1 s用力呼气量;慢性阻塞性肺病:慢性阻塞性肺疾病。)EPX和b) MMP-12表达式在航空公司(n = 40患者慢性气道疾病(哮喘或慢性阻塞性肺病)的诊断分类基于嗜伊红血球过多。Mann-Whitney测试。c)相关的痰MMP-12 IL-13 (n = 40)。斯皮尔曼等级。d, e) MMP-12表达式的航空公司d) (n = 16)哮喘和慢性阻塞性肺病(n = 24),嗜酸性粒细胞分类基于和e) COPD受试者,分类对嗜酸性粒细胞和肺气肿。克鲁斯卡尔-沃利斯和邓恩的多个校正。FEV的痰MMP-12 f)相关性1% pred COPD患者(n = 24)。斯皮尔曼等级。每个符号代表个体患者数据,在适当的地方,中值是表示每个子集。灰色象征(d)表明一个哮喘病人领空扩大的证据。p≤0.05被认为是重要的。
亚组分析,微分表达式的MMP-12哮喘对嗜酸性粒细胞是不起眼的子集(p > 0.99) (图5 d);然而,增加检测MMP-12明显的嗜酸性COPD气道(p = 0.05) (图5 d)。事实上,MMP-12水平在慢性阻塞性肺病患者高那些伴随的嗜酸性粒细胞和肺气肿相比之下,那些没有表现出(p = 0.02) (图5 e)。比较% LAA−950胡嗜酸性状态显示更高价值的嗜酸性粒细胞(中位数为1.4%与0.08%;Mann-Whitney测试,p = 0.04)。证实了肺气肿分组方法部分中描述的三个步骤。分组(由临床放射学家的报告)的准确性得到了显著提高% LAA−950胡肺气肿集团(中值1.97%与0.18%;p = 0.0073, Mann-Whitney测试)和确认的肺气肿蒙蔽放射科医生对每个主题。感兴趣的,病人嗜酸性哮喘组曾MMP-12的最高水平(标记为灰色的象征图5 d)CT大气空间扩大的证据。如果这个数据点被删除,MMP-12水平明显高于相比,嗜酸性COPD病人痰嗜酸性哮喘受试者(p = 0.01, Mann-Whitney),否则是相当(p = 0.43) (图5 d)。在多元回归模型中,MMP-12计算是预测(β= 0.361,R2= 0.13,0.47标准估计误差;p = 0.02)为肺气肿的存在证据(CT)和嗜酸性粒细胞不EPX或IL-13 (补充表S1)。最后,与FEV MMP-12水平负相关1% pred在COPD患者(r =−0.56;p = 0.006) (图5 f)和包含的这种联系仍然显著哮喘参与者(r =−0.45;p = 0.005)。
讨论
虽然2型比慢性阻塞性肺病更频繁地与哮喘有关,炎症或缺失的现状。在这项研究中,我们使用2型肺慢性炎症的小鼠模型(I5 /何)探索嗜酸性粒细胞和肺泡破坏之间的联系,没有任何内涵对于生理功能所需的诊断哮喘或慢性阻塞性肺病,或吸烟引起的参与途径。这些老鼠发展eosinophil-dependent肺部疾病,没有当过eosinophil-deficient老鼠(I5 /何/ PHIL),但可能与eosinophil-sufficient骨髓移植修复(14]。我们发现I5 /何老鼠eosinophil-dependent领空扩大发展。显著,MMP-12蛋白酶已知的关键中介肺泡破坏,高架在I5 /何肺部,这是完全依赖于嗜酸性粒细胞的存在。我们演示了体外,eosinophil-derived IL-13刺激生产MMP-12肺泡巨噬细胞。确认这些途径在活的有机体内我们走过I5 /何各种转基因小鼠和显示,嗜酸性粒细胞促进领空扩大依赖IL-13(和可能的il - 4,我们利用可用的液氧IL-4/13鼠标)和MMP-12。与这些观察结果相一致的是,之前的研究已经证实,MMP-12 IL-13诱导的肺(20.,36)和嗜酸性粒细胞是一个已知的IL-13[来源15,42]。此外,过度的IL-13鼠肺导致增加MMP-12水平和空域扩大36]。综上所述,这些数据显示一个明确的路径的嗜酸性粒细胞的破坏可能导致空域在慢性呼吸道疾病。
Eosinophil-derived IL-13已被证实能促进M2巨噬细胞分化以及积累在过敏性肺部炎症的小鼠模型15]。M2肺泡巨噬细胞已经被确认为MMP-12-producing细胞(了38])。值得注意的是,我们发现其他蛋白酶与肺泡的破坏,即。MMP-2和9,也提高肺的I5 /何老鼠依赖eosinophil-derived IL-4/13。嗜酸性粒细胞在哮喘气道显示表达MMP-9 [45)和嗜酸性粒细胞很可能是间接的联系,通过与其他细胞如巨噬细胞相互作用,众多的生产改造代理,包括MMP-2和9。事实上,我们表明,切除MMP-12只是部分减少肺泡毁灭在I5 /何肺部和观察到,在老MMP-12-deficient I5 /何小鼠肺泡破坏的程度接近的I5 /(数据未显示),建议其他调停人的角色。主要贡献者可能包括其他基质金属蛋白酶和组织蛋白酶以前观察到导致这些变化与超表达转基因小鼠的肺部IL-13 [21]。未来的研究需要确定其他关键eosinophil-associated中介(s) I5 /何肺肺泡杀伤性。综上所述,这些交互突出当地的嗜酸性粒细胞的作用,监管机构免疫反应和改造活动(46]。
I5 /合模型使我们孤立的贡献嗜酸性粒细胞领空扩大。很可能其他细胞类型可以参与这项工作的途径探索。特别是,组2先天淋巴细胞(ILC2s)和Th2 t细胞产生IL-13肺部(了47,48]);此外,气道上皮和平滑肌已经被确认为生产商MMP-12 [49,50]。然而,我们发现,嗜酸性粒细胞可以调解这些活动是有趣的。虽然IL-13是分泌的因素,有可能是嗜酸性粒细胞是这些交互的一个特别巨大的来源。显然,嗜酸性粒细胞和肺泡巨噬细胞之间的相互作用值得进一步研究,因为它是可能的空间,时间和/或多因素协会(如。IL-13结合其他信号)对这些活动很重要。
在慢性阻塞性肺病致病性嗜酸性粒细胞的作用一直被认为是。尽管在慢性阻塞性肺病的病理生理学他们潜在的重要性,努力目标嗜酸性粒细胞在慢性阻塞性肺病的临床试验中也会见了有限的成功。一个非常温和的临床效益已经注意到患者血液中嗜酸性粒细胞后处理与皮下mepolizumab(一个anti-IL-5抗体,结果在嗜酸性粒细胞损耗)(METREX试验)51]。在平行研究评估两剂mepolizumab作为附加治疗经常加剧慢性阻塞性肺病患者的特点是嗜酸性粒细胞水平(METREO试验),急性加重的年增长率与安慰剂相比手臂被认为是微不足道的(51]。这些发现证实这些报道在一个较小的研究药物降低痰液和血液嗜酸性粒细胞,然而没有任何明显的改善迹象在加重,肺功能或放射性疾病严重程度的证据52]。同样,针对嗜酸性粒细胞在慢性阻塞性肺病使用benralizumab (anti-IL-5α受体抗体导致嗜酸性粒细胞损耗)没有显示出临床改善恶化的速度与安慰剂相比。然而,FEV温和改善1在药物的手臂,表明嗜酸性粒细胞,推而广之,嗜酸性因素可能会影响肺功能(53]。
有限的改善临床试验检查在慢性阻塞性肺病anti-eosinophil代理可能是由于不可逆转的领空扩大。我们实验表明嗜酸性粒细胞的作用领空的起始/发展扩大,尽管是间接通过刺激MMP-12(可能还有其他蛋白酶)生产由肺泡巨噬细胞。事实上,在慢性阻塞性肺病患者嗜酸性粒细胞的证据有一个可以显著提升MMP-12,这是计算的预测存在的CT肺气肿的证据。这些发现表明战略目标中嗜酸性粒细胞嗜酸性COPD可能是有益的,但这与肺功能作为主要的长期研究结果可能需要欣赏这个好处。替代策略IL-5封锁这一目标嗜酸性粒细胞和其他细胞(如。ILC2s)可能会减少急性加重,并为未来的研究应考虑。一个这样的策略建议由以前的观测和来自本研究的发现是IL-33和IL-13封锁。
eosinophil-driven肺气肿的概念研究了在慢性阻塞性肺病军团之前,确定血嗜酸性粒细胞之间的关联和结缔组织杀伤性标记(54之间,痰液嗜酸性粒细胞和肺气肿指数定量CT (11]。此外,网络分析结合措施的血液,骨髓,以及临床变量,证明了免疫介导的修复能力是受损的血液嗜酸性粒细胞升高和/或肺气肿(55]。目前的研究提供了机械,小鼠模型的证据和确凿的数据从一个“真实的”COPD组,支持先前的结果。
总之,我们的研究结果揭示了角色eosinophil-derived IL-13 MMP-12肺泡破坏通过感应。哮喘和慢性阻塞性肺病诊断基于生理标准,前者展示可逆气流阻塞或气道高反应性,而后者证明固定气流阻塞。我们翻译研究慢性阻塞性肺病患者嗜酸性,表明发展的贡献MMP-12 eosinophil-mediated感应的肺气肿。哮喘或慢性阻塞性肺病患者的痰测试,考虑到嗜酸性炎症这些疾病之间可以共享组件,但肺气肿不是经典与哮喘有关。有趣的是推测,我们的发现可能扩展到其他慢性炎症性呼吸道疾病。值得注意的是,哮喘疾病进展和严重程度与嗜酸性粒细胞和可能发展成/重叠与慢性阻塞性肺病。事实上,哮喘病人最高MMP-12检测(水平与慢性阻塞性肺病子集)以及持续的嗜酸细胞增多症CT肺气肿的证据。最近的一份报告从Gelbet al。(56)基于证据的哮喘受试者2型表型发展中轻微的肺气肿和肺弹性损失。此外,报告一例不吸烟嗜酸性支气管炎病人发展肺气肿强调这种可能性(57]。总的来说,这些发现表明,关注治疗嗜酸性粒细胞肺管理IL-13和蛋白酶包括MMP-12可能放缓肺气肿的发展提供有效的策略在某些患者群体。
补充材料
确认
感谢实验室的所有成员李集团(美国梅奥诊所亚利桑那州斯科茨代尔,AZ)的支持,而且我们认识到优秀的行政支持由斯蒂芬妮·布伦德琳达Mardel和雪莉“查理”Kern(亚利桑那州梅奥诊所)。我们也承认梅兰妮Kjarsgaard,尼古拉·拉维妮,凯瑟琳·雷德福投资银行部Boylan(麦克马斯特大学和圣约瑟夫的医疗、汉密尔顿,加拿大)的专家技术援助。这项工作是献给我们亲爱的朋友和同事詹姆斯的记忆“杰米”李的比生活品质,其实是他的科学天才。我们深深地想念他。
脚注
可以从本文的补充材料www.qdcxjkg.com
作者的贡献:公元Doyle, J.J.修道士和J.J.李设计的研究。公元Doyle,星河LeSuer、结核病Bittner克里帕夏,J.J.兄弟,J.L.尼利J.A. Kloeber,伙夫垫片,S.I. Ochkur, t . Ho和m·穆克吉进行研究。公元Doyle,星河LeSuer、结核病Bittner克里帕夏,J.J.兄弟,S.I. Ochkur,文学士赖特,硕士,m·慕克吉p Nair J.J.李和电子艺界雅各布森分析数据。公元柯南道尔写了初稿的手稿。p . Nair莱特文学士、硕士,m·穆克吉和电子艺界雅各布森在修订过程中提供了重要的评估导致最后提交的手稿。所有作者都进行审核和批准的最终版本的手稿。
利益冲突:公元柯南道尔报告从NIH资助(F31HL124959),捐赠钱的梅奥诊所唐纳德·r·莱文家庭基金会和梅奥诊所的奖学金从梅奥诊所西德尼Luckman家庭博士前的奖学金,在进行这项研究的。
利益冲突:m·穆克吉没有披露。
利益冲突:星河LeSuer没有披露。
利益冲突:结核Bittner没有披露。
利益冲突:克里帕夏没有披露。
利益冲突:J.J.兄弟没有披露。
利益冲突:J.L.尼利没有披露。
利益冲突:正当Kloeber没有披露。
利益冲突:伙夫垫片没有披露。
利益冲突:S.I. Ochkur没有披露。
利益冲突:t .没有披露。
利益冲突:美国Svenningsen没有披露。
利益冲突:文学士赖特报告捐款支付给唐纳德·r·莱文家庭基金会的梅奥诊所,在进行这项研究的。
利益冲突:硕士排名没有披露。
利益冲突:J.J.李收到NIH资助(HL058723), NIH NCRR (K26 RR0109709)和梅奥医学教育和研究基金会,在本研究的开展;J.J.李死亡和这句话代表了作者的通讯作者。
利益冲突:p . Nair报告赠款和个人费用咨询和讲课从阿斯利康和Teva,从勃林格殷格翰集团资助,资助和个人费用从诺华公司讲课,赠款和个人费用咨询公司赛诺菲和葛兰素史克公司和个人费用咨询治疗先锋和Knopp外提交的工作。
利益冲突:电子艺界雅各布森报告从NIH资助(HL065228)和捐助的钱支付给唐纳德·r·莱文家庭基金会的梅奥诊所,在进行这项研究的。
支持声明:这项工作是在梅奥医学教育和研究基金会的支持下,国家卫生研究院NHLBI R01 HL058723 HL065228, NIH NCRR K26 RR0109709。公元柯南道尔得到了梅奥研究生院,梅奥诊所西德尼Luckman家庭博士前的奖学金,唐纳德·r·莱文家族基金会和NIH NHLBI F31HL124959。p .支持Nair弗雷德里克·e·Hargreave Teva创新椅子上气道疾病。资金信息,本文已沉积的Crossref资助者注册表。
- 收到了2018年7月12日。
- 接受2019年1月17日。
- 版权©2019人队