摘要
肝素的抗肿瘤和抗转移特性尚未在早期癌症患者中进行测试。研究了辅助低分子肝素(LMWH) tinzaparin是否影响切除术后非小细胞肺癌(NSCLC)患者的生存。
完全切除的I、II或IIIA期NSCLC患者随机分配皮下接受tinzaparin 100 IU·kg−1每天一次,持续12周或在标准护理之外不进行任何治疗。该试验是开放标签的,对研究结果进行了盲目的中央裁决。主要结局是总生存期。
在549例随机分为丁扎肝素组(n=269)或对照组(n=280)的患者中,均数±sd年龄61.6±8.9岁,II - III期190例(34.6%),辅助化疗220例(40.1%)。中位随访5.7年。两组间总生存期无显著差异(危险比(HR) 1.24, 95% CI 0.92-1.68;p = 0.17)。两组间的累计复发率无差异(子分布HR 0.94, 95% CI 0.68-1.30;p = 0.70)。
佐剂tinzaparin对完全切除的I - IIIA期NSCLC患者的总生存率和无复发生存率没有可检测到的影响。这些结果不支持LMWHs作为抗肿瘤药物的进一步临床评估。
摘要
肝素的抗转移特性是否有益于早期癌症患者尚不清楚。在这项III期试验中,肺癌切除术患者的辅助丁扎肝素对总生存期和肿瘤复发没有影响。http://ow.ly/RZt030lpCuQ
简介
凝血与癌症进展之间的相互作用以及肝素的抗肿瘤特性被广泛记录在体外在动物实验中[1- - - - - -6]。特别是,p -选择素抑制、内皮粘附减少和抗血管生成是肝素抑制微转移瘤播散和早期生长的主要机制。相比之下,少数专门探讨肝素对癌症患者生存影响的研究结果是相互矛盾的,而且大多是负面的[7- - - - - -12]。然而,这些研究不仅大多数是在患有各种类型癌症的患者中进行的,这使得他们的结果很难适用于一种特定的癌症类型[8,10,13],但所有研究都包括大多数局部晚期或转移性疾病患者,即。对于那些抑制转移过程早期阶段似乎无关紧要的患者。事实上,先前试验的亚组分析和事后对癌症相关血栓形成患者的随机试验分析表明,肝素对生存的影响可能在早期癌症患者中更为明显或仅限于早期癌症患者[9,11,14],但这个问题并没有得到具体的解决,并鼓励进行更多的研究[13,15]。
肺癌是全球癌症死亡的主要原因。非小细胞肺癌(NSCLCs)约占肺癌的80%。即使是早期可切除的NSCLC患者,5年总生存率仍保持在60%左右[16,17]。Tinzaparin in Lung Tumors (TILT)研究旨在前瞻性评估低分子肝素(LMWH) Tinzaparin能否提高I - III期NSCLC患者的总生存期。
方法
研究设计与监督
TILT试验是一项随机、多中心、开放、对照试验,对结果进行盲法判定。该试验根据赫尔辛基宣言和良好临床实践指南进行,并得到法国法兰西岛第一独立伦理委员会的批准。所有患者均获得书面知情同意。这项研究由一个执行指导委员会设计和监督,并由援助Publique-Hôpitaux de Paris赞助,该组织在提交手稿发表的决定中没有任何作用。一个独立的数据和安全监测委员会审查了安全数据。所有作者均可充分查阅数据,并保证数据的准确性和完整性,并证明试验是按照议定书和所有修正案进行的。该试验在ClinicalTrials.gov上注册,编号为NCT00475098.
病人
手术后8周内纳入18岁以上完全切除的I期、II期或IIIA期NSCLC患者。详细的纳入和排除标准载于补充附件.根据纳入时使用的TNM分期进行分期,即。第六版至2008年12月,其后为第七版[16,18]。
随机
符合条件的患者根据治疗分配的随机数字列表,以1:1的比例随机分配接受丁扎肝素或不接受抗凝剂。该列表由计算机生成,使用小尺寸(2,4,6)交替块使其不可预测,并根据中心和肿瘤分期(I与II−III)。一个互联网应用程序(CleanWeb)允许中央随机化。
干预措施
在实验组,tinzaparin (Innohep;Leo Pharma France, Vernouillet, France)的剂量为100 IU·kg−1在常规护理基础上,每日一次皮下注射,持续12周。治疗在纳入访视后尽快开始,手术后不超过8周。对于血小板计数低于每毫米3万的患者停止使用3.或疑似肝素诱导的血小板减少症。
常规治疗
在两组中,实施辅助化疗的决定都是在每个中心的常规多学科会议上做出的。该决定主要取决于病理阶段、表现状况、共病和患者偏好,独立于任何参与研究的提议。在接受化疗的患者中,推荐三到四个周期的铂基(最好是顺铂)双联治疗[19]。
患者管理及随访
在为期12周的研究治疗期间,tinzaparin组在研究治疗开始后的第4周和第8周安排了两次针对该试验的额外访问。在对照组中,这些访问是可选的。两组均安排了16周的随机随访。之后,两组患者每年至少安排一次访问,直到研究结束。当病人不去就诊时,当地调查员会尽一切努力与病人取得联系。在无法获得相关信息时,从患者出生地的出生和死亡登记处获得了患者的生命状况。
结果
该研究的主要结果是总生存期。次要指标包括丁扎肝素组或对照组在12周治疗期间记录的严重出血(补充附件),无复发生存率,癌症相关死亡率,以及整个随访期间记录的症状性静脉血栓栓塞事件(补充附件).所有疑似结局事件和死亡由一个独立的临床事件委员会裁决,该委员会的成员不知道治疗分配。
样本大小
主要疗效结局的样本量估计基于完全切除的I、II或IIIA期NSCLC患者的预期死亡率,对照组估计为每年10% [17]。为了检测到风险比(HR)为0.66,功率为80%,1型误差为5%,每位患者随访3年,需要纳入800例患者。
2010年6月,由于纳入率低于预期,且不了解事件率,决定重新评估样本量。我们决定对所有患者进行随访,直到固定的研究结束日期,即在最后一位患者纳入后3年,而不是对每位患者进行3年的固定随访。根据招募率,预期中位随访时间增加到4年。在相同的假设下,通过增加预期事件的数量,以检测0.66的风险比,需要纳入550例患者。使用nQuery Advisor 4.0软件进行计算。
统计分析
根据意向治疗原则进行分析,使用的数据更新于2016年6月15日。生存期计算从随机化日期到死亡日期(总生存期),复发日期(无复发生存期),或在审查情况下最后一次接触日期。在最后一次已知的随访中,对未达到主要结局或失去随访的患者的数据进行审查。每方案人群定义为纳入和排除标准无重大偏差的所有患者(补充附件),实验组接受丁扎肝素治疗≥30天。
使用Kaplan-Meier方法构建时间-事件曲线,并通过log-rank检验进行比较,使用Cox模型估计风险比和95%置信区间。使用Schoenfeld残差检验比例风险假设。为了估计复发的累积发生率,与肺癌指标无关的死亡被认为是竞争风险,并使用了累积发生率曲线。组间比较采用Gray检验,Fine和Gray模型用于估计子分布风险比[20.]。Fine和Gray模型的比例风险假设通过图形验证[21]。根据肿瘤分期对模型进行调整。
预先指定的亚组分析包括肿瘤分期(I与II-III)和辅助化疗(是或否)。使用Cox模型测试了治疗与分期之间以及治疗与辅助化疗之间的相互作用,以调查在预先计划的兴趣亚组中,治疗对主要结局的影响是否不同。所有测试都是双面的。使用SAS软件9.3版或R软件2.14.0版(survival和cmprsk包)进行分析。结果的呈报是根据CONSORT声明[22]。
出资人的角色
该研究得到了法国卫生部颁发的两项拨款(PHRC AOM05185和PHRC AOM12612)的支持。资助者在研究设计、数据收集、数据收集、数据解释或手稿写作中没有任何作用。Leo Pharma提供了研究药物和补充资助,但在研究设计、研究实施、数据分析和提交手稿的决定中没有任何作用。
结果
病人
从2007年8月到2013年6月,法国35个中心纳入了553名患者(补充附录)。4名患者撤回了参与研究和使用其数据的同意(3名tinzaparin和1名对照组)。其余549例患者被纳入意向治疗分析,对照组280例,丁扎肝素组269例(图1).基线人口统计和疾病特征在两个研究组之间很好地平衡(表1).
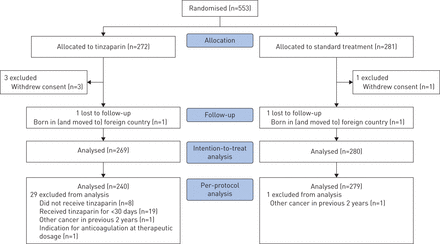
试验参与者的CONSORT流程图。意向治疗人群包括所有接受随机分组的患者减去4名撤回同意的患者。按方案人群定义为实验组中所有纳入和排除标准无重大偏差且接受丁扎肝素≥30天的患者。
在tinzaparin组,8例(3.0%)患者未接受任何剂量的研究药物,另外19例(7.1%)患者接受了<30天的研究药物,224例(83.3%)患者接受了8周的>治疗。中位随访5.7年(四分位数范围5.4-5.9年)。2016年6月15日,除两名患者外,其余患者均有生命状态。
主要的结果
对照组和tinzaparin组分别有79例和89例死亡。两组患者的总生存期差异无统计学意义(HR 1.24, 95% CI 0.92-1.68;p = 0.17) (图2).对照组和tinzaparin组的5年总生存率分别为74.2% (95% CI 68.9%-79.9%)和68.2% (95% CI 62.5%-74.4%)。
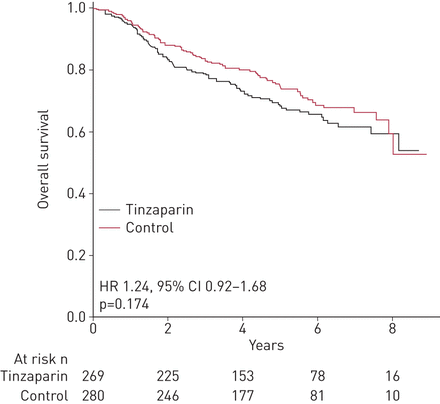
意向治疗人群的总生存期。Kaplan - Meier根据意向治疗人群的治疗组估计总生存期。tinzaparin组5年总生存率估计为68.2% (95% CI 62.5-74.4%)与对照组为74.2% (95% CI 68.9 ~ 79.9%)。p值采用log-rank检验计算。HR:风险比。
二次结果
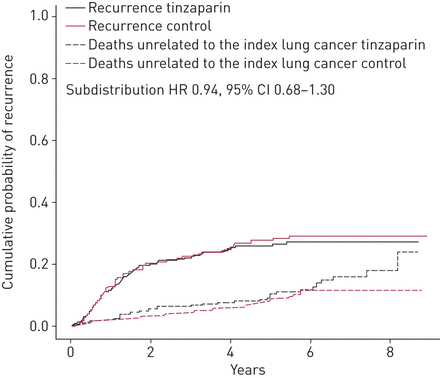
对照组和丁扎肝素组分别有46例(16.4%)和50例(18.6%)患者死于肺癌(SHR 1.17, 95% CI 0.78-1.74;p = 0.46) (表2).两组患者的累计复发率差异无统计学意义(SHR 0.94, 95% CI 0.68-1.30;p = 0.70) (图3).对照组和tinzaparin组5年累计复发率分别为27.8% (95% CI 22.4% ~ 33.2%)和25.9% (95% CI 20.6% ~ 31.3%)。丁扎肝素组2例(与对照组中无一人)在治疗期间发生严重的非致命性出血事件。对照组和丁扎肝素组在治疗期间分别有1例(0.4%)和19例(7.1%)发生轻微出血事件(p<0.001)。在整个随访期间,对照组20例(7.1%)患者和丁扎肝素组18例(6.7%)患者发生了症状性静脉血栓栓塞(SHR 0.95, 95% CI 0.68-1.32;p = 0.75)。
意向治疗人群中指标肺癌判定复发的累积风险。肺癌以外的其他原因导致的死亡是竞争风险(虚线)。HR:风险比。
亚组分析
在220例接受辅助化疗的患者中,使用丁扎肝素与总生存期显著降低相关(HR 1.78, 95% CI 1.13-2.81;交互作用P =0.03),而未接受辅助化疗的329例患者在各治疗组间无差异(图4).治疗组是接受辅助化疗患者死亡的唯一显著预测因素(补充附录,表A1).对照组和tinzaparin组分别有22例(20.0%)和33例(30.0%)患者的初始肺癌是死亡原因(表2),两治疗组的累计复发率差异无统计学意义(SHR 1.17, 95% CI 0.76-1.83;p = 0.47) (图5).
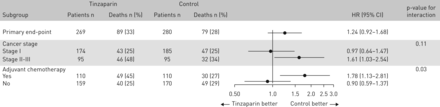
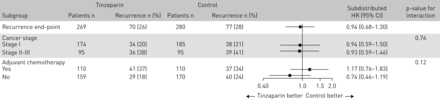
在两个预先计划的亚组分析中,使用辅助化疗和肿瘤期(I与II-III)(意图-治疗分析)。HR:风险比。
在使用辅助化疗和肿瘤分期的两个预先计划亚组分析中,指数肺癌复发的累积风险(I与II-III)(有意治疗人群)。肺癌以外的其他原因导致的死亡是竞争风险。HR:风险比。
在190例II - III期疾病患者中,使用丁扎肝素与总生存期降低相关(HR 1.61, 95% CI 1.03-2.54;交互作用的p值为0.13),而在359例I期疾病患者中,治疗组之间没有观察到差异(图4).在II - III期肺癌患者中,没有潜在的死亡预测因子(补充附录,表A2).对照组和tinzaparin组分别有24例(25.3%)和29例(30.5%)患者的初始肺癌是死亡原因(表2),两组间的累计复发率无显著差异(图5).
讨论
在这项大型多中心随机试验中,在完全切除的I - III期NSCLC患者中,tinzaparin作为辅助治疗,与提高总生存期或降低肿瘤复发风险无关。大样本量、单一癌症类型的同质研究人群、对研究药物的高依从性、随访期长、患者失访率极低以及总生存期的稳健主要终点都支持研究结果的可靠性。
以往探索肝素作为抗癌药物作用的临床试验大多或仅在局部晚期或转移性疾病患者中进行,因此无法回答一些实验结果提示的肝素在早期癌症中的作用问题。TILT研究的目的在于解决这一问题,该研究采用了在纳入时未检测到转移的非小细胞肺癌患者的独特同质人群。结合晚期癌症的阴性结果,目前的结果强烈反对低分子肝素作为抗癌治疗的任何临床显著效果。
在本试验中,治疗将在手术后2个月内开始,并延长3个月,并在需要时同时进行最终的辅助化疗。选择一种“中间”(既非预防也非治疗)tinzaparin剂量,以与某些表明抗癌作用的剂量-反应关系的实验结果相平行[23],并考虑到以往研究的结果,这些结果表明预防性剂量通常与生存率的增加无关[9,13,14],同时避免了与治疗剂量相关的出血风险。较高的剂量和/或较长的治疗时间是否会产生不同的结果尚不清楚,但目前的结果并不为此类研究提供支持。最后,在显示转移扩散减少的动物模型中,肝素在静脉注射肿瘤细胞之前施用[5]。因此,肝素给药时机不同的问题(如。在手术后或手术前尽早使用丁扎肝素)是有意义的,值得进一步研究。这一假设目前在一项大肠癌患者的试验中得到验证(NCT01455831).
预先计划的肿瘤分期亚组分析结果和辅助化疗的使用是出乎意料的,在阴性试验的背景下应谨慎解释。在肿瘤分期分析中,相互作用试验没有达到统计学意义,并且在每个方案人群中,在II - III期疾病中观察到的两组之间的生存差异不再显著。在接受辅助化疗的患者(其中71%为II - III期肿瘤)中,使用丁扎肝素与较低的生存率相关,并且在每方案人群中差异仍然显著。然而,与分期不同的是,辅助化疗的随机化没有分层,这可能导致两组间未知的不平衡。在该亚组中,两组间的累积复发风险未观察到差异,反对丁扎肝素和化疗之间的直接负相互作用。此外,在体外实验表明tinzaparin可逆转人卵巢癌细胞对顺铂的耐药[24]。因此,在接受辅助治疗的tinzaparin组患者中观察到死亡过多的原因难以确定。在任何情况下,这些亚群分析的发现,虽然耐人寻味,但只能被视为假设的产生。
该研究的局限性包括开放标签设计、完成纳入需要6年时间、低于预期的死亡率以及两组术后预防性低分子肝素的使用。关于开放标签设计,主要研究结果是总死亡率,这使偏倚的概率最小化,所有临床终点,包括死亡原因,都是盲目判定的。对于较长的纳入期和随访期,5年生存率仍然是比较癌症治疗的可靠终点,5年仍有大量患者存在风险加强了研究结果。此外,在整个纳入和随访期间,切除NSCLC的辅助治疗保持不变,使参考治疗成为有效的比较。高于预期的生存率可能是由于纳入了很大比例的I期患者(65%)和使用现代分期工具,包括正电子发射断层扫描和脑磁共振成像,提高了分期的准确性和人工预后[25]。最后,根据目前的指导方针,两组术后短时间(11天)给予低分子肝素,不太可能解释我们的负面发现。
这项研究不能证明tinzaparin作为切除的早期NSCLC的辅助治疗有任何临床益处。结合最近一项晚期肺癌试验的负面结果[13],这些结果表明,无论凝血在癌症进展中的作用如何,进一步探索肝素作为抗肿瘤药物,至少在肺癌中,不应再被认为是一种临床相关的方法。
补充材料
确认
我们感谢乔治·蓬皮杜欧洲医院临床试验部门负责试验组织、数据监测、收集和管理的所有善良和努力工作的人。
脚注
2018年10月4日在线发布;2018年10月10日重新发布,对利益冲突披露声明进行了修订。
这篇文章有补充资料可从www.qdcxjkg.com
部分内容于2017年7月12日在柏林举行的第二十六届国际血栓与止血学会会议上发表。
这项研究注册在ClinicalTrials.gov标识符编号NCT00475098.个人去识别参与者数据、研究方案和统计分析计划的请求应发送到G. Meyer (guy.meyer@aphp.fr)或G. Chatellier (gilles.chatellier@aphp.fr)。
作者贡献:G. Meyer, P. Girard和M. Alifano是TILT试验的协调研究人员,他们对试验的概念和设计做出了重大贡献,起草了手稿,并对重要的智力内容进行了批判性的修改。G.夏特列对审判的构想和设计做出了重大贡献,起草了手稿,并对重要的智力内容进行了批判性的修改。所有作者都阅读并批准了最终稿,并同意对工作的各个方面负责,以确保与工作任何部分的准确性或完整性相关的问题得到适当的调查和解决。
利益冲突:G. Meyer报告了来自Leo Pharma的拨款和非财政支持,在提交的工作之外。
利益冲突:贝丝没有什么可透露的。
利益冲突:H. Doubre没有什么可透露的。
利益冲突:A. Charles-Nelson没有什么可透露的。
利益冲突:S. Aquilanti报告称,在提交的工作之外,利奥制药提供了非财政支持。
利益冲突:A. Izadifar没有什么可透露的。
利益冲突:R. Azarian没有什么可透露的。
利益冲突:I.莫内没有什么可透露的。
利益冲突:C. Lamour没有什么可透露的。
利益冲突:R. Descourt没有什么可透露的。
利益冲突:G. Oliviero没有什么可透露的。
利益冲突:L. Taillade没有什么可透露的。
利益冲突:C. Chouaid没有什么可透露的。
利益冲突:F.吉罗没有什么可透露的。
利益冲突:pe。法尔考兹没有什么可透露的。
利益冲突:M-P。Revel没有什么可透露的。
利益冲突:V. Westeel没有什么可披露的。
利益冲突:A. Dixmier没有什么可透露的。
利益冲突:J. Tredaniel没有什么可透露的。
利益冲突:S. Dehette没有什么可透露的。
利益冲突:C. Decroisette没有什么可透露的。
利益冲突:A. Prevost没有什么可透露的。
利益冲突:E.皮雄没有什么可透露的。
利益冲突:E.法布尔没有什么可透露的。
利益冲突:J-C。Soria是Medimmune的全职员工(该职位是在研究完成后担任的),在提交的工作之外,她还从阿斯利康、罗氏、赛诺菲、施维雅、艾伯维和pharmacar获得了咨询费。
利益冲突:S. Friard没有什么可透露的。
利益冲突:J-B。斯特恩没有什么可透露的。
利益冲突:L. Jabot没有什么可透露的。
利益冲突:G. Dennewald没什么可透露的。
利益冲突:G. Pavy没有什么可透露的。
利益冲突:P. Petitpretz没有什么可透露的。
利益冲突:J-M。图拉尼没有什么可透露的。
利益冲突:M. aliifano没有什么可透露的。
利益冲突:查特利耶医生没什么可透露的。
利益冲突:P.吉拉德报告个人费用和来自利奥制药的非经济支持,在提交的工作之外。
支持声明:该试验由巴黎援助Publique-Hôpitaux组织赞助,并由法国卫生部诊所医院计划(PHRC AOM05185和PHRC AOM12612)提供两笔赠款。利奥制药公司提供了药物和额外的拨款。本文的资助信息已存入交叉参考基金注册.
- 收到了2018年6月30日。
- 接受2018年8月6日。
- 版权所有©ERS 2018