抽象
的肺血管功能障碍指数与在慢性过敏性肺炎死亡率相关http://ow.ly/1nwG30jwTSm
致编辑:
慢性过敏性肺炎(CHP)是经常与肺纤维化相关联的公共间质性肺病(ILD)[1]。间患者CHP,肺功能损害程度和纤维化的程度是公知的死亡的预测[2,3]。在其他形式中ILD的,例如特发性肺纤维化(IPF)和结节病,休息期间平卧右侧心脏导管插入术(RHC)另外与不良预后相关测量异常肺血液动力学[4-7]。在热电联产,然而,RHC的预测值是未知的。
We recently found that pulmonary hypertension (PH), defined by a mean pulmonary arterial pressure (mPAP) ≥25 mmHg at RHC, is a prevalent feature of CHP [8]。在本报告中,我们扩展我们的分析评估在这一人群的肺血流动力学和死亡率之间的关联。
这是一个观察性研究,评估在经历了一个标准化的PH评估协议,包括RHC [CHP患者以前发表的人群死亡率8]。据此前报道[8],分别在巴西圣保罗联邦大学ILD门诊2011年8月和2013年2月间收集的数据。1023名ILD连续门诊患者研究期间进行评价,以确定那些具有不CHP相关合并症或毛细血管后PH(N = 47)。死亡率进行了评估,直到2016年6月的数据以平均值±SD或中值(四分位数间距)为正常和非正态分布的变量,分别基于所述夏皮罗 - 威尔克统计量。幸存者和死亡组之间的比较用T检验用于正常或Mann-Whitney检验用于非正态分布变量所做的。分类变量比较采用卡方和Fisher精确检验比较。接收器工作特性(ROC)曲线用于获得最佳的血液动力学截止值用于预测。进行Cox比例风险和的Kaplan-Meier生存率分析,按照标准程序。用力肺活量(FVC)和动脉血氧饱和度之间的相关性分析(小号AO2)与进行肺血管阻力(PVR)和肺血管的顺应性(PVC)来检查ILD严重性和肺血管功能障碍之间的关联。P <0.05被认为是显著。
该研究的样品(N = 47)包含25个非PH和22预毛细管PH患者[8], with 12 subjects having severe pre-capillary PH, defined by mPAP >35 mmHg or mPAP ≥25 mmHg associated with a cardiac index <2.5 L·min-1·米-2[9]。中号edian follow-up was 40 (29–46) months. Overall mortality was 45% (21 out of 47 patients); 1-year, 2-year and 3-year mortality rates were 13% (six out of 47 patients), 21% (10 out of 47 patients) and 36% (17 out of 47 patients), respectively. Among severe PH patients, 1-year, 2-year and 3-year mortality rates were 33% (four out of 12), 42% (five out of 12) and 58% (seven out of 12), respectively. The mean age was 57±13 years for nonsurvivors and 64±9 years for survivors (p=0.06), without sex differences between these groups (76与77层%的女性,p值= 0.61)。FVC和小号AO2对于死亡者与幸存者44±4与预测72±18%(P <0.01)和89(84-94)与95(93-96)%(P <0.01),分别。Time from CHP diagnosis was 10 (1–25) months for nonsurvivors and 36 (9–82) months for survivors (p=0.03).
在静息RHC,死亡者有升高的肺动脉压,升高的肺梯度(TPG),升高的舒张肺梯度(DPG),升高的PVR和相比幸存者降低PVC(肺动脉压28±7与24±5 mmHg, p=0.05; TPG 19±7与14±4 mmHg, p=0.01; DPG 12±5与8±4 mmHg, p=0.02; PVR 4.1±1.8与2。8±0.9 Wood units (WU), p=0.01; and PVC 3.0 (1.8–4.0)与4。2(2.9–4.8) mL·mmHg-1,P = 0.07)。有幸存者和死亡组(2.7±0.4之间心脏指数无显着差异与2。7±0.5 L·min-1·米-2,P = 0.89)。
By ROC curve analysis, the optimal cut-off point to separate nonsurvivors from survivors was 24 mmHg for mPAP (area under the curve (AUC) 0.66, p=0.07), 15 mmHg for TPG (AUC 0.71, p=0.01), 10 mmHg for DPG (AUC 0.69, p=0.02), 3.3 WU for PVR (AUC 0.71, p=0.01) and 3.6 mL·mmHg-1为PVC(AUC 0.69,P = 0.03)。一种fter adjusting for age, sex and time from CHP diagnosis, a TPG ≥15 mmHg (HR 4.72, 95% CI 1.47–15.16, p=0.01), a PVR ≥3.3 WU (HR 3.23, 95% CI 1.29–8.09, p=0.01) and a PVC ≤3.6 mL·mmHg-1(HR 3.52; 95%CI 1.41-8.80,p值= 0.01)残留的死亡率预测因子。By Kaplan–Meier survival curve analysis, the aforementioned PVR and PVC thresholds dichotomised nonsurvivors from survivors starting at 6 months following RHC (图1)。决定系数(R2)FVC之间(%预计值)和PVR,和FVC之间(%预计值)和PVC为0.32(P <0.01)和0.15(分别为p <0.01)。测定之间的摩擦系数小号AO2和PVR,和小号AO2和PVC为0.47(P <0.01)和0.31分别(P <0.01)。
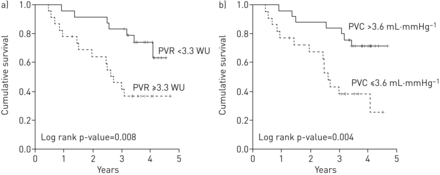
用于治疗慢性过敏性肺炎一)肺血管阻力(PVR)和b)肺血管顺应性(PVC)的Kaplan-Meier存活曲线。
总之,我们发现,在RHC异常血流动力学肺在患者CHP与死亡率相关。这些结果表明,肺血管功能障碍,其特征在于,升高的PVR和降低的PVC,在CHP负长期预后的影响。
In patients with sarcoidosis and IPF, PVR >3 WU [7] and >6.23 WU [6],已经分别与更差的存活相关。此外,肺动脉压的升高未成年人还发现,预测患者的预后在IPF [4,五]。在目前的研究中,肺动脉压本身并不是死亡率的一个强有力的预测;however, patients with PVR ≥3.3 WU encountered a more than three-fold increased mortality rate compared with patients with PVR <3.3 WU, despite a similar cardiac index. These observations might be indicative of a yet preserved relationship between the right ventricle (RV) contractility and the afterload, before pulmonary pressures significantly increase and/or the RV becomes dysfunctional [10],如对于肺血管疾病的早期阶段的情况下[11]。
一种long these lines, the optimal PVC cut-off value of 3.6 mL·mmHg-1从幸存者单独死亡者较先前在肺动脉高压(PAH)报道高得多[12,13]。中号ahapatra等。[12]和CAMPO等。[13] identified that PVC values of 0.83 mL·mmHg-1and 1.25 mL·mmHg-1用患者的死亡率分别为特发性肺动脉高压和硬皮病相关的PAH,相关的。因此,我们的研究结果PVC可能反映早期肺血管僵硬[14,15],并最终认为,PVC是ILD的病理临床相关性。
总之,我们的数据添加到理解肺血管供血不足的ILD预后作用的框架,这表明轻度增加RV后负荷影响患者的临床结果CHP。我们的研究结果,因此,当危险分层患者的热电联产和确定最佳的治疗策略,包括推荐或优先肺移植应该是有帮助的。
有趣的是,在目前的研究预测死亡率血液动力学测量是不完全由实质性肺病的严重性合理的,给定的FVC和PVR / PVC之间确定的弱/中等系数。此外,小号AO2解释<观测到的肺血管功能障碍的50%。因此,升高的PVR和降低CHP死亡者的PVC有可能的多种病理生理机制的结果对肺血管重构,例如慢性炎症,肺微循环(可能是由CHP bronchiolocentric图案增强),缺氧性血管收缩的畸变和内皮会聚和血管平滑肌细胞功能障碍。
目前的研究是由小的样本大小和相对低数量的事件限制。然而,据我们所知,这是患者最大的群体与CHP报道,迄今为止,前瞻性与侵入血流动力学和长期随访评估,正因为如此,目前的数据提供了重要的洞察在这一人群的肺血管功能不全预后的作用。
总之,肺血管功能障碍指数与热电联产死亡率相关,因此提供有价值的预后信息。除了所述识别的下降FVC和小号AO2,这也与死亡率相关,一个鉴定升高的PVR和减少在CHP访问预后和确定优先次序或推荐用于肺移植时PVC应该是有帮助的。
脚注
利益冲突:无申报。
支持声明:肺血管疾病服务,呼吸病科,医学系。圣保罗(Unifesp),圣保罗,SP,巴西联邦大学。本文资金的信息已交存交叉引用出资者注册。
- 收到2017年11月29日。
- 公认2018年3月25日。
- 版权所有©ERS 2018















