摘要
基于正电子发射断层扫描-计算机断层扫描(PET-CT)成像的临床N1 (cN1)非小细胞肺癌(NSCLC)患者中,四分之一存在隐性纵隔淋巴结累及(N2疾病)。在一项前瞻性研究中,单腔超声检测N2疾病的敏感性不令人满意(38%)。目前的前瞻性多中心试验研究了电视辅助纵隔镜(VAM)或vama -淋巴结切除术(VAMLA)术前纵隔分期的敏感性。
PET-CT成像后可手术和可切除(疑似)NSCLC和cN1的连续患者行VAM(LA)。主要研究结果是检测N2疾病的敏感性。次要终点为N2疾病患病率、阴性预测值(NPV)和VAM准确性(LA)。
我们发现105例CN1上成像,26%最终发展N2疾病。与VAM(LA)侵入性纵隔分期具有73%的灵敏度检测到N2疾病。的NPV是92%和准确性93%。VAM(LA)中分摊淋巴结站的位数为4(IQR 3-5),和在96%,至少三个站进行了评估。
VAM(LA)检测cN1肺癌纵隔淋巴结疾病的敏感性为73%,可作为该患者组切除前纵隔淋巴结评估的首选技术,PET-CT阴性后纵隔淋巴结隐匿阳性的几率为四分之一。
摘要
电视纵隔镜在cN1非小细胞肺癌患者中检测N2疾病的敏感性达到73%;N2的患病率是26%http://ow.ly/VrzL30gIOWm
介绍
在疑似非小细胞肺癌(NSCLC)和肺门或肺内淋巴结肿大或18f -氟脱氧葡萄糖(FDG) avid淋巴结或肺内淋巴结(临床N1疾病,cN1)的患者中,估计切除时未预料到的纵隔淋巴结阳性(N2疾病)的风险在20%至30%之间[1-5.].
指南建议这些患者与CN1微创术前纵隔分期,如。videomediastinoscopy(VAM)或腔内超声[6.那7.].
在之前的一项前瞻性多中心研究中,我们证明,单用超声内镜检测cN1肺癌纵隔阳性淋巴结的敏感性仅为38%。如果超声检查为阴性,则增加纵隔镜检查,这一比例增加到73% [1].在N2隐匿性患病率低于30%,而内镜检测N2疾病的灵敏度为38%的情况下,这种双重方法可能并不划算。
在缺乏VAM的前瞻性多中心数据的情况下,我们评估了VAM作为欧洲胸外科学会(ESTS)指南中cN1患者的拟议策略[7.].这项多中心前瞻性研究的目的是评估在一组明确的cN1患者中VAM的敏感性、阴性预测值(NPV)和准确性。
患者和方法
病人
如果患者符合以下条件:18岁或以上;能够给予知情同意的;基于fdg -正电子发射断层扫描-计算机断层扫描(FDG-PET-CT),具有医学上可手术、可手术切除(疑似)NSCLC和临床N1疾病。cN1的定义如下:淋巴结肿大(CT上最大短轴≥10 mm)或N1位fdg - pet阳性淋巴结,根据国际肺癌淋巴结图研究协会(IE。淋巴结站10-14)[8.].如果纵隔血池中FDG摄取高于背景摄取,则认为淋巴结FDG- pet阳性。临床T类型为T1、T2和选定T3的肿瘤(IE。实质内肿瘤>7 cm, T3侵犯胸壁,或T3基于原发肿瘤叶内的额外结节(TNM恶性肿瘤分类,第七版)。既往接受过肺癌治疗的患者;存在不能切除的疾病、cT4或分期为cT3的中心肿瘤(IE。invasion of mediastinal pleura, invasion of phrenic nerve or parietal pericardium, tumour in the main bronchus less than 2 cm from the main carina), enlarged or FDG-positive mediastinal nodes or distant metastases (cM1); or previous endobronchial ultrasound assessment of mediastinal nodes were excluded from the study.
颈动脉栓塞
VAM在由经验丰富的心胸外科专用的胸手术室进行,按照惯例机构。甲颈横切口颈切口上方制成,并且气管前的肌肉在中线分离以暴露气管的前表面。气管前筋膜切开,这筋膜下飞机制造。触诊使用,以免错过任何近端气管前的节点。视频辅助纵隔镜下进行进一步解剖。按照ESTS准则,所有可访问的纵隔淋巴结将被采样,具有最小站是以4L-4R-7。VAM-淋巴结清扫术(VAMLA)是允许的,这取决于医生的判断。在标准的VAM,在不同的站淋巴结通过取样评估并不必完全去除[9.],而在VAMLA中,通常隆突下淋巴结和右侧气管旁淋巴结连同周围脂肪一起被完全切除,而左侧气管旁淋巴结则分别切除,尊重左侧返神经[10].胸腔镜手术(VATS)或胸椎旁纵隔镜检查不被认为是术前纵隔分期的一部分。病例报告表格包括一个淋巴结图,查询哪些淋巴结站未取样、部分取样或完全切除。
手术切除
如果纵隔镜检查为阴性,患者接受手术与外科核查主要通过手术系统的淋巴结清扫术[11]。如果VAM(LA)期间的冰冻切片呈阴性,则允许在同一麻醉期间进行切除。可通过VATS或开胸手术进行切除。遵循ESTS关于术中系统性淋巴结剥离的指南[11].病例报告质疑在手术中评估了哪些站,有多少淋巴结被切除,以及站是否被完全切除。
研究设计
这是一项基于FDG-PET/CT的前瞻性多中心非随机试验,研究VAM(LA)(指数试验)对连续可手术和可切除cT1-3N1M0(怀疑)NSCLC患者纵隔分期的敏感性。手术切除和系统淋巴结清扫是参考标准。机构审查委员会批准。协调中心是鲁汶大学医院。病例报告表包含了数据的交叉核对,如。通过比较显像后的cTNM、VAM后的cTNM、最后的pTNM、VAM(LA)和/或切除的结果是否改变了TNM分期的问题,以及单个节点站水平的结果。根据国际良好临床实践协调指南会议(International Conference on Harmonization Guidelines of Good Clinical Practice)的要求,实施了这些程序,获得了数据并进行了匿名处理。这项研究登记在ClinicalTrials.gov标识号NCT02222194(ASTER 3)。
端点
主要终点是在检测由VAM(LA)纵隔淋巴结转移(N2病)的灵敏度。灵敏度被定义为阳性患者纵隔分期的VAM(LA)的所有患者的纵隔淋巴结病的比例。与淋巴结清扫(通过开胸或胸腔镜)手术切除被认为是VAM(LA)之后的患者的参考标准,而不纵隔淋巴结病。次要终点是NPV,准确性,阴性检测后概率和N2 / 3的患病率的评估。
统计数据
将总样本量设置为250名患者,根据20%的患病率,预计有50名N2患者。假设敏感性为70%,我们计算出敏感性置信区间(CI)的一半宽度最多为13%的概率大于90%。双侧(Wilson评分)的计算CI基于二项分布。
所有纳入的患者的敏感性、患病率、NPV和检测后阴性的概率都是在有意治疗的基础上计算的。对于缺乏参考标准的病人(IE。VAM阴性后无原发性手术),采用多重imputation分析评估所有受试者的敏感性、患病率、NPV和准确性。纵隔分期阳性的结果假定纵隔疾病的最大概率。计算结果为:(VAM成功后n个假阴性)+(缺失n个参考标准))/(VAM成功后n个阴性)。使用Rubin规则对1000个输入数据集的结果进行了组合。所有分析都使用SAS软件,SAS System for Windows的9.4版本。p-值<0.05被认为是显著的。
结果
2014年6月至2017年3月,纳入105例可手术和可切除(疑似)的临床N1 NSCLC患者(图1).权责发生率低于最初预期,该研究于2017年4月初结束。患者临床特征见表1.
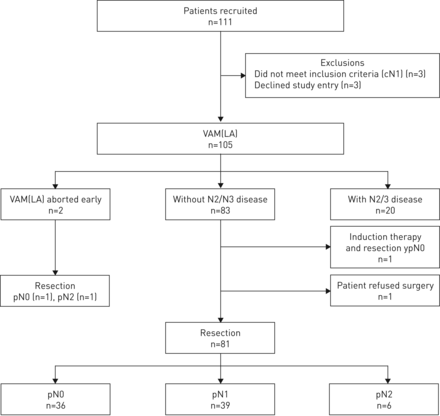
临床N1(疑似)非小细胞肺癌患者接受纵隔淋巴结分期的标准流程图。两个VAM(LA)早期流产:未评估淋巴结。VAM:视频辅助纵隔镜检查;VAM(LA):视频辅助纵隔镜淋巴结切除术;标准:报告诊断准确性研究的标准[23].
结果VAM
在20例患者中,VAM(LA)检测到阳性纵隔淋巴结。13例为单水平N2疾病,4例为多水平N2疾病,3例为N3疾病。活检淋巴结站的平均数量为3.9(标准偏差1.2),中位数为4(四分位间距3-5)。每位病人活检的淋巴结站总数的分布以及不同淋巴结站的活检频率如所示表2和3..31% (n=33)的病例标记为VAMLA。在两名患者中,在评估任何淋巴结之前流产了手术;在一个病例中,由于严重的后凸而不能使用纵隔镜,而在另一个病例中,由于手术过程中气管软化和呼吸系统问题而早期停止使用纵隔镜。在一个患者中,只有一个淋巴结被评估为N3病。4例(4%)患者报告了与VAM相关的不良事件:1例出血< 200ml, 1例无并发症伤口感染,2例短暂复发性神经麻痹。
切除和淋巴结切除术
共有85例患者接受了手术治疗。一个拒绝,另一个先接受新辅助治疗(图1), 83例患者接受了一期手术(68例肺叶切除术,7例双叶切除术和7例肺切除术)。46% (n=48)的患者在VAM(LA)当天进行手术,37% (n=39)的患者在第二阶段进行手术;后一组手术至VAM(LA)的中位延迟时间为14天(IQR 7-27)。7例患者在切除后发现纵隔淋巴结阳性(图1).其中之一是对他们来说,胸膈被提前终止的患者。错过纵隔转移为单级N2病5例,多层次的N2病两个例。临床特征可以发现表4,及淋巴结切除时的完整性表5.分析每个站的淋巴结移除数量被证明是不切实际的,因为碎片化;最多16个淋巴结(IE。片段)在一个站被报道。平均切除4个淋巴结。ESTS指南建议进行系统淋巴结清扫,至少切除三个部位(包括隆突下淋巴结),92%的右侧肿瘤和97%的左侧肿瘤获得了成功。
多重估算
对于两名患者,VAM(LA)阴性后的参考标准,IE。原发性手术与纵隔淋巴结评估缺失。83例VAM(LA)手术成功(未流产)后检测结果阴性的患者中,6例在手术时出现pN2/N3。如果两例pN2/N3信息缺失(无一期切除)的患者均为阳性,则VAM(LA)成功切除pN2/N3的概率为0.0964 (n=(6+2)/83)。这个数字被用于多重归因,作为两个没有参考标准的患者的纵隔疾病的最大概率。
讨论
这是首个评估cN1(疑似)NSCLC患者手术纵隔分期表现的前瞻性研究。我们的主要发现是,四分之一的cN1肺癌患者最终有N2疾病,这些患者中VAM(LA)检测阳性纵隔淋巴结的敏感性为73%。
目前的指南建议对cN1疾病和影像学上纵隔阴性的患者进行浸润性切除前分期[7.那12那13].然而,VAM或超声内镜作为首选的选择是开放的[7.].这些建议是基于包括I-III期肺癌患者在内的试验的亚组分析[14].绝大多数患者有临床N2疾病,只有少数患者有cN1疾病,影像学显示纵隔正常[15-17].在先前的研究中,我们测量前瞻性腔内超声的性能与CN1(怀疑)NSCLC选定的患者组。我们报道24%N2疾病和用于腔内超声的38%的灵敏度的患病率在单独检测纵隔疾病。这是提高到73%,如果加入VAM(表6)[1]在本研究中,我们报告N2疾病的患病率为26%,纵隔镜检查的敏感性为73%,测试后的概率为8%。因此,我们可以主张忽略内腔超声来评估纵隔淋巴结,而选择手术治疗在该患者组中,通过VAM(LA)进行al切除前分期。
文献中很少有报道评估临床分期为cN1的可切除和可手术NSCLC患者的最终病理分期分布。久田等.渡边和et al。据报道,仅基于CT的cN1患者中有30–37%在纵隔镜检查后纵隔淋巴结呈阳性[2那3.].金et al。报告称,包括FDG-PET在内的99例cN1显像后患者中,19%在肺切除术伴纵隔淋巴结清扫时发现有病理性N2病变[5.].在这项研究中,我们在三分之二发现26%的患病率,与单级N2疾病,多层次的N2疾病22%和N3疾病的11%。
我们的研究有一些局限性。招聘停在250 105例由于比原先预期的更慢的权责发生制率。可能的话,并没有在研究期间由于增加转诊腔内超声检查对纵隔淋巴结,这是一个排除标准的分期包括潜在患者。患者的较低数量增加了95%置信区间的宽度为诊断指标。然而,这是与患者病情CN1固体分析和结果上纵隔分期最大的前瞻性研究。其次,这项研究是由愿意参加关于分期手术的前瞻性研究机构进行的,结果可能会从手术前切除分期在日常实践中的表现不同[18].第三,我们没有报道切除淋巴结的数量,因为淋巴结的碎裂和患者之间的变异降低了其价值[19-21].按照ESTS指南进行标准的系统淋巴结清扫。第四,在31%的患者中,纵隔镜是VAMLA。理论上,VAM和VAMLA是不同的程序,但在现实中,程序通常可以被标记为“中间”,因为在同一操作中,一些站点被完全移除,而另一些站点被采样。VAM的可靠性在很大程度上取决于它的彻底性[13].在4例患者中,假阴性站在VAM期间被部分取样,如果完全移除站将会是阳性的。VAMLA在本研究中产生了良好的结果,没有报道并发症,也没有假阴性结果(表4).调用等.最近发表了在cN0-1 NSCLC患者中,VAMLA术后的敏感性为96%,NPV为99% [22].然而,VAMLA只在某些中心执行。未来的研究应该探讨这种技术是否能在更多具有类似结果的中心被采用。
总之,我们前瞻性地分析了在一组cN1(怀疑)NSCLC患者中手术前VAM(LA)纵隔分期的表现。我们确认四分之一的患者最终患有N2期疾病,我们发现VAM(LA)后敏感性为73%。在之前的前瞻性研究中,单靠超声检查在检测纵隔疾病方面的敏感性并不令人满意,因此我们建议VAM(LA)作为cN1 NSCLC患者切除前纵隔淋巴结分期的首选技术。
披露
补充材料
H.德卡鲁韦erj - 01493 - 2017 - _decaluwe
X.B. DjournoERJ-01493-2017_D'Journo
公共广播托马斯erj - 01493 - 2017 - _thomas
致谢
我们感谢Steffen Fieuws的统计支持(鲁汶生物统计学和统计生物信息学中心,L-BioStat)。
脚注
临床试验:本研究注册于ClinicalTrials.gov标识号NCT02222194.
支持声明:本研究得到了弗兰德斯研究基金对Herbert Decaluwe的资助(FWO申请40682)。本文的资金信息已存入交叉参考基金登记处.
利益冲突:可以在本文旁边找到披露www.qdcxjkg.com
- 收到了2017年7月22日。
- 公认2017年9月25日。
- 版权©2017人队















