摘要
与其他病因相比,结缔组织病相关性肺动脉高压(PAH-CTD)患者预后较差。潜在的CTD可以影响治疗效果和结果。我们对GRIPHON研究PAH-CTD亚组进行了特征描述,并评估了对selexipag的反应。
在334例PAH-CTD患者中,PAH与系统性硬化症(PAH- ssc)相关170例,系统性红斑狼疮(PAH- sle)相关82例,CTD/CTD-other混合相关82例。对于发病率/死亡率的主要复合终点,使用Cox比例危险模型计算危险比(HR)和95% CI。
与GRIPHON总体人群相比,CTD亚组年龄略大,女性比例较大,自诊断以来时间较短。PAH-SSc患者在基线时受损更严重,病程更进展。PAH-SLE则相反。Selexipag将PAH-CTD患者的综合发病/死亡事件风险降低了41% (HR 0.59;95% ci 0.41-0.85)。治疗效果与基线PAH治疗或CTD亚型无关(相互作用p分别为0.87和0.89)。不良事件主要与前列环素相关,并以selexipag治疗而闻名。
GRIPHON可以全面描述PAH-CTD患者的特征。Selexipag延缓了PAH的进展,在PAH- ctd患者(包括PAH- ssc和PAH- sle患者)中具有良好的耐受性。
摘要
Selexipag延缓疾病进展,并且在PAH- ctd中具有良好的耐受性,与亚型或其他PAH治疗无关http://ow.ly/SvIV30cqo9J
简介
结缔组织病(CTD)包括系统性硬化症(SSc)和系统性红斑狼疮(SLE)等不同类型的疾病[1- - - - - -3.].肺动脉高压(PAH)是CTD的严重并发症[2,4]而且,从历史上看,与特发性多环芳烃(IPAH)患者相比,与CTD相关的多环芳烃(PAH-CTD)患者的预后更差[5].根据CTD的不同,患者对PAH治疗可能有不同的预后和反应[6,7].最近的数据表明,PAH- ctd患者可能对联合PAH疗法的治疗方案反应良好;然而,这些报道很少[8,9].针对CTD亚型的多环芳烃治疗的专门评估更加有限,此类报告往往是观察性的或基于小数量的患者。
长期III期GRIPHON试验在1156名PAH患者中评估了选择性IP前列腺环素受体激动剂selexipag,其中大多数患者患有IPAH(649名患者)或PAH- ctd(334名患者)。在整个研究人群中,与安慰剂相比,selexipag将主要综合结局发病率/死亡率的风险降低了40% (p<0.001)。基线时,80%的患者接受PAH治疗,其中32.5%的患者同时接受内皮素受体拮抗剂(ERA)和磷酸二酯酶5型抑制剂(PDE-5i)。在PAH-CTD亚组中,与安慰剂相比,selexipag将主要终点事件的风险降低了41% [10].
当前分析的目的是详细描述加入GRIPHON的PAH-CTD患者,包括PAH-SSc和PAH-SLE患者,并从剂量、疗效和耐受性方面描述他们对selexipag的反应。
方法
研究人群
GRIPHON是一项全球性、双盲、随机、安慰剂对照、事件驱动的III期临床试验(www.clinicaltrials.gov标识符号码NCT01106014),并已在前面详细描述[10].符合条件的患者年龄为18-75岁,经右心导管检查确诊为PAH。研究人员指定PAH的病因为特发性、遗传性、与CTD有关、与修复的先天性分流管有关、与HIV有关或与药物/毒素接触有关。对于PAH-CTD患者,潜在的CTD可能被指定为SSc、SLE或混合性结缔组织病(MCTD)。在基线时,要求患者有6分钟的步行距离50-450米。naïve接受治疗的患者,以及接受PDE-5i、ERA或两者同时接受,且在随机分组前至少3个月剂量稳定的患者符合条件。接受前列环素或其类似物的患者不符合条件。
研究设计
经过28天的筛查期后,患者被随机分为1:1组,分别接受selexipag或安慰剂。在12周的滴定期间,研究药物以200µg开始,每天两次,每周滴定200µg,每天两次,直到最高耐受剂量。允许的最大剂量为1600µg,每天两次。从第26周开始,允许在定期就诊时增加剂量;任何时候都允许减少剂量。selexipag的个体化维持剂量(IMD)定义为研究中患者接受时间最长的剂量。预先指定了三个剂量组:低剂量(200和400µg每天两次)、中剂量(600、800和1000µg每天两次)和高剂量(1200、1400和1600µg每天两次),并根据患者的IMD将患者纳入这些组。患者接受双盲治疗,直到他们经历主要终点事件,过早停用研究药物,或研究结束。当达到预定的331个主要终点事件数量时,宣布研究结束。该试验遵守了《赫尔辛基宣言》,议定书由地方机构审查委员会或独立的伦理委员会批准。 Written informed consent was obtained from all patients.
结果测量
主要综合终点是从随机分组到首次发病/死亡事件的时间(即。疾病进展或PAH恶化导致住院,开始肠外前列腺素治疗或长期氧治疗,需要肺移植或球囊房间隔造瘘,或任何原因死亡),直到双盲治疗结束。疾病进展被定义为6分钟步行距离较基线减少≥15%,在另一天的第二次测试中证实,并且在世界卫生组织(WHO)功能分级(基线时为功能II/III级患者)中恶化或需要额外的PAH治疗(基线时为功能III/IV级患者)。一个不透明的独立委员会对所有主要终点事件进行裁决。次要终点包括从基线到第26周6分钟步行距离的变化和研究结束前的全因死亡。探索性终点包括脑钠肽n端原激素(NT-proBNP)水平从基线到第26周的变化。不良事件和严重不良事件分别在研究结束后7天和30天收集。
统计分析
我们进行了事后PAH-CTD亚组分析。对于所有事件时间终点,计算各治疗组的Kaplan-Meier估计值。使用Cox比例风险模型估计95%置信区间的风险比(HRs)。采用相互作用试验进行亚组分析。使用协方差非参数分析分析6分钟步行距离和NT-proBNP较基线的变化,并对各自的基线值进行调整。缺失的6分钟步行距离值如前所述[10].对观测数据进行NT-proBNP水平分析。
结果
患者和治疗暴露
在加入GRIPHON的1156例患者中,334例被诊断为PAH-CTD。其中170例为PAH-SSc, 82例为PAH-SLE, 37例为PAH-MCTD, 45例未进一步确定CTD (PAH-CTD-other)。由于患者数量较少,且主要终点事件数量相应,我们将PAH-MCTD组和PAH-CTD-other组的患者作为一组(PAH-MCTD/CTD-other)。
在334例PAH-CTD患者中,167例接受安慰剂,167例接受selexipag。安慰剂和selexipag的中位治疗时间分别为62.0周和67.1周,与整个研究人群的治疗时间相似[10].PAH-CTD亚组和三种CTD亚型的基线特征见表1.在PAH-CTD亚组中,大多数患者为女性:87.4%(安慰剂)和92.8% (selexipag)。均值±sd安慰剂组年龄为52.8±15.0岁,selexpag组年龄为51.8±14.1岁。PAH-SSc患者年龄大于PAH-SLE患者。此外还有区域差异:PAH-SSc在西方国家最常见,而PAH-SLE在亚洲最常见。在PAH- ctd亚组中,在基线时接受PAH治疗的患者比例(安慰剂组和selexipag组分别为74.9%和78.4%)与整个研究人群的比例相似[10].与其他CTD亚型相比,PAH- sle患者在基线时未接受任何PAH治疗的比例略高,而PAH- ssc患者同时接受ERA和PDE-5i的比例略高。
Selexipag剂量
在PAH-CTD亚组中,低剂量组有40例(24.0%)患者发生IMD,中剂量组有45例(26.9%)患者发生IMD,高剂量组有75例(44.9%)患者发生IMD(补充表S1)。这些比例与在整个GRIPHON种群中观察到的比例相似[10], CTD亚型与PAH-CTD总体亚型之间无显著差异(补充表S1)。
对selexipag治疗的反应
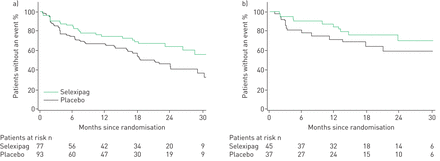
在PAH-CTD患者中,selexipag将主要综合终点发病率/死亡率的风险降低了41%与安慰剂(HR 0.59;95% ci 0.41-0.85) [10) (图1;补充图S1a)。这种反应与总体GRIPHON人群中观察到的反应一致,也与IPAH/遗传性PAH患者中观察到的反应一致(HR 0.61;95% ci 0.47-0.79;补充图S1b)。PAH- ctd患者的治疗效果与基线时PAH治疗无关(相互作用p=0.87;图1)和CTD亚型(相互作用p=0.89;图1).降低selexipag的风险与安慰剂为44% (HR 0.56;95% CI 0.34-0.91); 34% (HR 0.66;95% CI 0.30-1.48)在PAH-SLE患者(图2).在整个GRIPHON种群中观察到[10],疾病进展和住院占PAH-CTD患者主要终点事件的大多数(80.2%),与基础CTD无关(补充表S2)。到研究结束时,安慰剂组和selexipag组的PAH-CTD患者中有34人死亡,表明治疗组之间没有差异(补充表S2;人力资源0.98;95% ci 0.61-1.59)。在固定时间点和研究结束前对全因死亡的评估得出了一致的结果(补充表S3)。最常报告的死亡原因是多环芳烃、疾病进展和右心衰(补充表S4)。
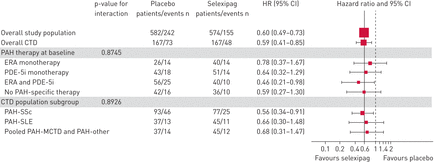
selexpag对基线肺动脉高压(PAH)治疗和结缔组织病(CTD)亚型发病率/死亡率主要复合终点的影响ERA:内皮素受体拮抗剂;PDE-5i:磷酸二酯酶5型抑制剂;SSc:系统性硬化症;SLE:系统性红斑狼疮;MCTD:混合CTD。
selexpag对a)系统性硬化症相关肺动脉高压和b)系统性红斑狼疮相关肺动脉高压患者发病率/死亡率主要复合终点的影响
在PAH-CTD亚组中,安慰剂组的6分钟步行距离中位数比基线减少了10.0米,selexipag组的6分钟步行距离中位数比基线减少了2.0米(治疗效果:12米[95% CI -4-27];补充表S5)。对于NT-proBNP,使用selexipag观察到中位数(Q1, Q3)从基线到第26周下降了−55.5 ng/L(−282.5,48.0),而安慰剂组中位数增加了13 ng/L(−99.0,404.0)(治疗效果:−140.0 [95% CI−265至−51];补充表S6)。CTD亚型6分钟步行距离和NT-proBNP的结果在补充表S5和S6中列出。
总体而言,在PAH-CTD亚组中,15例(9.1%)安慰剂治疗患者和32例(19.2%)selexipag治疗患者因不良事件而过早终止了他们的研究方案(表2).在治疗组中,PAH-CTD亚组和CTD亚型报告的不良事件和严重不良事件的频率相似。最常见的不良事件列于表2补充表7。针对前列环素通路的治疗相关的最常见不良事件,发生在滴定和维持期间,在表3和补充表S8。无论CTD的基础是什么,这些不良事件通常在12周滴定期间更频繁地被报道(补充表S8),当时它们被用来定义最高耐受剂量。
讨论
GRIPHON试验纳入了迄今为止在双盲、随机对照试验中评估的最多的PAH-CTD患者。对于PAH-CTD患者,selexipag对发病率/死亡率主要复合终点的治疗效果与GRIPHON总体人群一致[10].治疗效果的一致性与基线PAH治疗无关,与CTD亚型无关。Selexipag在PAH-CTD亚组和每种CTD亚型中普遍耐受良好。这些结果支持selexipag治疗在不同PAH-CTD患者中的临床益处,以及与ERA、PDE-5i或两者联合治疗的设置。
PAH-CTD患者与总体GRIPHON人群在人口统计学和基线特征上存在一些差异[10],以及CTD亚型之间的差异。与总体GRIPHON人群相比,PAH-SSc患者的基线特征表现为更差的6分钟步行距离和WHO功能等级[10].相反,PAH-SLE患者的特征表明损害较小。这些发现与先前报道的PAH-SSc和PAH-SLE的自然史一致[6,11- - - - - -13],并反映在主要终点Kaplan-Meier曲线的描述性分析中,该曲线说明了该疾病的病程。与整体PAH-CTD亚组相比,PAH-SSc患者的疾病进展更快,而PAH-SLE患者的疾病进展更慢。这在一项随机对照试验中首次证实,先前的观察数据表明PAH-SSc患者比其他PAH-CTD亚型患者预后更差[11,14,15].
从历史上看,与IPAH患者相比,PAH- ctd患者被认为对PAH治疗表现出更微弱的反应[5,16- - - - - -20.].随着越来越多来自结果驱动研究的证据,以及在PAH中采用联合治疗方案,这种观点正在改变。在SERAPHIN试验中,155名PAH-CTD患者被随机分配到安慰剂组或马西坦10mg组,与安慰剂组相比,马西坦将发病率/死亡率的主要综合终点风险降低了42% [8].AMBITION试验招募了新诊断的treatment-naïve例患者,包括187例PAH-CTD患者。在该亚组中,与单药治疗相比,氨布里森坦和他达拉非联合治疗可将临床失败事件的风险降低57% [9].在GRIPHON中,大量的PAH-SSc和PAH-SLE患者首次允许根据CTD亚型对患者进行有意义的探索。尽管这些亚型之间存在先天差异,但在PAH-SSc和PAH-SLE患者中,观察到的selexipag对发病率/死亡率复合终点的治疗效果是一致的,并且是由疾病进展和住院率的减少所驱动的。虽然患者数量不允许通过基线PAH治疗对每种CTD亚型的主要终点进行正式分析,但大多数PAH- ssc患者在基线时已经接受了ERA或PDE-5i,或两者都接受了ERA。这些数据表明,selexipag可以为PAH- ssc患者现有的PAH治疗提供增量效益。
在PAH-CTD患者中,在研究结束时或在研究期间的固定时间点,治疗组之间的全因死亡没有差异。虽然与安慰剂组相比,selexipag组观察到的死亡人数更多,但主要终点的死亡人数很少。这种差异很可能是由于主要终点的复合性质造成的,主要终点涉及到每个患者直到治疗结束的首次发病或死亡事件。经历了非致命主要终点事件的患者随后停止了双盲治疗,并且对主要终点没有进一步的事件,包括死亡;这就是所谓的信息审查。在研究结束前的全因死亡意向治疗分析中,捕获了导致主要终点的死亡和所有其他死亡。后者主要发生在已经经历过非致命主要终点事件的患者中。这些患者不再接受双盲治疗,可以接受进一步的PAH治疗,包括开放标签的selexipag或静脉注射前列环素类似物,由研究者自行决定。这种杂交的效果可以用建模技术来估计,从整个GRIPHON种群的结果来看,selexipag [21].这些考虑突出表明,在一项并非旨在单独评估死亡率的研究中,解释死亡人数所面临的一些挑战,并强调此类研究中的死亡率评估应谨慎解释。
在PAH-CTD亚组以及PAH-SSc和PAH-SLE亚型中,治疗对6分钟步行距离的影响与在整个GRIPHON人群中观察到的效果相似。在PAH-CTD亚组中,与selexipag治疗的患者相比,安慰剂治疗的患者的反应更严重。这种恶化在PAH-SSc患者中更为明显。考虑到SSc涉及肌肉骨骼的程度,这并不令人惊讶,并且与另一项PAH-CTD研究一致[19].相比之下,在PAH-SLE患者6分钟步行距离的治疗效果是由selexipag组的改善驱动的,而安慰剂组几乎没有变化。鉴于PAH-SLE患者的发表数据很少,这一观察尤为重要。在我们的研究中评估的患者普遍存在,大多数已经接受PAH治疗。在这种情况下,通过额外的治疗来提高运动能力是具有挑战性的。6分钟步行距离相对温和的改善与主要终点更明显的治疗反应形成对比。这进一步强调了6分钟步行距离的改善与PAH进展延迟之间缺乏相关性[22],并支持最近的一份报告,该报告显示,在普遍的PAH患者中,预防6分钟步行距离的恶化可能比确保改善更具有预后相关性[23].
对于GRIPHON PAH-CTD亚组,NT-proBNP结果特别有趣,因为它们不受与潜在疾病相关的共病(如肌肉骨骼损伤)的影响。此外,样品在一个中心实验室进行分析,从而最大限度地减少了中心之间的变异性。在PAH-CTD亚组以及三种CTD亚型中,NT-proBNP的治疗效果与整体GRIPHON人群相当[10].PAH-SSc患者的结果尤其令人鼓舞,因为他们的NT-proBNP基线水平相对较高。尽管这些结果很有希望,但考虑到患者数量低和置信区间宽,应谨慎解释这些结果。
PAH-CTD患者由于合并症的肌肉骨骼和胃肠道受累,通常有较高的症状负担,并可能接受多种伴随治疗[24].因此,与其他PAH患者相比,PAH- ctd患者的耐受性可能较差。然而,PAH-CTD患者对selexipag的耐受性与GRIPHON人群总体一致;PAH-CTD亚组中因不良事件导致的selexipag治疗停药率(19.2%)仅略高于GRIPHON总体人群(14.3%)[10].这些数据与其他靶向前列环素途径的药物的数据相比是令人鼓舞的,这些药物显示在更短的治疗周期内停药率为10-14% [25- - - - - -27].在我们的研究中,发生的大多数不良事件反映了selexipag对IP受体的作用方式(如。头痛、腹泻和恶心),高、中、低剂量组患者的分布在PAH-CTD患者和整体GRIPHON人群中相似。再加上主要终点治疗效果的一致性,这些数据支持基于PAH-CTD患者耐受性的个体化给药方法。
这些分析受到一些限制。虽然PAH-CTD人群是评估主要终点的预先指定的亚组,但这里描述的更详细的分析本质上是探索性的。此外,研究者在没有裁决的情况下记录了CTD亚型的分类,也没有提供血清学或其他疾病特异性参数的描述。
结论
GRIPHON研究包括迄今为止在前瞻性随机对照试验中研究的最大的PAH-CTD患者群体。对这些患者的评估强调了患者特征和病程的差异,这取决于潜在的CTD。在我们的研究中,无论CTD亚型和基线PAH治疗如何,selexipag治疗具有良好的耐受性,并延缓了PAH的进展。这些数据支持在治疗PAH- ctd患者时使用多种PAH疗法,并强调这种治疗策略可以在以前被认为难以治疗的人群中产生益处。
补充材料
补充材料
请注意:补充材料不是编辑部编辑的,上传时是作者提供的。
图S1。selexpag对PAH-CTD或IPAH/HPAH患者发病率/死亡率主要复合终点的影响erj - 02493 - 2016 - _figure_s1
表S1。个性化维持剂量erj - 02493 - 2016 - _table_s1
表S2。肺动脉高压和死亡相关事件erj - 02493 - 2016 - _table_s2
表S3。PAH-CTD患者安慰剂组和selexipag组在研究结束前因任何原因死亡的人数erj - 02493 - 2016 - _table_s3
表S4。PAH-CTD患者研究结束前所有死亡的死因erj - 02493 - 2016 - _table_s4
表S5。在第26周,6分钟步行距离从基线改变erj - 02493 - 2016 - _table_s5
表S6。从基线到第26周n端脑钠肽前体的变化erj - 02493 - 2016 - _table_s6
表S7。多环芳烃- ssc、多环芳烃- sle或多环芳烃- mctd /-CTD-other患者最常见的不良事件erj - 02493 - 2016 - _table_s7
表S8。在研究中,PAH-CTD亚型的滴定和维持期报告了前列环素相关的不良事件erj - 02493 - 2016 - _table_s8
披露的信息
补充材料
美国的盒子erj - 02493 - 2016 - _gaine
k .下巴erj - 02493 - 2016 - _chin
g . Coghlanerj - 02493 - 2016 - _coghlan
r . Channickerj - 02493 - 2016 - _channick
L. Di Scalaerj - 02493 - 2016 - _di_scala
n Galieerj - 02493 - 2016 - _galie
希拉。Ghofranierj - 02493 - 2016 - _ghofrani
贝聿铭朗erj - 02493 - 2016 - _lang
诉麦克劳克林erj - 02493 - 2016 - _mclaughlin
r . Preisserj - 02493 - 2016 - _preiss
l·j·鲁宾erj - 02493 - 2016 - _rubin
g . Simonneauerj - 02493 - 2016 - _simmoneau
o . Sitbonerj - 02493 - 2016 - _sitbon
音频Tapsonerj - 02493 - 2016 - _tapson
M.M. Hoepererj - 02493 - 2016 - _hoeper
确认
医学写作协助由Anoushka Thomas (nspm ltd, Meggen, Switzerland)提供,Actelion Pharmaceuticals ltd (Allschwil, Switzerland)资助。
脚注
这篇文章有补充资料可从www.qdcxjkg.com
这项研究注册在www.clinicaltrials.gov标识符号码NCT01106014.
支持声明:本研究得到Actelion Pharmaceuticals的支持。本文的资助信息已存入交叉参考基金注册.
利益冲突:可以在本文旁边的网站上找到信息披露www.qdcxjkg.com
- 收到了2016年12月19日。
- 接受2017年5月10日。
- 版权所有©ERS 2017。
这篇ERJ开放文章是开放获取的,并根据创作共用署名188滚球软件非商业许可4.0的条款发布。