抽象的
表征假单胞菌铜绿假单胞菌在非囊性纤维化支气管扩张患者的慢性肺部感染过程中的种群,我们使用全基因组测序为1)评估多样性P.铜绿假单胞菌和多素感染的患病率;2)寻求交叉感染或共同来源收购的证据;3)表征P.铜绿假单胞菌适应。
189年分离株,从英国参加16名成人支气管扩张中心的91名患者的患者中获得,是全基因组测序。
支气管扩张分离物是宽的代表P.铜绿假单胞菌人口。在检查多个分离株的24名患者中,有七种多素感染的例子,可能来自多种感染事件。来自不同患者的分离物基因组之间的核苷酸变体的数量在一些情况下类似于各个患者的分离物之间观察到的变化,这意味着可能发生跨感染或共同源采集。
我们的数据表明,在支气管扩张患者的感染期间,P.铜绿假单胞菌群体通过累积功能丧失突变来适应,导致表型变化,包括不同铁采集模式和生物膜相关多糖的变化。人口内多元化表明,将需要在早期阶段捕获跨感染或共同源采集事件的更大规模的纵向监测研究。
抽象的
P.铜绿假单胞菌在支气管扩张中发生共感染;细菌种群通过突变调整和多样化http://wly/fmhj308zuv0.
介绍
支气管扩张是一种慢性渐进性呼吸系统疾病,与Bronchi的不可逆转扩大相关[1]。最近的数据表明,在英国,女性和男性的发病率分别上升至35.2和26.9分别[2]。在美国,成年支气管扩张的患病率估计在100 000人中52人,女性和老年人的患病率较高[3.]。执着的假单胞菌铜绿假单胞菌支气管扩张患者的肺部感染发生在左右的案件中,与较差的结果和过早死亡率相关[4.那5.]。
慢性研究的研究P.铜绿假单胞菌肺部感染的重点是囊性纤维化(CF) - 分配支气管扩张,患者被诊断,监测,并从一个非常休眠中监测和进行抗生素治疗。这与非CF支气管扩张患者对比,他在更旧的年龄呈现并往往具有较短的治疗干预史。因此,与来自成年人CF患者的分离物相比,来自非CF支气管扩张患者的细菌分离株表现出对抗生素的抗性较少[6.]。以前的研究表征了进化P.铜绿假单胞菌在CF患者的慢性肺部感染期间[7.那8.]。高分辨率分析显示出广泛的异质性P.铜绿假单胞菌CF肺中的种群[9.-12.],包括多种不同谱系的共存[13.]。
在CF中,许多可传递菌株P.铜绿假单胞菌已被确定,导致引入控制交叉感染的措施[14.]。研究P.铜绿假单胞菌与非CF支气管扩张不那么先进。在我们的50岁的单中心学习中P.铜绿假单胞菌使用分子打字的40名支气管扩张患者的分离物,没有令人信服的交叉感染或显性克隆证据[15.]。然而,尚未进行多个支气管扩张分离物的全基因组序列分析。在这里,我们报告了基因组学的使用来评估多样性P.铜绿假单胞菌在多个英国中心导致非CF支气管切除感染的菌株,以鉴定多种中原感染,并寻找交叉感染或共同源采集的证据。此外,我们还表征了适应性突变,并在群体内发散的情况表征P.铜绿假单胞菌支气管扩张患者的慢性肺部感染。
方法
患者和细菌分离株
189年P.铜绿假单胞菌本研究中使用的分离物(在线补充表S1)与从93例支气管扩张和慢性患者获得的痰样品中分离出痰液P.铜绿假单胞菌感染(定义为前面12个月的两种或更多种持续的呼吸道培养物)参加英格兰和威尔士的16个成年支气管扩张中心。这些包括收集的分离物作为多期雾化抗生素试验的一部分[16.],如果患者在完成抗癫痫抗生素过程的21天内注册,以加剧抗生素。在观察研究期间收集来自纽卡斯尔(n = 8)和利物浦(n = 53)的附加分离株。用于隔离的方法P.铜绿假单胞菌从患者痰液中描述在线补充材料中。
对于24名患者,分析了来自同一样品的分离株(两种或更多种),以寻找多重细胞感染的证据。对于这些患者中的三种(患者147-149患者),对单个样品的14或15个分离物进行测序,用于较高分辨率分析的群体内均相。对于一些分析,为了避免从同一患者中包含多个克隆基因组产生的偏见,使用来自91例患者的99种基因组的子集。该子集由每个患者每个克隆谱系的一种随机选择的基因组(在线补充表S1)。我们使用术语“克隆谱系”来描述与共享多层序列类型(MLST)谱的分离物,并根据核心基因组单核苷酸多态性(SNP)的基因发生。
DNA制备和全基因组测序
基因组DNA提取的细节P.铜绿假单胞菌使用Illumina(San Diego,CA,USA)短读测序技术的分离物,图书馆制备和全基因组霰弹枪测序在线补充材料。研究的欧洲核苷酸存档登录号是PRJEB14952。
用于基因组序列组装的方法,用核心基因组和变体调用的MLST数据提取到PAO1的基因组[17.]在线补充材料中描述了识别SNP或小插入或缺失。
鉴定大缺失和毒力因子基因
基因组序列与参考基因组对齐P.铜绿假单胞菌pao1(nc_002516 [17.]) 和P.铜绿假单胞菌LESB58(FM209186 [18.])使用BLAST环图像发生器(BRIG)识别出大的克隆特异性缺失(≥10kb)[19.]。通过将基因组序列与“与”对齐基因组序列来确定缺失的界限P.铜绿假单胞菌pao1基因组使用紫红色[20.],作为诅咒包的一部分实施(www.geneious.com.)。使用可缓冲测定基因组组件中毒力因子基因的存在和不存在(www.github.com/bawee/blastable.able.)。这假单胞菌基因组数据库(beta.pseudomonas.com.)[21.[用于促进基因功能的分析。
结果
多样性P.铜绿假单胞菌非CF支气管扩张株和证据P.铜绿假单胞菌多百吉共同感染
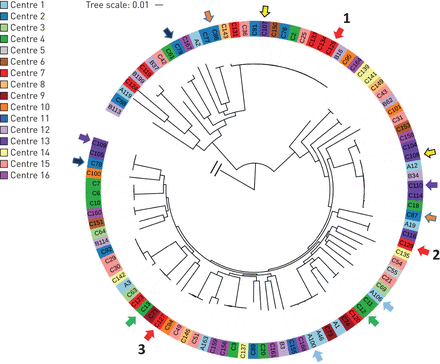
核心基因组SNP系统发育分析与331的集合P.铜绿假单胞菌分离不同临床来源的基因组[22.]表明支气管扩张分离株广泛分布(在线补充图S1)。从189个分离器中,可以提取160(在线补充表S1和S2)的完整MLST配置文件,其中最广泛的序列类型(STS)为ST-253(PA14-yaki)[23.];14名患者,八个中心),ST-179(7名患者,四个中心),ST-17(克隆C [23.];五名患者,三个中心),ST-252(四名患者,四个中心)和ST-260(四名患者,三个中心)。使用核心基因组SNP系统发育,之前的研究细分较宽P.铜绿假单胞菌人口分为两个主要群体(包括应变Pao1的组,其中包括菌株PA14的第II组)和一个小组大多数不相关的克隆谱系[24.那25.]。99个基因组的子集,由每位患者的每个克隆谱系中的一种随机选择的基因组,71位位于II组和27组中(图1)。基于MLST基因型和核心基因组SNP系统的组合,24名患者的样品进行了多种分离株,有七种多素感染的例子。在一个患者(患者92)中,三个不同的克隆谱系P.铜绿假单胞菌被确定了。在42,72,73,84,85和148患者中,有两种共存谱系(图1)。
七名患者在七位患者中多数组织的证据。显示核心基因组单核苷酸多态性系统发育,用于99个分离物的子集,证实所有单独的(B113)簇中的两个主要组中的一种。每个支气管扩张中心由不同的颜色表示。共享相同颜色的箭头表示从同一患者获得的分离物。来自同一患者92样品的三个分离物编号为1-3。
共用谱系的证据引起不同患者的感染,参加同一中心
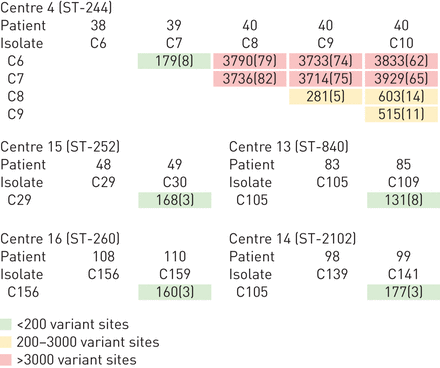
核心基因组SNP系统发生鉴定了许多例子,其中与参加同一中心的多于一个患者分离密切相关的克隆谱系(在线补充表S3)。为了获得更高的分辨率比较,在整个基因组(在线补充表S3)上使用成对比较来分析这些分离株,鉴定了在<200位点(C6 /)的不同患者的分离患者的分离株的基因组(C6 /C7,C29 / C30,C105 / 109,C139 / C141和C156 / C159;图2)。这种基因组相似性大于来自相同痰样品的同一谱系的当代分离物的一些成对比较(在线补充表S3;来自184个变体部位(C110 / C111)至> 750变体部位(C125 / C126)))。
示例分离与分离与出席同一中心的患者分离的相同克隆血管谱系之间的分离比较。指示单核苷酸多态性变化的数量,具有小插入和折扣变化的数量。完整的详细信息显示在在线补充表S3中。其中分离共享<200变量站点的五个例子是绿色突出显示的。比较来自参加中心4患者的ST-244的所有分离株,相似性根据变体部位分级。
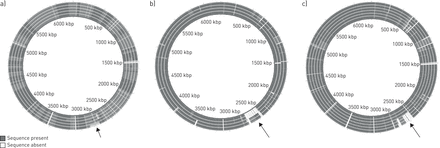
检查99个支气管扩张分离株子集的基因组序列草案,用于存在大(> 10kb)缺失(图3.)。鉴定了总共36种不同的缺失(25> 100 kB),范围为11至300 kB,代表独立的遗传事件(在线补充表S4)。这些分布在99-成员基因组子集中的28个基因组上。大多数基因组只有一次缺失,尽管两种(C54和C164)有三次缺失,并且四(A119,C4,C85和C119)有两个。在大多数情况下,来自同一患者的相同克隆谱系的分离物共享相同的缺失。然而,在患者45,55,79和92中并非所有相同谱系的所有分离物都具有相同的缺失。来自不同患者的分离对C6 / C7,C29 / C30,C105 / 109,C139 / C141和C156 / C159的基因组,但在<200位点(表格1),通过Brig分析难以区分(所示的示例图3B.)。
支气管扩张菌株与参考应变菌株的基因组对准的实例假单胞菌铜绿假单胞菌pao1。表明了PaO1基因组中鉴定为存在(深灰色)或不存在(白色)的序列。a)来自同一患者的相同谱系(ST-253)的分离物。从最里面到最外面的:C95,C97,C98,C99和C96。突出显示孤立C96中存在的删除(箭头)。b)分离物对(从最内部到最外面的:C6和C7;和C156和C159),两者都与参加同一医院的不同患者共享相同的克隆血统。隔离C6和C7共享大删除,分离C156和C159共享较小的重叠删除(在线补充表S4),如所示(箭头)。c)来自同一患者的不同谱系的分离物。从最里面到最外面的:A77,A80和A85(所有ST-175);A78,A81和A82(所有ST-17)。 A large deletion present in the ST-17 isolates is indicated by an arrow. The figures were generated using the BLAST Ring Image Generator [19.]。
患者内分离株的基因组多样性可以与患者之间的多样性相似
为了进一步评估患者内部展示的多样化P.铜绿假单胞菌种群,分析了来自单次痰样品的较大分离株3例:147(15分离物),148(15分离株)和149(14个分离物)(表格1)。对于其中两个患者,P.铜绿假单胞菌人口包括一个单一的克隆谱系。对于患者148,鉴定了两个不同的克隆谱系,并分别分别分析这两组分离株。在分析的所有四个隔离集中,两个分离谱系的相同谱系的最大成对SNP变化> 300,中值≥79(表格1),表明患者内部多样化的发生。
多个分离液中识别的功能突变和删除
我们使用了变体呼叫方法来识别99个支气管扩张分离基因组的子集中的独立出现的功能突变。这产生了许多具有已知功能的基因的示例,其中多个分离株中携带独立的功能突变(表2.和在线补充表S5)。这些包括与粘液,毒力,渗透,生物膜形成,运动,DNA修复和抗微生物抗性有关的基因(表2.)。编码MEXAB-OPRM Efflux泵的所有三个组分的基因出现在最常见的功能突变中。此外,多个分离物在编码调节器的基因中携带功能丧失(包括拉斯尔那阿尔谷那倒和VFR.)。在99个支气管扩张分离物中,如所列功能突变的基因数量表2.从零到六(在线补充图S2和表S6)。
高度能力是CF分离株中的常见性状P.铜绿假单胞菌。在99面板分离株中,11例中的11例携带的功能丧失突变丧失的DNA错配修复基因静脉要么乌尔(在线补充表S1)。除了两种中,其中两种都被确认为具有高端表型。
含有缺失的所有基因组的对准> 10kb相对于菌株Pao1的基因组显示出惊人的非原子分布,其中36个缺失中的30个缺失位于菌株PaO1基因组的1.9-2.8mb部分内。该地区内的基因包括PSL.基因,编码细胞外多糖[26.]编码编码VI分泌装置的Sigrosophore Pyoverdine和基因的基因[27.]。
接下来,我们专门检查了99个克隆谱系中的每一个的一个代表,用于存在或不存在与致病性相关的基因(在线补充表S6)。这些基因组中的23个缺乏一个或多个PSL.基因。相比之下,所有的基因组都包含了所有的all.制备藻酸盐所需的基因和PEL.制备PEL外偶糖所需的基因。11个基因组缺乏合成百voverdine所需的基因,其中九个也缺乏一个FPVA.用于摄取Ferripyoverdine的受体基因,尽管在所有情况下都存在合成替代载体的基因替代植物。另外,11种基因组缺乏VI分泌系统的两种或更多种基因(PA2360(HSIA3.)-pa2373(vgrg3.))(在线补充表S6)。这些发现与在多个分离株中含有PSL,百voRdine和VI型分泌基因的基因组区域的缺失的发生,尽管在一些分离物中,检测到较小的缺失(<10kb)。
讨论
我们使用全基因组测序以获得多样性的横截面P.铜绿假单胞菌在英国支气管扩张中引起感染的菌株。我们的数据表明分配P.铜绿假单胞菌在支气管扩张中发现的谱系孤立集合广泛代表全球范围P.铜绿假单胞菌人口。与cf相反[14.[我们发现没有数据表明英国非CF支气管扩张群落中存在广泛的传播应变。然而,我们的研究没有包括来自个别中心的大量患者。PA14样和克隆C等谱系,其自然是自然的更丰富的[23.],是支气管扩张素收集中最丰富的。由于一些谱系自然更丰富,因此在多个患者中的发生(基于MLST)不一定指示常见的源或交叉感染。全基因组测序提供比MLST等方法更高的分辨率,允许我们解决这个问题。
在前面比较同一支气管扩张中心内的患者的配对分离物中,在大多数患者(10个中)的两种分离株共享常见基因型,发现一名患者同时用两个菌株感染15.]。在这项研究中,24名患者检查了多种分离株的样品,7例具有多素感染。CF中还报告了类似的多素感染,通常与儿童相关[28.]。此外,CF中的许多研究也证明了表型[9.那11.那12.]和基因组[10.那13.那29.单谱系的多样化P.铜绿假单胞菌CF肺的种群。在这里,我们首次显示在非CF支气管扩张患者的感染期间发生类似的多样化。在感染过程中发生多线性感染和多样化的患病率强调,在解释基于单个分离株的痰样品分析时需要谨慎P.铜绿假单胞菌。
我们发现来自参加同一中心的患者的若干例子,不仅共享相同的克隆谱系,还可以通过<200位点分别不同。来自同一患者样品的分离物之间的基因组变化显示出类似的,并且在某些情况下,变化水平较高。不同患者中具有非常高的遗传相关性的分离株的发生强烈意味着存在常见的来源或交叉感染。区分两个分离株的核苷酸变化的程度将取决于自变速事件以来的时间长度,2)突变率P.铜绿假单胞菌感染过程中的人口。需要进一步研究以更好地确定该患者组中交叉感染或常见源采集的作用。
通过突变和缺失的积累,对肺环境的细菌适应有明确的证据,包括先前在CF中常见的基因中的功能突变失去突变,例如粘膜(粘液)和拉斯尔(群体感应)。然而,值得注意的是,编码在先前的CF研究中突出的一些调节器的基因中的突变(MEXT.那ret那exsd.和AMPR.)不经常观察(两个MEXT.和二AMPR.突变体或根本不(在线补充表S5)。全球监管机构的突变可能影响众多过程。在CF中,不同研究中鉴定的病理进入基因多样化,表明有多个途径适应CF肺部[7.那8.],可能也适用于非CF支气管扩张的场景。
编码MEX-OPRM Efflux泵的基因中的功能突变在支气管扩张分离物中是常见的。虽然通常被认为是作为抗生素抗性重要重要的多药渗透系统,但该系统涉及毒力[30.]。因此,虽然它可能看起来违反了这一点P.铜绿假单胞菌应通过损失抗生素抗性相关的流出泵来调节,可能是驾驶员选择与抗生素外排以外的功能有关。相比之下,功能损失突变Mexs.可以直接与抗生素抗性相关联,因为突变Mexs.促进MEXEF-OPRN MDR Efflux泵的上调[31.]。
非CF支气管扩张的缺失在编码百voverdine和psl多糖的特定基因组区域中的缺失的分离株高于331的数据集P.铜绿假单胞菌临床孤立基因组[22.],其中22种基因组缺少一个或多个PSL.基因,只有三个缺少一个或多个百多百多葡萄酒合成基因,只有一个没有一个没有FPVA.受体基因。P.铜绿假单胞菌可以利用多种途径进行铁采集[32.]。在CF的慢性肺部感染期间,P.铜绿假单胞菌支持血液利用途径的血液利用途径而不是百voverdine铁道系统[33.]。我们的观察结果表明非CF支气管扩张的适应性。
为了保护自己免受敌对的环境条件或寄主防御P.铜绿假单胞菌可以生产有助于生物膜形成的三种外糖:藻酸盐,PSL和PEL [26.]。已经提出了PSL是关键表面附件的决定因素[34.]而在CF肺无浮动生物膜结构中可能更重要[35.]。有利于PEL的产生而不是PSL的其他突变包括突变BIFA[36.],RBDA.[37.],OPRF.[38.] 和小伙子[39.]。因此,我们的观察结果表明,在非CF是慢性肺部感染中,PEL和藻酸盐外偶联在PSL上受到青睐。
其他常见的功能丧失突变(在PILJ.那chpa.和FIMV.)涉及丢失或修改的抽搐运动,在CF中也看到了适应性[8.[人工痰生物膜模型[40暗示这可能是与痰环境的粘度有关的适应。
我们的研究代表了多个比较基因组学分析P.铜绿假单胞菌与非CF支气管扩张患者的慢性肺部感染相关的分离物。虽然较大,更具靶向的研究,但每种样品分析更多数量的分离物,则需要确定多素感染的真正患病率,但这种观察表明它是多个常见的P.铜绿假单胞菌谱系在支气管扩张感染中共存。我们的研究还表明,样品内的多样性可以与参加同一中心的不同患者的分离物之间发生的遗传变异相当。这些观察结果表明,迫切需要在非CF患者中更详细和更大规模的纵向研究,以及捕捉中心内的多样性的监测,并将识别早先识别交叉感染或共同源采集事件,允许采取措施为了使这种重要病原体的传播最小化。
补充材料
补充材料
请注意:编辑部没有编辑补充材料,并随着作者提供的,上传。
补充材料ERJ-02108-2016_SUPPOREMENT.
图S1。核心基因组SNP系统发育,显示支气管扩张分离物的分布。该图显示了本研究中使用的所有支气管扩张分离物的基因组(以蓝色突出显示)与KOS的基因组突出等等。[14]以及常用菌株PAO1(标记PAO1107),PA14(UCBPPPA14109),PA7和LESB58的基因组。线颜色表示两个主要集群P.铜绿假单胞菌(I,绿色; II,蓝色)以及那些在两个主要组(红色)中没有聚类的隔离物。ERJ-02108-2016_FIGURE_S1
表S4。特定于PAO1的克隆缺失。ERJ-02108-2016_TABLE_S4
致谢
我们要感谢调查人员和参与PROMIS审判的患者(ISRCTN 49790596.)。我们还感谢Paul Roberts(Royal Liverpool和Broadgreen大学医院NHS Trust,Liverpool,UK)用于技术援助。
脚注
本文提供了补充材料www.qdcxjkg.com.
通过回答有关本文的问题,获得CME认证。你会发现这些www.qdcxjkg.com/journal/cme.
支持声明:这项工作得到了英国医学研究委员会的支持,作为Bronch-UK Grant(参考MR / L011263 / 1)的一部分,授予A. de Soyza作为主要调查员,其中C. Cinstanley在共同调查员中。I.L.Lamont希望承认新西兰新西兰囊性纤维化的资金支持,新西兰彩票(卫生)和国家卫生和医学研究委员会(澳大利亚)。M.P.摩尔和C.Winstanley希望承认囊性纤维化信托的支持(授予RS34)。本文的资金信息已存入开放式资助服务员注册表。
利益冲突:没有宣布。
- 已收到2016年10月28日。
- 公认2017年1月21日。
- 版权所有©2017
此ERJ开放文章是开放式访问,并根据Creativ188滚球软件e Commons归因许可证4.0的条款分发。