文摘
Gastro-oesophageal回流一直怀疑的起源和发展的含义特发性肺纤维化(IPF)。我们提出,食管裂孔疝可能更频繁的在IPF比其他间质性肺病(ILD),食管裂孔疝可能在IPF与更严重的临床特点。
我们回顾性比较食管裂孔疝的患病率在79年计算机断层扫描(CT)与其他ILD IPF患者和103例(17硬皮病,54其他结缔组织疾病和慢性过敏性肺炎32)。IPF组中,我们比较了临床、生物、功能性、CT扫描特征和食管裂孔疝患者的死亡率(n = 42岁),没有食管裂孔疝(n = 37)。
食管裂孔疝的患病率在IPF诊断为53%,CT扫描与ILD与硬皮病相关类似,但明显高于其他两个ILD组。食管裂孔疝的大小也不是与纤维化CT扫描分数,或在任何组肺功能下降。呼吸导致的死亡率明显高于在IPF患者食管裂孔疝比那些没有食管裂孔疝(p = 0.009)。
食管裂孔疝在IPF成因可能有特定的作用,可能是由于病理gastro-oesophageal反胃。
文摘
食管裂孔疝在特发性肺纤维化与死亡率有关呼吸的原因http://ow.ly/
介绍
特发性肺纤维化(IPF)是一种罕见而严重的疾病的中位数生存∼3年(1]。一些已确定的风险因素,如年龄、遗传易感性、烟草暴露和gastro-oesophageal回流(工资)2]。患病率IPF的气油比高,可能会影响患者的87%,其中47%报告症状(2,3]。在回顾性研究中,质子泵抑制剂(ppi)治疗或手术fundoplication似乎稳定IPF患者肺功能,减少急性加重(4,5]。气油比长期以来一直与IPF的起源和发展重复microaspiration胃分泌物,导致复发性肺组织损伤(6]。支持这一假说,Lee等。(7)观察支气管肺泡灌洗液中胃蛋白酶浓度高(BALF)的IPF患者,甚至更高的浓度在IPF的发作。最近,一个协会之间被观察到抗体的存在幽门螺杆菌在血清和IPF(严重程度增加8]。美国胸科学会(ATS) /欧洲呼吸学会(人)/日本呼吸协会(青年队)/拉188bet官网地址丁美洲胸协会(ALAT) 2011 IPF的管理指南推荐治疗气油比即使是无症状(1]。这个建议是基于“非常低质量的证据”。2015年指南更新(9]表明,临床医生使用常规抗酸治疗,还强调了需要额外使用随机临床试验研究。食管裂孔疝一直被认为是一个主要因素,容易使人产生气油比(10]。它可能增加下食管括约肌松弛的持续时间和食管炎的风险。符合在IPF患病率高气油比,发现食管裂孔疝使用计算机断层扫描(CT)在39%的IPF患者与13.3%,慢性阻塞性肺疾病(COPD)和16.7%的哮喘(11]。然而,这还有待确定食管裂孔疝的存在对IPF患者预后的影响,还是食管裂孔疝的形成只是增加肺回缩力的结果(肺纤维化所致)膈食管裂孔的肌肉向上,与对IPF发病和疾病过程的影响可以忽略不计。
为了解决这个问题,我们回顾性比较食管裂孔疝的患病率在IPF患者和患者的CT扫描其他间质性肺病(ILD)的类似的严重程度。我们测试了两个假设:1)食管裂孔疝是IPF更频繁;2)食管裂孔疝并不是与纤维化的严重程度有关。评估是否食管裂孔疝在IPF的发展中所起的作用,我们也调查是否存在区别IPF患者的生存,没有食管裂孔疝。
材料和方法
病人
入选标准是慢性ILD,定义为持续ILD在CT扫描≥6个月,和肺功能的可用性测试执行最初的6个月内诊所访问。肺纤维化患者的文件(n = 352)参加呼吸医学大学旅游(旅游、法国)2006年10月至2013年5月进行了综述(图1)。我们排除了170名患者,由于缺乏肺CT扫描(n = 46)或由于样本过小(结节病n = 2;矽肺n = 1;石棉肺n = 10;特发性非特异性间质性肺炎n = 11),或因药物引起的间质性肺疾病的诊断(n = 34)。另外66名患者被排除在外,因为ILD不可归类的(定义为患者没有特定ILD诊断临床多学科评审后,放射和病理数据)。研究对象包括IPF患者,ILD与结缔组织疾病(CTD-ILD)和慢性过敏性肺炎(CHP)符合既定标准。IPF的诊断是基于at /人/青年队/ ALAT标准(1]。CHP的诊断是基于标准建立了Lacasse等。(12]。供肺参与了标准文献中描述的基础上(13- - - - - -15]。
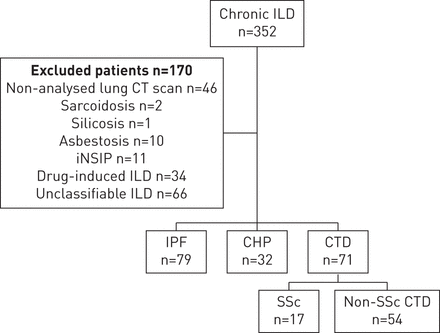
审判的间质性肺病(ILD) 2006年10月至2013年5月大学医院的旅游(旅游、法国)。CT:计算机断层扫描;iNSIP:特发性非特异性间质性肺炎;IPF:特发性肺纤维化;共和人民党:慢性过敏性肺炎;CTD:结缔组织疾病;SSc:硬皮病。
道德声明
法国立法不需要病人的知情同意的回顾性收集数据,符合当前的实践。然而,研究协议被评估和批准的机构审查委员会的法国呼吸医学学会(法国de Pneumologie de法语语言)(CEPRO # 2012 - 015)。数据库是匿名和遵守的严格要求委员会国家de l 'Informatique et des自由,这保证了应用程序的数据隐私法在法国。
数据收集
数据收集从电子病历的回顾性研究。我们收集临床数据(在诊断时年龄、性别、体重指数、吸烟习惯,倾心于症状包括胃灼热,存在与否与PPI治疗,氧气疗法与免疫抑制药物和治疗),呼吸道症状(咳嗽或呼吸困难分类的修改医学研究委员会规模),肺动脉高压(收缩期肺动脉压力> 40毫米汞柱由超声心动图评估),生物参数(乳酸脱氢酶,肺动脉栓塞,脑利钠肽和血液中性粒细胞),肺功能数据表示为一个百分比的预测价值,动脉血液气体,BALF细胞计数和急性发作的发生16]。此外,IPF患者,我们收集的数据之间的死亡率诊断和研究结束的。死亡率呼吸道被定义为死亡的发生原因的时候IPF的恶化或结束阶段。
肺功能测试
肺功能测试使用Sensormedics执行Vmax安可体积描记法(美国Carefusion,圣地亚哥,CA)按照ATS /人建议[17)和欧洲共同体对钢铁和煤炭参考方程(18]。用力肺活量(FVC)、肺活量和用力呼气量在1 s值被表示为百分数预测值根据性别、身高和年龄。
胸CT
回顾性分析182例患者的胸CT扫描。使用64片胸CT扫描进行CT扫描仪(荷兰飞利浦医疗保健、DA最好)。他们被蒙蔽的胸部放射学家同时分析(o . Favelle)和肺专家(s . Marchand-Adam),达成明确共识关于病变的量化。观察家失明病人的临床和功能细节,按照以前公布的标准(19]。
简而言之,肺异常进行评估的存在,数字,范围和分布,如所描述的年代umikawaet al。(20.]。透明包括毛玻璃混浊,micronodules和肺泡合并作为牙槽炎被认为是积极的肺泡损伤和量化分数;透明如线性混浊、牵引支气管扩张、支气管扭曲,大疱形成,囊肿和蜂窝被认为纤维化病变表达式和纤维化病变评分量化。这两个模式都取得了另外六个地区的肺癌,定义为:上部区域上方的船底座的水平;水平之间的中间区域位于船底座和下肺静脉的水平;和较低的区域位于下肺静脉的水平以下。肺泡透明薄片上的强度高分辨率CT在每个领域得分)方法,从0(缺席)到4(出现在< 25%,25 - 50%,50 - 75%和> 75%的肺实质区)。纤维化的透明的强度是由相同的量化过程,从0(缺席)到4(出现在< 5%,5 - 25%,25 - 50%和> 50%)在每个区域。总肺泡和纤维化的分数介于0和24之间。使用相同的方法,我们还记录了小叶衰减和网状。
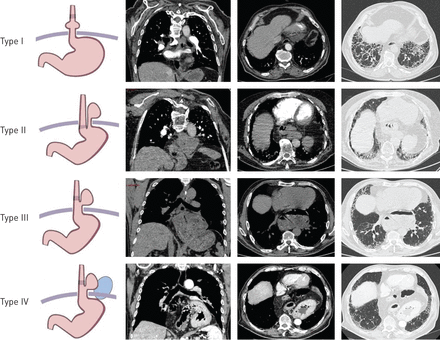
此外,CT扫描评估食管裂孔疝的存在与否。如果存在,食管裂孔疝分为I-IV类型,如前所述(图2)[21]。放射科医生和肺癌专家之间的协议是好的(κ= 0.715,95% CI 0.621 - -0.793)。额叶和矢状的测量直径(毫米)的较低部分的食管纵隔(劣质第三)轴向部分使我们能够计算出食管或胃胸内的区域。空气或食物的存在的存在/液体/因此水平食道被记录。
代表计算层析图像与I型特发性肺纤维化患者,II, III和IV食管裂孔疝。I型:迁移oesophagogastric结通过向头部地方向的差距。II型:oesophagogastric结隔膜下仍在正常位置;迁移胃底部的胸部。类型III:迁移oesophagogastric结的胸部,眼底和胃的其他部分。IV型:迁移其他结构和器官的胸部。
统计分析
非参数方法,所有数据值(范围)。连续数据使用克鲁斯卡尔-沃利斯检验ILD组之间比较。的Mann-Whitney紫外线测试进行比较IPF患者组I型食管裂孔疝,类型II, III或IV食管裂孔疝,没有食管裂孔疝。卡方和费舍尔测试是用于比较分类数据为每个组。相关性评估使用枪兵的等级次序测试。
我们研究了死于呼吸的发生原因IPF组使用一个生存与竞争风险模型。《纽约时报》认为在这个日期的分析诊断死亡日期,几个月。G雷的(22测试比较的累积发病率曲线组。我们估计的危害比(人力资源)与F快乐和G雷的(23)多态模型竞争风险,其95%置信区间和假定值。首先,进行单变量分析,以食管裂孔疝的存在为唯一解释的变量。然后,我们使用多变量模型随着年龄的增长,肺活量和纤维化评分covariables除了食管裂孔疝的存在。呼吸死因的累积发病率曲线绘制每组(有无食管裂孔疝)。统计学意义是定义为p < 0.05。
结果
临床、功能和IPF患者的CT扫描数据和其他ILD
ILD患者被分为四组:IPF (n = 79), CHP (n = 32)、肺参与由硬皮病(SSc);n = 17)和其他CTD排除硬皮病(non-SSc仪;12 n = 54,包括17类风湿性关节炎,自身免疫性肌炎,11干燥综合征,三个微观polyangiitis与自身免疫功能和11间质性肺炎(要诀))。IPF诊断标准是基于一个明确的模式通常的间质性肺炎(摘要)CT扫描(n = 71)或CT摘要本文可能的组合模式和一个明确的组织病理学摘要模式所示外科肺活检(n = 8)(在线补充表S3)。硬皮病是分开对待其他ctd因为它经常伴随着特定的食管损伤。一个要诀患者特定的食管损伤。
介绍了临床和功能数据表1。IPF患者比那些SSc (p = 0.001)。没有差别的IPF患者和其他ILD的时代。有较小比例的女性和更多的吸烟者比共和人民党(CHP) IPF组,SSc和non-SSc CTD组(p < 0.05)。有呼吸道症状的差异不显著。急性发作的频率是相同的在IPF CHP病人,但这是高于其他组(p = 0.01)。FVC IPF患者高于CHP患者(p = 0.01),但与其他ILD组相似。BALF细胞计数S1在线补充表所示。总IPF患者纤维化分数高于那些SSc (p = 0.03),但与其他组相似。
比较倾心于症状和食管裂孔疝的IPF患者与其他ILD的病人
SSc和IPF患者显示,倾心于症状(没有区别图3)、PPI治疗食管裂孔疝特征(患病率、食管或胃胸内的区域和存在的食物/液体/食管因此水平)(表2)。
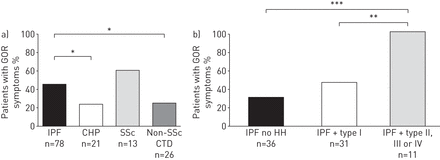
gastro-oesophageal频率(工资)症状)四组诊断间质性肺病(特发性肺纤维化(IPF),慢性过敏性肺炎(CHP)硬皮病(SSc),和non-SSc结缔组织病(CTD))和b) IPF患者食管裂孔疝(HH),与I型HH和类型II, III或IV HH。IPF患者更倾心于比共和人民党和non-SSc CTD患者症状。IPF患者类型II, III或IV HH倾心于症状比IPF患者类型没有HH我HH或IPF患者。*:p < 0.05;* *:p < 0.01;* * *:p < 0.001。
气油比症状,药物与PPI和食管裂孔疝的发生率更频繁的在IPF CHP (p < 0.05)和non-SSc CTD (p < 0.05) (图3和表2)。的流行阶段II, III或IV食管裂孔疝IPF患者明显高于non-SSc CTD患者(p = 0.027)。食管或胃胸内的区域的下三分之一的纵隔是IPF组大于non-SSc CTD患者(p = 0.003)。
IPF患者比较,没有食管裂孔疝
IPF患者I型食管裂孔疝(n = 31)或II型,III或IV食管裂孔疝(n = 11)比那些没有食管裂孔疝(分别为p = 0.01, p = 0.001),报道更倾心于症状(58%与31%,p = 0.034) (表3)。倾心于症状明显更频繁的IPF患者类型II, III或IV比其他两组食管裂孔疝(图3 b)。BALF细胞计数、PPI治疗吸烟、咳嗽、肥胖和恶化率IPF患者没有差异,没有食管裂孔疝。CT纤维化分数和呼吸功能IPF患者没有差异,没有食管裂孔疝。
死亡率的预测因素
生存中值为31个月的42 IPF患者食管裂孔疝,和40个月的37 IPF患者食管裂孔疝。IPF组食管裂孔疝,26(62%)患者死亡,23日从呼吸的原因,两个来自心血管疾病和肺癌,而在IPF集团没有食管裂孔疝,21例(57%)患者死亡:14从呼吸的原因,三个从心血管疾病,三个从肺癌和败血症。死于呼吸之间的时间诊断和IPF患者食管裂孔疝的原因是低于无食管裂孔疝(格雷的测试:p = 0.009) (图4)。所示表4多元分析与竞争风险识别两个呼吸引起的死亡率的独立预测因子:IPF患者食管裂孔疝(HR 2.41, 95%可信区间1.09 - -5.35;p = 0.030)和更高的CT肝纤维化评分(HR 1.13, 95%可信区间1.03 - -1.24;p = 0.011)。结果是相同的,只考虑接受PPI治疗的病人(在线补充表S2)。两个IPF患者食管裂孔疝fundoplication, 29岁,66年去世几个月后IPF诊断。
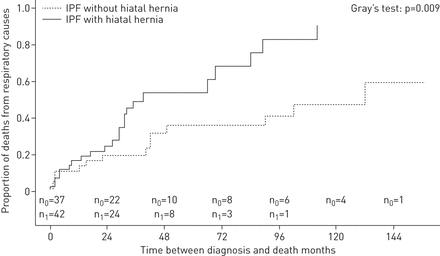
比较死亡率由于呼吸道导致特发性肺纤维化(IPF)患者和无食管裂孔疝(n1和n0分别)。
讨论
我们研究的主要结果是1)食管裂孔疝发病率的增加在IPF相比其他ILDs研究协会和2)增加死亡风险从呼吸道引起的食管裂孔疝。
我们调查是否存在食管裂孔疝的劣质第三使用胸CT扫描后纵隔。食管裂孔疝的诊断是经典通过食管造影剂或食管内镜过境,但胸和腹部CT扫描也被认为是一个可靠的工具,食管裂孔疝的诊断和评估(24- - - - - -26]。食管裂孔疝可以重建CT图像分类的冠状面(图2)[25]。重建CT图像使我们计算的最大区域测量食管和胃的矢状面和冠状直径的三分之一的纵隔低劣。这种定量方法被Vonket al。(27),报告患者的食管扩张62%的SSc的测量冠状平面食管的直径,与12%的控制。在我们的研究中,59%的患者有食管裂孔疝SSc,表明CT扫描的确是一个健壮的食管裂孔疝的诊断方法。
在我们的研究中,53%的IPF患者有食管裂孔疝。这个结果是一致的ee等。(7),而N另外一些et al。(11)观察到的频率在IPF食管裂孔疝的39%,相比之下,13%在哮喘,慢性阻塞性肺病和17%,接近食管裂孔疝一般人群的患病率(17%)(28]。这种差异可能反映了不同的方式解释CT扫描。除了已知的IPF食管裂孔疝的发生频率增加,我们的数据显示更高的频率更严重的食管裂孔疝(类型II, III或IV)比其它ILD IPF (14%与2 - 6%)。食管裂孔疝是公认的作为一个独立的预测因素的回流29日]。因此,我们的IPF患者食管裂孔疝(特别是类型II, III或IV食管裂孔疝)报道更倾心于症状比没有食管裂孔疝的病人。
食管裂孔疝的更高频率的IPF引发了这样一个问题:食管裂孔疝是一种疾病,结果或IPF的司机。食管裂孔疝的风险因素包括腹腔压力增加,在肥胖、妊娠、慢性腹水,腹部创伤、慢性咳嗽、先天性异常(短食道)和吸烟28]。IPF患者、咳嗽、肥胖和吸烟组没有差异,没有食管裂孔疝。食管裂孔疝的发生率随着年龄的增加;其患病率估计∼10%的人年龄< 40年,56%的人年龄> 70岁(30.]。在我们的研究中,IPF患者食管裂孔疝是比那些没有食管裂孔疝。然而,除了ILD SSc, IPF患者的年龄没有明显不同于其他ILDs患者(平均74岁),而53%的患者有食管裂孔疝与IPF相比,28%的共和人民党患者或non-SSc CTD患者的33%。因此,我们认为,老年的IPF患者可能不是关键的解释更高频率的食管裂孔疝病。
一种可能性的食管裂孔疝的患病率更高IPF是减少肺合规次要广泛纤维化可能导致膈柱的侧移,其次是胃上升到胸腔。然而,我们没有观察到任何不同CT肺纤维化评分或FVC,间接反映了肺合规,CHP IPF患者与患者之间,而食管裂孔疝IPF的频率高于后者。同样,CT纤维化分数和呼吸功能IPF患者没有差异,没有食管裂孔疝。因此,尽管我们没有测量胸内的压力在我们的病人,这些结果表明,肺纤维化引起收缩力不扮演主要角色在IPF食管裂孔疝的频率增加。
相反,食管裂孔疝的发病机理可能发挥作用在IPF通过增加工资的可能性的风险,因此microaspirations在肺31日]。年代avarino等。发现了一个很好的相关性程度的回流和CT扫描纤维化评分为硬皮病(32]和IPF [33]。microaspiration的角色在《创世纪》或IPF的进展是由Lee等。(7]报告衡量的胃蛋白酶浓度IPF患者BALF的稳态和发作期间,这表明microaspirations IPF的胃液体频繁;和安慰剂的临床试验的数据提取,IPF患者抗酸缓慢下降FVC相比,患者没有接受这些药物(5]。
我们的研究的主要发现是食管裂孔疝的存在是死亡率的预测IPF患者呼吸的原因。相比之下,N另外一些等。(11)没有观察到任何联系IPF的食管裂孔疝的存在和严重性,除了IPF患者食管裂孔疝和回流PPI治疗,比IPF患者肺功能,食管裂孔疝和未经处理的回流。在我们的研究中,我们不知道antireflux疗法启动时对患者已经在IPF诊断治疗,或如果它是启动后对治疗那些没有条目。没有控制治疗,我们也没有任何结果数据。这限制了结果的解释关于IPF PPI治疗保健的作用。由于食管裂孔疝是增加乳腺癌的复发及药物治疗的失败,包括PPI (25),这将是有趣的评估这些患者的食管裂孔疝的手术矫正。
我们认识到,这项研究有一定的局限性。首先,我们的研究观察,收集的数据。第二,我们的样本小,尤其是在IPF组型II, III或IV食管裂孔疝。这个小样本大小限制任何公司可以从数据中得出结论。第三,研究pirfenidone nintedanib变得可用。antifibrotic治疗的效果在IPF患者食管裂孔疝是未知的。最后,我们没有使用pH-metry调查气油比的存在。我们不能确认食管裂孔疝总是伴随着气油比,即使在患者证明倾心于症状。
最后,我们发现更高的IPF患者食管裂孔疝发病率比与其他ILD和类似的肺纤维化的严重程度。食管裂孔疝的存在与呼吸道导致死亡率的风险更高。我们的研究结果支持假设的上消化道功能障碍可能扮演一个特定角色的IPF的生理病理学。
脚注
可以从本文的补充材料www.qdcxjkg.com
利益冲突:披露可以找到与这篇文章www.qdcxjkg.com
- 收到了2015年10月30日。
- 接受2016年4月3日。
- 版权©2016人队