摘要
已经提出了几种复合标记物用于慢性阻塞性肺疾病(COPD)的风险评估。然而,参数的选择和评分的复杂性限制了临床的适用性。我们的目的是提供并验证一个独立于肺功能的简化的COPD风险指数。
PROMISE研究(n=530)用于开发一种新的预后指标。评估2年慢性阻塞性肺病相关死亡率和全因死亡率的指标表现。外部有效性在ProCOLD、COCOMICS和COMIC队列中稳定和加重的COPD患者中进行测试(总n=2988)。
采用混合临床和统计方法,体重指数(B)、慢性阻塞性肺病严重急性加重频率(AE)、医学研究委员会改进的呼吸困难严重程度(D)和copeptin (C)被确定为最合适的简化标记组合。每个参数分别取0、1或2分,总分为B-AE-D或B-AE-D- c。结果表明,B-AE-D和B-AE-D- c在预测2年全因死亡率方面,至少与BODE(体重指数、气流阻塞、呼吸困难、运动能力)、ADO(年龄、呼吸困难、气流阻塞)和DOSE(呼吸困难、气流阻塞、吸烟、加重)指数一样好(c统计量分别为0.74、0.77、0.69、0.72和0.63;Hosmer-Lemeshow检验均p>0.05)。两项指标均与COPD相关(预测COPD相关2年死亡率的c统计值分别为0.87和0.89)。在COCOMICS和COMIC中进行了B-AE-D的外部验证(1年全因死亡率的c统计:0.68和0.74;2年全因死亡率的c统计:0.65和0.67;Hosmer-Lemeshow检验均p>0.05)。
B-AE-D指数,加上copeptin(如果有的话),可以对copd相关风险进行简单而准确的评估。
摘要
B-AE-D指数可以在无肺功能的情况下对copd相关风险进行简单而准确的评估http://ow.ly/XFBox
简介
慢性阻塞性肺疾病(COPD)是导致死亡和残疾的主要原因之一,已成为世界各地的一个主要全球流行病[1,2].慢性阻塞性肺病属于“不完全可逆气道阻塞”范畴,是一种异质性很强的疾病,具有多种分子和临床模式[3.].为了克服慢性阻塞性肺病的复杂性和肺功能的局限性,我们引入了许多复合标志物来评估预后。几个评分,包括BODE指数(体重指数(BMI)、气流阻塞、呼吸困难、运动能力)、ADO指数(年龄、呼吸困难、气流阻塞)和DOSE指数(呼吸困难、气流阻塞、吸烟、加重),比单独气流阻塞更能预测copd相关的预后[4- - - - - -6].然而,指标参数的一些特征难以评估,可能会限制常规临床应用。运动测试以及肺功能测试与一定的测试努力有关,依赖于患者的动机。年龄和大多数共病等参数无法改善,因此不符合序列评估的条件[7].合并肺功能参数的评分不能在COPD急性加重期(AECOPD)进行危险分层。然而,许多患者可能不进行随访,或可能在病情稳定评估前反复恶化。也许最重要的是,简单的工具,如CURB-65(混淆,尿素7 mmol·L−1,呼吸频率≥30次呼吸·min−1,血压< 90mmhg(收缩期),≤60mmhg(舒张期),年龄≥65岁,常用于肺炎危险分层[8,但许多临床医生非常不愿意使用更复杂的评分。copd相关风险的新指标,特别是如果包括压力和炎症标记,可能符合简化的风险评估。
本研究的目的是为稳定期和加重期疾病的临床应用提供一种新的简化的copd特异性风险指标,并评估排除肺功能参数是否限制了风险预测。
方法
研究设计与患者
研究人员驱动的PROMISE(使用全身标记物预测慢性阻塞性肺疾病严重加重期的预后;www.isrctn.comISRCTN99586989)队列研究用于开发一个新的风险指数。PROMISE是一项多中心慢性阻塞性肺病纵向研究,在11个欧洲三级呼吸中心进行,评估慢性阻塞性肺病在病情稳定和加重期间的预后预测因素[9,10].纳入全球慢性阻塞性肺疾病倡议(GOLD) II-IV级的稳定期COPD患者。在ProCOLD、COCOMICS和COMIC组中进行索引验证。ProCOLD(降钙素原引导的抗生素治疗慢性阻塞性肺病急性加重)是一项单中心慢性阻塞性肺病试验,包括住院的慢性阻塞性肺病加重患者[11].患者被要求符合严重AECOPD的定义和肺活量测定的COPD标准。COCOMICS(评估西班牙慢性阻塞性肺病多成分指数的协作队列)包括西班牙几个慢性阻塞性肺病队列的个体患者数据[12].7个COCOMICS队列,包括稳定的COPD患者(Requena [13,塞维利亚[14,特内里费[15,萨拉戈萨[16)和加重的COPD患者(Terrassa I-III [17,18])用于索引验证。COMIC (COPD死亡和炎症队列)是一项单中心研究,包括来自荷兰的稳定和加重的COPD患者[19].所有研究均经当地机构审查委员会批准,所有患者均给予书面知情同意。详细的研究特点在补充材料中有描述。
预测
基线时评估病史,包括前一年发生AECOPD和严重AECOPD的次数、临床评估和其他预后预测因素(纳入研究)。按上文所述进行肺功能测试、6分钟步行距离及经修订的医学研究理事会(mMRC)问卷调查[20.- - - - - -23].测定PROMISE和ProCOLD组血清copeptin水平。AECOPD定义为慢性阻塞性肺疾病(COPD)患者呼吸困难、咳嗽和/或痰液的急性持续恶化,超过正常的日常变化;严重AECOPD被定义为COPD加重,需要住院治疗[24,25].如果非慢性阻塞性肺病是主要原因,根据主治医生的评估,恶化不被视为AECOPD。在COCOMICS的队列中,严重的AECOPD被定义为需要急诊室就诊或住院的加重。在PROMISE中,1年的研究评估用于内部验证。已建立的指数BODE、更新的BODE(重新校准的BODE指数)、ADO和DOSE按先前报道的方法计算[4- - - - - -6].
结果
主要结果是全因死亡率。在PROMISE中,在2年的研究随访中评估生存率。对于每一例死亡,医生将死亡原因定义为COPD相关、COPD无关或未知。在纳入研究5年后,我们又联系了一部分PROMISE患者(所有纳入瑞士巴塞尔研究中心的患者),以评估生存状况。索引开发和验证队列的后续情况见图E1和E2。
变量的选择
使用临床和统计学方法选择指标变量。所有参数必须满足四个标准。1) COPD特异性:要求参数与COPD合理相关;2)可修改性:为了捕捉病程期间的恶化和改善,要求参数是可修改的;3)适用性:为了便于临床使用,参数必须易于适用;4)独立预测结果。由于缺乏COPD特异性和不可修改性,年龄和共病等参数不符合条件。6分钟步行距离、肺功能测试和圣乔治呼吸问卷由于适用性的限制而不符合要求,特别是在病情加重期间。采用单因素和多因素cox回归分析(表E1和E2)评估预后预测性能。由于表现不佳,排除了吸烟状况和总(中度和重度)加重次数。 BMI, the number of severe AECOPD, mMRC and copeptin remained the clinically most suitable and well-performing parameters. Furthermore, an entirely statistical approach was used to identify the best predictors for 2-year all-cause-mortality out of 58 parameters [26].选取了10个参数,包括BMI、严重AECOPDs的数量、mMRC和copeptin(数据未显示)。在第二种方法中,将几个其他预测因子添加到模型中以测试其性能(表E3)。当年龄、性别、用力呼气量在1 s (FEV)1)、吸烟状况或6分钟步行距离添加到这些参数后,预测2年全因死亡率的回归模型的c统计量改善<0.01,仅提供少量的额外预测性能。
简化和优化指数的发展
BMI (B)、严重AECOPD频率(AE)、mMRC呼吸困难严重程度(D)和copeptin (C)四个参数符合新的风险指标。每个参数被分成三个风险组。拨款主要是根据既定的分拨额(表1而且2).在两个简化评分(简化B-AE-D和简化B-AE-D- c)中,每个风险组分别为0分、1分或2分(表1).Cox比例危险生存分析用于开发两个优化分数(优化B-AE-D和优化B-AE-D- c),并分配了单个点数(表2和表E4)。分数的增加表明风险增加。
统计数据
离散变量用计数(%)表示,连续变量用平均值±表示sd.存活者和非存活者在基线和死亡前特定月的copeptin水平的组内分析采用Wilcoxon标记等级检验进行评估。采用Cox回归模型进行指标制定、优化指标的分值分配、指标性能评估和验证。预测模型的性能可以通过鉴别和校准的方法进行评估。辨别是指辨别能力,校准是指观察结果与预测结果的一致性[27].采用c统计量作为区分度的度量,采用Hosmer-Lemeshow拟合优度检验进行校准。后者评估在不同的风险组中预测的和观察到的风险是否不同。死亡时间用Kaplan-Meier生存曲线描述,用log秩检验分析。所有检验均为双侧检验,p值<0.05为显著性。使用SPSS 20版本(IBM, Armonk, NY, USA)和R项目(www.r-project.org)分析数据。
结果
530例患者来自PROMISE人群,平均±sd年龄为67±10岁,主要为男性(70%),平均±sd年龄sdFEV1(49±17%)pred被纳入(图E1)。基线特征总结见表E5。随访2年以上的患者发生肺动脉高压、既往肺减容手术和肺康复的可能性更大(p=0.047、0.017和0.026)。相比之下,被排除或失去随访的患者更有可能吸烟,有更多的既往加重次数,需要更多的长期氧疗(p分别为0.022、0.001和0.047)。所有其他基线特征在两组间相似。2年全因死亡率为12% (n=54)。2年内死亡原因中46% (n=25)与COPD相关,37% (n=20)与COPD无关,17% (n=9)死因不明。巴塞尔研究中心的233名患者中有231名进行了5年的随访。5年全因死亡率为36% (n=82)。
预测2年全因死亡率的个别参数
为了评估预测2年全因死亡率的个别参数,采用单变量Cox回归模型(表E1)。除年龄外,BODE参数(BMI, FEV1% pred, mMRC和6分钟步行距离),严重AECOPD的数量,圣乔治呼吸问卷和copeptin预测2年全因死亡率(均p<0.01)。有趣的是,GOLD联合评估组(A、B、C、D)和中重度AECOPD总人数对预后的预测效果较差(p=0.076和0.055)。
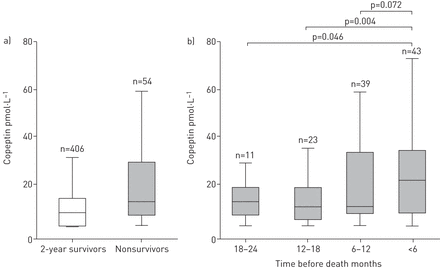
采用多变量Cox回归模型确定全因死亡率的独立预测因子(表E2)。FEV1并不是一个独立的预测指标。相比之下,mMRC在所有指标中独立预测死亡。在所有研究模型中,Copeptin是2年全因死亡率的独立预测因子(当添加到BODE、更新BODE、ADO和DOSE参数时也是如此;P合计≤0.001)。Copeptin水平在稳定期或加重期COPD(稳定期疾病)之间无差异与中度加重(n=100):平均copeptin差异1.8±12.5 pmol·L−1, p = 0.2;稳定的疾病与重度加重组(n=41):平均copeptin差异10.7±40.9 pmol·L−1, p = 0.10)。有趣的是,copeptin水平在死亡前6个月内最高(图1).
copeptin水平的分布:a)基线时2岁存活者和非存活者的copeptin水平分布;b)死亡前特定时间点的copeptin水平分布组内分析采用Wilcoxon符号秩检验。
预测全因死亡率的指标表现
采用c统计量(判别)和Hosmer-Lemeshow拟合优度检验(校准)对评分表现进行评估。简化和优化的B-AE-D和B-AE-D- c指数的点分配描述在表1而且2.在已建立的指标中,BODE和更新BODE评分在预测1年全因死亡率(表3).在随访5年的亚组患者中,3年和5年全因死亡率的最佳预测因子是ADO指数(表4).BODE和ADO是2年全因死亡率的最佳预测因子。在预测3年和5年全因死亡率方面的歧视下降。简化和优化的B-AE-D和B-AE-D- c指数在预测5年全因死亡率方面至少与其他指数一样好。肺功能参数没有改善B-AE-D或B-AE-D- c在预测2年全因死亡率方面的表现(表E3)。所有评分均可接受校准(p>0.05)。指标点的增加与较差的预后相关(所有指标:对数秩p<0.001) (图2).

简化和优化的B-AE-D和B-AE-D- c指数的2年生存率Kaplan-Meier估计。B:体重指数;AE:慢性阻塞性肺疾病严重急性加重的频率;D:改良医学研究委员会呼吸困难严重程度;C: copeptin。
预测慢性阻塞性肺疾病相关死亡率的指数表现
评估指标是否能预测copd相关结局(copd相关死亡率)与使用Cox回归模型(表5).对2年慢性阻塞性肺病相关死亡率进行了类似分析。B-AE-D和B-AE-D- c在预测copd相关死亡率方面优于现有指标。ADO和B-AE-D-C是预测copd相关生存率的唯一指标。以年龄和调整后的Charlson共病指数作为对照。两者在预测慢性阻塞性肺疾病相关死亡率方面的表现并不优于预测非慢性阻塞性肺疾病相关死亡率。
内部验证
为了进行内部验证,我们在疾病稳定的研究纳入1年后使用所有B-AE-D-C参数,而不是统计方法。分数的分配如上所述。评价1年和4年预后评分表现(n=299和185)。简化B-AE-D预测1年和4年全因死亡率(c统计(95% CI) 0.74(0.63-0.86)和0.62 (0.54-0.69);Hosmer-Lemeshow检验:p分别=0.7和0.3)。当纳入copeptin (B-AE-D-C)时,观察到预测4年全因死亡率的性能改善(1年和4年全因死亡率的c统计:0.75(0.62-0.88)和0.68 (0.61-0.76);Hosmer-Lemeshow检验:p分别=0.2和0.9)。由于优化后的索引仅以简化为代价提供了微小的性能改进,所以我们没有验证它们。
B-AE-D-C的外部验证
评分性能在160名因AECOPD住院的患者的不同队列中得到验证(图E2)。患者平均±sd年龄71±10岁,以男性(56%)为主,平均±1岁sdFEV141±18% pred(表E6)。2年全因死亡率为23% (n=36)。呼吸困难严重程度(mMRC)未进行评估,因此不可用。简化B-AE和简化B-AE- c预测2年和5年全因死亡率(2年全因死亡率:c统计量分别为0.60(0.52-0.69)和0.69 (0.60 - 0.78);Hosmer-Lemeshow检验:p=0.17, p= 0.8;5年全因死亡率:c统计0.59(0.52-0.66)和0.65 (0.57-0.72);Hosmer-Lemeshow检验:p=0.08和0.2)。
B-AE-D的外部验证
B-AE-D指数在来自西班牙的COCOMICS队列和来自荷兰的COMIC研究中得到验证。来自7个COCOMICS队列的2153例患者被纳入B-AE-D验证(图E2)。患者平均±sd年龄66±10岁,以男性(93%)为主,平均FEV152±20% pred(表E6)。2年全因死亡率为15% (n=307)。B-AE-D预测1年、2年和3年全因死亡率(c统计:0.68(0.63 - 0.72)、0.65(0.62-0.69)和0.63(0.61-0.66))(表E7)。B-AE-D校正良好(Hosmer-Lemeshow检验:p分别=0.5、0.3和0.2)。对COMIC研究中的675例患者进行进一步的B-AE-D验证(图E2)。COMIC患者平均±sd年龄67±10岁,以男性(60%)为主,平均±10岁sdFEV153±19% pred(表E6)。2年全因死亡率为12% (n=82)。稳定期B-AE-D预测1年、2年和3年全因死亡率(c统计:分别为0.74(0.65-0.83)、0.67(0.61-0.72)和0.66(0.61-0.70))。B-AE-D可很好地用于预测全因死亡率(Hosmer-Lemeshow检验:p分别为0.2、0.5和0.5)。
讨论
在此,我们提出了一种新颖、简单、独立于肺功能的COPD风险评估工具。B-AE-D和B-AE-D- c指数与建立的更复杂的预测结果的指数一样有效。这两项指标都是慢性阻塞性肺病特异性的,并可预测稳定期和加重期慢性阻塞性肺病的死亡。
入选参数的临床适用性和意义是我们在编制指标时优先考虑的因素。因此,参数主要是根据临床特征而不是统计表现来选择的。BMI、严重AECOPD频率、呼吸困难严重程度和copeptin被确定为易于应用、可预测和相关的COPD参数的组合。所有四个单独参数的相关性和预测属性之前已经报道过。
超重似乎具有保护作用,而低体重则是众所周知的死亡率预测因素[28- - - - - -30.].值得注意的是,体重变化与预后变化相关[31,32].除了已确定的COPD BMI阈值(21 kg·m−2),我们发现BMI <18.5 kg·m的患者风险进一步增加−2,正常人群中已确定的低体重临界值[4,33].低住院死亡率和高长期死亡率是严重AECOPD的常见现象[34].几项研究报告称,AECOPD住院后2年死亡率很高,高达49% [13,17,34,35].有趣的是,中度AECOPD和COPD联合评估组(仅以频繁加重(GOLD C2)定义)与较差的预后无关,强调加重严重程度可预测预后[13,36,37].这与我们的发现一致,即总AECOPD频率不能预测死亡率,而严重的AECOPD预示着不利的结果。在大多数COPD患者中,呼吸困难是与生存率差相关的主要和最痛苦的症状,其他参数未反映[38,39].最近有报道称,尽管C组患者肺功能较差和/或AECOPD较多,但COPD GOLD B组患者的生存率低于C组患者[40].因此,在预测风险方面,呼吸困难似乎比肺功能和AECOPD频率更相关。然而,呼吸困难可能波动,特别是在加重期间,潜在地影响预测表现不利。最近,AECOPD频率和呼吸困难被纳入了GOLD推荐的COPD分级系统,进一步强调了这两个参数的重要性。与之前的COPD风险评分相比,我们没有包括FEV1在小说指数中。这是由于AECOPD期间和之后的肺容量短暂减少,以及在加重期难以进行可靠的肺功能测量[41].重要的是,B-AE-D和B-AE-D- c以及包括气流阻塞在内的其他指标均表现良好,添加FEV后指标没有进一步改善1.然而,肺功能是COPD诊断的基础。然而,一旦确诊,肺量测定的实际和内在困难限制了其在风险预测方面的有用性,特别是在严重的COPD中。
遍布全身的多个受体感知信息,并在需要时促进自主神经和内分泌系统等随后的代偿变化。这些性能良好的系统可用于临床目的。通过这种方式,低氧血症、高碳酸血症、炎症和其他一些应激源导致精氨酸加压素(AVP)合成和释放增加;因此,提示AVP是一种可能的COPD标志物[42- - - - - -44].然而,AVP的半衰期短,阻碍了其临床应用。Copeptin是一种糖肽,包含AVP前激素的c端部分,是一种稳定、更可靠的AVP测量替代品[22].copeptin在预测死亡率方面的性能先前有报道,其阈值为40 pmol·L−1建议[45].本文证明:1)copeptin水平在稳定期和加重期COPD中相似;2) copeptin水平在死前几个月内增加;3) copeptin是一个独立的、表现良好的死亡率预测因子;所有这些都是预后标志物的重要特征。
对于指标点分配,我们提出了简化和优化的指标。然而,在预测结果方面的表现是相似的。出于简单的主要目的,我们建议使用简化的B-AE-D指数进行COPD风险评估,如果有的话,再加上copeptin。包括copeptin在内的B-AE-D- c在预测1年和2年全因死亡率方面的表现与B-AE-D相似。然而,2年后,性能有了适度的改善。重要的是,在未来的研究中需要更好地定义copeptin的附加价值。此外,有必要评价业绩的改善是否值得增加费用。
这些指标由三到四个参数组成,有三个容易记住的风险组。0-1-2分配可能是迄今为止COPD风险评估最简单的指标。尽管正如内部和外部验证的那样,简单并不是以索引性能为代价的。在漫画组和COCOMICS组中进行了B-AE-D的外部验证。大量的患者和慢性阻塞性肺病严重程度、表型、种族和社会背景的可变性允许在广泛的慢性阻塞性肺病谱系中进行验证。B-AE-D-C在纳入PROMISE(内部验证)和ProCOLD 1年后进行验证,无呼吸困难(外部验证)。不同队列内和跨不同队列的群体异质性导致了指标性能的变化,但也确保了最佳的B-AE-D验证。
我们还证明了B-AE-D和B-AE-D- c可以预测copd相关死亡率。因此,低BMI、严重AECOPD、呼吸困难严重程度和高copeptin水平的主要决定因素是COPD的基线严重程度;即。COPD的严重程度越高,低BMI、严重AECOPD、严重呼吸困难、高copeptin和死亡的可能性就越大。
合并症在COPD中很常见,具有重要的治疗和预后意义[46,47].此外,合并症,特别是心脏病,可能增加严重aecopd的数量和偏向性呼吸困难的评估。与之前的研究结果一致,几种共病对AECOPD的频率和预后有影响。但重要的是,共病并不限制B-AE-D或B-AE-D- c在预测预后方面的表现(数据未显示)。此外,表型可能会影响索引的性能。在之前的一项研究中,BODE和ADO与COPD表型的相关性很低[48].在PROMISE中,反映COPD表型的几个标记物(每年超过两次COPD加重、慢性咳嗽、休息和运动时的氧饱和度)对B-AE-D性能没有影响(数据未显示)。
我们承认有一些限制。首先,我们使用mMRC呼吸困难量表对呼吸困难进行分层。尽管其使用频率高且验证效果良好,但仍有更精确的呼吸困难评估工具可用,并可能进一步提高预测性能[6,49].其次,ProCOLD验证队列中没有评估呼吸困难;因此,评价B-AE-C而不是B-AE-D-C。呼吸困难可能进一步提高B-AE-C的预测性能,但这不能被证实。第三,由于纳入标准和研究地点的不同,各队列的患者特征不同,指标表现不一;尽管人口异质性可能反映了现实生活条件。最后,种族和呼吸困难感知的差异可能影响B-AE-D点分配和潜在的表现。因此,需要在欧洲以外的一系列疾病严重程度和不同人群中进一步验证。
然而,大样本量、足够数量的事件、5年的随访时间、全因和COPD相关死亡率的评估以及内部和广泛的外部验证是当前研究的优势,而在其他新型COPD指标的报道中大多没有提供。这项研究使我们能够建立一个非常简单的肺功能独立的COPD风险指数。B-AE-D很容易获得,具有慢性阻塞性肺病特异性,可用于稳定和加重的慢性阻塞性肺病。此外,B-AE-D的评估几乎不需要费用,因此在高收入和低收入国家都可以获得。
总之,B-AE-D指数加上可用的copeptin可以在无肺功能的情况下对copd相关风险进行简单而准确的评估。
确认
A. Schötzau为PROMISE进行数据管理,并因此获得经济补偿。
脚注
编辑评论欧元呼吸2016;47: 1601 - 1605。
本文的补充资料可从www.qdcxjkg.com
支持声明:Thermo Scientific Biomarkers (Hennigsdorf, Germany)提供了copeptin测量的所有试剂。本文的资助信息已存入FundRef
利益冲突:没有声明。
- 收到了2015年9月7日。
- 接受2016年1月18日。
- 版权所有©ERS 2016