摘要
IL-22R1在非小细胞肺癌中的高表达是总生存率较差的独立指标http://ow.ly/WZxKh
致编辑:
最近十年,人们对癌症机制的看法发生了变化。目前有相当多的证据表明肿瘤微环境状态与疾病结局密切相关。特定免疫细胞类型或分子的存在决定了在微环境中是亲肿瘤免疫反应还是抗肿瘤免疫反应占主导地位[1].因此,提高对调节肿瘤微环境的因素的理解对于制定有效的未来癌症管理策略至关重要。
在这方面,白细胞介素(IL)-22作为IL-10家族的一员,因其与癌症的发生和发展密切相关而引起了广泛的关注[2].IL-22由先天淋巴样细胞产生,介导其细胞效应通过由两种不同亚基(IL-22受体亚基1 (IL-22R1)和IL-10R2)组成的异二聚体受体复合体,以及通过信号换能器和转录激活剂(STAT)分子传递的信号[3.].IL-10R2亚基普遍表达。IL-22R1决定细胞对IL-22的敏感性,并仅由上皮细胞表达[4].因此,IL-22在白介素中是不寻常的,因为它不直接调节原型免疫细胞的功能,即.而不是靶向于体外屏障的细胞,如呼吸道上皮细胞,并诱导参与组织稳态的基因的表达[3.].
值得注意的是,IL-22信号是促生存、细胞迁移、有丝分裂和抗凋亡作用的关键调控因子,这些功能可被侵袭性癌症劫持,以促进肿瘤生长和转移[2].此外,小鼠模型系统的功能研究表明,IL-22/IL-22R具有免疫调节特性,包括在癌症中[2].IL-22的表达与胃肠道肿瘤的发生和分期以及肝细胞癌呈正相关[2].IL-22也被证明通过增加基质金属蛋白酶9来提高胰腺癌细胞系的侵袭能力[2].然而,值得注意的是,关于肺癌中IL-22/IL-22R改变的研究有限[5- - - - - -7].2008年,Z挂et al。[7]报道了6例组织学诊断为原发性非小细胞肺癌(NSCLC)患者的肿瘤组织中IL-22基因表达增强。Koboldet al。[5]证实了这种IL-22在NSCLC中的异常表达,但不能将这种过度表达与NSCLC的发生和进展联系起来,尽管有一项针对更大患者队列的研究。无论如何,我们认为,当人们考虑肺癌时,更贴切的是关注IL-22R的调控本身而不是细胞因子IL-22,因为与分泌IL-22的先天淋巴细胞相比,携带il - 22r的上皮细胞可能更容易立即暴露于有害的空气污染物,包括烟草相关的致癌物。重要的是,我们和其他研究人员先前证明,IL-22R1亚单位的表达在肺屏障表面受到调节(正或负),在肺屏障表面上皮细胞在免疫反应的启动、调节和解决中发挥积极作用[8- - - - - -10].
鉴于此,我们的研究首先旨在调查一个大型肺癌患者队列中的IL-22R1失调,其次,更重要的是,评估其与总生存期的关系。
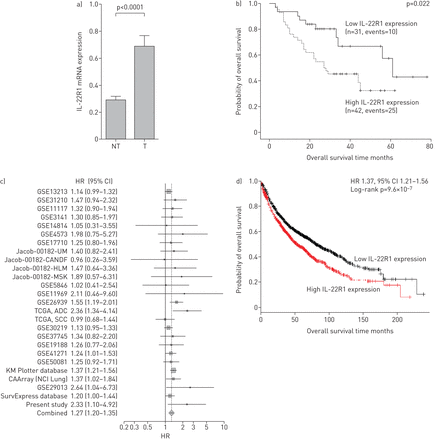
我们收集了2006年至2011年间接受NSCLC手术的患者的肺组织(申报申请编号为Ministère de l’enseignement Supérieur et de la Recherche: DC-2008-308)。获得每位参与者的知情书面同意。为了确定IL-22R1亚基表达是否在基因转录水平上受到调控,从肿瘤的匀浆和肿瘤邻近的组织学上非癌性肺组织中分离出总RNA (n=81)。所有样品均进行定量逆转录酶PCR处理。如图1一个IL-22R1基因在肺癌组织中的表达比非癌组织高两倍以上。从不同患者(随机选择)中提取的聚合蛋白的Western blot也一致显示,与正常组织相比,癌性样本中IL-22R1的表达增加(数据未显示)。由于IL-22R1具有相当有限的上皮组织分布[8- - - - - -10],我们进一步检查了IL-22R1在我们大型患者队列中两种主要NSCLC组织学表型中的过表达:鳞状细胞癌(SCC;n=36)和腺癌(ADC;n = 45)。最常见的是,SCCs起源于近端气道的含il - 22r的伪分层支气管上皮细胞,并与吸烟密切相关,而adc通常具有腺体组织学,出现在远端气道[11].值得注意的是,IL-22R1在SCC中显著上调(配对癌性/非癌性组织比较,均值±se4.5±0.8倍;p<0.0001, Wilcoxon符号秩检验),但在ADC样本中没有(配对癌/非癌组织比较,均值±se2.1±0.4成倍增加;p = 0.153)。此外,SCC中IL-22R1的上调比ADC组织型高3倍以上(p=0.005, Mann-Whitney U-test)。肺肿瘤中IL-22R1 mRNA的表达与吸烟状态无关(不吸烟者和当前/曾经吸烟者IL-22R1 mRNA表达比较,Mann-Whitney u检验p=0.944)。然而,在吸烟者中,与中度吸烟者相比,重度吸烟者(>49包年)肿瘤中IL-22R1表达显著上调(3.6倍)(p<0.001, Mann-Whitney U-test)。
白细胞介素22受体亚基1 (IL-22R1)高表达与原发性非小细胞肺癌(NSCLC)相关,并降低总生存率。通过定量逆转录酶PCR检测IL-22R1 RNA的表达,并归一化至内参基因(β-肌动蛋白而且Hprt181例组织学诊断为原发性NSCLC的外科患者。a)在来自NSCLC患者的配对组织中评估IL-22R1 mRNA在肿瘤(T)组织和非肿瘤(NT)组织对应物中的表达。数据以均数±表示扫描电镜.p值采用Wilcoxon符号秩检验计算。b) 73例NSCLC患者根据肿瘤中IL-22R1基因表达水平的总生存Kaplan-Meier图。通过X-tile算法确定将患者分为低IL-22R1表达和高IL-22R1表达的最佳分界点(分界点=0.297,肿瘤中IL-22R1表达的第42百分位)。p值由log-rank检验计算。c)基于预后扫描、PROGgeneV2、Kaplan-Meier (KM) Plotter和SurvExpress平台获得的数据,按队列划分的IL-22R1表达和总生存率的危险比(HR)森林图。d)通过Kaplan-Meier Plotter数据库检测1926例NSCLC患者IL-22R1表达的预后价值。IL-22R1肿瘤表达分为高表达与低根据中值表达式。
我们首次进一步评估了IL-22R1表达在原发性肺癌中的预后价值。为此,采用Kaplan-Meier方法计算患者总生存率,并使用log-rank检验进行比较。通过X-tile算法确定将患者分为IL-22R1低表达和IL-22R1高表达的最佳分界点[12].通过SPSS统计(17.0版)软件(SPSS Inc.,芝加哥,伊利诺伊州,美国)进行分析。在73例NSCLC患者和可用的随访数据中,Kaplan-Meier生存分析显示,肿瘤中IL-22R1高表达的NSCLC患者的总生存结局明显低于肿瘤中IL-22R1低表达的NSCLC患者(p=0.022) (图1 b).多变量Cox回归证实了IL-22R1与不良生存的相关性,并对重要的临床病理特征(包括组织类型和分期)进行了调整(危险比(HR) 2.8, 95% CI 1.2-6.5;p = 0.014)。为了进一步验证我们发现的潜在预后意义,我们询问了公开可用的表达分析平台,包括Kaplan-Meier Plotter [13],预后扫描[14], PROGgeneV2 [15]及SurvExpress [16].26项研究/数据集中具有相应95%置信区间的总生存风险比在森林图中绘制(使用StatsDirect软件3.0;StatsDirect Ltd, Altrincham,英国)(图1 c).IL-22R1表达与较低的总生存率密切相关(合并HR 1.3, 95% CI 1.2-1.4;p < 0.0001)。最后,我们通过Kaplan-Meier Plotter数据库(probe #220056_at)研究了IL-22R1表达在NSCLC患者中的预后价值,该数据库包含了1926名NSCLC患者的最新基因表达数据和生存信息。IL-22R1 mRNA的高表达与较差的总生存率相关(HR 1.4, 95% CI 1.2-1.6;p < 0.0001) (图1 d).调整了分期和组织型的多变量分析也证实了IL-22R1水平衍生预后信息的独立性(HR 1.5, 95% CI 1.2-1.9;p = 0.0011)。
总的来说,通过使用两个独立的数据集,我们的研究揭示了IL-22R1在NSCLC中的高表达是总生存率较差的独立指标,并支持IL-22/IL-22R通路在肺癌发展中的贡献。目前还需要进一步的研究来检验IL-22R是否能代表一种有吸引力的NSCLC治疗靶点。
脚注
支持声明:安托万·吉永是由Inserm“post d'accueil”资助的。该资助机构在研究设计、数据收集和分析、发表决定或手稿准备方面没有任何作用。没有其他支持源需要声明。
利益冲突:没有声明。
- 收到了2015年9月22日。
- 接受2015年12月15日。
- 版权所有©ERS 2016