文摘gydF4y2Ba
巢蛋白,一个著名的神经干细胞的标志物,最近建议描述干细胞的祖细胞在non-neuronal结构发展和组织修复。集成的小说形态方法(清晰),我们调查是否巢蛋白表达定义基本上驱动器血管重塑的增殖细胞群在肺动脉高压的发展。gydF4y2Ba
巢蛋白的作用研究的肺nestin-GFP(绿色荧光蛋白)小鼠模型的肺动脉高压(鼠:野百合碱,SU5416 /缺氧;鼠:缺氧),肺动脉高压患者的样本和人类肺血管平滑肌细胞(VSMCs)。gydF4y2Ba
巢蛋白仅发现增殖VSMCs肺脉管系统和局部的,但不是支气管平滑肌细胞。巢蛋白可以影响细胞的数量,显著提高肺早期在肺动脉高压的发展,关联与VSMC增殖,增加表达的磷酸化(激活)血小板源生长因子受体β的差别,对这些calponin平滑肌细胞分化标志。在以后当肺动脉高压临床明显,巢蛋白表达和增殖回到控制水平。增加nestin-positive VSMCs还发现在人类肺动脉高压,在媒体和neointima。gydF4y2Ba
巢蛋白表达似乎是专为VSMC增殖,并指定肺血管壁细胞驱动改造和(重新)生成。我们的数据保证新型诊断工具和肺动脉高压的治疗目标。gydF4y2Ba
文摘gydF4y2Ba
在肺癌、巢蛋白仅存在于血管平滑肌细胞在肺动脉高压和驱动重装gydF4y2Bahttp://ow.ly/StPCSgydF4y2Ba
介绍gydF4y2Ba
巢蛋白是一个类VI中间丝。它第一次被发现在神经干细胞(gydF4y2Ba1gydF4y2Ba),虽然在祖细胞巢蛋白表达被描述的其他器官在成人组织开发和维修期间,审查的WgydF4y2Baiese商学院gydF4y2Ba等gydF4y2Ba。(gydF4y2Ba2gydF4y2Ba]。Nestin-expressing细胞来自不同组织被分配特征类似于干细胞(gydF4y2Ba2gydF4y2Ba]。gydF4y2Ba
只有少数先前的研究局部血管壁细胞巢蛋白,包括血管平滑肌细胞(VSMCs)和周gydF4y2Ba3gydF4y2Ba- - - - - -gydF4y2Ba6gydF4y2Ba]。我们演示了巢蛋白gydF4y2Ba+gydF4y2BaVSMCs和周的祖细胞testosterone-producing睾丸间质细胞(gydF4y2Ba4gydF4y2Ba),而他们的克隆细胞自我更新和分化为神经和间充质细胞谱系是最近描述gydF4y2Ba7gydF4y2Ba]。gydF4y2Ba
描述了居民祖细胞在不同的细胞群的肺gydF4y2Ba8gydF4y2Ba,gydF4y2Ba9gydF4y2Ba),但研究表情,本地化和巢蛋白在肺功能,开发和维修期间,被我们和其他人(最近才开始gydF4y2Ba10gydF4y2Ba- - - - - -gydF4y2Ba12gydF4y2Ba]。成人肺、结构变化被发现在各种病理条件下,gydF4y2Ba如。gydF4y2Ba肺动脉高压,改造的脉管系统占了主导地位。在肺动脉高压、血管收缩、血栓形成和改造可以找到病理三合会的阻力血管的肺gydF4y2Ba13gydF4y2Ba]。在改造的过程中,重建与内皮细胞内膜的赘生物,VSMCs扩散和产生的血管闭塞的描述(gydF4y2Ba13gydF4y2Ba,gydF4y2Ba14gydF4y2Ba]。与此同时,有越来越多的证据表明,内皮细胞在低氧诱导肺动脉高压(不扩散gydF4y2Ba15gydF4y2Ba),但动脉外膜也参与了肺动脉高压的发展(gydF4y2Ba8gydF4y2Ba]。生长因子如血小板源生长因子(PDGF)及其受体(PDGFR)是必不可少的肺动脉高压的发展,中介VSMCs的增殖和迁移gydF4y2Ba16gydF4y2Ba]。然而,血管的增殖细胞群媒体尚未详细描述。特别是,没有数据显示血管的增殖细胞媒体是否代表nestin-expressing祖细胞。gydF4y2Ba
本研究调查的相关性巢蛋白表达与细胞增殖和血管重塑在肺动脉高压的发展。gydF4y2Ba
材料和方法gydF4y2Ba
动物和组织gydF4y2Ba
代nestin-GFP(绿色荧光蛋白)转基因小鼠,表达GFP的控制下巢蛋白基因启动子和转录增强器位于第二内含子的基因,是前面描述的(gydF4y2Ba17gydF4y2Ba]。gydF4y2Ba
缺氧性肺血管重塑的老鼠被暴露诱导C57BL / 6小鼠(查尔斯河实验室、Sulzfeld、德国;至少五个老鼠为每个时间点)慢性缺氧(normobaric;10%啊gydF4y2Ba2gydF4y2Ba)在一个通风室如前所述gydF4y2Ba18gydF4y2Ba]。gydF4y2Ba
诱导大鼠肺动脉高压,成年男性Sprague-Dawley老鼠(Charles River)皮下注射60 mg·公斤gydF4y2Ba−1gydF4y2Ba野百合碱(MCT);σ,德国慕尼黑)[gydF4y2Ba19gydF4y2Ba]。另外,老鼠皮下注射血管内皮生长因子受体2抑制剂SU5416 (20 mg·公斤gydF4y2Ba−1gydF4y2Ba)其次是暴露于慢性缺氧(normobaric;10%啊gydF4y2Ba2gydF4y2Ba5周。gydF4y2Ba
人类移植肺组织肺移植期间获得。供体肺样本来自肺部,没有被移植。gydF4y2Ba
免疫印迹分析、肺样本直接冻结。石蜡包埋,样本在Bouin固定剂固定。cryosections,肺直接冻结或者固定用4%多聚甲醛在室温和浸渍sucrose-PB为30%。gydF4y2Ba
所有地方当局批准的实验(Regierungsprasidium吉森;17 a-10c 20/15 (1) -Gi20/10-3/95和25.3 -19 c (1) -Gi20/10-20/99) 20/15。组织捐赠的研究方案是医学院伦理委员会的批准(李比希大学吉森,德国)根据国家法律和“协调好临床实践/国际会议”的指导方针。获得书面同意从每个病人或病人的近亲(AZ) 31/93。gydF4y2Ba
疣状gydF4y2Ba
免疫组织化学进行冷冻或石蜡包埋组织从老鼠,老鼠和人类和人类肺动脉平滑肌细胞(HPASMCs)有房间的幻灯片。微波后揭露(anti - ki - 67),部分与以下抗体:孵化单克隆鼠标anti-nestin(克隆R401;Chemicon、Schwalbach、德国;1:10 0,老鼠样品),鼠标anti-nestin (BD转导、海德堡、德国;1:50,鼠标样品),鼠标anti-nestin(圣克鲁斯、海德堡、德国;1:50,人类样本),兔子anti-calponin-1 (Epitomics,汉堡,德国;1:1000),鼠标anti-CD31 (BD Pharmingen、海德堡、德国;1:50 0)、鼠anti-CD31 (Dianova,汉堡,德国;1:10 0),兔子anti-von血友病因子(vWF)(美国微孔,Billerica的;1:10 0),鼠标anti-α-smooth肌肉肌动蛋白(SMA) (Serotec、牛津大学、英国; 1:500), mouse anti-proliferating cell nuclear antigen (PCNA) (Chemicon; 1:25) and polyclonal rabbit anti-Ki-67 (Novocastra, Wetzlar, Germany; 1:1000). For paraffin sections, an EnVision double-staining kit (DAKO, Hamburg, Germany) was used for primary antibody detection according to the manufacturer's instructions. For frozen sections and cultured cells, primary antibodies were detected by incubating the slides with secondary antibodies conjugated with Cy3 (Jackson ImmunoResearch, West Grove, PA, USA; 1:500), Alexa Fluor 488 (Molecular Probes, Eugene, OR, USA; 1:1000) or Alexa Fluor 594 (Molecular Probes; 1:1000). Cell nuclei of frozen sections were additionally stained with 4′,6-diamidino-2-phenyl-indole (DAPI) (Sigma).
清晰gydF4y2Ba
描述的清晰过程在线补充材料。gydF4y2Ba
小干扰RNA转染和评估gydF4y2Ba
HPASMCs瞬变与巢蛋白转染小干扰RNA (siRNA) (sc - 36032;圣克鲁斯)使用Lipofectamine RNAiMAX转染试剂(表达载体,卡尔斯鲁厄,德国)。细节给出了核和细胞计数程序在网上补充材料。gydF4y2Ba
蛋白质制备和免疫印迹gydF4y2Ba
制备膜和胞质蛋白从肺组织和HPASMCs,减少条件下通过sds - page分离,蛋白质硝基转移膜进行如前所述[gydF4y2Ba4gydF4y2Ba]。染色后膜与朱红色年代(σ)和阻塞非特异性结合位点,屁股被暴露于主要抗体:单克隆鼠标anti-nestin (Chemicon;1:1000),鼠标anti-nestin (BD转导;1:1000),鼠标anti-nestin(圣克鲁斯;1:200),鼠标anti-vinculin(σ;1:30 000),鼠标anti-β-actin(σ;1:20 000),鼠标anti-SMA(σ;1:5000)、多克隆兔anti-PDGFR-β(北部、Schwalbach、德国;1:50 0),兔子anti-phospho-PDGFR-β(p-PDGFR-β)(圣克鲁斯;摘要),兔子anti-poly (ADP-ribose)聚合酶1 (PARP1)和兔anti-cleaved PARP(细胞信号技术,法兰克福,德国; 1:1000). After washing, the membranes were probed with peroxidase-conjugated goat anti-rabbit IgG or goat anti-mouse IgG (Pierce, Rockford, IL, USA; 1:2000). Immunoreactive bands were visualised by enhanced chemiluminescence [4gydF4y2Ba]。光密度量化进行了使用ImageJ软件(NIH,贝塞斯达,医学博士,美国)。gydF4y2Ba
统计分析gydF4y2Ba
执行统计分析使用棱镜4 (GraphPad、圣地亚哥、钙、美国)。所有数据都意味着±gydF4y2Ba扫描电镜gydF4y2Ba。建立了统计学意义,p < 0.05,使用未配对t检验与韦尔奇的修正。gydF4y2Ba
结果gydF4y2Ba
巢蛋白在肺血管gydF4y2Ba
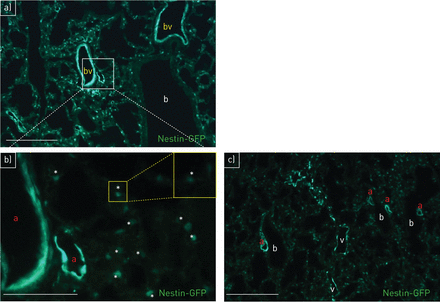
Nestin-GFP转基因小鼠进行了本地化的中间丝巢蛋白在肺。不同的观察和独家nestin-GFP表达血管(gydF4y2Ba图1gydF4y2Ba和在线补充视频使用新的清晰的方法)。Nestin-GFPgydF4y2Ba+gydF4y2Ba细胞被发现在动脉,毛细血管和静脉(gydF4y2Ba图1 bgydF4y2Ba和gydF4y2BacgydF4y2Ba)。相比之下,缺乏nestin-GFP呼吸道系统gydF4y2Ba+gydF4y2Ba细胞(gydF4y2Ba图1一个gydF4y2Ba和gydF4y2BacgydF4y2Ba和在线补充视频;另请参阅gydF4y2Ba图2我gydF4y2Ba- - - - - -gydF4y2BakgydF4y2Ba)。gydF4y2Ba
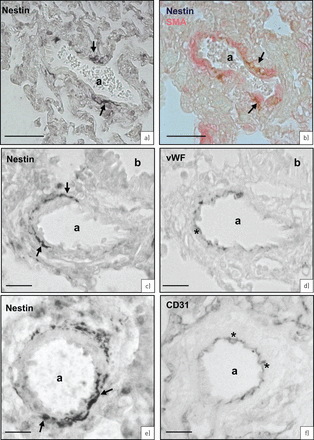
本地化的nestin-GFP(绿色荧光蛋白)在肺血管。一)Nestin-GFPgydF4y2Ba+gydF4y2Ba细胞中检测到肺血管(bv);bronchioli nestin-GFP (b)gydF4y2Ba−gydF4y2Ba;第一天。b)(细节面板在较高放大)Nestin-GFPgydF4y2Ba+gydF4y2Ba细胞在动脉(a)和毛细血管(星号标志着腔);第一天。c) Nestin-GFPgydF4y2Ba+gydF4y2Ba细胞在动脉(a)和静脉(v);bronchioli nestin-GFP (b)gydF4y2Ba−gydF4y2Ba;第一天。规模的酒吧:a、c) 100μm;50μm b)。gydF4y2Ba
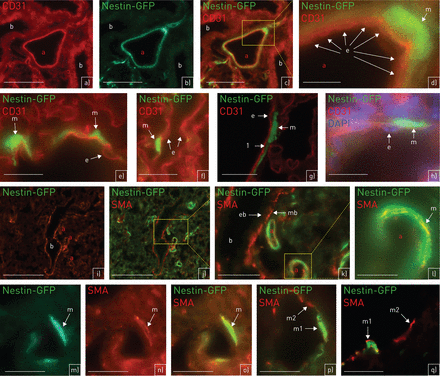
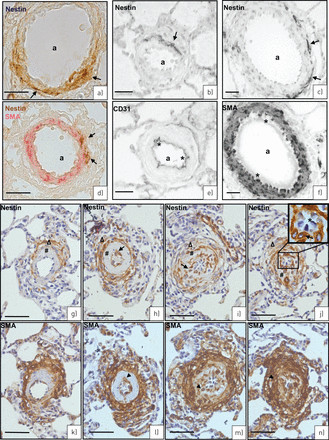
Nestin-GFP(绿色荧光蛋白)与平滑肌细胞标记co-localised平滑肌肌动蛋白(SMA),而不是与内皮细胞CD31标志。a) Nestin-GFP(绿色)和CD31(红色)(模拟h:第一天;例如:成人)。模拟)动脉(a): nestin-GFP不是co-localised CD31。Bronchioli nestin-GFP (b)gydF4y2Ba−gydF4y2Ba(答:CD31;b: nestin-GFP;c:合并)。d)(细节面板c在较高放大)nestin-GFPgydF4y2Ba+gydF4y2Ba血管平滑肌细胞(VSMC) (m)是CD31的外面gydF4y2Ba+gydF4y2Ba内皮细胞(e), e, f)单一nestin-GFPgydF4y2Ba+gydF4y2BaVSMCs (m)。他们不是co-localised CD31gydF4y2Ba+gydF4y2Ba内皮细胞(e), g)(共焦显微镜)明确分离CD31之间(“1”标签)gydF4y2Ba+gydF4y2Ba内皮细胞层(e)和nestin-GFPgydF4y2Ba+gydF4y2Ba层VSMCs (m)。与4′h)额外的染色,6-diamidino-2-phenyl-indole (DAPI);从CD31 DAPI清楚地揭示了原子核gydF4y2Ba+gydF4y2Ba内皮细胞(e)。m: nestin-GFPgydF4y2Ba+gydF4y2BaVSMC。我)Nestin-GFP(绿色)和SMA(红色)(投入:第一天;p, q:成人)。Nestin-GFP i, j)gydF4y2Ba+gydF4y2Ba/ SMAgydF4y2Ba+gydF4y2Banestin-GFP动脉(一)相邻gydF4y2Ba−gydF4y2Ba/ SMAgydF4y2Ba+gydF4y2Babronchiolus (b)(我:SMA;j: SMA和nestin-GFP)。k)(细节面板j在较高放大)Nestin-GFPgydF4y2Ba+gydF4y2Ba/ SMAgydF4y2Ba+gydF4y2BaVSMCs动脉(一个);平滑肌细胞的bronchioli SMA (mb)gydF4y2Ba+gydF4y2Ba/ nestin-GFPgydF4y2Ba−gydF4y2Ba。bronchioli上皮(eb) SMAgydF4y2Ba−gydF4y2Ba。l)(动脉的细节面板k在较高放大)Nestin-GFPgydF4y2Ba+gydF4y2Ba/ SMAgydF4y2Ba+gydF4y2BaVSMCs (m)的动脉(a)。m-o) (m: nestin-GFP;n: SMA;o: Nestin-GFP合并)gydF4y2Ba+gydF4y2Ba/ SMAgydF4y2Ba+gydF4y2BaVSMC (m)。SMA存在于细胞质(n:红色),Nestin-GFP位于细胞质(o:黄色)和原子核(o:绿色)。p, q)只有一个族群的VSMCs nestin-GFPgydF4y2Ba+gydF4y2Ba。Nestin-GFPgydF4y2Ba+gydF4y2Ba/ SMAgydF4y2Ba+gydF4y2BaVSMCs (m1);nestin-GFPgydF4y2Ba−gydF4y2Ba/ SMAgydF4y2Ba+gydF4y2BaVSMCs (m2)(问:共焦显微镜)。规模的酒吧:a - c) 75μm;d, m, n, o) 15μm;例如,q) 20μm;h、l p) 25μm;i, j) 100μm;μm 50 k)。gydF4y2Ba
巢蛋白是VSMCs本地化gydF4y2Ba
在这里,我们专注于巢蛋白表达在肺的动脉。探讨细胞表达巢蛋白,我们使用了内皮平滑肌细胞特异性标记SMA CD31和标志。Nestin-GFPgydF4y2Ba+gydF4y2Ba细胞CD31可以清楚地区别开来gydF4y2Ba+gydF4y2Ba细胞(gydF4y2Ba图2一个gydF4y2Ba- - - - - -gydF4y2BahgydF4y2Ba),而co-localisation nestin-GFP和观察SMA (gydF4y2Ba图2我gydF4y2Ba- - - - - -gydF4y2Ba问gydF4y2Ba)。平滑肌细胞的bronchioli还显示SMA染色,但没有nestin-GFP信号(gydF4y2Ba图2我gydF4y2Ba- - - - - -gydF4y2BakgydF4y2Ba)。GFP染色,观察到细胞质和细胞核如前所述[gydF4y2Ba17gydF4y2Ba)(见gydF4y2Ba图2 lgydF4y2Ba- - - - - -gydF4y2BaogydF4y2Ba),是可见的只有在SMA的族群gydF4y2Ba+gydF4y2Ba细胞(gydF4y2Ba图2 pgydF4y2Ba- - - - - -gydF4y2Ba问gydF4y2Ba)。gydF4y2Ba
巢蛋白表达和细胞增殖肺动脉高压的动物模型gydF4y2Ba
我们调查潜在的巢蛋白表达的变化在不同的肺动脉高压模型的特点是肺的结构变化与高细胞增殖有关。gydF4y2Ba
缺氧小鼠模型gydF4y2Ba
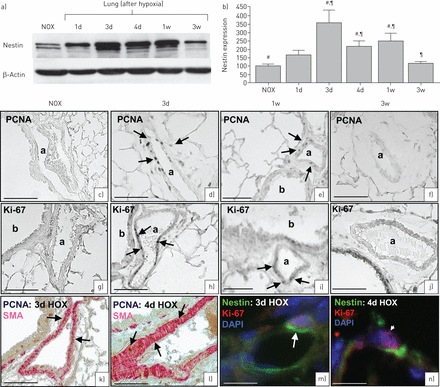
细胞增殖(ki - 67和PCNA)和时间的巢蛋白表达进行了缺氧小鼠模型(gydF4y2Ba图3gydF4y2Ba)。巢蛋白表达显著增加肺的hypoxia-exposed动物3天到1周,但3周后回到常氧水平(gydF4y2Ba图3一gydF4y2Ba和gydF4y2BabgydF4y2Ba)。在这个模型中,血管重塑是组织学检查可见在之后的时间点和肺动脉高压临床明显不同的天巢蛋白峰值。SMA的表达,然而,几乎不同在单个时间点(在线补充图S1)。gydF4y2Ba
缺氧小鼠模型。巢蛋白表达和细胞增殖在野生型小鼠缺氧(HOX)。一)免疫印迹演示缺氧后巢蛋白表达增加;巢蛋白表达的最大是3天到1周后缺氧其次是减少表达式3周后(120μg胞质蛋白)。巢蛋白的b)光密度定量。酒吧展示意味着±gydF4y2Ba扫描电镜gydF4y2Ba从三个评估得分与β-actin加载控制。gydF4y2Ba#,¶gydF4y2Bap < 0.01 (gydF4y2Ba#gydF4y2Ba:normoxia (NOX)与3天,4天,1周;gydF4y2Ba¶gydF4y2Ba:3周与3天,4天,1周)。氟)增殖细胞核抗原(PCNA)免疫染色。c) Normoxia:没有PCNA-marked细胞。d, e) 3天缺氧(d)和1周缺氧(e):许多PCNA-marked血管平滑肌细胞(VSMCs)。f) 3周缺氧:没有PCNA-marked细胞。g-j) ki - 67免疫染色。g) Normoxia:没有ki - 67标记细胞。h i) 3天缺氧(h)和1周缺氧(我):许多ki - 67 VSMCs标记。j) 3周缺氧:没有ki - 67标记细胞。k, l) 3天(k)和4天(l)缺氧:PCNA(布朗)局部平滑肌肌动蛋白(SMA)gydF4y2Ba+gydF4y2BaVSMCs(红色)。m, n) 3天(m)和4天(n)缺氧:扩散标记ki - 67(红色箭头)是co-localised巢蛋白(绿色箭头)位于相同的单元中。核染色4′,6-diamidino-2-phenyl-indole (DAPI)(蓝色)。1 d: 1天;3 d: 3天;4 d: 4天;w: 1周;3 w: 3周。规模的酒吧:a、g、k - n) 75μm;75μm d-f h-j)。gydF4y2Ba
PCNA的数量增加gydF4y2Ba+gydF4y2Ba和ki - 67gydF4y2Ba+gydF4y2BaVSMCs 3天到1周后检测缺氧治疗(gydF4y2Ba图3 cgydF4y2Ba和gydF4y2BangydF4y2Ba)。3周后,细胞核抗原gydF4y2Ba+gydF4y2Ba和ki - 67gydF4y2Ba+gydF4y2BaVSMCs不能观察到(gydF4y2Ba图3 fgydF4y2Ba和gydF4y2BajgydF4y2Ba),对应于低巢蛋白表达。gydF4y2Ba
缺氧的双重染色样品与SMA和PCNA表明,SMAgydF4y2Ba+gydF4y2Ba细胞是主要的细胞群中显示增殖诱导血管重塑是(gydF4y2Ba图3 kgydF4y2Ba- - - - - -gydF4y2BalgydF4y2Ba)。巢蛋白被发现在增殖VSMCs证明了co-localisation巢蛋白和ki - 67 (gydF4y2Ba图3米gydF4y2Ba- - - - - -gydF4y2BangydF4y2Ba)。gydF4y2Ba
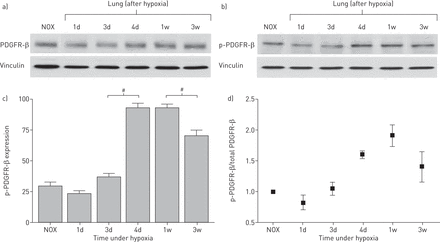
此外,免疫印迹分析(磷酸化)PDGFR-β激活的时间进程,这是众所周知的,导致肺动脉高压的发展,也显示是暂时性升高表达缺氧4 - 7天(gydF4y2Ba图4 bgydF4y2Ba- - - - - -gydF4y2BadgydF4y2Ba),而总PDGFR-β稍微增加的表达与进步肺动脉高压(gydF4y2Ba图4一gydF4y2Ba)。gydF4y2Ba
血小板源生长因子受体β(PDGFR-β)表达在缺氧小鼠肺样本。a) PDGFR-β免疫印迹显示仅稍有增加PDGFR-β表达在低氧暴露对3周(30μg膜蛋白)。b)磷(p) -PDGFR-β免疫印迹显示激活的峰值(磷酸化)PDGFR-β4天后缺氧(30μg膜蛋白)。c)的光密度量化p-PDGFR-β表达式。酒吧展示意味着±gydF4y2Ba扫描电镜gydF4y2Ba分数从三个评估。gydF4y2Ba#gydF4y2Ba:p < 0.01表示显著差异p-PDGFR-β表达式3至4天,以及1 - 3周。Vinculin作为加载控制。d) PDGFR-β活动表示为p-PDGFR-β/ PDGFR-β比率。氮氧化物:normoxia;1 d: 1天;3 d: 3天;4 d: 4天;w: 1周;3 w: 3周。gydF4y2Ba
在协议与缺氧模型,肺血管的重塑在产后快速发展也以高巢蛋白表达和大量的增殖细胞核抗原gydF4y2Ba+gydF4y2Ba)VSMCs(在线补充图S2),产后3和10天之间的峰值和下降到成年。有趣的是,平滑肌细胞分化标志calponin(几乎完全表达的支气管平滑肌细胞;数据未显示)表明一个逆相关,巢蛋白(在线补充图S2),而表达的平滑肌细胞标记SMA(表达的平滑肌细胞;数据未显示)保持不变。同样被发现在VSMCs缺氧性肺动脉高压模型(数据未显示)。gydF4y2Ba
巢蛋白表达在大鼠肺动脉高压模型gydF4y2Ba
调查是否巢蛋白gydF4y2Ba+gydF4y2Ba/ SMAgydF4y2Ba+gydF4y2Ba细胞也参与了大鼠的血管重塑,巢蛋白表达在MCT-treated评估(gydF4y2Ba图5gydF4y2Ba)和SU5416 / hypoxia-treated (gydF4y2Ba图6克ydF4y2Ba)大鼠肺。gydF4y2Ba
鼠野百合碱(MCT)模型。巢蛋白免疫染色MCT鼠肺3周后治疗。)单一巢蛋白gydF4y2Ba+gydF4y2Ba血管平滑肌细胞(VSMCs)(箭头)的动脉(a)。b)巢蛋白(棕色、箭头)是本地化的分组人口平滑肌肌动蛋白(SMA)gydF4y2Ba+gydF4y2Ba细胞(红色)。c, d)串行部分的巢蛋白(c:箭头)和血管性血友病因子(vWF) (d:星号)免疫染色。Bronchioli (b)。e, f)串行部分的巢蛋白(e:箭头)和CD31免疫染色(f:星号)。规模的酒吧:a、b) 50μm;25μm氟)。gydF4y2Ba
SU5416 /缺氧大鼠肺动脉高压模型。巢蛋白染色(棕色、箭头)在动脉壁(a)。b)双重染色,巢蛋白(棕色、箭头)的分组人口平滑肌肌动蛋白(SMA)gydF4y2Ba+gydF4y2Ba血管平滑肌细胞(VSMCs)(红色)。c, d)串行部分的巢蛋白(c:箭头)和CD31免疫染色(d:星号)。e、f)串行部分的巢蛋白(e:箭头)和SMA (f: SMA星号标记gydF4y2Ba- - - - - -gydF4y2Ba内皮细胞免疫染色。()neointima发展的不同等级。串行部分染色为巢蛋白(g, k, m:箭头)和SMA (h, j, l, n:箭头)在(neo)内膜(#)和媒体(Δ)的动脉(60 - 80µm)单一阶段(g和h、i和j、k和l, m和n),注意巢蛋白的减少gydF4y2Ba+gydF4y2Ba/ SMAgydF4y2Ba+gydF4y2Ba细胞在媒体与他们(neo)增加内膜从g / h m / n。内皮细胞在面板m是标有星号的插图。规模的酒吧:a、b() 50μm;c, d) 25μm;10μm e、f)。gydF4y2Ba
MCT老鼠模型gydF4y2Ba
免疫组织化学分析显示巢蛋白gydF4y2Ba+gydF4y2Ba细胞特定治疗后3周(gydF4y2Ba图5一个gydF4y2Ba)。如图所示,双染色,观察co-localisation巢蛋白和SMA VSMCs (gydF4y2Ba图5 bgydF4y2Ba)。染色的串行部分巢蛋白和vWF内皮细胞标记(gydF4y2Ba图5 cgydF4y2Ba和gydF4y2BadgydF4y2Ba)和CD31 (gydF4y2Ba图5 egydF4y2Ba和gydF4y2BafgydF4y2Ba),然而,可以排除巢蛋白表达于内皮细胞。gydF4y2Ba
MCT-treated样品中,巢蛋白upregulation只是观察肺动脉。然而在主动脉,没有区别在MCT-treated巢蛋白表达检测和控制/未经处理的动物(在线补充图S3)。我们因此建议巢蛋白表达的改变其特定治疗后特定肺循环,反映其特定代谢的特点(gydF4y2Ba20.gydF4y2Ba]。gydF4y2Ba
SU5416 /缺氧大鼠模型gydF4y2Ba
同样,在肺SU5416 /缺氧模型,巢蛋白表达VSMCs动脉媒体可以通过双染色证实与SMA (gydF4y2Ba图6gydF4y2Ba和gydF4y2BabgydF4y2Ba)以及由串行部分巢蛋白和CD31染色(gydF4y2Ba图6 cgydF4y2Ba和gydF4y2BadgydF4y2Ba)和SMA (gydF4y2Ba图6 egydF4y2Ba和gydF4y2BafgydF4y2Ba)。gydF4y2Ba
在某些动脉(∼60 - 80µm直径)的老鼠从这个模型,也以独特的neointima形成(gydF4y2Ba21gydF4y2Ba),增厚内膜不同的表型可以观察到。在所有这些动脉,巢蛋白表达了SMA的族群gydF4y2Ba+gydF4y2Ba细胞的媒体,最有趣的是,同样在SMAgydF4y2Ba+gydF4y2Ba内膜的细胞(gydF4y2Ba图6克gydF4y2Ba与gydF4y2BahgydF4y2Ba,gydF4y2Ba我gydF4y2Ba与gydF4y2BajgydF4y2Ba,gydF4y2BakgydF4y2Ba与gydF4y2BalgydF4y2Ba和gydF4y2Ba米gydF4y2Ba与gydF4y2BangydF4y2Ba)。当不同的动脉内膜增厚,关联不同等级的新生内膜发展(gydF4y2Ba21gydF4y2Ba),比较,巢蛋白的减少gydF4y2Ba+gydF4y2Ba/ SMAgydF4y2Ba+gydF4y2Ba细胞内的一部分媒体一起增加巢蛋白gydF4y2Ba+gydF4y2Ba/ SMAgydF4y2Ba+gydF4y2Ba(neo)细胞内膜变得明显在开发过程中(gydF4y2Ba图6克gydF4y2Ba- - - - - -gydF4y2BangydF4y2Ba)。内皮细胞的血管形成复杂neointima也没有显示巢蛋白免疫染色(gydF4y2Ba图6 kgydF4y2Ba和gydF4y2Ba米gydF4y2Ba插图)。gydF4y2Ba
巢蛋白表达和功能在人类样本gydF4y2Ba
接下来,我们研究人类巢蛋白的作用。gydF4y2Ba
人类从肺动脉高压患者的样本gydF4y2Ba
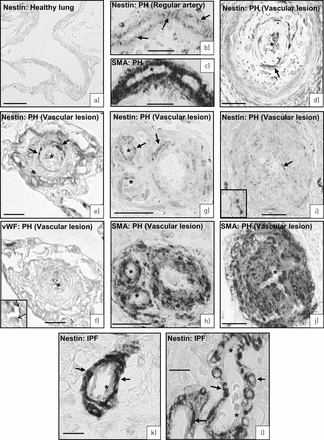
在健康对照组(gydF4y2Ba图7gydF4y2Ba),巢蛋白gydF4y2Ba+gydF4y2Ba难以觉察的细胞。然而,在人类肺动脉高压,巢蛋白的数量增加gydF4y2Ba+gydF4y2Ba细胞被发现在媒体上定期肺部动脉(gydF4y2Ba图7 bgydF4y2Ba)以及在特定的血管病变也有被描述特征为人类肺动脉高压(gydF4y2Ba22gydF4y2Ba)(gydF4y2Ba图7 dgydF4y2Ba,gydF4y2BaegydF4y2Ba,gydF4y2BaggydF4y2Ba和gydF4y2Ba我gydF4y2Ba)。与动物模型一致,巢蛋白表达可以归因于平滑肌细胞的染色串行部分的巢蛋白和SMA (gydF4y2Ba图7 bgydF4y2Ba和gydF4y2BacgydF4y2Ba,gydF4y2BaggydF4y2Ba和gydF4y2BahgydF4y2Ba,gydF4y2Ba我gydF4y2Ba和gydF4y2BajgydF4y2Ba巢蛋白和vWF)或(gydF4y2Ba图7 egydF4y2Ba和gydF4y2BafgydF4y2Ba)。一般来说,巢蛋白的数量gydF4y2Ba+gydF4y2BaVSMCs较低的血管病变已经明显。相比较而言,样本与特发性肺纤维化(IPF)进行调查和有趣的是也表现出巢蛋白gydF4y2Ba+gydF4y2BaVSMCs动脉媒体(gydF4y2Ba图7 kgydF4y2Ba和gydF4y2BalgydF4y2Ba)。gydF4y2Ba
人类的肺。健康的肺。没有nestin-expressing细胞。b-j)肺动脉高压(PH)肺。b, c)串行部分的常规动脉彩色巢蛋白(箭头)和平滑肌肌动蛋白(SMA c:星号标记gydF4y2Ba- - - - - -gydF4y2Ba内皮细胞)。巢蛋白d)与复杂病变动脉彩色(箭头)。e-j)串行部分的三个不同的复杂病变动脉彩色巢蛋白(e:箭头)和血管性血友病因子(vWF) (f,插图:箭头)以及巢蛋白(g,我:箭头)和SMA (h, j:星号标记SMA negative-endothelial细胞)。k-l)特发性肺纤维化(IPF)的肺。巢蛋白免疫反应性动脉平滑肌细胞(箭头)的媒体。星号标记缺乏内皮细胞巢蛋白染色。规模的酒吧:模拟,g-j) 50μm;e、f、k, l) 10μm。gydF4y2Ba
人类孤立肺VSMCsgydF4y2Ba
解决巢蛋白功能,我们采用基因消融方法使用巢蛋白核孤立HPASMCs和显示细胞数量减少与巢蛋白降低(在线补充图S4)。在这种情况下,没有证据表明,增强细胞凋亡(在线补充图S4)。巢蛋白siRNA-treated HPASMCs没有显示表达的细胞凋亡标记裂解PARP(半胱天冬酶裂解产生的),这是不同的长篇PARP酶。Staurosporine-treated海拉细胞作为一个积极的控制在这些免疫印迹分析。gydF4y2Ba
在协议,未经处理的HPASMCs显示双染色巢蛋白和增殖标记ki - 67(在线补充图S4)。只有少数细胞的分化表型未能表达巢蛋白,而分化的平滑肌细胞的阳性标记,如calponin [gydF4y2Ba23gydF4y2Ba,gydF4y2Ba24gydF4y2Ba)(在线补充图S4)。gydF4y2Ba
讨论gydF4y2Ba
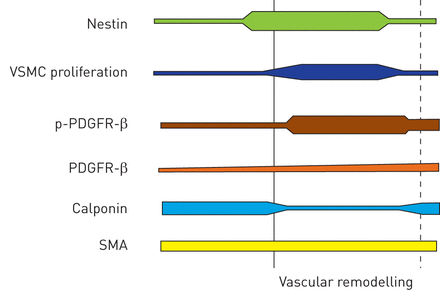
我们能够确定中间丝巢蛋白,已知描述祖细胞在神经系统中,在一个族群的VSMCs参与血管重塑在肺动脉高压的发展。总结不同的数据模型和人类肺动脉高压的样本,我们建议增加巢蛋白表达是第一个证据的脉管系统的变化,立即巢蛋白扩散紧随其后gydF4y2Ba+gydF4y2Ba/ SMAgydF4y2Ba+gydF4y2Ba细胞,激活PDGFR-β[gydF4y2Ba16gydF4y2Ba,gydF4y2Ba19gydF4y2Ba途径和减少calponin,而SMA表达(几乎保持不变gydF4y2Ba图8gydF4y2Ba)。gydF4y2Ba
示意图展示颞血管重塑的变化在肺动脉高压的发展。巢蛋白出现结构性变化的第一指标与血管平滑肌细胞(VSMC)增殖祖细胞随后激活血小板源生长因子受体β(PDGFR-β)(磷(p) -PDGFR-β)和calponin的减少。平滑肌肌动蛋白(SMA)表达式保持不变。虚线显示临床上肺动脉高压。gydF4y2Ba
使用不同的方法,包括小说清晰(gydF4y2Ba25gydF4y2Ba)方法,巢蛋白表达在VSMCs只发现,从来没有在(para)发现支气管平滑肌细胞或其他增殖细胞类型的肺癌、支气管上皮细胞等。因此我们建议巢蛋白既不是一个简单的肺细胞的增殖标记也不是一个简单的标志肺平滑肌细胞。相反,巢蛋白标志专门VSMCs在扩散,这是一种罕见的事件在生理条件下(gydF4y2Ba26gydF4y2Ba),但期间引起血管重塑gydF4y2Ba27gydF4y2Ba,gydF4y2Ba28gydF4y2Ba]。在几乎所有以前的文件处理nestin-expressing细胞巢蛋白标志着祖或干细胞gydF4y2Ba1gydF4y2Ba,gydF4y2Ba2gydF4y2Ba]。因此,可以认为巢蛋白gydF4y2Ba+gydF4y2Ba细胞肺癌也标签的一种特殊类型的细胞。目前,我们不能决定是否巢蛋白gydF4y2Ba+gydF4y2Ba细胞代表真正的干细胞/祖细胞的血管媒体或马克VSMCs合成表型。gydF4y2Ba
在后一种情况下,我们的研究结果将提供令人信服的证据为一个特定的和功能相关的标记蛋白质合成VSMCs,允许他们从所有其他歧视平滑肌细胞。VSMCs被认为de-differentiate和改变他们的表型从收缩在一定条件下合成gydF4y2Ba27gydF4y2Ba),包括血管重塑(gydF4y2Ba26gydF4y2Ba,gydF4y2Ba27gydF4y2Ba]。在这项研究中,表达式calponin标记有区别的平滑肌细胞(gydF4y2Ba23gydF4y2Ba,gydF4y2Ba24gydF4y2Ba),在更一般的收缩标记SMA相比,负相关VSMCs巢蛋白表达和增殖。同样,巢蛋白表达在孤立肺VSMCs (HPASMCs)被发现在增殖ki - 67gydF4y2Ba+gydF4y2Ba细胞,但是不在calponingydF4y2Ba+gydF4y2Ba细胞。gydF4y2Ba
假设巢蛋白gydF4y2Ba+gydF4y2Ba细胞确实代表干细胞/祖细胞在肺,我们的数据认为挑衅的理论,只有一定数量的血管平滑肌(干)细胞能够增殖血管媒体(gydF4y2Ba27gydF4y2Ba]。我们之前的结果在睾丸gydF4y2Ba4gydF4y2Ba)也显示出巢蛋白gydF4y2Ba+gydF4y2Ba祖细胞在血管壁驻留。gydF4y2Ba
3周后缺氧,有趣的是,当完整的组织学特征和不同的临床症状,表达巢蛋白和增殖再次回到低水平。PgydF4y2BaaddenberggydF4y2Baet al。gydF4y2Ba(gydF4y2Ba29日gydF4y2Ba)提出,细胞增殖在第一周后跟VSMCs肥大。现在我们的研究使我们能够识别增殖SMA的族群gydF4y2Ba+gydF4y2Ba细胞的表达巢蛋白,可以视为一个初始指标结构血管的变化。gydF4y2Ba
在肺动脉高压模型,我们能够证明巢蛋白gydF4y2Ba+gydF4y2Ba/ SMAgydF4y2Ba+gydF4y2Ba细胞在动脉媒体。SU5416 /缺氧模型可以区分血管病变特点,包括形成neointima [gydF4y2Ba21gydF4y2Ba]。Neointima形成血管细胞的增殖和迁移的结果向腔,和平滑肌细胞被认为是这一过程的主要贡献者(gydF4y2Ba14gydF4y2Ba,gydF4y2Ba26gydF4y2Ba,gydF4y2Ba30.gydF4y2Ba,gydF4y2Ba31日gydF4y2Ba]。在我们的研究中,我们发现neointima SMAgydF4y2Ba+gydF4y2Ba肺血管的细胞也表达巢蛋白与balloon-injured颈动脉(gydF4y2Ba6gydF4y2Ba]。neointima病变的类型我们发现SU5416 /缺氧模型对应不同等级的新生内膜病变发生一段时间后,如前所述[gydF4y2Ba21gydF4y2Ba]。因此,巢蛋白gydF4y2Ba+gydF4y2Ba/ SMAgydF4y2Ba+gydF4y2Ba细胞可能是特定的内膜细胞迁移和增殖。gydF4y2Ba
人类肺部终末期肺动脉高压的特点是复杂的血管病变(gydF4y2Ba22gydF4y2Ba),还包括血管形态变化尚未可见。巢蛋白VSMCs也表达了两种类型的船舶。在常规血管,巢蛋白表达可以发现在绝大多数VSMCs,而血管病变的特点是只有几个分散的巢蛋白gydF4y2Ba+gydF4y2BaVSMCs。这个特征关系表明巢蛋白的参与gydF4y2Ba+gydF4y2Ba/ SMAgydF4y2Ba+gydF4y2Ba细胞在血管病变的人类肺动脉高压的形成,在积累“SM-like细胞”是描述gydF4y2Ba9gydF4y2Ba]。gydF4y2Ba
Nestin-ablated HPASMCs没有显示细胞数量的增加而控制细胞凋亡的没有证据。这些发现支持功能协会巢蛋白表达与调控的细胞数量,在先前的研究也被唤起,巢蛋白降低,核被证明有效地抑制C6星形细胞瘤细胞的生长(gydF4y2Ba32gydF4y2Ba]。此外,微gydF4y2Bamir - 125 bgydF4y2Ba最近发现神经祖细胞增殖抑制目标巢蛋白(gydF4y2Ba33gydF4y2Ba]。巢蛋白的分子作用仍不明确,但巢蛋白的磷酸化和去磷酸化可能调节细胞骨架组装和营业额gydF4y2Ba34gydF4y2Ba),可能扮演重要的角色在增加细胞质贩卖干/祖细胞发生增殖,迁移和分化gydF4y2Ba1gydF4y2Ba,gydF4y2Ba35gydF4y2Ba,gydF4y2Ba36gydF4y2Ba]。关于巢蛋白的功能,然而,它被认为巢蛋白基因敲除小鼠似乎是可行的(gydF4y2Ba37gydF4y2Ba]。gydF4y2Ba
在目前的研究中,以及在我们先前的研究在睾丸gydF4y2Ba4gydF4y2Ba),我们发现巢蛋白不仅在VSMCs,而且在周毛细血管,与最近的报告(gydF4y2Ba12gydF4y2Ba,gydF4y2Ba38gydF4y2Ba]。周,除了其他功能(gydF4y2Ba39gydF4y2Ba),已被证明代表干细胞/祖细胞脂肪细胞等细胞类型,内层,成骨细胞、骨骼肌纤维、睾丸间质细胞和神经细胞(gydF4y2Ba4gydF4y2Ba,gydF4y2Ba5gydF4y2Ba,gydF4y2Ba39gydF4y2Ba]。睾丸间质细胞祖细胞被发现不仅巢蛋白gydF4y2Ba+gydF4y2Ba周,还巢蛋白gydF4y2Ba+gydF4y2BaVSMCs [gydF4y2Ba4gydF4y2Ba]。巢蛋白是否gydF4y2Ba+gydF4y2BaVSMCs肺也表示没有血管的细胞的祖细胞仍然是投机,但最近讨论了内皮的密集剥蚀颈动脉损伤(gydF4y2Ba27gydF4y2Ba,gydF4y2Ba40gydF4y2Ba]。有趣的是,组织慢性血栓栓塞肺动脉高压患者描述包含祖细胞能产生脂肪细胞和接受成骨分化(gydF4y2Ba9gydF4y2Ba]。gydF4y2Ba
TgydF4y2Ba盎gydF4y2Ba等gydF4y2Ba。(gydF4y2Ba40gydF4y2Ba)测试巢蛋白表达在几天后他们提出的VSMC祖细胞在细胞培养。作者解释巢蛋白表达的发展一步细胞神经血统。巢蛋白表达在细胞之前或之后立即隔离,然而,并不是调查。我们建议,巢蛋白表达并不意味着神经分化,但代表一个特定的祖细胞/ VSMCs涉及扩散的特征。gydF4y2Ba
内皮细胞巢蛋白gydF4y2Ba−gydF4y2Ba并没有表现出任何扩散在肺血管重塑。这一发现与先前的数据是一致的,内皮细胞并没有显示增殖与低氧诱导小鼠和大鼠肺动脉高压gydF4y2Ba在活的有机体内gydF4y2Ba下,也在人类肺动脉内皮细胞缺氧gydF4y2Ba在体外gydF4y2Ba(gydF4y2Ba15gydF4y2Ba]。然而,一系列的相关研究也表明内皮祖细胞(gydF4y2Ba9gydF4y2Ba]。gydF4y2Ba
有趣的是,在人体组织中,我们发现高巢蛋白表达在动脉媒体除了肺动脉高压也IPF的肺。肺纤维化患者纤维化与血管相关变更事项也可能发展成严重肺动脉高压(gydF4y2Ba41gydF4y2Ba]。这些巢蛋白gydF4y2Ba+gydF4y2Ba细胞可能导致纤维化的过程作为myofibroblasts来源,在协议与其他研究gydF4y2Ba11gydF4y2Ba]。gydF4y2Ba
在这里,我们描述巢蛋白的功能相关的标记未分化细胞促进组织再生和修复。在肿瘤学,巢蛋白被描述为对生存预后标记,允许个性化治疗方案的发展(gydF4y2Ba42gydF4y2Ba,gydF4y2Ba43gydF4y2Ba]。在我们的缺氧模型,巢蛋白表达早于临床和组织学的症状出现在肺动脉高压的进展。因此,某些血管细胞可以被巢蛋白与增殖,并可作为预后标记和新的治疗靶点毁灭性的疾病,如肺动脉高压。gydF4y2Ba
确认gydF4y2Ba
我们感谢Sabine Tasch, Ingrid Schneider-Huther家Lubberstedt,卡琳Quanz和英格丽Breitenborn-Muller为技术支持,并加芙Krasteva-Christ寻求帮助在我们的共焦显微镜研究的开始。gydF4y2Ba
脚注gydF4y2Ba
可以从本文的补充材料gydF4y2Bawww.qdcxjkg.comgydF4y2Ba
支持声明:脱硫,卓越集群做心肺系统,卢安克的黑森州,BMBF,德国肺中心;吉森大学医学中心和马尔堡(UKGM,格兰特研究);NIMH, NIA R01AG040209 NYSTEM C029569,俄罗斯联邦教育部和科学11 g34.31.0071。为这篇文章一直存放在资助信息gydF4y2BaFundRefgydF4y2Ba。gydF4y2Ba
利益冲突:没有宣布。gydF4y2Ba
- 收到了gydF4y2Ba2015年4月11日。gydF4y2Ba
- 接受gydF4y2Ba2015年9月17日。gydF4y2Ba
- 版权©2016人队gydF4y2Ba
引用gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba