抽象的
维生素D在防御病原体中具有免疫调节性质。其功能不全是囊性纤维化(CF)患者的广泛特征,其患有鼻病毒(RV)诱导的肺癌。
为了研究维生素D是否具有抗病毒活性,我们对CF儿童的原代支气管上皮细胞进行维生素D预处理并感染RV16。评估维生素D的抗病毒和抗炎活性。测定RV感染CF患儿支气管肺泡灌洗(BAL)中RV和LL-37水平。
在CF细胞中,维生素D以剂量依赖的方式降低RV16负荷(10−7m,p <0.01)。由干扰素介导的抗病毒反应在CF细胞中受维生素D保持不变。维生素D在RV感染的CF细胞中没有施加抗炎性质。维生素D增加了抗微生物肽L1-37至17.4倍的表达(P <0.05)。在CF细胞中添加外源LL-37减少4.4倍的病毒复制(P <0.05)。观察到病毒载荷和LL-37水平之间的反比相关性(R = -0.48,P <0.05)。
通过诱导LL-37,通过维生素D降低初级CF支气管细胞中的RV复制。需要临床研究来确定维生素D适当控制用于预防病毒诱导的肺癌加剧的重要性。
抽象的
通过维生素D通过诱导抗微生物肽LL-37中的CF细胞中的鼻病毒复制http:////wly/snsyo.
介绍
囊性纤维化(CF)患者体验病毒诱导的肺癌的急性发作,对CF肺病具有显着的临床影响[1-4.].鼻病毒(RV)占绝大多数病毒相关的肺癌CF恶化[5.-7.].迄今为止,预防病毒诱导的CF肺劣化的治疗选择是罕见的。最近,维生素D在天生的免疫防御方面对病原体的作用变得越来越认识到[8.那9.].维生素D是一种类固醇激素,通常与骨骼和钙的代谢有关,并被认为参与调节先天免疫反应。尽管常规口服补充维生素D,但超过90%的CF患者血清维生素D水平不足(<30 ng·mL)-1) [10那11].流行病学研究表明,维生素D水平在血清中的逆关联和上部的感染[12那13]和较低[14那15]呼吸道。此外,据报道,维生素D状态和代谢调节病毒感染,如呼吸道合胞病毒(RSV)[16那17]和流感病毒(IAV)[18那19,表明该分子在对呼吸道病毒的先天免疫反应中起着核心作用。这些观察和CF患者经常出现维生素D水平不足的事实表明,维生素D在CF患者抗病毒反应中的潜在作用。因此,我们假设维生素D在CF气道细胞中具有抗病毒活性。我们使用了一个体外基于RV感染的原发性支气管上皮细胞与CF儿童分离的模型评价维生素D的抗病毒性质。
材料和方法
研究患者
在伯尔尼和苏黎世(瑞士)的大学医院收集了5.5(1.1-16.1)年中位数(范围)的CF和健康志愿者儿童的主要支气管上皮细胞。17 CF和10对照细胞培养物已成功建立。研究参与者的临床特征显示在表1和2.本研究招募的CF患者1-11的细胞数据之前已发表[21].另外招募12-17例CF患者仅进行重组LL-37治疗实验。排除标准以前定义为有出血倾向、使用抗凝剂和/或免疫抑制剂治疗、过去三个月内使用类固醇和特应性(后两种仅作为对照)。本研究获得了所有研究参与者和/或照顾者的书面知情同意,研究得到了伯尔尼州伦理委员会和Zürich的批准。
细胞培养和鼻病毒繁殖
如前所述,获得了淹没的初级CF和对照支气管上皮细胞,并在支气管上皮生长培养基(瑞士Lonza)中生长[21].来自A种(美国类型培养收集,Manassas, VA, USA)的主要类群RV16股票在俄亥俄-海拉细胞(欧洲细胞培养收集,索尔兹伯里,英国)上生长和滴定7.TCID.50毫升-1(中位组织培养感染剂量)如前所述[22].
维生素D3治疗和鼻病毒感染
在第2代,用活性维生素D3 (1,25-(OH))预处理原始支气管细胞。2D.3.;Sigma-Aldrich,圣路易斯,莫,美国)在10−9M,10−8m或10.-7M,置于支气管上皮基底培养基(BEBM;瑞士龙沙),24小时不补充。用96%的乙醇将活性维生素D3还原为10-4 M. Vitamin D was then further diluted in BEBM to the desired concentration giving a final ethanol concentration of 0.1% for 10-7M, 0.01%为10-8 M and 0.001% for 10-9 M vitamin D. 10-7 M of vitamin D equals 40 ng·mL-1,这是人血清中维生素D的典型浓度;因此,用于实验的剂量在生理范围中[8.].使用4,0-90%汇合细胞的多种感染感染RV16 1小时。24小时后感染后,收集细胞裂解物和上清液并在-80℃下储存直至进一步分析。
RNA提取和cDNA合成
根据制造商手册使用Nucleospin RNA套件(Macherey-Nagel,瑞士)进行总RNA分离。通过使用OMNIScript RT试剂盒(Qiagen,Basel,Switzerland),通过200μg总RNA合成cDNA。
RT-PCR.
通过使用2μlcDNA和18μlAtaqman快速通用PCR主混合物(Thermo Fisher Scientific,MA,MA,USA)进行定量RT-PCR,含有特异性引物(20μm)和探针(5μm)18s [21],RV(细胞内病毒RNA)[21]、干扰素(IFN) λ2/3 [21]、viperin(病毒抑制蛋白,内质网相关,干扰素诱导)、toll样受体3 [21],视黄酸诱导基因I(Rig-I)[21]黑色素瘤分化相关蛋白5(MDA5)[21]、β-防御素2(正向引物:5 ' -ACAAATTGGCACCTGTGGTCT-3 ';反向引物:5“-GCAGCTTCTTGGCCTCTC-3”;调查:5“-FAM-CCTGGAACAAAATGCTGCAAAAGCC-TAMRA-3”)(23]和LL-37(正向引物:5 ' -CATCGATTTCTTCCCTGTGAA-3 ';反向引物:5“-TCTTGGAGCTTATTAAAGGCATTC-3”;探针5 -FAM-ACAAGAGCAAGGCCGTGGAGCA-TAMRA-3) (24].在7500个快速实时PCR系统(Thermo Fisher Scientific)上进行PCR反应。ΔΔCT方法用于量化内源基因的mRNA表达水平,其被标准化为管家基因18s rRNA。通过产生具有含有RV cDNA的质粒的连续稀释的标准曲线来获得病毒RNA复制数。
ELISA
在维生素D处理的细胞培养上清液中测量白细胞介素(IL)-8和IL-6的蛋白质水平(10-8 M and 10-7 M) and untreated CF cells by commercially available ELISA kits for human IL-8 and IL-6 (both R&D Systems, Abingdon, UK).
重组LL-37治疗
将原发性支气管CF细胞置于两孔板中,在第二孔板中,在BeBM中生长24小时。来自CF患者的细胞12-17感染RV16,随后用20μg·mL进行后处理-1在Bebm中重组LL-37(Hycult Biotech,Plymouth会议,Pa,USA)24小时。基于可用文献选择这种浓度[25]使用不同浓度的初步实验(1,4和20μg·ml-1)(数据未显示)。
支气管肺泡灌洗
如前所述收集CF儿童的RV阳性支气管肺泡灌洗(BAL)样本[20.].研究参与者的临床特征和RV载荷的测量源自前一项研究[20.].根据制造商手册,使用ELISA试剂盒评估LL-37蛋白水平,使用ELISA试剂盒(HYCLUT BIOTECH,US)。
统计分析
除非另有说明,数据均以中位数表示。非参数配对Wilcoxon检验用于确定两组之间的差异。相关性采用Spearman秩相关检验。采用GraphPad Prism 5软件(GraphPad software Inc., US)进行统计分析。p值<0.05被认为有统计学意义。
结果
维生素D以CF支气管上皮细胞的维生素D压制病毒复制,以剂量依赖的方式
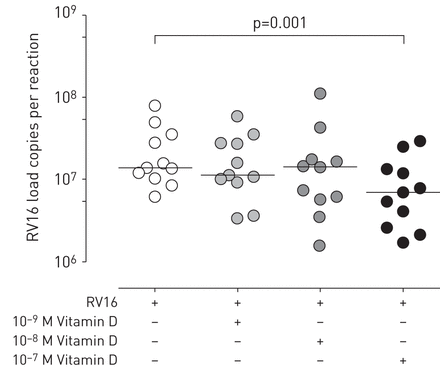
为了确定维生素D对病毒复制的影响,将维生素D处理过的原代CF支气管细胞感染RV16并观察病毒复制情况。结果表明,10-7 M of vitamin D significantly reduced virus replication by two-fold (p=0.001;图1),而病毒复制没有通过10的治疗压抑-9 M or 10-8 M of vitamin D in CF cells compared to untreated cells (图1).病毒复制下降不是由于维生素D诱导的细胞死亡(未显示数据)。
维生素D在原发性囊性纤维化支气管上皮细胞中以剂量依赖性的方式抑制鼻病毒(RV)载量。维生素D预处理24小时或不预处理24小时的细胞内病毒RNA (10-910米,-8 M and 10-7 M) was measured at 24 h post-RV16 infection by quantitative RT-PCR in primary cystic fibrosis bronchial epithelial cells. Data are presented as median of 11 independent experiments. Statistical analysis was done with the paired non-parametric Wilcoxon rank test.
维生素D不刺激CF支气管上皮细胞中干扰素途径介导的抗病毒反应
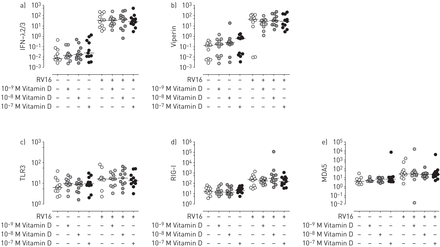
通过IFN途径介导气道上皮细胞引发的经典抗病毒反应。最近已经表明,IFN途径可以通过与TLR途径激活的协同方式通过维生素D调节[8.那26].因此,在RV感染中评估了IFN-λ2/ 3的潜水抗病毒机制,IFN-λ2/ 3的表达,IFN-λ2/ 3,通过气道上皮产生的典型IFN,并在RV感染中评估了原型的IFN刺激的基因(ISG)VIPERIN治疗或未治疗的CF细胞-9 M to 10-7结果发现,与未处理细胞相比,感染CF细胞中IFN-λ2/3和蝰蛇素的表达均无明显差异(p < 0.05)。图2一个和B.).为了证实IFN途径不参与维生素D在CF细胞中的抗病毒活性,我们进一步研究了维生素D处理后CF细胞中模式识别受体TLR3、RIG-I和MDA5的表达。房车以一种协调的方式被气道上皮细胞中的这三个prr识别[27]导致ifns下游诱导。根据IFN-λ2/ 3和viperin数据,与未处理的细胞相比,通过在RV感染的CF细胞中进行维生素D治疗评估的PRRS表达式(图2C.-E.).
干扰素(IFN)-λ2/ 3,Viperin和模式识别受体(PRRS)表达,标准化为105.在鼻病毒(RV)感染的原发性囊性纤维化(CF)支气管上皮细胞中,维生素D未调控18S mRNA的表达。a)在RV16感染24 h后,采用定量RT-PCR法检测IFN-λ2/3和b) viperin mRNA的表达情况-910米,-8 M and 10-7 M) in primary CF bronchial epithelial cells. mRNA levels of the PRRs, c) Toll-like receptor 3 (TLR3), d) retinoic acid inducible gene I (RIG-I), and e) melanoma differentiation-associated protein 5 (MDA5) were measured at 24 h after RV16 infection by RT-PCR in primary CF bronchial epithelial cells treated or not treated with vitamin D (10-910米,-8 M and 10−7m)24小时。数据以11个独立实验的中位数表示。用配对的非参数型WILCOXON等级试验进行统计分析。
在CF支气管上皮细胞中,维生素D在病毒感染时促进炎症细胞因子分泌物
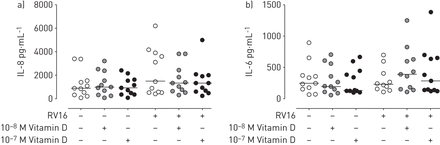
CF肺疾病的特征是炎症反应失控,在基线状态和病毒感染时炎性细胞因子如IL-8和IL-6分泌增加[28那29].此外,有报道称维生素D对气道上皮细胞有抗炎作用[4.那30.].因此,我们研究了维生素D治疗是否在CF细胞中降低了RV诱导的细胞因子产生。与未处理的细胞相比,我们发现维生素D治疗没有减少CF细胞中的rv诱导的IL-8和IL-6分泌(图3.).
维生素D在鼻病毒(RV)感染的原发性囊性纤维化支气管上皮细胞中没有抗炎特性。在RV16感染24小时后,检测细胞培养上清液中白细胞介素(IL)-8 (a)和IL-6 (b)的蛋白水平(10-8米和10-7 M) for 24 h by ELISA. Data are presented as median of 11 independent experiments. Statistical analysis was done with the paired non-parametric Wilcoxon rank test.
LL-37由维生素D治疗在RV感染的CF支气管上皮细胞中诱导
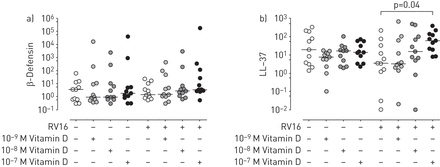
包括β-防御素和LL-37在内的抗菌肽(AMPs)有助于气道上皮细胞复杂的先天免疫反应,以防止微生物感染[31那32].众所周知,在健康和CF气道上皮细胞中LL-37和β-防御素可被维生素D诱导[33那34,我们研究了维生素D处理rv感染的CF细胞后β-防御素和LL-37的表达。我们发现,与未处理的细胞相比,维生素d处理的CF细胞中β-防御素的表达没有增加(图4A).然而,与未处理的细胞相比,感染CF细胞中l -37的表达量呈浓度依赖性增加,10倍后显著增加17.4倍-7 M vitamin D (p=0.04;图4B.).
在原发性囊性纤维化(CF)支气管上皮细胞中,维生素D刺激LL-37的表达,但不刺激β-防御素的表达。a) β-防御素mRNA表达,归一化为107.18S mRNA和B)LL-37 mRNA表达,标准化为105.用RT-qPCR检测鼻病毒(RV)16感染24 h后,经维生素D处理或未处理的原代CF支气管上皮细胞的18S mRNA (10-910米,-8 M and 10-7M) 24小时。数据以11个独立实验的中位数表示。用配对的非参数型WILCOXON等级试验进行统计分析。
重组LL-37处理可降低CF支气管上皮细胞中的RV复制
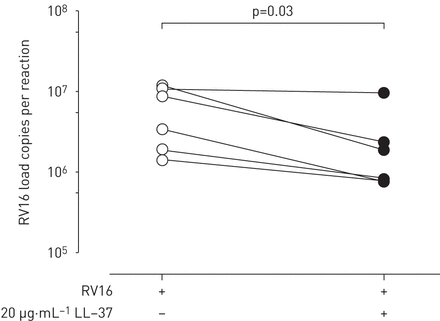
LL-37对诸如RSV和IAV等几种病毒具有有效的抗病毒活性[35].因此,为了评估LL-37的产生是否与维生素D的抗病毒活性有关,我们在CF细胞中评估了重组LL-37处理后的病毒复制。我们观察到,与未处理细胞相比,LL-37处理的CF细胞中RV复制显著减少4.4倍(p=0.03;图5.).
通过在原代囊性纤维化(CF)支气管上皮细胞中的重组LL-37处理,rhInovirus(RV)负荷降低。具有或不含24小时的细胞内病毒RNA用重组L1-37处理(20μg·mL-1), RT-qPCR检测RV16感染后24 h CF原代支气管上皮细胞。给出了六个独立实验的数据。用配对的非参数型WILCOXON等级试验进行统计分析。
LL-37水平与CF患者的rv载荷与RV负载相比
为了确认我们的体外观察在活的有机体内,我们测量了RV感染的CF儿童BAL中的维生素D水平[20.].发现CF BAL中的维生素D水平可测义,如ELISA评估(数据未显示)。因此,我们在RV感染的CF儿童BAL中测量了LL-37蛋白水平,发现RV载荷和LL-37水平之间的显着逆相关(R = -0.48; P = 0.03;图6.).
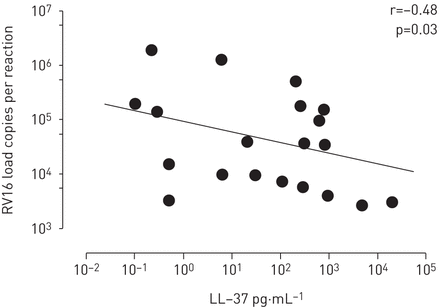
支气管血管灌洗(CF)患者支气管肺泡灌洗液(CF)患者的鼻病毒(RV)载荷和LL-37水平的负相关性。通过RT-QPCR评估RV载荷,并通过CF的儿童BAL中的ELISA测量LL-37蛋白水平(n = 20)。数据显示为散点图。统计分析是用Spearman等级相关测试完成的。
维生素D在健康支气管上皮细胞中具有抗病毒性质
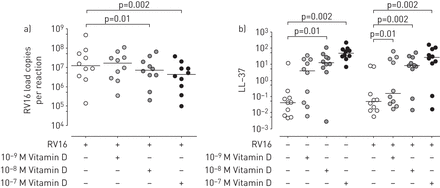
由于次优血清维生素D状态(<30 ng·ml-1)在健康儿童中也很常见(40%)[36[我们评估了维生素D处理和未经处理的对照细胞中的病毒复制。我们发现用10的对照细胞中发现1.7倍降低的病毒复制-8(p=0.01),病毒复制减少2.8倍10−7与未处理的细胞相比,对照细胞中的M维生素D(p = 0.002)(图7).为了研究维生素D是否诱导LL-37,我们通过维生素D治疗在对照细胞中评估了LL-37表达。在基线时,我们发现与未处理的细胞相比,随着对照细胞的增加的维生素D浓度的浓度,发现LL-37表达的显着诱导(10-8米,p = 0.01;10-7米,p = 0.002)。同样,我们报道了LL-37的表达量呈剂量依赖性增加10-910米,−8M和10.−7与未处理的细胞相比,M维生素D处理(分别为3.2-,166-,539倍,分别)在RV感染的对照细胞中(p = 0.01,p = 0.002,p = 0.002;图7 b).
鼻病毒(RV)载荷降低,并且通过在初级健康支气管上皮细胞中通过维生素D治疗增加LL-37表达。a)在治疗或未用维生素D处理或未治疗的初级健康支气管上皮细胞的RT-QPCR后24小时评估细胞内病毒RNA。(10-910米,-8 M and 10-7 M) for 24 h . b) LL-37 mRNA expression, normalised to 105. 18S mRNA, was measured at 24 h post RV16 infection by RT-qPCR with or without 24 h pre-treatment with vitamin D (10-910米,-8 M and 10-7 M) in primary healthy bronchial epithelial cells. Data are presented as median of 10 independent experiments. Statistical analysis was done with the paired non-parametric Wilcoxon rank test.
讨论
维生素D缺乏是CF患者的共同特征,在一定程度上也是健康儿童的共同特征。CF中维生素D水平低的原因是肠道吸收不良、代谢受损和阳光照射减少[37].最近的证据表明,维生素D在CF中具有重要的抗菌特性[38].然而,维生素D状态对CF航空公司抗病毒反应的影响仍然难以捉摸。因此,我们彻底研究了维生素D治疗对RV感染的CF细胞中宿主抗病毒反应的影响。这可能与CF肺病有关,其通常由呼吸道病毒恶化。在此,我们观察到维生素D治疗在CF细胞中减少病毒复制,最有可能通过刺激AMP LL-37的表达。实际上,重组L1-37治疗抑制CF细胞中的病毒复制。在诱导LL-37的同时,维生素D不影响IFNS途径介导的抗病毒反应,并且在RV感染的CF细胞上没有发挥抗炎性质。这些体外研究结果得到了在活的有机体内数据,我们发现在感染RV的CF患者的患者中RV载荷和LL-37蛋白水平之间的反比相关性。
最近的文献报道了维生素D在防御病毒感染(包括呼吸道病毒,如RSV)方面的潜在作用[16那17]或IAV [18那19].在我们的研究中,我们观察到维生素D抑制RV复制体外在人类CF和对照细胞中,进一步巩固了维生素D作为呼吸道病毒感染先天性免疫反应调节剂的作用。与我们的发现相反,B洛克曼- schneider等等。[39发现,在健康人气气道上皮细胞中,维生素D治疗没有减少RV复制。研究设计的差异(使用细胞培养模型和使用的维生素D浓度)可能会占我们结果的差异。
我们发现维生素D的抗病毒活性与IFN途径介导的先天免疫应答刺激无关。根据我们的发现,上述研究报道,与未经处理的细胞相比,维生素D处理对rv感染的人气道上皮细胞产生IFN-λ1没有影响[39].Hansdottir等等。[4.[甚至发现IFN-β的mRNA表达和ISGS肌瘤病毒抗性蛋白1和ISG15在RSV感染的人气通道上皮细胞中的治疗均下降。
令人惊讶的是,我们只观察到CF支气管上皮细胞对RV感染的微小增加炎症细胞因子分泌。这可能归因于,仅在感染后24小时进行上清液的取样。因此,在稍后的采样时间点,在稍后的时间点可能会看到对RV感染时细胞因子分泌的更大效果。实际上,最近的研究表明,感染后48小时,初级CF气道上皮细胞的增强的RV诱导细胞因子释放[40].此外,与RV1B等其他RV菌株相比,RV16是一种较弱的炎症细胞因子诱导剂[40].
有趣的是,与先前的文献报告了CF呼吸道细胞中维生素D的抗炎性质[38],我们没有观察到维生素D治疗rv感染的CF细胞后炎症细胞因子的分泌减少。最近的一项研究甚至报道,在rv感染的健康气道上皮细胞中,维生素D处理可增加促炎细胞因子IFN γ诱导蛋白10 (IP-10)的分泌[39].但是,M的一个有趣的研究CN盟国等等。[30.[维生素D受体激动剂是否响应于抗原攻击,维生素D受体激动剂通过CF气道上皮释放促炎细胞因子(例如IL-8和IL-6)。相互矛盾的结果可能是由于病原体挑战不同(假单胞菌铜绿假单胞菌相对RV),由于所使用的细胞培养模型[28](细胞系相对这可能导致不同的炎症反应。
现在已经确定维生素D具有抗菌特性体外在CF通过诱导β-防御素和LL-37中的几种细胞类型,例如巨噬细胞和气道上皮细胞[38].在感染时,维生素D的代谢与TLR途径激活协同诱导抗菌反应,包括AMPs的诱导[8.那26],从而提高局部增强先天免疫的可能性。安培在其基因启动子中含有维生素D响应元素(VDRE),其中维生素D直接诱导LL-37和β-防御素基因表达[34].此外,血清维生素D水平与肺功能之间的正相关[41]在CF患者中,还证明了肺癌患者的CF患者中的改善临床结果[42].
实际上,我们观察到通过维生素D在RV感染的CF细胞中进行显着诱导,但不受维生素D的表达,并且还与未处理的细胞相比控制细胞。在我们的研究中,通过常规定量RT-PCR(CT值> 35)几乎可以检测到CF细胞中的β-防御素表达。值得注意的是,维生素D诱导β-防御素的转录需要与核因子κB(NF-κB)的合作。实际上,促进剂上的VDRE附近的NF-κB响应元素介导β-防御素的协同转录[43].相反,通过钙和维生素D以协同方式诱导LL-37 mRNA表达[44].因此,其他因素比维生素D如炎症细胞因子或钙调节L1-37和β-防御素的转录,这可能解释为什么在CF细胞中的维生素D上诱导LL-37但不是β-防御素表达。有趣的是,LL-37已被证明对呼吸病毒的抗病毒性能[35提示LL-37可能通过维生素d的直接诱导参与了抗微生物宿主反应的调控。我们发现,与未处理的CF细胞相比,重组LL-37处理rv感染的CF细胞可显著降低病毒复制。实验证据表明LL-37通过破坏和破坏IVA和牛痘病毒的病毒包膜介导其抗病毒特性,而对rv等非包膜病毒的作用模式尚不清楚,需要进一步研究[35].
有趣的是,我们观察到RV患者的RV载荷和LL-37蛋白水平之间的负关联,患有RV的CF患者的患者,表明LL-37水平较低的患者可能更容易受到肺部RV感染的影响。评估健康儿童的RV阳性BALS中的LL-37水平将是有趣的,然而由于获得此类样品的困难是不可能的。
此外,健康的儿童通常具有不足的血清维生素D水平,特别是在冬季曝光减少时[36].我们发现维生素D治疗后健康支气管细胞中的病毒复制减少,这可能与维生素D的LL-37表达增加相关。这些发现表明维生素D的抗病毒性质与航空公司的健康状况无关。值得注意的是,与对照细胞相比,我们观察到CF细胞中LL-37的更高表达。然而,这可能是由于LL-37是支气管炎的标志物,这在CF肺病中发音[45].
在解释我们的结果时,应考虑以下限制。我们使用了基于浸没细胞培养物的细胞培养模型,其没有完全分化。因此,在空气液界面生长的完全分化的气道上皮培养物中重复我们的实验将是有趣的。此外,在研究中没有考虑细菌和呼吸病毒之间的相互作用。此外,我们没有表现任何鼻拭子以排除上航道中正在进行的感染。该研究的一个主要限制是,在CF儿童的母羊中评估的维生素D水平低于检测极限(11 ng·ml-1)和CF患儿在接受支气管镜检查时的血清维生素D值均未获得。
总之,我们报告了维生素D对CF和健康儿童的原发性支气管上皮细胞中RV复制的抑制作用,可能与AMP LL-37的诱导相关,其中我们证明了CF细胞中的抗病毒性能免受RV感染的抗病毒性质。CF儿童的BALS中的LL-37蛋白与RV载荷与RV载荷相关,揭示了LL-37在防御呼吸道病毒中的重要性。我们的数据表明,维生素D可以是CF患者抗病毒反应的调节剂,并指出患有CF患者的维生素D充分控制的重要性。需要临床研究来研究维生素D在预防病毒相关肺劣化中的作用。
致谢
作者要感谢所有的研究参与者和他们的家人。这项研究得到了德国波恩Mukoviszidose Institut gGmbH的资助,该机构是德国囊性纤维化协会的研发部门。
脚注
支持声明:MukovisziDose EV提供资金。
利益冲突:没有宣布。
- 收到了2015年4月28日。
- 公认2015年8月24日。
- 版权©2016人队