摘要
早产儿是肺发育最常见的干扰因素。我们的研究目的是通过多次呼气冲洗(MBW)测量来检查前早产儿较脆弱的外周气道的功能。
8.6.school-aged children, born between 24 and 35 weeks of gestation and 49 term-born children performed nitrogen MBW. Lung clearance index (LCI), and slope III-derived Scond and Sacin were assessed as markers for global, convection-dependent and diffusion–convection-dependent ventilation inhomogeneity, respectively.
我们分析了77名9.5岁(7.2-12.8岁)的前早产儿的数据 年)和46名足月出生的儿童(平均年龄9.9岁(6.0-15.9岁) 早产儿和足月儿的LCI和Sacin没有差异。与足月儿参与者相比,早产儿的Scond显著升高(平均差异z评分1.74,95%可信区间1.17–2.30;p<0.001)在多变量回归分析中,Scond仅与胎龄显著相关(R2.= 0.37)。
正常的Sacin表明肺泡腔功能正常,而升高的ssecond则表明更近端传导的气道功能受损。总之,我们的发现支持持续肺泡化的概念,尽管在前早产儿中存在“发育不良”的肺生长。
摘要
与早产相关的前早产儿肺发育不良的证据http://ow.ly/RUXUl
介绍
在全球范围内,早产儿的比例在过去几十年稳步上升[1.].尽管在新生儿和围产期护理方面取得了显著进展[2.,支气管肺发育不良(BPD)的发病率仍然很高,存活的极早产儿中有高达40%受到影响[3.,4.].自从大约50年前首次被描述以来[5.],呼吸窘迫综合征的管理进展(产前类固醇、表面活性剂的使用、最大限度地减少氧中毒和气压创伤)已导致BPD的基本病理特征的改变。因此,该疾病的当代形式的特点是肺泡和血管发育受损,导致异常隔膜,更少和更大的肺泡和更小的血管床,但只有最小的支气管周围纤维化和气道肌肉肥大[6.–8.].
尽管后表面活性剂时代出生的极早婴儿的肺病理明显较轻,但长期的呼吸损害仍然存在。几项研究显示了气道阻塞的证据[9–13.]和空气捕捉[10.,12.,13.]然而,很少有研究将通气不均匀性作为外周肺功能的生物标志物进行专门研究,结果没有定论。两项早产儿研究显示了相互矛盾的结果,一项是通气不均匀性升高[14.],另一组无通风不均匀迹象[15.].学龄时,只有一项研究检查了前早产儿童的通气不均匀性,其中58%的儿童通气不均匀性轻度升高[10.].目前,BPD主要影响肺发育早期囊泡期出生的早产儿。因此,由于随后的肺泡发育期被破坏[16.,17.,对肺功能的长期不良影响是意料之中的。
因此,我们研究的目的是使用多呼吸洗脱(multiple-breath washout, MBW)测量,一种成熟的评估小气道功能的技术,来检查学龄前儿童最脆弱的周围肺区域的功能[18.–21.].除了肺间隙指数(LCI)和矩比作为衡量整体通气不均匀性的指标,我们特别关注区域通气不均匀性的具体参数,即Sacin用于肺泡肺区域,second用于传导气道。我们假设,由于正常肺发育的过早中断,前早产儿可能出现异常的通气分布,特别是肺泡区。
方法
研究人群
2012年2月至2014年6月,我们在伯尔尼大学儿童医院(瑞士伯尔尼)前瞻性招募了6-16岁的前早产儿和足月出生儿童。早产儿(妊娠<37周)的参与者是从先前描述的研究中招募的[22.]排除患有先天性支气管肺畸形或胸腹部手术的早产儿。根据胎龄,早产儿被分为极低胎龄新生儿(ELGAN)(<28 怀孕数周)或没有埃尔根(≥28 孕周)。足月出生的对照组,出生体重与胎龄相适应(即。>2500 g in all cases) were recruited from local schools and playgroups. Term-born children with asthma or other chronic respiratory diseases were excluded. Exclusion criteria for both preterm and term-born participants were respiratory infections within the last 3 weeks.
这项研究得到了瑞士伯尔尼州伦理委员会的批准。获得了孩子们的同意,父母或看护者提供了书面知情同意书。
前早产儿呼吸系统症状和特应性过敏反应的评估
在早产儿中,与哮喘和过敏相关的症状由父母完成的国际儿童哮喘和过敏研究(ISAAC)问卷评估[23.].For later subgroup analysis, we focused on four binary outcomes (yes/no): wheeze over the past 12 months; cough without cold; shortness of breath due to cough or asthma; and doctor-diagnosed asthma. “Current asthma” was defined as wheeze or use of asthma medication in the past 12 months or doctor-diagnosed asthma. Atopic sensitisation was assessed by positive skin-prick testing on at least one common inhalant allergen (mixed trees, mixed grasses, cat, dog, house dust mite and来自烟曲霉属真菌)我们进一步测量了呼出的一氧化氮的分数(F依诺)采用单呼吸法,使用市售分析仪(CLD 77 AM;Eco Medics AG, Duernten,瑞士)。患儿吸入无一氧化氮空气至总肺容量(TLC)后,顶着呼气阻力呼气,流量50 mL·s−1.≥6 s。
为了证明我们的研究结果的有效性,而不考虑肺发育的其他可能变化,我们对早产儿的三个亚组与足月出生的对照组进行了敏感性分析:1)没有呼吸道症状(如果上述四个调查问题均为阴性,则不存在);2)目前没有哮喘;3)没有过敏反应(皮肤点刺试验阴性和F依诺< 20磅;[24.])。
氮气多次呼气冲洗
所有患儿均行氮MBW (N2.根据目前的共识[25.使用先前描述的设置[]26.,27.) (Exhalyzer D;Eco医生AG)。使用100%的氧气会冲洗掉肺部的氮气。氮信号是由氧、二氧化碳和估计的氩馏分间接测量的。孩子进行N2.坐直,戴着鼻夹,通过通气管口片进行潮汐呼吸。至少两个成功的N2.获得MBW运行2.如果两次试验的功能剩余容量(FRC)变化<10%,三次试验的变化<25%,则接受MBW运行[25.].不包括泄漏的测量值。
所有数据均使用Spiroware 3.1.6 (Eco Medics AG)进行记录和分析。结果按目前推荐的方法计算[25.];LCI由累积过期容积除以FRC,得出肺周转单位。我们使用LCI和矩比(M1./ M0和M2./ M0)作为全球通风不均匀性的度量。至于周肺通气的特异性标志物,我们分析了氮expirogram的肺泡阶段III(SIII)的斜率。第一SIII值被认为是反映内通风不均匀扩散对流依赖性腺泡气道(Sacin),而SIII值从肺周转后续演进1.5至6.0被认为是反映内对流依赖性传导气道通气不均匀性(Scond)[25.].second是根据一种经过验证的自动算法计算的,其SIII确定在过期量的65%至95%之间,并排除呼吸量偏离中值潮气量的>25%,并附加呼吸质量的视觉控制[28.].排除呼气图中无清晰线性III期部分的呼吸,或不规则呼气和振荡。SIII值在其计算间隔内的平均气体浓度标准化,并根据潮气量进行校正[29.].如果SIII值不足,即。如果去掉所有SIII值>的33%,则排除second [25.].此外,我们评估了微通气和气道死腔体积(vD)使用F猫头鹰的(30.洗脱呼吸二氧化碳呼气图的测定方法。
肺量测定法
仅在洗脱后使用MasterLab设置(德国维尔茨堡耶格尔)并根据标准指南进行肺活量测定[31.].1秒用力呼气量(FEV)1.)和强迫呼气流量在25-75%的强迫肺活量(FEF25 - 75%)以z分数表示[32.].如果两种FEV均为正常肺活量测定1.和FEF25 - 75%我们>−1.64 z分数[33.].
数据分析
样本量的计算是基于基线平均值±SD.使用相同设置测量20名健康学龄儿童的0.01±0.01秒[28.].每组22名儿童的样本量将提供90%的能力来检测指数组和健康对照组之间一个群体标准偏差的洗出参数差异,双侧显著性水平为5%。
连续变量经正态分布验证后,采用t检验进行比较。分类变量比较采用卡方检验。肺功能参数的正常上限(ULN)定义为均值+1.64SD.[33.]进行肺活量测定的健康参考人群[32.]从我们的术语“清洗”参数的born控件。
通过单变量和多变量回归分析评估洗脱参数与围产期因素及其他肺功能参数的关系。多变量模型根据体长、性别和胎龄进行调整。所有分析均使用Stata统计软件进行(第11版;StataCorp LP, College Station, TX, USA)。
结果
研究人群
共有86名前早产儿和49名足月出生的儿童被纳入研究。至少两个有效的N2.在77名(90%)早产儿和46名(94%)足月出生的参与者中获得了MBW测量值。排除的原因是泄漏、不规则呼吸模式和FRC变异性在两个有效试验中>10%,或在三个有效试验中>25%。77名(42名男性)前早产儿的平均年龄(范围)为9.5岁(7.2-12.8岁) 在46名(21名男性)足月出生的受试者中,年龄和性别为9.9岁(6.0-15.9岁) 年。被排除在外的儿童在年龄、性别、体重、身高或胎龄方面与被包括的儿童没有差异(数据未显示)。
早产儿和足月儿在纳入时表现出相似的特征(表1).早产儿的平均(范围)胎龄为28.7(23.9-34.7) 周和平均(范围)出生体重1139(420-2980) g、 75%的受试者患有BPD,21%的受试者在学龄时符合当前哮喘的标准。早产儿受试者与其胎龄(ELGAN和no-ELGAN)相关的特征见表2.
氮气多次呼气冲洗
此外,14早产和八个学期出生的孩子被排除Scond分析,七个早产和九个长期出生的孩子被排除Sacin分析,由于后呼吸质量控制左不足SIII值由目前的共识规定[25.].排除无效Scond和Sacin孩子没有从那些包含在年龄,性别,重量,长度或胎龄方面不同(数据未显示)。
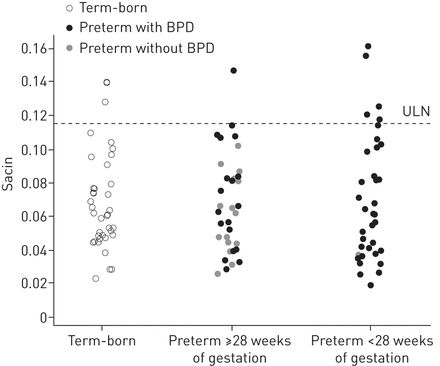
LCI和M2./ M0在早产儿和足月出生的儿童之间无显著差异(表3,图1).此刻比M1./ M0显著高于早产儿(平均差异0.49 z得分,95% CI 0.05-0.92;p = 0.028) (表3), 77个早产儿中有11个(14%)患有M1./ M0值>ULN。而Sacin在早产儿和足月出生的参与者之间没有差异(图2),与足月出生的儿童相比,前早产儿的第二项指标显著更高(平均差异1.74 z-scores, 95% CI 1.17-2.30;p < 0.001) (图3)63名早产儿中有34名(54%)的Scond值>ULN。在无呼吸道症状、当前哮喘、特应性过敏或无上述三项标准(数据未显示)的早产儿亚组中,Scond仍显著升高(p<0.001)。此外,在肺功能正常的早产儿中,Scond显著升高。未经潮气量校正的原始Scond和Sacin值的结果仍然相似(数据未显示)。在早产儿中,ELGAN和no ELGAN之间的Scond无显著差异(表3),而与未患BPD的早产儿相比,患有BPD的早产儿患病率略高(平均差异0.008,95% CI 0.001-0.015;p = 0.026)。然而,在调整胎龄后,BPD与无BPD的差异消失。
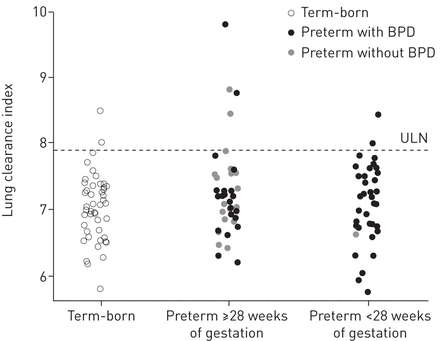
对46例足月产儿、39例妊娠≥28周早产儿和38例妊娠<28周早产儿进行氮气多次呼吸洗脱肺清除率(LCI)测定。在LCI高于正常上限(ULN)的5例早产儿中,4例目前有哮喘、呼吸道症状和/或肺活量异常。桶:支气管肺的发育不良。
对37例足月产儿、34例妊娠≥28周的早产儿和36例妊娠<28周的早产儿进行氮气多次呼吸洗脱试验。桶:支气管肺的发育不良;ULN:正常上限。
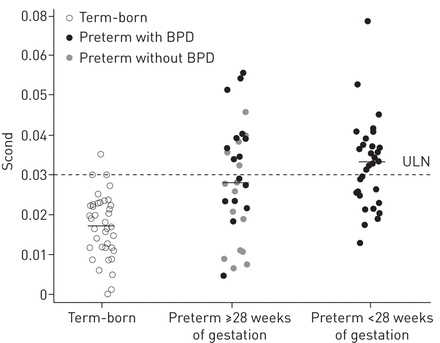
其次是早产儿和足月出生的儿童。对38名足月出生的儿童、32名妊娠≥28周的早产儿和31名妊娠<28周的早产儿进行氮气多次呼吸洗脱测量,每组测量值均为平均值。桶:支气管肺的发育不良;ULN:正常上限。
FRC,每分钟通气量和vD所有校正体重,显示早产儿和足月出生的孩子没有什么区别,也没有ELGAN和无ELGAN(间表3).
肺量测定法
我们发现了一些气道阻塞的证据:平均值±SD.钒铁1.前早产儿为- 0.60±1.11 z-score (表3),其中18%(14个77)已经减少的值(<-1.64 z得分)32.].均值±SD.FEF25 - 75%是−0.97±1.20 z分数(表3),其中30%(77人中有23人)的价值下降。FEV无显著性差异1.和FEF25 - 75%ELGAN和no-ELGAN之间(表3)也不包括患有和不患有BPD的早产儿。
与Scond升高相关的因素
全研究人群的回归分析显示,在单变量模型中,所有与second显著相关的围产期因素(胎龄、BPD、补充氧天数、呼吸支持、插管、在对孕龄、体长和性别(r2.37%)(表4).当组早产儿内,用于ELGAN分层,Scond和孕龄之间的关系的ELGAN组内仍然显著(-0.004,95%CI -0.008--0.001; P = 0.010),而它是不是在没有显著-ELGAN组。对于Sacin和肺功能检查(FEV1.和FEF25 - 75%)没有围产期因素显著相关(数据未显示)。包括肺功能参数作为暴露变量(Sacin, LCI,vD·公斤−1.FRC·公斤−1.,每分通气量·公斤−1.,钒铁1.和FEF25 - 75%),在单变量和多变量模型(数据未显示)中,只有单位体重的分钟通气与second升高显著正相关。
讨论
这项研究是第一个使用MBW技术专门检查学龄前早产儿周围气道肺功能的研究。反映整体通气不均匀性的LCI在足月出生和前早产儿参与者(包括ELGAN和BPD患者)之间没有差异。与我们的假设相反,我们没有发现在腺泡水平上存在弥散依赖性通气不均匀性的证据,这反映在我们的研究组之间的Sacin值相似。然而,超过一半的早产儿中,second值升高,表明在更近端对流依赖的气道中,通气不均匀。在我们的队列中,胎龄是最强的第二预测因子,独立于其他混杂因素,但相关性相当弱。这些发现为学龄前早产儿童的肺泡室功能正常提供了证据,尽管在小的对流依赖气道的近端水平上气道功能受到干扰。
对前者的早产儿肺功能以前的报告已经提供了气道阻塞的证据[9–13.,空气滞留[10.,12.,13.]及减低肺部对一氧化碳的扩散能力[10.,12.,13.].然而,只有一项研究评估了极端早产学龄儿童的全球通风分布[10.].尽管这些研究人员报告58%的儿童LCI轻度升高,肺活量测定在鉴别早产或BPD方面表现更好。更具体的外周通气不均匀性指标,如Sacin和second未被评估。与L相反嗯等. [10.,我们发现前早产儿和足月出生儿童的LCI没有相关差异,而只有6%的早产儿的LCI升高。这种差异可能是由于他们的研究包括了仅妊娠26周出生的儿童,哮喘患病率高达55% [10.].
作为特定的区域通气参数,second和Sacin已被证明反映不同的疾病特征的发病机制,如囊性纤维化[19.],哮喘[18.]及闭塞性细支气管炎[20.].我们的研究结果显示了前早产儿区域通气不均匀性的显著模式:我们发现正常的Sacin值表明腺泡水平的通气分布正常。因此,我们的研究为前早产儿肺泡腔功能正常提供了证据。相反,Scond始终是超过一半的早产儿没有哮喘症状或其他肺功能异常,这表明近端传导气道的通气分布受损。多变量回归分析证实了Scond与早产之间的关联,显示胎龄可以解释37%的变量Scond的可预测性独立于其他混杂因素。在多变量模型中,其他围产期因素之间缺乏相关性,如BPD、补充氧气的天数以及调整胎龄后使用Scond或肺活量测定法插管,强调了新BPD的病理生理学[34.]:功能改变主要不是由治疗引起的(气压伤或氧中毒),而是由早产引起的本质上. 然而,仍然很难弄清不同相关因素的确切影响,主要是因为在我们的观察研究中,胎龄和BPD表现出强烈的共线效应。早产儿中ELGAN和no ELGAN之间的Scond没有明显差异。此外,在ELGAN组中,Scond与孕周之间的相关性最强。因此,早产肺的病理生理学是复杂的,有许多因素促成和相互作用。我们的数据无法回答分钟通气与Scond的关联是否表明Scond增加时存在适应性机制,或者是否存在主要调节反应[15.].通风不均匀性的机制,这种模式可以解释为这些孩子出生晚canalicular-early囊状肺发展的时期,当外围进行航空公司已经开发并因此脆弱,而肺泡地区发展后,出生后继续增长(35.].因此,我们的研究结果表明,在早产儿中,外周传导气道和肺实质的生长不匹配,支持“发育不良”肺生长的概念[36.,37.],有关早产。
总体而言,没有证据表明早产儿的整体通气不均匀性增加2./ M0在早产儿和足月出生的儿童中,M1./ M011名儿童的血压升高。由于给冲刷后部分的权重从M开始增加1./ M0对M2./ M0可以推测周围气道的近端受累。
成像技术的最新进展[38.]及立体计数方法[35.]提供了新的证据,表明健康肺在婴儿期至青年期仍有肺泡形成。特别有趣的是,最近一项使用氦磁共振的研究显示,健康青少年在学龄时仍有肺泡化的迹象[38.]和前早产儿[39.,后者有一半被诊断为BPD。鉴于新BPD的主要病理生理特征被描述为肺泡发育的“停止”[6.],这些发现表明肺泡形成和潜在肺修复发生的时间范围可能比以前认为的要宽得多。目前尚不清楚是否可以用持续肺泡形成的形态学术语来描述肺功能。尽管如此,我们的研究为功能性肺损伤提供了证据在前早产儿中,肺泡持续完整,因此与结构研究结果一致。然而,我们的横断面数据无法回答这个复杂过程的确切潜在机制或结构相关性的问题。
我们的研究的主要局限性是基于模型对Sacin和second的解释,因此缺乏其与特定肺形态关联的证据。因此,我们的结果的解释在很大程度上依赖于这样一个假设,即second和Sacin分别是对流和扩散对流依赖肺区的区域通风分布的有效代理[18.–20.].另一个限制是足月出生的对照组缺乏肺活量测定,因此仅与参考值进行有限的比较[32.].在术语出生控制中缺乏准确的出生体重记录,阻碍了回归模型中出生体重的调整。然而,在仅限于早产儿的分析中,出生体重与second没有显著关联。关于早产儿,我们主要包括非常早产的儿童。这可能代表了对呼吸系统后遗症发生率较高的儿童的选择偏倚。足月出生和早产儿童的年龄分布不平等,足月出生组中年龄较大的儿童所占比例更大。然而,平均年龄是相似的,并且在调整年龄后结果保持稳定,因此影响似乎可以忽略不计。最后,胎龄对second的影响大小虽然存在,但相对较弱。在解释围产期因素和对流依赖通气不均匀性之间的关系时,必须考虑到我们研究亚组的样本量相当小。尽管胎龄低,一些极端早产的参与者也有正常的second值。 Presumably, there are additional factors (如。基因、表观遗传和环境暴露)可能会影响未成熟肺的易感性,并决定肺损伤的长期结局。
总之,我们的研究提供了前早产儿在学龄一个功能正常的肺泡隔第一手的证据,但传导气道,支持早产相关dysanaptic肺生长模式的受损通风不均匀性。未来的研究需要详细说明外围肺功能和潜在的结构性赤字之间的确切关系,从而有助于推进预防和治疗策略过早出生的婴儿。
确认
作者要感谢所有儿童及其家庭参与本研究。我们感谢桑德拉·鲁塞尔、卡门·卡萨尔塔、莫妮卡·格拉夫、琳达·贝金、吉塞拉·维尔兹和莎伦·施密德(瑞士伯尔尼伯尔尼大学儿童医院)所做的宝贵工作和支持。
脚注
支持声明:本文的工作由瑞士国家科学基金会(grant 324730_144280/1)、Linde AG、Gottfried和Julia Bangerter-Rhyner基金会、德国-瑞士-奥地利儿科肺科协会(GPP) (a . Schmidt)的长期研究员和Botnar基金会资助。资助方在研究设计、数据收集和分析、决定发表或准备手稿方面没有作用。本文的资金信息已存入基金参考.
利益冲突:未声明任何利益冲突。
- 已收到2015年3月25日。
- 认可的2015年8月18日。
- 版权所有©ERS 2016