摘要
18F-fluoro-2-deoxy -d-葡萄糖正电子发射断层扫描(PET)补充了诊断和分期肺癌的常规成像。两项基于文献的元分析表明,最大标准化摄取值(SUV马克斯)在非小细胞肺癌(NSCLC)中具有单因素预后价值。我们分析了来自12项研究的个人数据,以评估二元SUV的独立预后价值马克斯为了整体生存。
在检索已发表的文献并确定未发表的数据后,联系研究协调员并要求提供个别患者的数据。采用分层的Cox回归模型进行研究。
收集了1526例患者的数据(中位年龄64岁,60%为男性,34%为鳞状细胞癌,47%为腺癌,58%为I-II期)。SUV的综合单因素风险比马克斯为1.43 (95% CI 1.22-1.66),如果按组织学分层计算SUV阈值,则几乎相同。对I-III期疾病患者进行多因素分析,确定年龄、分期、肿瘤大小和接受手术为独立预后因素;加入SUV (HR 1.58, 95% CI 1.27-1.96)显著改善模型。唯一检测到的相互作用是SUV和IV期疾病之间。
SUV似乎在I-III期NSCLC、鳞状细胞癌和腺癌中具有独立的预后价值。
摘要
SUV在I-III期NSCLC中具有独立的预后价值,无论是鳞状细胞癌还是腺癌http://ow.ly/Q2FKI
介绍
在世界范围内,肺癌是男性癌症相关死亡的主要原因,是女性癌症相关死亡的第二大原因[1]。尽管有了新的治疗方法,但患者的存活率仍然相对较低[2]。虽然许多临床和组织病理学特征、实验室标记物、分子生物学标记物和基因标记物已被测试其潜在的预后价值,但目前在临床实践中,很少有经过验证和准确的预后因素用于管理或预测个别患者的结果。尽管有大量关于这一主题的文献,但到目前为止,只有两个特征被明确确定为独立的预后因素:表现状况(特别是在疾病晚期)和疾病分期[3.],已得到国际肺癌研究协会(IASLC)分期项目的确认。在此背景下,我们收集了>10万例患者的数据,并用于构建第7版肺癌TNM(肿瘤、淋巴结、转移)分类[4]。预后因素也进行了研究,但研究结果受到现有全球数据库中少量协变量的限制。这进一步间接说明,很少有因素被普遍接受为预测肺癌预后的重要因素。
TNM分期评估传统上是基于手术结果和常规影像学。然而,二十多年来,正电子发射断层扫描(PET)与葡萄糖类似物2-[18-fluoro-2 -脱氧- F)d-葡萄糖(FDG)已广泛用于肺癌的疾病分期。的确,一些meta分析表明FDG-PET的使用提高了分期的准确性[5,6]。
我们的研究小组对文献进行了两次系统综述和荟萃分析(第二篇是对第一篇的更新),分析FDG-PET对生存的可能预后价值[7,8]。2008年1月和2010年5月发表的结果表明,具有较高的最大标准化吸收值(SUV马克斯)可能是影响预后的不良因素。总共分析了21项研究[9- - - - - -29]。
在这些荟萃分析中,我们对低SUV和高SUV患者的比较得出,高SUV患者的总体综合危险比为2.08,与1有显著差异(95% CI 1.69-2.56)。较老的研究与较新的研究之间(p=0.60)或排除或纳入转移性疾病患者的研究之间(p=0.46)未发现相互作用。
考虑到基于文献的元分析的局限性[30.],特别是由于缺乏多变量分析,以前的工作通过对个体患者数据进行汇总分析进行了扩展,这是IASLC分期项目认可的项目。主要目的是评估原发肿瘤FDG-PET SUV的预后价值马克斯(体重校正)的总生存率,并考虑或不考虑已确定的预后因素,特别是TNM分类。作为次要目标,进行了亚组分析,并研究了SUV与患者或肿瘤特征之间可能的相互作用。
方法
联系了以前纳入系统评价的研究的所有通讯作者,并向他们提供了进一步分析个人数据的方案和计划。参与该项目的人员被要求向协调机构(比利时布鲁塞尔Jules bordt研究所)提供这些数据和预先指定的变量,以更新他们的生存数据,并完成一份关于测量FDG吸收方法的问卷。还包括一个未出版的系列。
然后在协调机构审查、汇总和分析来自不同系列的数据。对SUV与其他可能的预后因素之间的相关性进行了描述性分析。Cox回归模型用于获得每项单独研究中SUV对总生存期影响的风险比估计值。在这些比较中,SUV被表示为一个二进制变量(低水平或高水平),每个单独系列中的中位数被选择为阈值。使用分层Cox模型评估SUV的整体影响。在可能的情况下,计算从PET日期到死亡(任何原因)或最后一次随访日期的总生存期。否则,使用个别数据集中提供的总生存期。
采用相同的方法进行亚组分析,并进行相互作用试验。最后,通过研究分层的多变量Cox回归模型来评估SUV的独立预后价值,并评估在已知预后变量的基础上将SUV添加到模型中的益处。为此目的,使用除SUV外可用的协变量对每项研究进行分层的多变量分析。采用逆向选择方法。之后,强制SUV进入模型,对模型改进进行评估。只有数据完整的患者被纳入分析(没有缺失值)。报告的风险比估计有95%的置信区间,所有的p值都是双尾的。SAS软件(版本9.4;SAS研究所公司,Cary, NC, USA)。
测量SUV的方法和FDG-PET扫描仪的类型显然很重要,测量中心之间的可重复性取决于标准化协议的使用。然而,较大的测量变异性是可能的,并且已经在其他地方描述过(见[7])。简单来说,不同的因素和误差会导致SUV测量的差异:临床/生理因素(如血糖、注射和图像之间的时间、禁食、运动和患者舒适度)、误差来源(为正确的衰减时间而对时钟进行交叉校准、剂量校准器和摄像机的准确交叉校准、准确的注射活动和对静脉注射)和物理影响(采集设置,如每个床位的时间、床位之间的重叠百分比、二维或三维采集模式、衰减校正类型、图像重建方法和图像分辨率)。出于这些原因,我们向作者发送了一份特定的问卷(在线补充材料),以收集有关FDG-PET测量和SUV测量的临床和技术信息。完成的问卷旨在用于构建协变量,代表在获取SUV值的方法中可能被认为是同质的研究子组。
结果
联系了25位通讯作者。五人没有回答[14,21,22,26,31];另外九个[9,10,12,15,17,24,28,32,33]没有提供参与批准,或在初步协议后没有发送数据,或在我们询问他们时没有可用的数据。其余11项研究[11,13,16,18- - - - - -20.,23,25,27,29,34],个别资料均已提供及收到。此外,收集了一系列未发表的患者的数据。
在患者数量方面,根据出版物(包括未发表的系列),确定了3578名潜在符合条件的患者,并收到了其中1563名患者(44%)的相关数据。研究的基线特征以及从分析中排除一些患者的原因在表1.
患者特征,包括存在于1526例纳入分析的患者的大部分数据集中的协变量,显示在表2.已制定计划调整其他已知预后因素的分析(如。生物学因素),但由于缺乏数据,这是不可能的。预先指定的无进展生存期分析是不可能的,因为现有数据只允许计算约65%的患者的无进展生存期。
在12个系列中的10个中,SUV被认为是连续的协变量。在一个系列中,将SUV作为二元协变量[27],另一种是混合提供SUV [19]。然而,在这两个系列中,个体风险比可以使用中位数作为SUV阈值来估计。12个系列中有10个是SUV马克斯,两个没有[13,20.]。在一项研究中[29],都是SUV马克斯和SUV的意思是是可用的。
使用方差分析调整研究,SUV(作为连续协变量)与性别之间存在关联,男性患者代谢活性更高(因此SUV也更高)(p=0.04)。相反,腺癌的代谢活性较低(p<0.001)表1和图1)和I期或II期疾病(p<0.001)。最后,SUV与肿瘤大小呈显著正相关(两个变量均连续,p<0.001),但与年龄无显著正相关。

经研究的鳞状细胞癌或腺癌亚组患者标准化摄取值(SUV)的边际均值。
SUV对总体生存的影响表现在表3,以及我们在基于文献的荟萃分析中获得的事件发生率和风险比。基于文献的危险比估计值与目前获得的危险比估计值之间的主要差异来自于SUV的使用中位数作为阈值或生存数据的更新或对患者群体的轻微变化进行分析。
合并危险比为1.43 (95% CI 1.22-1.66):高SUV患者的生存率明显低于低SUV患者。如果这两项研究在哪个SUV的意思是排除使用,合并危险比为1.46 (95% CI 1.23-1.73),结论相同。生存曲线描述在图2.
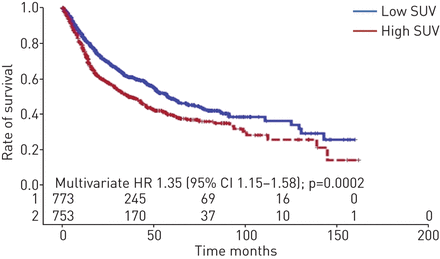
根据标准化摄取值(SUV),在每个数据集的中位数上进行二分。1:低档SUV;2:高SUV。
经组织学分层,按中值对SUV进行二分(腺癌与鳞状上皮细胞与其他组织学亚型),159例(10%)患者的SUV类别发生改变(低值向高值转变的88例,高值向低值转变的71例)。然而,合并危险比没有明显变化(HR 1.43, 95% CI 1.23-1.67)。
亚组分析结果见表4.唯一确定的相互作用是与分期,这表明SUV对IV期疾病患者的预后价值很小或没有。
第一个拟合的多变量模型包括年龄、分期、肿瘤大小和接受手术作为解释变量(981例患者和337例事件)。由于模型中没有性别,因此进行了改装,添加了性别类别未知的患者(1117例患者,374例事件)。高龄(HR 0.51, 95% CI 0.40 - 0.66;p<0.0001), I期(HR 0.42, 95% CI 0.29-0.60;p<0.0001)或II期(HR 0.60, 95% CI 0.40-0.91;P <0.0001)为有利预后因素;肿瘤体积较大(HR 1.09, 95% CI 1.04-1.14;p=0.0006)和缺乏手术(HR 2.98, 95% CI 2.04-4.35;P <0.0001)为不良预后因素。值得注意的是,由于肿瘤大小不适用于任何IV期疾病患者,因此该模型不包括任何IV期患者。 Addition of SUV to this previous model significantly improved it (表5).危害比为高与低SUV为1.58 (95% CI 1.27-1.96;p<0.0001),如果用于分类的阈值取决于组织学,则略有增加(HR 1.61, 95% CI 1.30-2.00)。SUV与模型中包含的其他协变量之间的交互作用不显著。
当不考虑肿瘤大小时,可以将IV期患者添加到分析中,同样没有性别统计学意义。在没有SUV的情况下,最佳模型(1526例患者,669例事件)包括年龄、分期和有无手术,其风险比如下。年龄≥70岁:0.66 (95% CI 0.55-0.78;p < 0.0001);I期:0.20(95%可信区间0.13-0.29;p < 0.0001);II期:0.31 (95% CI 0.20-0.48;p < 0.0001);III期:0.48 (95% CI 0.37-0.62;p < 0.0001); and lack of surgery: 2.46 (95% CI 1.94–3.13; p<0.0001). The addition of SUV to this model improved its predictive ability, as shown in表5(两种不同类别的SUV的结果相似)。在后一种情况下,分期和SUV之间的相互作用是显著的,SUV对IV期患者没有可检测到的影响。
用于获得SUV的方法所收集的数据如所示表6.该表显示,不同的研究没有相同的临床或生理患者制剂,可能没有相同的物理效果,并且有一些不可评估的错误来源,因为一些研究是回顾性的。这种显著的异质性不允许我们按计划构建研究组,因此阻止了我们将SUV作为一个连续变量进行研究。
讨论
我们根据来自12个不同系列的1526名患者的个人数据进行了汇总分析;换句话说,44%的符合条件的患者被纳入分析。我们证实了我们之前工作的结果:原发肿瘤摄取高SUV的患者比代谢率低的患者生存时间更短,我们现在已经确定高SUV是一个独立的预后因素,这是我们之前基于文献的荟萃分析无法得出的结论。但是,正如预期的那样,点数估计数低于以前得到的估计数;事实上,我们用的是SUV中位数将每个系列中的值作为阈值,以二分化SUV测量,而不是所谓的“最佳分割”,这已知会增加假阳性结果的几率[35];其他预后协变量的调整也可以解释较低的点估计值。正如预期的那样,肿瘤代谢活性与组织学有关。为了在评估SUV的预后价值时纠正这一因素,我们计算了按组织学分层的单独阈值,但我们没有发现这样做对SUV对生存的影响程度有任何改变。同样,我们也没有发现SUV与组织学之间的相互作用。这也是由于使用患者个人数据而获得的新发现。
这项研究有几个局限性。与我们的方案相比,协变量的数量受到限制;如前所述[3.,4],这说明了标准化肺癌预后因素研究的必要性。引用的单个患者数据元分析的优点之一[30.]是为了提供更成熟的数据,但在目前的分析中,我们发现至少在临床试验之外,很难执行搜索来更新生存状态。最后,我们没有足够数量的数据集,包括疾病进展的信息,因此我们无法计算无进展生存期,这将是我们以前的系统综述的进一步优势。
我们基于文献的元分析[7,8]使我们无法解决关于评估SUV方法的研究异质性问题,以及随后测量中的大变异性问题。这就是为什么我们的SUV作为一个连续变量与其他基线特征之间的相关性分析应该仔细解释,尽管它们为研究进行了调整。一些科学协会,如欧洲核医学协会,不仅发布了肿瘤学中半定量FDG-PET评价指南[36],但亦建立了PET/计算机断层扫描中心认证系统[37],考虑到人员培训、临床检查情况、机器校准、重建方法和衰减算法等。然而,评审并不能完全解决结果的可重复性问题[38]。通过问卷调查,我们具体询问了每项研究中使用的方法,我们无法确定同质组,我们只能得出结论,SUV值越高意味着风险越高。一些作者认为,患者不应分为两个离散的组,而是随着SUV的增加而显示出危险的持续增加[23,39]。然而,我们的数据不允许我们提出一个或几个阈值。在代谢成像这一领域,可能比其他任何前瞻性标准化多中心研究都要多先天的估计样本量不足以提供足够的统计能力,但这是非常需要的。
发表偏倚是另一个重要问题,显然我们的研究很可能受到这种偏倚的影响:我们漏掉了56%的“合格”患者,许多其他系列可能存在但没有发表。这就是为什么我们的研究必须被解释为汇总数据分析,而不是现有证据的元分析。由于患者数量有限,不存在功率问题,因为确定了高SUV的显著独立预后价值,但存在发表偏倚问题,这是任何预后因素的meta分析固有的问题,因为不存在此类研究的注册表。这是在进行个体患者数据元分析时要付出的代价,因为从所有数据库所有者那里获得共享数据的批准是非常困难的;尽管我们与所有作者共享了本研究的方案和预先计划的分析,但我们在这项研究中部分失败了。然而,当回到我们基于文献的荟萃分析并计算有或没有个体患者数据的研究的联合风险比时,发现相似的点估计值:2.15 (95% CI 1.57-2.93)和2.03 (95% CI 1.54-2.69),异质性检验的p值为0.79。这表明我们的亚组研究可能很好地代表了总体证据,发表偏倚并不重要。由于与已出版丛书作者讨论数据交换需要大量时间,我们没有尝试获取最近发表的数据。然而,如果高SUV真的对生存没有任何影响,就需要进行非常大规模的研究(或许多中等规模的研究)来将我们的结果转化为非统计显著性的结果。
然而,由于上述原因,有必要进行一项前瞻性研究,以检测与我们获得的点估计值相似的风险比,以证实我们的结果。
尽管混合了SUV的尺寸,但只有两个系列提供了SUV的意思是与10个衡量SUV的系列相比马克斯.这两个序列的排除没有显著影响结果,也没有改变高SUV患者的生存率明显低于低SUV患者的结论。
有趣的是,我们证实肺腺癌在肿瘤组织学中表现出最低的SUV值,正如几位作者所报道的那样[32,40- - - - - -42]。在不使用SUV作为连续协变量的情况下进行分析,这种相关性并没有改变SUV的预后价值。
众所周知的部分体积效应[43至少可以部分解释I-II期肺癌患者代谢摄取较低的发现。尽管如此,SUV在从I期到III期的每个阶段都始终显示出预后价值,但我们的结果表明SUV对IV期疾病患者的预后无效。有可能,一旦肺肿瘤显示转移扩散,肿瘤的解剖范围比原发肿瘤的代谢活动更重要的预测预后。尽管这一假设应在更多的IV期疾病患者中得到证实,但这可能是引入其他代谢活动测量方法(如肿瘤糖酵解和代谢量)以及异质性和纹理分析作为预后因素非常有前途的原因[44- - - - - -49]。然而,这些“新的”衍生代谢参数似乎在大肿瘤中更有趣,因为PET由于其有限的空间分辨率而无法表征小肿瘤中的示踪剂分布。然而,已经描述和测试了多个纹理参数来描述肿瘤的异质性,但尚未达成共识,以得出最佳和最稳健的结论。此外,这些参数在NSCLC IV期患者中也非常有趣,我们未能确定SUV的任何独立预后价值马克斯.在我们看来,需要多中心大型前瞻性试验来测试这些新衍生参数,以得出在哪些病例/阶段使用它们最相关的结论。
结论
尽管我们的研究存在选择偏倚和缺乏标准化的SUV评估,但我们的研究结果表明,在原发肿瘤上测量诊断时的SUV是I-III期NSCLC患者的独立预后标志物。组织学和SUV之间没有可检测到的相互作用,尽管已证实的观察表明,鳞状细胞癌中SUV的摄取高于腺癌。SUV在预测IV期患者生存中的应用需要进一步研究。
确认
作者感谢Claude Hossein-Foucher(核医学,CHRU de Lille, Lille,法国)和Arnaud Scherpereel(肺和胸部肿瘤学,CHRU de Lille)对工作的支持和对手稿的批判性阅读。
脚注
这篇文章有补充资料可从www.qdcxjkg.com
利益冲突:可以在本文的在线版本中找到信息披露www.qdcxjkg.com
- 收到了2015年1月20日。
- 接受2015年7月5日。
- 版权所有©ERS 2015















