文摘
最近,一位轨迹集中在rs9273349hla dq地区出现在成人哮喘的全基因组关联研究。我们旨在进一步研究人类白细胞抗原(HLA)类的作用二世在成人哮喘和与职业暴露可能的交互。
我们估算古典HLA-II等位基因从7579年的6025例单核苷酸多态性与成人哮喘的(1202)从欧洲军团:ECRHS, SAPALDIA, EGEA B58C,面包师和农业工人的调查。基于asthma-specific从2629受试者曾暴露于高分子量(高分子量)过敏原。我们探索了23常见HLA-II等位基因之间的关联和成人哮喘,和测试与职业暴露于高分子量过敏原基因-环境相互作用。交互是rs9273349还测试了。
古典的边际协会HLA-II等位基因和成人哮喘未达到统计上的显著水平。交互之间的检测DPB1 * 03:01等位基因和暴露于高分子量的过敏原(p = 0.009),特别是乳胶(p = 0.01)。在未曝光的集团DPB1 * 03:01等位基因与成人哮喘(或0.67,95%可信区间0.53 - -0.86)。高分子量过敏原暴露没有修改rs9273349协会与成人哮喘。
常见的古典HLA-II等位基因不略与成人哮喘有关。乳胶协会曝光和成人哮喘可能会修改DPB1 * 03:01。
文摘
在分析> 6000年欧洲成年人,古典HLA-II等位基因不与成人哮喘有关http://ow.ly/xTdFm
介绍
高度多态的人类白细胞抗原(HLA)二类分子(博士、DQ和DP)表面的抗原递呈细胞”表示,他们目前的肽外生起源对CD4 t细胞受体+细胞。因为HLA-II关键作用的分子识别的allergen-derived肽,HLA等位基因被广泛研究的假说驱动的候选基因关联研究过敏敏化作用和哮喘(1,2]。HLA也是最评价职业性哮喘的遗传风险因素。虽然结果不一致,的作用HLA-DQB1轨迹在职业性哮喘的病因学是合理的3]。
几个独立的证据全基因组关联研究(GWAS)提供进一步支持HLA-II位点参与哮喘、过敏敏化作用,增加总IgE水平(4- - - - - -11]。加布里埃尔财团进行了最大的哮喘GWAS迄今为止,由365型哮喘患者和16 110控制招募了23个研究[4]。的轨迹集中在rs9273349hla dq区域显示的有力证据协会在整个样本(p = 7×10−14;或1.18 C等位基因)。这是唯一的单核苷酸多态性(SNP)与全基因组意义哮喘发作在16岁以上(p = 4×10−8;或1.26)。有趣的是,一个更明显的效果观察rs9273349 later-onset哮喘的儿童哮喘,尽管并没有显著的差异。最近GWAS复制这个SNP与哮喘和协会也报道尤其是强关联在成人与儿童人口相比6]。
有人建议,调查的HLA基因-环境交互作用可能有助于理解关联发现哮喘GWAS [12]。事实上,协会的力量与哮喘HLA变异可能取决于伴随的环境因素。考虑个人的哮喘发作时可以帮助揭示基因-环境相互作用[13,14]。GWAS的年龄相关性的影响,观察可能提供线索HLA的角色,因为晚发性哮喘可能有不同的底层环境比儿童哮喘的危险因素。在成年人中,职业暴露事件哮喘的一个重要原因,15%左右的人口由于风险(15- - - - - -17]。调查基因-环境HLA等位基因之间的相互作用的影响和职业暴露对哮喘风险可能揭示机制由特定的HLA等位基因和引发的职业感光剂如乳胶、面粉或动物蛋白质。
本研究的目的是进一步调查HLA-II在成人哮喘的作用以人群为基础的和workforce-based研究的荟萃分析。我们估算古典HLA-II从7579个snp等位基因,允许评估HLA-II等位基因之间的联系和成人哮喘。此外,我们探讨是否职业暴露于高分子量(高分子量)过敏原修改的影响估算HLA-II等位基因和rs9273349 SNPhla dq地区从加布里埃尔研究成人哮喘。
方法
人口
我们研究所有欧洲军团都包含在加布里埃尔与职业的详细数据历史:EGEA [18,19],SAPALDIA [20.,21]和ECRHS [15,22](称为“ESE军团”)(23),1958年英国出生队列(B58C) [16,24),和工业群荷兰和丹麦农业工人(农业)25),和荷兰的面包房工人(面包)26]。我们包括嵌套的哮喘病例对照样品(SAPALDIA ECRHS,阿勒和面包店)如前所述[4),所有科目从EGEA B58C与全基因组基因分型数据,职业历史和成人哮喘。成人哮喘被定义为做过哮喘的发作≥16年(4]。那些从未有过哮喘被用作参考。伦理批准了为每个队列从适当的机构伦理委员会。给出详细的队列描述在线补充材料。
基因分型
全基因组基因分型进行了使用数组Human610四面板(美国Illumina公司,圣地亚哥,CA) (4]。更多细节的pcr B58C给出在线补充材料。我们调查是否加布里埃尔的协会与成人哮喘的主要信号(rs9273349)修改了职业暴露。出于完整性的考虑关于GABRIEL HLA-II结果,我们进一步选择的一个子集18标记snp使用Haploview (Broad研究所、剑桥、马、美国)(27),检测基因-环境相互作用与职业暴露于高分子量过敏原(在线补充材料)。
归责的古典HLA-II等位基因
所有军团在目前的分析中,我们使用7579个snp的扩展主要组织相容性复合体(MHC) (20 - 40 Mbp 6号染色体上)来嫁祸于经典HLA类型II级位点在四位数的决议。罪名进行使用小软件(美国华盛顿大学、西雅图、佤邦)的基础上,2767年单体型模式无关的欧洲血统的人(这个参考面板包括B58C科目),如前所述[28]。估算数据之间的一致性和基因分型(Dynal贫SSO化验;表达载体,Carslbad、钙、美国)(29日)是评估DRB1和DQB1等位基因在2310年B58C主题包含在本文不参考面板的一部分小猎犬号罪名(在线补充表E1)。归责质量一般高,常见的等位基因(r2> 0.8)。成对r (D′和连锁不平衡措施2古典HLA-II等位基因和rs9273349之间)和其他18个snp被估计使用Haploview(表E2和E3) [27]。
职业暴露于高分子量过敏原
职业暴露评估详细描述在线补充材料。简单地说,在所有人群,职业与一个asthma-specific从工业化与当地专家重新评估步骤(19]。我们只考虑七个高分子量过敏原高风险物质(即动物蛋白、鱼或贝类、螨虫、乳胶、面粉、其他植物抗原和酶)通过一个类似的,可能会导致哮喘,主要IgE-associated机制。受试者所接触到的任何七高分子量过敏原被归类为“暴露”。未曝光的参照群体包括那些从未接触过任何高风险和低风险的工作。
统计分析
ESE军团被集中提高统计能力和避免收敛问题,就像做过EGEA和ECRHS数据(30.]。原始数据从B58C不能用于汇总分析。我们测试协会23常见的古典HLA-II等位基因与等位基因频率> 5%在每个人口与成人哮喘,假设一个加性遗传模型。在ESE军团,考虑了人口外加剂包括主成分的欧洲内部的多样性不关联分析。遗传效应估计分别在每一个世代,分层的接触状态。整体(exposure-adjusted)基因效应估计的标准固定后果分析ESE暴露,ESE未曝光,B58C暴露和B58C未曝光的科目。评估基因-环境相互作用,导致暴露和未曝光的主题从ESE B58C通过固定后果结合起来分析获得的优势比暴露和未曝光的团体。标准1自由度(df)测试基因-环境相互作用和边际2 df联合测试的遗传效应和基因-环境交互进行,后者通常被认为有更大的权力比边际测试时表达的遗传效应只是暴露个人(31日,32]。额外的分析包括荟萃分析工业群的高分子量过敏原暴露工人,和执行互动的联合测试和测试。工业军团并不包括评估边际遗传效应,因为所有的科目在这些人群被暴露,因此,交互效应不能被认为是独立于只面对优势比。我们没有调整之前的多个测试,因为HLA-II参与几个GWAS的证据。相反,我们使用的假定值阈值< 0.01的测试边际协会联合测试和测试交互。给出更多的细节在网上补充材料。
结果
高分子量的描述性特征过敏原暴露和被曝光的归纳了研究对象表1。主题与儿童哮喘发病的年龄(n = 685)或失踪(n = 59)被排除在数据分析,使数据从6025例进行分析。乳胶是一般人群的主要科目中职业暴露人群被归类为高分子量过敏原暴露在SAPALDIA B58C暴露(从64%至84%)。职业暴露于高分子量与成人哮喘的过敏原呈正相关在一般人群的四个军团,固定后果总结优势比为1.33 (95% CI 1.11 - -1.60) (图1)。
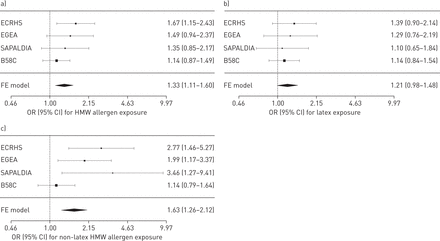
森林图的优势比和95%置信区间为协会的职业暴露)高分子量(高分子量)过敏原,b)乳胶和c)高分子量与成人哮喘的过敏原除了乳胶在ECRHS EGEA, SAPALDIA B58C。摘要优势比计算使用固定后果分析(FE模型)。
表2协会测试结果显示23估算古典HLA-II等位基因,rs9273349 C / T,成人哮喘在ESE B58C军团。边际HLA-II等位基因关联不显著(p > 0.01),但rs9273349,正如预期的那样,与成人哮喘的显著相关(或T等位基因0.82,p = 0.002)。
rs9273349与成人哮喘之间的关系类似于暴露和未暴露的个人(测试基因-环境相互作用p = 0.95)。为DPB1 * 03:01联合测试统计上显著的交互(p = 0.007, p = 0.03)。在未曝光的个体,DPB1 * 03:01与成人哮喘的风险降低(或0.67,p = 0.002),但不接触学科(或1.08,p = 0.64)。一些具体的估计表明,ESE军团是由的交互(或暴露1.34,p = 0.20;或未曝光的0.62,p = 0.0009)。在ESE受试者携带至少一个DPB1 * 03:01等位基因,与成人哮喘的科目的比例高于那些暴露于职业高分子量在未曝光的过敏原(35.6%)和低(15.0%),而同一团体ESE非携带者(分别在暴露和未曝光的28.4%和22.2%;图E1)。因此,在这些军团,更强的关联成人哮喘和职业高分子量过敏原检测至少一个运营商DPB1 * 03:01等位基因(或3.13,95% CI 1.87 - -5.23)比非携带者(或1.39,95%可信区间1.08 - -1.81)。在B58C,DPB1 * 03:01没有与哮喘有关,无论暴露状态(或暴露0.84,p = 0.48;或未曝光的0.89,p = 0.62)。协会DPB1 * 03:01和rs9273349成人哮喘是独立的:每个遗传多态性的影响并没有改变,当两人都共同纳入一个多元回归模型。
高分子量的过敏原接触工业军团(阿勒和面包店的荟萃分析),DPB1 * 03:01不是与哮喘相关(表3)。然而,基因-环境相互作用的试验DPB1 * 03:01和高分子量曝光后更重要的包括工业军团一起的以人群为基础的群组分析(p = 0.009)。协会的等位基因DQB1 * 06:02与哮喘(p = 0.007)仅限于工业群,与类似的效果在农业工人(或0.72,p = 0.05)和面包房工人(或0.65,p = 0.07)。
作为大多数暴露对象的大众人群暴露于乳胶,执行一个额外的灵敏度分析在ESE和B58C,通过测试基因-环境相互作用的两个相互排斥的暴露组:“有没有接触乳胶”和“接触高分子量过敏原,但从来没有乳胶”,与未暴露的参照组(表E4和E5)。之间的基因-环境相互作用DPB1 * 03:01和整体高分子量曝光只是观察到乳胶暴露与未曝光的主题互动(p = 0.01)。因此,在ESE受试者携带至少一个DPB1 * 03:01等位基因,一个强大的乳胶接触和观察成人哮喘之间的联系(或3.12,95%可信区间1.73 - -5.65)。
联系HLA-II地区18个标记snp和成人哮喘相似在职业性暴露和未暴露的个人(交互p > 0.05;表E6)。
讨论
在欧洲军团的荟萃分析中,我们没有发现证据表明常见HLA-II等位基因与成人哮喘的风险。然而,当分析被职业高分子量过敏原,分层DPB1 * 03:01等位基因似乎与成人哮喘相关负面未曝光的主题,和之间的相互作用被发现DPB1 * 03:01和接触乳胶。DQB1 * 06:02显示一致的逆与哮喘协会群面包房工人和农业工人,而不是高分子量过敏原暴露从普通人群的研究主题。
我们表明,rs9273349,苏格兰民族党hla dq地区从加布里埃尔GWAS [4),在同等程度上影响成人哮喘在高分子量过敏原暴露和未曝光的职业人。因此,没有发现证据表明职业过敏原暴露可能参与rs9273349协会,或任何其他的18所选标记snp HLA-II地区和成人哮喘。rs9273349与成人哮喘合并ESE显著相关,B58C研究(或0.82,p = 0.002)。我们也计算这个协会其他GABRIEL成人群体,并不包括在本研究由于没有详细的职业历史信息,显示相似的结果(或0.80,p = 0.001)。我们已经证明rs9273349区域扩展的连锁不平衡(D′)所显示的那样,包括DRB1,DQA1和DQB1,但不DPA1或DPB1。然而,没有一个古典HLA-II等位基因与rs9273349 (r有紧密的关联2= 0.00 - -0.32;表E2和E3)和rs9273349协会信号不是解释为古典HLA-II等位基因在多个回归模型。尽管描述过敏原HLA-II分子识别的作用,目前还不清楚rs9273349协会与成人哮喘可能意味着。它可以推测这个SNP可能会影响HLA分子的表达水平。另外,non-HLA基因可以扮演一个角色。MHC是最复杂的地区之一的人类基因组,广泛的连锁不平衡,跨越了数以百计的HLA与non-HLA基因。连杆和HLA变异和哮喘之间的联系可能部分是由于附近non-HLA基因之间的联系在连锁不平衡(HLA)和哮喘,例如TNFA(33]。后者的解释意味着不同的机制的作用,这也解释了为什么我们没有发现一个互动rs9273349和职业接触过敏原。
我们的研究人群是足以揭示温和的古典HLA-II等位基因之间的关联和成人哮喘,和完整的没有边际协会可能不是由于缺乏统计力量。当考虑到职业暴露,携带DPB1 * 03:01似乎防止成人哮喘在未曝光的个人。然而,在ESE携带DPB1 * 03:01等位基因,一个强大的积极联系接触乳胶和观察成人哮喘(> 3)。这一发现表明,DPB1 * 03:01可能带来在成年后罹患哮喘的风险增加,但只有那些与特定的工作场所的风险敞口。我们只能推测一个相反的效果背后的机制未曝光。更好的防止呼吸道感染或过敏的发展对其他抗原成分。一个德国的病例对照研究调查的作用hla dq和HLA-DR(但不HLA-DP)在269年卫生保健工作者和乳胶过敏和90年nonatopic对照组(34]。DRB1 * 04 / DQB1 * 03:02单体型与风险增加有关的IgE主要乳胶过敏原(戊肝病毒b 6.02) (34]。我们还发现积极的,但不显著,协会DRB1 * 04:01和DQB1 * 03:02与成人哮喘在我们1123 latex-exposed工人。只有少数其他研究研究HLA等位基因与哮喘或过敏结果工人暴露于高分子量过敏原,即实验动物过敏原(35),牛皮屑(36和鱼的食物37]。DQB1 * 06:02,这里与哮喘在面包房工人和农业工人,没有摆脱这些其他的研究。
研究大规模基因-环境相互作用的研究有一些固有的局限性。人口抽样的一般人群(或哮喘病人和他们的家属如EGEA),职业有很大的异质性和相关风险敞口。大多数工人列为“暴露于高分子量代理”latex-exposed医疗专业人士通常暴露于其他代理,如清洁产品,可能会导致哮喘通过non-IgE介导机制(38]。尽管曝光的异质性,职业暴露于高分子量过敏原之间的关联和成人哮喘可比在军团和显示显著增加风险,类似于早些时候出版协会(级15,16,19]。在目前B58C样本,高分子量的曝光和哮喘协会似乎弱于出版协会早些时候在一个更大的样本B58C [16]。这种差异似乎是由于偶然变异,随着优势比B58C样本之间没有显著差异,没有可用的基因。
男性的比例中暴露的科目在SAPALDIA低(12%)和ECRHS(14%)比EGEA(29%)和B58C (33%)。ESE暴露组之间的联系DPB1 * 03:01和成人哮喘在男性更为明显(或2.71,p = 0.055)比女性(或1.18,p = 0.52),但交互作用不显著(p = 0.18),由于小样本大小。本协会没有ESE未曝光的男性和女性之间的差异。workforce-based研究也不同于以人群为基础的群组曝光,表型和比例的男性受试者。因此,我们进行了单独的分析在以人群为基础的群组和暴露在所有科目。还在workforce-based军团,异质性来源,性质和水平的过敏原暴露存在。面包房工人可以暴露于过敏原过敏酶和面粉,还要清洁产品,而农业工人(如。种粮农民和奶农)可能暴露于过敏原从动物皮屑,存储螨虫、谷物和面粉。农业环境中的各种风险,如木糖醇,消毒剂,也与(nonallergic)哮喘有关。协会DQB1 * 06:02与哮喘之间面包师和农民可以提供进一步解释为什么这些工人呼吸健康发展问题,而其他具有类似暴露水平保持健康(39]。
在这种大规模的荟萃分析,我们不能学习特定的IgE职业过敏原(如。乳胶、小麦和α-amylase)或者临床评估职业性哮喘表型。相反,我们使用成人哮喘,一直与高分子量过敏原接触(图1在GWAS)和rs9273349。我们旨在进一步研究HLA在GWAS信号,因此,我们决定不包括其他哮喘表型或在本研究过敏性敏化作用。虽然很大一部分成人哮喘是由于职业暴露,其他危险因素,触发器和并存状况如吸烟,雌性激素、呼吸道感染和肥胖也与成年哮喘的发展(40]。HLA-II大部分这些决定因素的相关性,然而,不太明显。
总之,估算常见HLA-II等位基因并不相关本身与成人哮喘的荟萃分析欧洲军团。然而,当考虑到职业过敏原暴露,结果呈负相关性DPB1 * 03:01和adult-asthma未曝光,建议之间的基因-环境相互作用DPB1 * 03:01等位基因和乳胶。此外,DQB1 * 06:02与哮喘在面包房工人和农业工人,暗示作用为特定职业过敏原。职业高分子量过敏原暴露没有修改rs9273349之间的关联,苏格兰民族党hla dq从加布里埃尔GWAS的地区,成人哮喘。
确认
作者的从属关系如下。上午Lidwien Smit:分工环境流行病学、风险评估科学研究所(ira)、乌得勒支荷兰;大卫·p·斯特:人口健康科学和教育部门,圣乔治伦敦大学,伦敦,英国;Roel Vermeulen:分工环境流行病学、风险评估科学研究所(ira)和朱利叶斯健康科学中心和初级保健,乌特勒支大学医学中心,乌特勒支,荷兰;保罗:他I.W. de朱利叶斯健康科学和初级保健中心和分子医学研究所,乌特勒支大学医学中心,乌特勒支,荷兰;佛罗伦萨Demenais: INSERM U946,巴黎狄德罗大学,巴黎索邦神学院引用,大学医疗研究所d 'Hematologie,巴黎,法国;Orianne杜马斯:INSERM、流行病学与人口健康研究中心(CESP) U1018,呼吸和环境流行病学的团队,和巴黎Sud 11日umr 1018年,瑟法;Anne-Elie Carsin:环境流行病学研究中心(来),市医学研究所(IMIM-Hospital del Mar)和cib Epidemiologia y祝您健康上市(CIBERESP),巴塞罗那,西班牙;保罗克利兰:职业和环境医学部门,国家心肺研究所,帝国理工学院、伦敦、英国;伊凡Curjuric:瑞士热带和公共卫生学院和巴塞尔大学,巴塞尔瑞士; Rebecca E. Ghosh: Respiratory Epidemiology and Public Health Group, National Heart and Lung Institute, and Small Area Health Statistics Unit, MRC-PHE Centre for Environment and Health, Imperial College, London, UK; Dick Heederik: Division of Environmental Epidemiology, Institute for Risk Assessment Sciences (IRAS), Utrecht, The Netherlands; Medea Imboden: Swiss Tropical and Public Health Institute, and University of Basel, Basel, Switzerland; Deborah Jarvis: Respiratory Epidemiology and Public Health Group, National Heart and Lung Institute, Imperial College, London, UK; Mark Lathrop: Commissariat à l’Energie Atomique, Institut de Génomique, Centre National de Génotypage (CNG), Evry, France, and McGill University, Montreal, QC, Canada; Nicole Le Moual: INSERM, Centre for Research in Epidemiology and Population Health (CESP), U1018, Respiratory and Environmental Epidemiology Team, and Université Paris Sud 11, UMRS 1018, Villejuif, France; Amar Mehta: Swiss Tropical and Public Health Institute, and University of Basel, Basel, Switzerland, and Harvard School of Public Health, Dept of Environmental Health, Boston, MA, USA; David Miedinger: University of Basel, Basel, and Swiss Accident Insurance Fund (Suva), Lucerne, Switzerland; Torben Sigsgaard: Dept of Environmental and Occupational Medicine, Aarhus University, Aarhus, Denmark; Valérie Siroux: INSERM, U823, and Université Joseph Fourier, Grenoble, France; David Vernez: Institute for Work and Health, Lausanne, Switzerland; Jan Paul Zock: Centre for Research in Environmental Epidemiology (CREAL), CIBER Epidemiologia y Salud Pública (CIBERESP), and Universitat Pompeu Fabra (UPF), Barcelona, Spain; Francine Kauffmann: INSERM, Centre for Research in Epidemiology and Population Health (CESP), U1018, Respiratory and Environmental Epidemiology Team, and Université Paris Sud 11, UMRS 1018, Villejuif, France; Nicole Probst-Hensch: Swiss Tropical and Public Health Institute, and University of Basel, Basel, Switzerland; Manolis Kogevinas: Centre for Research in Environmental Epidemiology (CREAL), Municipal Institute of Medical Research (IMIM-Hospital del Mar), and CIBER Epidemiologia y Salud Pública (CIBERESP), Barcelona, Spain, and National School of Public Health, Athens, Greece; Emmanuelle Bouzigon: INSERM, U946, and Université Paris Diderot, Sorbonne Paris Cité, Institut Universitaire d’Hématologie, Paris, France.
我们感谢所有的研究成员和员工参与每个队列的数据收集。对于1958年的出生队列,asthma-specific从工业化应用的专家重新评估一步英国专家在职业性肺部疾病(保罗•克利兰大卫斐(工作场所健康中心、谢菲尔德、英国),珍妮弗·霍伊尔(北曼彻斯特总医院,曼彻斯特,英国)和克里斯•沃伯顿(北曼彻斯特总医院,曼彻斯特,英国))。进一步确认了在线补充材料。
脚注
可以从本文的补充材料www.www.qdcxjkg.com
支持声明:这个基因-环境相互作用分析支持伊阿古anr - 2010中扼要介绍- 003,和荷兰科学研究组织(NWO) /法国外交部和欧洲事务梵高French-Dutch合作项目。的pcr ESE和工业群,和部分B58C由GABRIEL哮喘遗传财团支持的合同来自欧盟委员会(018996年)和法国的资助研究、英国威康信托基金会(WT084703MA)、哮喘和小马的基础。B58C,英国哮喘提供资金asthma-specific从编码的职业暴露和调查对哮喘,和小马基金会提供资金扩展的工作看其他过敏的结果。进一步的资金来源为军团有参与在线补充材料。资助者都没有任何作用,研究设计、数据收集和分析或制备的手稿。
利益冲突:披露可以找到与本文的在线版本www.www.qdcxjkg.com
- 收到了2014年4月9日。
- 接受2014年6月9日。
- ©2014人队















