摘要
职业暴露是一种公认的哮喘可修正的危险因素,但尚未研究职业暴露和哮喘控制之间的关系。我们旨在研究来自欧洲社区呼吸健康调查(ECRH)的工作年龄成年人之间的协会。
7077名参与者的数据可用(平均年龄43岁,45%从不吸烟,5867人没有哮喘,1210人目前有哮喘)。使用logistic和多项回归评估了特定哮喘源的职业暴露与哮喘控制状态(根据全球哮喘倡议指南,有33%的人哮喘未控制)之间的关联,并根据年龄、性别和吸烟状况进行了调整,研究区域作为随机效应纳入。
在不受控制的成人发作哮喘和过去12个月和10年内接触任何职业哮喘(或(95%CI)1.6(1.0-2.40)和1.7(1.2-2.5)之间的统计学上显着的阳性缔缔吻期;高(1.7(1.0-2.8)和1.9(1.3-2.9))分别和低(1.6(1.0-2.7)和1.8(1.2-2.7)分子量剂;和清洁剂(2.0(1.1-3.6)和2.3(1.4-3.6)),长期暴露有更强的关联。这些关联主要是由哮喘控制的加剧结构域解释,并且在哮喘和部分控制的哮喘之间没有观察到缔合。
这些结果表明,职业暴露asthmagens与不受控制的成人哮喘有关。职业危险因素,应迅速识别,防止不受控制的哮喘。
摘要
职业暴露于哮喘服与Ecrhs II中的不受控制的成人发病哮喘有关http://ow.ly/reN8g
介绍
从以人群为基础的角度研究哮喘有助于更好地理解临床疾病表现的决定因素,包括职业风险因素[1-3.]。尽管哮喘严重程度(反映疾病的内在严重程度)和哮喘控制(反映疾病在短时间内的活动)这两个不同概念的重要性,但所应用的术语常常可以互换使用,且不具有标准化[4]。哮喘严重程度是困难的流行病学定义[4那5],所使用的定义并不总是恰当的[3.]。最近的指导方针已经从严重程度的概念转移到更多地关注哮喘控制[3.那4]。
研究哮喘控制已经主要在临床研究和大量人口的流行病学研究进行了评估以全面的方式哮喘控制。以下全球哮喘(GINA)指南多维尺度已经被应用在流行病学定义的哮喘控制两者欧洲共同体呼吸健康调查(ECRHS)和哮喘的遗传与环境法国流行病学研究(EGEA)6-10.]。在分类量表,结合日和夜间呼吸道症状,哮喘发作,活动受限,肺功能,加重哮喘控制的这项措施,尚未正式生效。然而,哮喘控制的,通过在临床环境GINA专家意见进行评价分类是类似于从具体控制分数问卷[11.那12.]。流行病学结果还支持这种控制规模的有效性[7]。几个流行病学研究已经评估哮喘控制的环境危险因素[6那8]。例如,研究发现,家庭接触喷雾剂和空气污染与控制不良的哮喘有关[6那9]。
职业性暴露于哮喘原(包括>350制剂)是一个可改变的哮喘危险因素,涉及多达15%的成人发病哮喘病例[1]。与工作有关的哮喘通常被归类为职业性哮喘,由在工作中接触药剂引起(出现在成年期)或因工作而加重的预先存在的哮喘[2]。在EGEA调查中[5]在成人发作哮喘中职业暴露与哮喘严重程度的职业暴露和哮喘严重程度之间发现了强烈关联。由于工作导致的哮喘恶化开始受到增加的关注[2]。通过反映该疾病急性和慢性活动的各个方面评估职业性暴露在不受控制的成人哮喘中的作用,尚未进行研究。
基于ECRHS中用于哮喘控制的特征明确的可用数据[10.]和职业接触哮喘[13.],本分析的主要目的是调查过去12个月和10年对特定哮喘源(包括高分子量和低分子量(分别为HMW和LMW)致敏剂和刺激物)的职业暴露与成人发作的不受控哮喘之间的关系。
方法
研究设计
ECRHS是一项多中心的一般人群研究(www.ecrhs.org).基线研究(ECRHS I)于1991年至1993年进行,如前所述[14.那15.]。简而言之,联系了20-44岁年龄较大的个体的随机样本,以完成呼吸系统症状的短筛选问卷。在第二步中,邀请整个组的20%随机样品和呼吸道症状的亚群(参见在线补充材料)完成第二次详细问卷并进行临床检查(肺功能测试,包括肺活量测定法和非特异性支气管反应性测试)。
来自14个国家的29个中心的ECRH I的参与者被邀请到1998年至2002年间的后续调查(ECRHS II),并完成面对面的问卷(关于哮喘,呼吸道症状的精确信息职业历史)和临床检查(肺功能测试和血液样本)[13.那16.]。收集的信息包括年龄,吸烟状态(从不,前或目前的吸烟者),体重指数(BMI)(超重:BMI≥25千克·m-2),使用吸入的皮质类固醇(IC),哮喘控制和敏化对常见过敏原(见在线补充材料)。常见过敏原的致敏定义为特定的血清IgE抗体,以至少一项常见的过敏原(房屋粉尘,猫,蒂莫西草或枝孢属herbarum),浓度≥0.35 U·mL−1.根据基线1秒用力呼气量(FEV)1),根据Q的参考值uanjer等.[17.],参与者被归类为“与”(<80%的预测值)或“没有”低fev1.支气管高反应性(BHR)定义为最大FEV下降1对≤1 mg的甲胆碱剂量,其生理盐水后值≥20%。随访患者的总有效率为~ 65%。这项分析仅限于来自12个国家26个研究中心的ECRHS II参与者[10.那13.]。这些信息用于评估曾经使用的参与者的哮喘控制和职业暴露,以及性别,年龄,吸烟习惯和当前哮喘的可用数据(n = 9019)。排除1942年参与者,796来自富集的样品(所有没有当前哮喘的个体)和来自随机样品的1146(具有过去的哮喘(n = 167)或没有电流哮喘,但在ECRHS II中有哮喘症状或治疗(n = 979)),分析是在7077名参与者(1210带目前哮喘和5867,而不是哮喘的5867)进行分析(而是1).
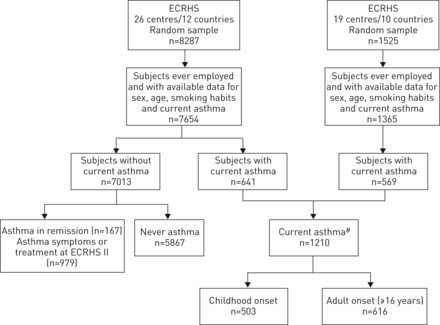
欧洲共同体第二次呼吸健康调查选定人口的流程图。#: 91例哮喘发病年龄缺失值。
哮喘
参与者随机样本的分类为“永不哮喘”(n = 5867)如果他们从未报道医生诊断哮喘(ECRHS我和ECRHS II)或任何电流会(气喘或吹口哨不感冒或气短吵醒攻击),和没有使用哮喘药物ECRHS II。随访时,参与者按既往定义分为“当前哮喘”(n=1210) [10.那18.]如果他们报道了医生诊断哮喘,如果在过去的12个月内,他们报告呼吸系统症状(喘息,夜间胸闷,活动后的呼吸攻击后,在休息或夜间,或至少有一个哮喘发作)或使用ECRHS II中的哮喘药物。如前所述azzoletti等等。[10.],将目前有哮喘的参与者分为:1)如果存在以下所有特征:日间症状少于一周一次,无夜间症状,无哮喘发作,短效β2在过去的3个月内每周两次或多或少以上,没有活动(工作或其他活动)限制,并且在过去12个月和FEV中没有使用口腔类固醇1≥80%pred;2)如果不存在对照的上述一个或两个特征,部分控制的哮喘;3)不受控制的哮喘如果哮喘,呼吸急促或喘息率引起了过去12个月的医院/应急录取,口服皮质类固醇在短期课程或过去12个月内不断使用,受试者有12个哮喘袭击(超过一个)一周)在过去的3个月内,或上面列出的3个以上的受控哮喘功能缺席(见在线补充材料)。
我们将首次发病年龄≥16岁的成人哮喘定义为(参见在线补充资料)。对于包括发病年龄在内的分析,91名参与者被排除在外,原因是该变量的两项调查的值缺失或反应不一致。
职业暴露评估
在过去的12个月和10年的职业暴露中到22名代理商(18个类别的哮喘,患有高风险哮喘和四类先验“非活泼”代理[5]分类在低风险哮喘(参见在线补充材料))通过特定哮喘作业曝光矩阵(JEM的应用被分配)(cesp.vjf / inserm.fr / asthmajem)19.],然后是专家重新评估步骤,如其他地方所述[13.]。非哮喘性药物的分类[5,特别是对于可能接触刺激物的情况。研究了职业性暴露与哮喘控制之间的关系:1)暴露于任何哮喘源;2)三大类哮喘药(HMW剂、LMW剂和混合暴露或刺激峰);3)≥5%的受试者暴露于特定哮喘源(乳胶、高活性化学品和工业清洁化学品);4)仅使用非哮喘源(不暴露于哮喘源),参与者被归类为非暴露于哮喘源的参照类别。
分析策略
具体的假设已经过测试。1)不受控制的哮喘与职业暴露于哮喘,包括暴露于HMW剂,LMW剂和清洁剂,但不是先验确定的非哮喘致敏剂[5那19.]。2)预期这些协会对成人发作哮喘,但为儿童发病哮喘而言是意外的[5]。还进行了其他分析,以评估职业暴露与四个哮喘控制域(肺功能、症状、恶化和活动限制)之间的关联[6那8在哮喘控制定义中不包括加重范围。为了检查我们主要报告结果的一致性,分析按照BMI、吸烟习惯、性别和对常见过敏原的敏感性进行了分层,正如之前所建议的[13.那20.]。
使用多项逻辑回归测试职业暴露和哮喘控制之间的关联。没有任何哮喘历史的参与者作为具有受控,部分控制和不受控制的哮喘是标称结果类别的指称类别。所有与P≤0.05的关联都被认为是统计学意义的。使用Q统计,评估各地地区(英语(英国和美国),北部,中央或南部地区的潜在异质性。调整所有分析的年龄,性别和吸烟地位,随着随机效应包括的区域[21.]。在线补充材料中描述了其他附加分析。
结果
参与者的平均年龄为43岁,45%为不吸烟者和17%的电流哮喘(表E1)。更多的女性比男性报告当前哮喘,尤其是对于成人发作哮喘(P <0.001)。女性更容易接触到职业asthmagens比男性(21.1%与(表E1),尤其是清洁剂(8.8%)与分别为0.8%;P <0.001);在目前患有哮喘的参与者中,儿童期发病的哮喘患者平均年龄更小,受教育程度更高,目前吸烟者较少,对普通过敏原和BHR的敏感性高于成人发病的哮喘患者。在患成人哮喘的参与者中,分别有30%和40%的哮喘未得到控制和部分得到控制(表1).根据对照定义,随着加剧的参与者总是被归类为不受控制的,并且具有不受控制的哮喘的人更常用的皮质类固醇并具有更多的症状。为儿童发育哮喘观察到类似的趋势(表E2)。
对于儿童期发病哮喘,哮喘控制与过去12个月和10年职业暴露之间没有观察到关联,或<1(表2和表E3)。
对于成人发作的哮喘,在过去的12个月职业暴露于任何哮喘,HMW和LMW哮喘和清洁剂和清洁剂和不受控制的哮喘之间观察到统计学上显着的联合。表2).在家庭宠物或敏化以敏化以常见过敏原(未示出)进行调整后,结果非常相似。我们对所使用的IC进行分层进行了额外的分析。在考虑ICS用户(或(95%CI)1.6(1.0-2.8))和非用户(1.4(0.7-2.9))时,过去12个月哮喘暴露和不受控制的哮喘之间的关联和不受控制的哮喘之间的幅度相似。对于其他特定的哮喘或者没有任何关联或先验非哮喘性刺激物(低哮喘风险)和无法控制的成人哮喘(表2).
在过去10年的职业暴露和成人哮喘控制之间进行的分析显示了更强的相关性(表3).没有观察到显著的异质性,当我们按面积进行了荟萃分析(而是2).然而,过去10年的职业暴露asthmagens和不受控制的哮喘之间的关联是更强的三个地理区域(英语,北欧和中欧)。观察过去12个月的职业暴露asthmagens类似的趋势(未显示)。职业暴露于HMW剂和清洁剂和不受控制的成人发作哮喘之间观察到间正常体重的参与者和非吸烟者中(图E1)更高的比值比。比值比分别为男性和女性暴露于HMW剂类似,但对于LMW剂,包括工业清洗剂,只观察到女性显著关联。关于宣传,以常见的过敏原(图E1),在用于暴露于HMW剂敏化的参与者和nonsensitised参与者暴露于LMW剂,包括工业清洗剂,观察到更高的比值比。观察过去12个月的职业暴露类似的趋势(未显示)。
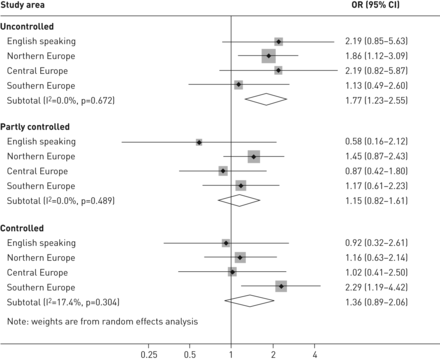
按地理区域进行的荟萃分析结果:10年暴露。调整年龄,性别,吸烟习惯和国家(随机效应)。从未患过哮喘的参与者为参照组。暴露于非哮喘源或暴露于哮喘源的参与者与未暴露于哮喘源的参与者进行比较。
在分别研究职业暴露和成人发病哮喘控制的每个结构域之间的关联时,仅针对恶化领域观察到的显着关联(表4).此外,HMW药物暴露12个月与口服糖皮质激素治疗的成人哮喘显著相关(OR (95% CI) 2.7(1.1-6.3))。哮喘、低分子量和工业清洗剂的OR (95% CI)分别为1.8(0.8-4.0)、0.6(0.1-2.6)和1.1(0.2-4.8)。进一步的分析不包括哮喘控制定义中的加重域(当前临床控制域)(表3).观察到12个月职业暴露的不可显着的关联观察到较低的差距,而每组哮喘的10年职业暴露和不受控制的哮喘则观察到显着的联合。
不受控制的成人哮喘的人群归因危险度为12个月的接触asthmagens为9.4%。
讨论
我们的研究显示,在一项以人群为基础的大型研究中,职业性暴露于哮喘原与不受控制的成人发病哮喘相关。与当前的职业暴露相比,长期暴露的相关性更强。观察到的与哮喘不控制的相关性主要是由哮喘控制的加重域解释的。我们的研究结果表明,暴露于致敏剂和刺激物都与哮喘失控和恶化有关。由于过去12个月的职业暴露而导致的不可控哮喘的人群归因风险为9%,约为成人发病哮喘总体人口归因风险的一半[1]。
我们研究的优势是使用的三级哮喘控制量表,其通过整合疾病的几个维度以综合评估,以及评估患有哮喘特异性的JEM的职业暴露于哮喘。其他优势是结果的特异性,没有与之相关的先验非哮喘致敏剂和哮喘与成人发病哮喘的强相关性。
在ECRHS II中,发现职业接触粉尘、气体和烟雾(由ALOHA JEM评估)与严重哮喘恶化之间存在显著关联[21.]。在目前的分析中,我们通过哮喘特异性JEM结合专家审查步骤评估了特定哮喘源的职业暴露[13.那19.]。由不了解疾病状况的专家重新评估,确保了方法的客观性。为了限制误分类的错误,倾向于特异性;只有当某项工作中有相当数量的受试者暴露于哮喘原的概率很高时,该工作才被归类为暴露于哮喘原[19.]。没有证据表明在工作经历中存在回忆偏见[22.,但我们没有意识到错误的分类错误,特别是10年的曝光。这种方法比自我报告的暴露更不容易产生偏见[23.]并给出了暴露在asthmagen可靠的估计[5那13.那19.]。哮喘特异性JEM旨在评估对导致哮喘的物质的暴露,但在评估对加重哮喘的物质的暴露时可能不太合适。然而,暴露在低风险的哮喘可能是工作加重哮喘的危险因素。在目前的分析中,我们研究了与工作相关的哮喘,因为我们不能区分这两个实体(职业性或工作加重的哮喘)。OR<1与儿童期哮喘缺乏相关性,与健康雇佣工人效应一致[24.]。此外,最近的一项研究表明,患有儿童期哮喘的人往往比没有哮喘的人具有更高的教育水平[25.],这一发现也是在我们的研究中观察到。因此,这些人可能会少在成年期,这与我们的研究结果一致暴露。
观察过去10年比成人发病不受控制的哮喘,在EGEA一个报告发现一致过去12个月的职业暴露强商会研究长期暴露于空气污染[6]。这种现象可能是由于长期接触哮喘原可能直接导致哮喘失控或更严重的疾病[5那26.]。在EGEA中,哮喘源的职业暴露与严重的成人发病哮喘相关,但与轻度哮喘无关[5]。成人哮喘缓解率很低,如果发病数年后仍未缓解,则该病倾向于慢性发作[27.那28.]。目前成人发作的哮喘与残疾有关[29.]。大多数不再接触病原的工人仍有持续的症状和BHR [26.]。职业性哮喘的预后可通过早期完全消除暴露得到改善[30.]。因此,由于持续暴露,与工作相关的哮喘可能更容易得到控制。哮喘患者目前可能在工作或接触较少,因为活动限制被用来评估未控制的疾病。调查10年的职业暴露可以减少这种偏差,但不能完全消除这种偏差,除非只对在随访期间工作的参与者进行研究。因此,我们的结果可能被低估了。
我们首次根据GINA指南(2006-2010年)调查了不受控哮喘与职业暴露的相关性。然而,可以认为,由于在EGEA中有关哮喘活动和治疗的信息有限,来自EGEA的发现可能反映了职业性暴露与哮喘失控之间的关系,而不是严重程度[5]。在EGEA中,病例是从胸部诊所招募的,那里的哮喘可能比一般人群更严重。在两项调查中均观察到一致的结果,但EGEA的优势比要高得多,置信区间较大[5]。在ECRHS,少数受试者暴露于可能已经感兴趣的具体危害(面粉和二isocyanantes(<科目1%暴露)),这是我们分析的限制。暴露于清洁剂,我们的结果与国内曝光之间观察到的那些清洁喷雾剂和控制不佳的哮喘是一致的[9]。
与观察到的生活质量或空气污染与哮喘控制之间的关系相反[6那7],关联asthmagens之间观察到并且部分地控制哮喘不是在两者之间的那些具有受控哮喘和哮喘不受控制观察。此不存在对哮喘的控制趋势的假设是,对于不受控的哮喘中观察到的关联,主要是由于加重其不是部分地控制哮喘的定义的一部分。哮喘控制由两个主要结构域组成:1)缺乏障碍(没有症状,最低治疗用途,正常活动水平和肺功能水平)的;和2)缺乏的未来风险的病人(无哮喘加重的,预防的随时间的肺功能加速下滑并从药物没有副作用)4那11.]。有人建议,恶化应与当前的临床控制分开考虑,因为即使患者目前对症状有充分的控制,活动限制很少,它们也可能发生[4]。工作引起的哮喘加重尚未被广泛报道;然而,这可能是职业环境中的一个关键问题[2]。我们对恶化的定义包括医院/应急录取以及在过去12个月内或不断使用口腔皮质类固醇的使用[10.]。连续使用口服皮质激素也可被认为是哮喘的严重程度的标志。在以前的研究中,加重了只有住院或急诊方面[定义31.]或除了“在需要时使用口腔皮质类固醇”以评估严重的加剧[21.]。在ECRH中,加剧的各个方面似乎与司法人有关的职业暴露[21.]。关于流行病学研究中哮喘加剧定义的标准化需要更多的工作。
我们分析的进一步强度是我们的研究结果的一致性。职业暴露和不受控制的哮喘之间的关联未被性别,吸烟习惯,BMI或对常见过敏原的敏化进行修饰,尽管在非闻人和女性中观察到更强的联合。暴露于LMW代理人在没有敏感的情况下,在参与者中不受控制哮喘的风险增加了一倍,而暴露于HMW代理人的风险将增加了致敏的风险。这些结果与上一个报告一致[32.]。我们的研究结果表明,超重的参与者不职业照射比低BMI更容易,如之前的空气污染建议[6]。职业暴露asthmagens和不受控制的哮喘之间的关联似乎是由三个地理区域(英语(英国和美国),北欧和中欧),这可能部分是主要驱动因哮喘未控制的欧洲[普遍存在的异质性10.]或对地理区域的职业暴露,药物措施或其他未测量相关的区域差异。
该研究具有潜在的局限性(横断面研究和中心不能代表国家的),如先前所讨论的[10.]。哮喘控制可能很难在流行病学中定义,尽管这种控制量表的有效性得到了流行病学结果的支持[7那10.]。尽管所有哮喘源(哮喘的已知危险因素)和未控制的哮喘之间的关联都是根据先验假设[5那6那8那13.],也可以这样说,我们就具体asthmagens结果需要谨慎的解释是由于多重检验[33.]。
我们的研究表明,在不受控制的成人哮喘发病中,职业性暴露于哮喘源具有强烈的有害影响。这些结果与假设一致,即职业性暴露于哮喘源可以迅速导致哮喘失控[5]。我们观察到与部分控制的哮喘无关,这与前一个哮喘严重程度的结果一致[5]。将暴露于LMW和HMW剂和清洁剂似乎与不受控制的哮喘有关。职业暴露是可预防的风险因素,最近强调了预防的重要性[21.那30.那34.]。预防哮喘加重,一个重要的哮喘控制域[4那11.,因为严重哮喘加重与肺功能加速衰退有关[2]。此外,哮喘失控与较差的健康相关生活质量有关[7]。重要的是要迅速识别潜在的职业危险因素,并尽快减少这些暴露,以防止不可控的哮喘。
致谢
作者的隶属关系如下。N.Le Moual:Inserm,流行病学研究中心和人口健康(CESP),U1018,呼吸和环境流行病学,Villejuif和Paris Sud,UMRS 1018,Villejuif,法国;A-e。Carsin:环境流行病学研究中心(CREARO),巴塞罗那,医院德尔MAR医学研究所(IMIM),巴塞罗那和CIBEREPIDEMIOGíaYSSaludPública(Ciberesp),巴塞罗那,西班牙;V. Siroux:Inserm,U823,Albert Bonniot中心,环境流行病学应用于复制和呼吸健康,格勒诺布尔和大学Joseph Fourier,Grenoble,法国;K. Radon:Ludwig-Maximilian,大学慕尼黑,德国慕尼黑大学职业,社会和环境医学研究所;D.诺特·诺特:乌普萨拉大学医学院,瑞典乌普萨拉;K. Toren:瑞典哥德堡大学萨哈格伦卡学院职业与环境医学科;M. Olivieri:意大利维罗纳大学职业医学单位;I.乌鲁鲁特:呼吸部,嘉达科医院,西班牙省嘉达科; L. Cazzoletti: Unit of Epidemiology and Medical Statistics, Dept of Medicine and Public Health, University of Verona, Verona, Italy; B. Jacquemin: Inserm, Centre for Research in Epidemiology and Population Health (CESP), U1018, Respiratory and Environmental Epidemiology, Villejuif; Université Paris Sud, UMRS 1018, Villejuif, France; and Centre for Research in Environmental Epidemiology (CREAL), Barcelona, Spain; G. Benke: Dept of Epidemiology and Preventive Medicine, Monash University, Melbourne, Australia; H. Kromhout: Institute for Risk Assessment Sciences, Environmental Epidemiology Division, Utrecht University, Utrecht, The Netherlands; M.C. Mirabelli: Dept of Epidemiology and Prevention, Division of Public Health Sciences, Wake Forest School of Medicine, Winston-Salem, NC, USA; A.J. Mehta: Swiss Tropical and Public Health Institute, Basel; School of Medicine, University of Basel, Basel, Switzerland; and Dept of Environmental Health, Harvard School of Public Health, Boston, MA, USA; V. Schlünssen: Section of Environment, Occupation and Health, Dept of Public Health, Aarhus University, Aarhus, Denmark; T. Sigsgaard: Section of Environment, Occupation and Health, Dept of Public Health, Aarhus University, Aarhus, Denmark; P.D. Blanc: Division of Occupational and Environmental Medicine, Dept of Medicine, University of California, San Francisco, CA, USA; M. Kogevinas: Centre for Research in Environmental Epidemiology (CREAL), Barcelona; Hospital del Mar Medical Research Institute (IMIM), Barcelona; CIBER Epidemiología y Salud Pública (CIBERESP), Barcelona, Spain; and National School of Public Health, Athens, Greece; J.M. Anto: Centre for Research in Environmental Epidemiology (CREAL), Barcelona; Hospital del Mar Medical Research Institute (IMIM), Barcelona; CIBER Epidemiología y Salud Pública (CIBERESP), Barcelona; and Universitat Pompeu Fabra (UPF), Barcelona, Spain; J-P. Zock: Centre for Research in Environmental Epidemiology (CREAL), Barcelona; Hospital del Mar Medical Research Institute (IMIM), Barcelona; and CIBER Epidemiología y Salud Pública (CIBERESP), Barcelona.
本文中包含的本地ECRHS II研究由以下机构提供资金。Albacete,西班牙:Fondo de Investigacions Santarias(FIS)(赠款代码:97 / 0035-01,99 / 0034-01和99 / 0034-02),医院De Albacete,Consejeria de Sanidad;安特卫普,比利时:FWO(科学研究基金) - 法利人(授予守则:G.0402.00),安特卫普大学,佛兰芒卫生部;巴塞罗那,西班牙:分离,公共卫生服务(授予代码:R01 HL62633-01),Fondo De Investigacions Santarias(FIS)(授权代码:97 / 0035-01,99 / 0034-01和99 / 0034-02)。(授予代码:1999SGR 00241),Red Respira Iscii;巴塞尔,瑞士:瑞士国家科学基金会,瑞士联邦教育与科学办公室,瑞士国家事故保险基金(SUVA),USC Niehs Center(授予守则:5P30 ES07048);卑尔根,挪威:挪威研究委员会,挪威哮喘和过敏协会(NAAF),Glaxo Wellcome As,挪威研究基金;Erfurt,德国:GSF-国家环境与健康研究中心,Deutsche Forschungsgemeinschaft(DFG)(补助代码:FR 1526 / 1-1);嘉达子,西班牙:巴斯克卫生部;瑞典哥德堡:瑞典心灵基金会,瑞典工作生活和社会研究(FAS),瑞典癌症和过敏基金会; Grenoble, France: Programme Hospitalier de Recherche Clinique-DRC de Grenoble 2000 no. 2610, Ministry of Health, Direction de la Recherche Clinique, Ministere de l'Emploi et de la Solidarite, Direction Generale de la Sante, CHU de Grenoble, Comite des Maladies Respiratoires de l'Isere; Hamburg, Germany: GSF-National Research Centre for Environment and Health, Deutsche Forschungsgemeinschaft (DFG) (grant code MA 711/4-1); Ipswich and Norwich, UK: Asthma UK; Huelva, Spain: Fondo de Investigaciones Santarias (FIS) (grant codes: 97/0035-01, 99/0034-01 and 99/0034-02); Oviedo, Spain: Fondo de Investigaciones Santarias (FIS) (grant codes: 97/0035-01, 99/0034-01 and 99/0034-02); Paris, France: Ministere de l'Emploi et de la Solidarite, Direction Generale de la Sante, UCB-Pharma (France), Aventis (France), Glaxo France, Programme Hospitalier de Recherche Clinique-DRC de Grenoble 2000 no. 2610, Ministry of Health, Direction de la Recherche Clinique, CHU de Grenoble; Pavia, Italy: GlaxoSmithKline Italy, Italian Ministry of University and Scientific and Technological Research (MURST), Local University Funding for Research 1998 and 1999 (Pavia, Italy); Tartu, Estonia: Estonian Science Foundation; Turin, Italy: ASL 4 Regione Piemonte (Italy), AO CTO/ICORMA Regione Piemonte (Italy), Italian Ministry of University and Scientific and Technological Research (MURST), GlaxoSmithKline Italy; Umeå, Sweden: Swedish Heart Lung Foundation, Swedish Foundation for Health Care Sciences and Allergy Research, Swedish Asthma and Allergy Foundation, Swedish Cancer and Allergy Foundation; Uppsala, Sweden: Swedish Heart Lung Foundation, Swedish Foundation for Health Care Sciences and Allergy Research, Swedish Asthma and Allergy Foundation, Swedish Cancer and Allergy Foundation; Verona, Italy: University of Verona, Italian Ministry of University and Scientific and Technological Research (MURST), GlaxoSmithKline Italy; USA: Dept of Health, Education and Welfare Public Health Service (grant code: #2 S07RR05521-28).
我们要感谢外地工作人员和所有参与设立研究和参加各中心各方面考试的人员,他们为ECRHS的成功作出了宝贵贡献。我们感谢所有的参与者,没有他们,这项研究就不可能完成。
研究负责人,高级科研小组成员如下。M.艾布拉姆森,R.伍兹,E.H.沃尔特斯,F.添和G.本科科技(澳大利亚,墨尔本);P. Vermeire,J.韦勒,M.范Sprundel和V. Nelen(南安特卫普和安特卫普市,比利时);R.乔吉和A.顺(爱沙尼亚塔尔图);F. Neukirch的,B. Leynaert,R.利亚德和M. Zureik(巴黎,法国),I.引脚和J.费兰-昆汀(格勒诺布尔,法国);J.海因里希,M. Wjst,C.弗莱和I.迈耶(爱尔福特,德国);T. Gislason的(雷克雅未克,冰岛);M. Bugiani,P.皮乔尼,A. Carosso,W. Arossa,E.卡里亚,G.卡斯蒂格尼,E.米利,C.罗马诺,D.法布罗,G.奇科内,C.马尼亚尼,P. Dalmasso,R.Bono, G. Gigli, A. Giraudo, M.C. Brussino, C. Bucca and G. Rolla (Turin, Italy), R. de Marco, G. Verlato, E. Zanolin, S. Accordini, A. Poli, V. Lo Cascio and M. Ferrari (Verona, Italy), A. Marinoni, S. Villani, M. Ponzio, F. Frigerio, M. Comelli, M. Grassi, I. Cerveri and A. Corsico (Pavia, Italy); J. Schouten (Groningen, the Netherlands); A. Gulsvik, E. Omenaas, C. Svanes and B. Laerum (Bergen, Norway); J.M. Antó, J. Sunyer, M. Kogevinas, J.P. Zock, X. Basagana, A. Jaen and F. Burgos (Barcelona, Spain), J. Maldonado, A. Pereira and J.L. Sanchez (Huelva, Spain), J. Martinez-Moratalla Rovira and E. Almar (Albacete, Spain), N. Muniozguren and I. Urritia (Galdakao, Spain), F. Payo (Oviedo, Spain); C. Janson, G. Boman, D. Norback and M. Gunnbjornsdottir (Uppsala, Sweden), K. Toren, L. Lillienberg and A. Dahlman-Höglund (Gothenburg, Sweden); E. Norrman, M. Soderberg, K. Franklin, B. Lundback, B. Forsberg and L. Nystrom (Umeå, Sweden); N. Künzli, B. Dibbert, M. Hazenkamp, M. Brutsche and U. Ackermann-Liebrich (Basel, Switzerland); P. Burney, S. Chinn and D. Jarvis (London, UK), D. Jarvis and B. Harrison (Norwich, UK), D. Jarvis, R. Hall and D. Seaton (Ipswich, UK); M. Osborne, S. Buist, W. Vollmer and L. Johnson (Portland, OR, USA).
脚注
本文提供了补充材料www.www.qdcxjkg.com
有关编辑评论,请参阅319页.
支持声明:本研究由西班牙教育部(授予:SAB2011-0075)。ECRHS II的职业哮喘组分的协调由授予1 R01 HL62633-01支持美国NIH / NORA / NHLBI.ECRHS II的协调得到支持欧洲委员会(作为他们生活质量计划的一部分),来自研究合同Nofood_ct_2004_506378,GA2len项目和全球过敏和哮喘欧洲网络。本文中包括的本地ECRHS II研究的资金来源列在致谢中。
利益冲突:可以在本文的在线版本旁找到披露www.www.qdcxjkg.com
- 收到2013年2月26日。
- 接受2013年6月28日。
- ©ers 2014.















