摘要
我们的目的是评估一种血清型特异性尿液抗原检测多重试验在社区获得性肺炎患者尿液中鉴定13种肺炎球菌血清型(1,3,4,5,6a, 6B, 7F, 9V, 14,18c, 19A, 19F和23F)的诊断准确性和临床应用。
包括临床怀疑为社区获得性肺炎的成年患者。除了标准的诊断程序,尿液样本被收集来执行尿抗原检测试验。收集人口学、临床、放射学和微生物学数据。
1095例社区获得性肺炎患者链球菌引起的肺炎使用常规诊断方法时,257例(23%)被鉴定为致病病原体,添加尿抗原检测时,357例(33%)被鉴定为致病病原体。在尿抗原检测涵盖的13种血清型中的一种引起的49例菌血症发作中,有48例通过尿抗原检测检测到,表明敏感性为98%。在77例“非尿抗原检测”致病菌的社区获得性肺炎病例中,没有一例尿抗原检测结果为阳性,特异性为100%。
添加尿抗原检测试验到常规诊断方法增加患病率肺炎链球菌社区获得性肺炎增加39%。以菌血症发作为参考,尿抗原检测的敏感性和特异性分别为98%和100%。
摘要
在常规诊断方法的基础上增加尿抗原检测,可提高患病率肺炎链球菌帽http://ow.ly/nSA1l
简介
社区获得性肺炎(CAP)是全球发病率和死亡率的主要原因。链球菌引起的肺炎是所有年龄组中最常见的CAP致病菌[1,2].有90种不同的血清型肺炎链球菌,以荚膜多糖为基础,疾病患病率存在明显的血清型特异性差异[3.]和侵袭性肺炎球菌病的临床转归[4].
肺炎球菌CAP的诊断通常基于肺炎的临床和影像学证据,结合血液和痰样本的微生物学结果,以及尿液中肺炎球菌抗原的检测。然而,许多肺炎球菌性CAP发作仍未得到诊断。菌血症与肺炎链球菌仅在3.6-9.6%的CAP成人病例中得到证实[5],而敏感性会因先前使用抗生素而降低[6,7].此外,只有36-64%的CAP患者会产生痰液[8,9],而且样品经常受到上呼吸道菌群的污染。最后,在尿液中检测肺炎球菌抗原,通常采用BinaxNOW公司(Alere International, Galway,爱尔兰)的免疫层析法(ICA),可能具有较高的特异性,然而报道的敏感性在从无菌部位(如血液和胸膜液)分离的肺炎球菌患者亚组中的769 - 100%和仅从痰中分离的肺炎球菌患者的437 - 69.2%之间变化[10- - - - - -12].只有从无菌部位和痰中分离出的肺炎球菌才可能进行血清分型。因此,这里的血清型分布和变化(例如,由于疫苗接种策略)只能在一小部分CAP病例中测量。
为了准备一项大型随机安慰剂对照双盲试验[13],我们评估了一种新型血清型特异性尿抗原检测(UAD)多重检测的诊断特性和临床应用[14]用于13种血清型特异性多糖的鉴定肺炎链球菌(血清型1,3,4,5,6a, 6B, 7F, 9V, 14, 18C, 19A, 19F和23F)。13种多糖抗原与13价肺炎球菌结合疫苗中使用的血清型相对应。
材料与方法
病人
2008年1月至2009年4月,我们在23家荷兰医院(4家学术医院、15家教学医院和4家非教学医院)进行了一项前瞻性、观察性、队列研究。并非所有医院同时开始(最后一家医院于2008年7月开始),17家医院在2008年10月因为一项竞争性肺炎试验而停止了患者注册。
年龄≥18岁、临床怀疑有CAP或下呼吸道感染(LRTI)、在参与医院急诊室就诊的成年患者符合条件。临床怀疑CAP或LRTI被定义为以下标准中的至少两项:发热或体温过低;咳嗽或慢性咳嗽模式改变;呼吸困难、呼吸急促或缺氧;叩诊或听诊结果与肺炎相符;胸片显示白细胞增多、白细胞减少、左移或浸润。在每家医院,专门的研究护士每周检查两到三次通过急诊室入院的患者的入院诊断。不包括在急诊室的符合条件的患者可包括在入院后48小时内。该研究得到了所有当地研究伦理委员会的批准,并获得了所有参与者的书面知情同意。
诊断方法
除了病史记录、体格检查、实验室血液分析和胸片外,诊断程序还包括血液、痰和胸膜液(如果存在)的微生物培养,以及在就诊后立即或至少在入院后48小时内收集尿样。
尿液样本在当地以标准化方式处理(用0.5 M PIPES缓冲液处理至最终浓度为25 mM),随后在-70°C冷冻,直到在辉瑞疫苗研究参考实验室(美国纽约州珠江)进行处理。由于ICA不是大多数医院标准护理的一部分,ICA的局部处理不属于研究方案的一部分。在参考实验室中,UAD测试和市售泌尿系肺炎球菌抗原ICA (BinaxNOW肺炎链球菌尿液抗原测试,Alere International)根据制造商的说明分批进行。ICA结果由两名分析人员解读,不考虑任何临床信息。当前两位分析师意见不一致时,第三位分析师对结果进行了解释。UAD检测是一种基于Luminex技术的多种UAD检测方法,可以同时检测13种不同的血清型UAD肺炎链球菌(血清型1、3、4、5、6A、6B、7F、9V、14、18C、19A、19F和23F)通过捕获人尿液中分泌的血清型特异性多糖[14].的在体外其他地方已报道了该检测在未感染个体中的验证(基于当前研究人群的子集)和特异性测定[14].
微生物检测(血液和痰培养和BinaxNOW尿军团菌抗原检测,如果临床适用)根据当地和制造商的协议在当地实验室进行。肺炎链球菌根据制造商的方案,在荷兰细菌性脑膜炎参考实验室(阿姆斯特丹,荷兰)使用抗血清(Statens血清研究所,哥本哈根,丹麦),通过共凝集和囊囊肿胀法(Quellung反应)分型,对血液分离物进行血清分型[15,16].血培养中凝固酶阴性葡萄球菌被认为是“污染物”,而不是致病病原体。
数据收集
由每家医院训练有素的研究护士和/或医生在标准化病例记录表中记录人口统计学、以前使用抗生素、感染的体征和症状、放射学和微生物学测试结果以及体检结果。在入院期间或入院后不久收集数据。CAP的临床严重程度根据肺炎严重程度指数(PSI)评分进行分类[17].
定义
CAP定义为入院后48小时内胸片出现浸润,根据当地放射科医生的诊断,并伴有以下症状或体征中的至少两种:咳嗽、咳痰、发热、与肺炎相符的听诊结果、白细胞增多或白细胞减少、c反应蛋白>是正常上限的3倍、患者呼吸室内空气时氧张力<60 mmHg的低氧血症或呼吸困难/呼吸急促的体征。
如果CAP的致病微生物是从血液或任何其他无菌体液中培养出来的,或者如果尿液抗原测试呈阳性(无论是对肺炎球菌或军团菌抗原进行ICA或UAD测试),则被认为是“确定的”。被视为污染物的细菌(如.凝固酶阴性葡萄球菌)不被认为是致病病原体。一种微生物被认为是CAP的“可能”原因,如果没有明确的病原体,当它在痰培养中作为主要菌群存在时。肺炎球菌性CAP定义为CAP肺炎链球菌作为“确定的”或“可能的”致病微生物。
数据分析
描述性分析通过使用SPSS统计软件包(17.0版,SPSS公司,芝加哥,伊利诺伊州,美国)计算频率、平均值或中位数进行。为了比较各组,二分行列式采用皮尔逊卡方检验,连续数据采用t检验或Mann-Whitney u检验。p值<0.05被认为是显著的。
为了计算UAD试验的敏感性,将“真阳性”定义为由UAD试验的13种血清型中的一种引起的CAP合并菌血症(血培养阳性),并将UAD试验阳性的数量与“真阳性”的数量进行比较。仅基于痰培养的疑似肺炎球菌CAP发作被排除在本分析之外。“真阴性”定义为由其他病原体引起菌血症的CAP病例,或由UAD试验未覆盖的肺炎球菌血清型引起的CAP病例,或仅由军团菌尿抗原试验阳性的CAP病例。特异性由UAD阴性试验次数与“真阴性”次数的比较来确定。
结果
研究人群
共纳入1758例临床怀疑CAP或LRTI患者,其中552例(31%)入院48小时内胸片未见浸润。101例患者未获得尿样,10例患者未获得知情同意,研究总人数为1095例CAP患者(图1).这1095例患者的中位年龄为69岁(四分位数范围57-79岁),大多数为男性(62.7%),50例(4.6%)患者是门诊患者。就诊前投诉的中位持续时间为4天(四分位数范围2-7天)。PSI分类的I-V类的分布分别为9.9%、22.1%、23.0%、34.6%和10.4%。4例(0.4%)患者报告接种了肺炎球菌疫苗。有1077名患者在入院前使用抗生素的信息,其中325名患者在入院前使用了抗生素。
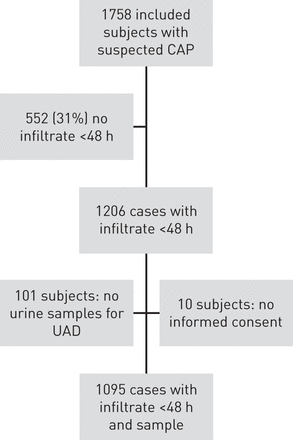
流程图显示疑似社区获得性肺炎(CAP)的研究人群。UAD:尿抗原检测。
病因学
922例(84.2%)患者进行了血液培养,570例(52.1%)患者进行了痰培养,762例(69.6%)患者进行了军团菌尿抗原检测。所有1095份尿液样本均在参考实验室进行了ICA和UAD检测。有3例CAP发作,尿抗原检测均为肺炎球菌和军团菌阳性。在所有三次发作中,ICA和UAD测试均为阳性,在一次发作中,还出现了肺炎球菌菌血症。肺炎链球菌在所有三次发病中都被认为是CAP的致病病原体。一例CAP发作与大肠杆菌菌血症,ICA肺炎球菌尿抗原试验阳性,UAD试验阴性。在这节课中,肺炎链球菌被认为是CAP的致病菌。
根据微生物培养结果和ICA,在403例(36.8%)病例中可以确定CAP的病因(表1).将UAD检测结果添加到这些方法中,493例(45.0%)发作可确定病因,未纳入UAD检测结果的肺炎球菌CAP发作比例为23.5% (n=257),纳入UAD检测结果的肺炎球菌CAP发作比例为32.6% (n=357)。这代表了诊断产量的相对增加肺炎链球菌增长39%,绝对增长9.1%。
诊断准确性
研究人群中249例(22.7%)UAD检测阳性,211例(19.3%)ICA检测阳性。249例uad阳性标本中,ICA阴性标本122例。
有49株菌血症分离株属于UAD试验中包括的13种血清型中的一种,其中48株是由UAD检测到的,对UAD试验中包括的血清型的菌血症性肺炎球菌CAP的敏感性为98% (表2).唯一的阴性尿样产生的阳性信号未达到血清型3的预定义阳性临界值,血清型3是血液培养分离物的血清型。ICA在这49例中有34例产生阳性结果,对UAD试验中包括的13种肺炎球菌血清型中的一种的细菌性CAP的敏感性为69.4%。ICA检测到77例细菌性肺炎球菌CAP病例中的49例(包括未包括在UAD中的血清型),总体敏感性为63.6%。
有76例CAP发作的致病病原体肺炎链球菌UAD试验中包括的血清型:23例非UAD试验引起的菌血症发作肺炎链球菌血清型,28例非肺炎球菌菌血症,25例由单一感染引起嗜肺性军团菌.在该队列中没有UAD检测阳性,表明UAD检测特异性为100%。28例非肺炎球菌菌血症病例和25例由退伍军人ICA检测1例阳性,特异性为98%。
血清型分布
77例细菌性肺炎球菌CAP发病中,1型和14型是最常见的血清型(n=9),其次是19A和7F型(n=7)和22F型(n=6)。5株菌株无法进行血清分型。根据UAD结果,纳入的13种血清型的血清型分布出现了变化(图2).血清型1仍然是最常见的血清型(n=38) (表3),但血清型3和18C的相对频率增加,而血清型14的相对频率下降(从18.4%(95%置信区间7.5 ~ 29.2%)下降到8.4%(4.7 ~ 11.3%))。
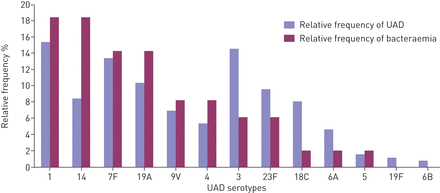
基于尿抗原检测(UAD)数据(n=261,包括多种血清型)和菌血症数据(n=49)的相对血清型分布。UAD数据的绝对数量请参见表3.
根据UAD结果,1111例CAP发作(由UAD诊断的肺炎球菌CAP病例的4.4%,所有测试样本的1.0%)似乎是由多种血清型引起的,这是由重新测试和抑制实验证实的(数据未显示[14])。10例发作由UAD测试中包括的两种血清型引起,1例发作由三种血清型引起。其中两例患者还伴有菌血症,在这两例中,分离菌血症的血清型与UAD检测到的一种血清型相匹配。
讨论
在常用的标准诊断方法(如微生物培养和尿中肺炎球菌抗原的ICA)中添加一种新的血清型特异性UAD测试,提高了对肺炎球菌抗原的诊断率肺炎链球菌CAP降低39%。UAD测试对UAD测试中包括的一种血清型引起的肺炎球菌CAP发作的敏感性为98%,而ICA的敏感性为69%。在成人CAP患者尿液中检测13种血清型特异性肺炎球菌抗原的特异性为100%,与ICA试验相似。此外,通过UAD测试诊断的肺炎球菌CAP发作的4%是由多种血清型的联合感染引起的。虽然还没有商业化,但这种方法可以提高我们对肺炎球菌感染的诊断率,并可以提供感染相关肺炎球菌血清型的流行病学更详细的信息。
在尿液中检出肺炎球菌抗原最早于1917年提出[18],并于1999年随着ICA BinaxNOW (Alere International)的商业可用性而得到广泛应用。以前曾尝试在尿液中检测血清型特异性抗原,其特异性(98-99%)非常好,但与之相比,敏感性(55-84%)令人失望肺炎链球菌在无菌部位检出的分离株[19- - - - - -22].本研究ICA检测的敏感性为63%。
在常规诊断方法中加入UAD检测后,由UAD引起的CAP发作比例明显降低肺炎链球菌从23.3%增加到32.6%。然而,UAD测试仅检测到13种血清型,仅通过ICA阳性结果诊断出71例肺炎球菌CAP发作。ICA检测对细菌性CAP的敏感性为63%,由此推断,UAD检测未覆盖的血清型引起的肺炎球菌CAP有113例,而不是71例。这意味着由肺炎球菌引起的CAP发作的总比例为36.4%(1095人中有399人)。本研究中使用的UAD测试对肺炎球菌CAP的发作进行了三次“血清分型”(从无菌部位和痰中分离出的肺炎球菌为249例,而从无菌部位和痰中分离出的肺炎球菌为77例),因此,提高了我们调查肺炎球菌CAP血清型流行病学的能力肺炎链球菌.此外,如果该测试的周转时间可以减少到实时测试,演示肺炎链球菌可以帮助快速降低不必要的广泛的CAP经验抗生素治疗。由于许多血清型将不会被检测到,阴性的检测结果将对临床决策没有帮助。
在UAD检测到的肺炎球菌CAP病例中,4.4%似乎是由多种血清型引起的。尽管存在多种血清型的携带已被描述[23- - - - - -25],由多种血清型引起的感染仅零星报道[20.,21,26,27].最近,366例肺炎球菌性CAP患者中,有5例因两种血清型引起肺炎,这是基于尿样中14种血清型的多重免疫分析[28].因此,除了更高的敏感性,UAD测试还提高了我们检测多种血清型合并感染的能力。
我们的研究有一些局限性。在所有研究非侵入性诊断的临床研究中肺炎链球菌传染病,我们因缺乏真正的“黄金标准”而遭受痛苦。这导致“真阳性”(n=49)和“真阴性”(n=76)的数量较低。然而,在这一点上,没有其他参考标准来更好地检测血清型特异性诊断工具的准确性。其次,肺炎球菌抗原可在感染后的尿液样本中存留长达7天[19,29]至3个月[30.].虽然我们没有CAP临床发作前几周的详细病史信息,但我们可以确定只有8名(0.7%)患者在CAP发作前几周住院。此外,当使用浓缩尿液时,持续抗原阳性的可能性更大[11,30.].在我们的研究中,只使用未浓缩的尿液,减少了假阳性检测的可能性。因此,我们认为既往肺炎球菌感染导致的假阳性检测结果不太可能影响我们的研究结果。最后,101名患者的尿样缺失可能造成了选择偏差。事实上,这101例患者更常被归类为“严重CAP”(PSI V级)(p=0.012;数据未显示)和先前的研究表明ICA在重症患者中更敏感[21,31],虽然这一发现并没有得到其他人的证实[10,32].如果CAP的严重程度与尿液中抗原检测的可能性较高相关,那么UAD测试的诊断率实际上可能比本文报道的要高。
致谢
作者要感谢Marcel Peeters(荷兰蒂尔堡圣伊丽莎白医院)对本研究做出的重大贡献,他于2011年6月不幸去世。此外,他们要感谢所有CAP诊断调查人员所付出的时间和努力。
脚注
支持声明:本研究由惠氏制药公司该公司于2009年10月被辉瑞(Pfizer)收购。
利益冲突:可以在本文的在线版本中找到信息披露www.www.qdcxjkg.com
- 收到了2012年8月30日。
- 接受2013年1月15日。
- ©2013人队















