摘要
人类疱疹病毒(HHV)-8是一种致癌的伽马疱疹病毒,于1994年首次在卡波西肉瘤病变中被描述。HHV-8参与了多中心Castleman病(MCD)和原发性积液淋巴瘤(PEL)的病理生理特征,这两种都是罕见的b细胞淋巴增生性疾病。hhv -8相关的肿瘤几乎只发生在免疫缺陷患者中,大多数是HIV感染患者。联合抗逆转录病毒疗法降低了卡波西肉瘤的发生率,但对MCD和PEL无效。
hhv -8相关疾病经常表现为肺受累,这可能表明该疾病。肺卡波西肉瘤通常无症状,但可能需要特定的治疗。主要表现为皮肤或黏膜受累。典型的MCD患者表现为发热和淋巴结病变伴间质性肺疾病,无机会性感染。具体治疗可能是紧急的。PEL引起发热,淋巴细胞渗出性胸腔积液,计算机断层扫描未见胸膜肿块。快速诊断可以避免不必要的检查,并导致具体、快速的治疗。治疗很复杂,需要结合抗逆转录病毒治疗和化疗。
摘要
hhv -8相关疾病经常表现为肺受累,这可能表明该疾病http://ow.ly/ngJ65
介绍
人类疱疹病毒(HHV)-8,或卡波西肉瘤疱疹病毒,是第8个也是最近发现的HHV成员。它于1994年在卡波西肉瘤病灶中发现[1].HHV-8后来与多中心Castleman病(MCD)和原发性积液淋巴瘤(PEL)有关[2- - - - - -4].HHV-8感染的肺部表现几乎只发生在免疫功能低下的患者,主要发生在HIV感染期间。HHV-8被怀疑参与了肺动脉高压、结节病或多发性骨髓瘤的发病机制,但未得到证实[5- - - - - -7].
这种叙事审查简要介绍了HHV-8的特征,然后侧重于HHV-8感染和Kaposi Sarcoma,MCD和PEL的肺表现的临床表现,主要是在HIV感染期间。该评论涉及在HHV-8和肺部的文献中搜索文献。我们搜索了Medline.通过在2012年6月至2012年6月出版的文章中,术语“HHV-8”,“卡普斯曼病”,“Kaposi”和“初级效果淋巴瘤”的术语。我们在临床相关文章中掌握了其他文章的参考列表。筛选标题,然后读取摘要以选择相关文章。例如,描述了描述局部Castleman疾病的研究的摘要未读。
人类疱疹病毒8型
和所有疱疹病毒一样,HHV-8是一种双链DNA病毒。HHV-8属于γ2疱疹病毒Rhadinovirus.基因型,它是致癌的HHV最近的HHV(EBV)(EBV)(图1) [9].
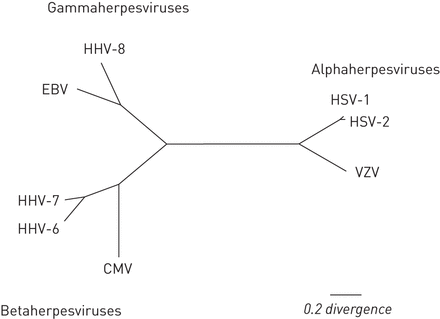
人类疱疹病毒(hhv)系统发育树。EBV:巴尔病毒;HSV:单纯疱疹病毒;VZV:水痘带状疱疹病毒;巨细胞病毒:巨细胞病毒。根据[8].
和所有疱疹病毒一样,HHV-8病毒有两种复制模式:溶解期和潜伏期。在潜伏期,只有少数病毒基因在受感染细胞中表达,病毒基因组随着细胞有丝分裂复制。PCR显示,在这一阶段,HHV-8在血液中没有可检测到的复制[10].在溶解阶段,许多基因被表达,人类促炎细胞因子的病毒同源物,如病毒白细胞介素6 (vil6),导致炎症、血管生成和细胞生长。MCD的大多数临床效应是次级的病毒蛋白,如vil6 [11- - - - - -13].
HHV-8病毒的宿主完全是人类。它是地方性的,并在非洲和地中海周围的潜伏阶段持续存在。撒哈拉以南非洲的患病率接近50%,西西里岛为30%,北欧和亚洲低于1% [14].
主要HHV-8感染是无症状的或导致非特异性感染迹象,很少被诊断出来。报道了HHV-8原发性感染的回顾性诊断:患者呈现发烧,关节痛和多元症,这可能误认为是无数病毒原发性感染[15].
在低流行率国家,HHV-8主要通过性行为传播,主要发生在具有高危性行为的人群中,HIV和HHV-8同时感染的频率很高[14,16].HHV-8可通过输血或器官移植传播[17,18].在高流行国家,血液中普罗旺斯在童年期间增加,这表明母亲和孩子或兄弟姐妹或玩伴之间的传播。唾液可能是在性和家族性传输中涉及的生物液,因为它可以含有高水平的HHV-8 [19,20.].
为了评估其在流行病学研究中的流行程度,HHV-8感染是通过免疫球蛋白(Ig) g阳性血清学结果诊断的[15].过去的研究结果受到现有测试的高可变性的影响[21].目前HHV-8血清学检测的敏感性和特异性分别为89-98%和83-97% [22,23].这种低准确性解释了为什么血清学不用于临床实践,以及为什么HHV-8感染是通过临床检查、组织学或PCR (表1).可通过免疫组织化学鉴定用HHV-8感染的细胞,因为它们表达潜伏期相关的核抗原(LANA)。实时PCR提供分析HHV-8病毒载荷的定量方法,结果与感染细胞数和疾病类型相关[10,24].
HHV-8是一种致癌病毒,在潜在的状态下感染大多数B细胞。然而,在Kaposi Sarcoma中,感染的细胞是表达内皮细胞的一些标记的主轴细胞[25];在MCD中,它们是幼稚的单型b细胞[26];在PEL中,它们是生发后b细胞[27].梭形细胞感染后的增殖低于肿瘤b细胞感染后的增殖。pcr评估的HHV-8病毒载量在PEL中高于卡波西肉瘤。事实上,血液病毒载量可能小于2 log copies / 105卡波西肉瘤的外周血单个核细胞(PBMCs),每10个2-4 log拷贝5MCD和>中的pbmc每10个日志拷贝4份5PBMC在PEL中[28].然而,仅PCR不能用于诊断,必须结合临床和组织学数据(表1).此外,疾病缓解期患者或无症状HHV-8携带者的PCR结果往往为阴性[10,29].
HHV-8疾病可能出现在患有经典地中海卡波西肉瘤和MCD的老年患者中,偶尔也会在免疫抑制治疗期间出现。然而,它们最常出现在艾滋病毒感染期间[30.,31].
卡波西肉瘤
流行病学
皮肤卡波西肉瘤150年前在地中海地区和中东国家的男性中被描述[32].在艾滋病阶段的HIV感染期间经常发现Kaposi Sarcoma。此外,在20世纪80年代,Kaposi Sarcoma是导致艾滋病描述的机会主义感染之一,并且是艾滋病指标。自20世纪90年代中期以来,组合的抗逆转录病毒治疗(推车)已被广泛使用,Kaposi Sarcoma的患病率从每1000百年每1000〜0.03的30%下降[33].目前,卡波西肉瘤主要发生在未使用cART或cART未控制疾病的患者,但也可在使用cART治疗的低病毒血症患者中看到。CD4细胞计数中位数约为150个细胞·mm−3[34].HIV感染期间卡波西肉瘤也可出现在cART的开始阶段。事实上,与卡波西肉瘤相关的一系列免疫重建综合征已被报道[35].
临床表现
皮肤卡波西肉瘤病变为斑疹、丘疹或结节,可发展为溃疡性或硬化性肿瘤。它们的界线很清楚,呈红色或紫色(图2).病变是无痛而不是瘙痒。它们的直径可能不同于几毫米至> 10厘米。慢性病变可能与淋巴水肿有关,称为Kaposi Sarcoma相关的大脑病症[36].病变可能是漫射或局部的,尤其是躯干。重新分配可能因免疫缺陷的类型而异。地中海Kaposi Sarcoma主要影响腿和艾滋病毒相关的Kaposi Sarcoma The Trunk [31].
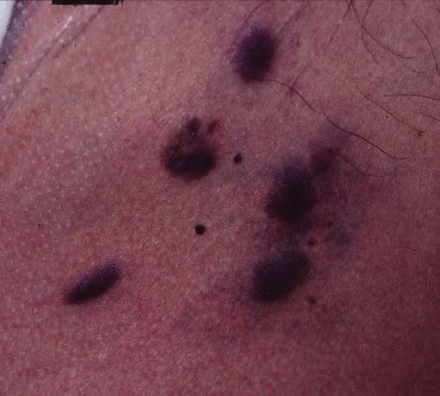
典型的紫色斑纹典型的皮肤病肉瘤的皮肤病变。
一半的患者在口腔,喉,咽部,较少,鼻子上存在粘膜病变。病变是可能生长和溃疡的紫色结节。宫颈淋巴结病或区域腺病变可能存在[37,38].
卡波西肉瘤的内脏定位可能是一个主要问题,在hiv相关的卡波西肉瘤中比非hiv相关的卡波西肉瘤更常见[31].最常发生在肺部和胃肠道。胃肠道卡波西肉瘤大多无症状,但可能导致出血。
肺表现
近45%皮肤卡波西肉瘤的hiv感染患者表现出卡波西肉瘤的胸膜或肺部表现。相反,85-95%的肺卡波西肉瘤患者也累及皮肤[39- - - - - -41].肺部卡波西肉瘤通常无症状,如怀疑感染,可在胸片或支气管镜检查时发现。当出现症状时,它们不是特异性的(咳嗽或呼吸困难)。胸膜痛或咯血多提示,但较少发生。无热咳嗽,开始隐匿,影像学表现提示水肿,卡波西肉瘤的皮肤定位提示肺定位[39].
胸片显示结节状阴影或肿块,可单发或多发,致密,均匀,或界限不清,可合并。也可见线状、双侧、支气管血管周围、肺门周围的不透明,以基部为主,周围延长为薄网状不透明(图3).小、中、单侧或双侧胸腔积液多见[40,42].另外,胸部x线检查可能显示正常结果,也可能显示卡波西肉瘤和机会性感染的叠加异常。

肺部卡波西肉瘤患者胸片显示双侧多发结节状阴影,主要在基底部。
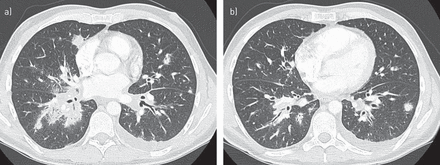
胸部x线照片上的异常显示在计算机断层扫描(CT)扫描几乎没有改善。CT扫描显示双侧小叶中央边界不清的结节,在下位区更明显。结节周围为磨玻璃样混浊物,形成晕圈。典型的支气管血管周围从肺门融合,隔膜增厚,实变,纵隔淋巴结肿大,或小或中度胸腔积液(图4) [39,40,42,43].
计算机断层扫描显示小叶中央一个边界不清的结节被毛玻璃阴影(a)包围,支气管血管周围从肺门融合增厚和少量左侧胸腔积液(b),所有这些都是典型的卡波西肉瘤。
支气管镜检查对肺部卡波西肉瘤的诊断是必要的。它显示气管或支气管上圆形、隆起、不易碎、红色、不规则形状的病变,直径从0.2到1厘米,特别是从隆突到支气管分支。宏观方面足以由经验丰富的肺科医生(图5).支气管肺泡灌洗液(BALF)分析揭示了正常的细胞计数,但可能揭示肺泡出血,因此排除了机会性感染[44,45].经PCR评估,BALF中HHV-8病毒载量的增加可具有100%的敏感性和98%的特异性[46].支气管活检并不是必须的诊断,因为结果可能是假阴性,理论上有出血的风险。目前,由于卡波西肉瘤的患病率下降和该领域专家的流失,诊断很困难。
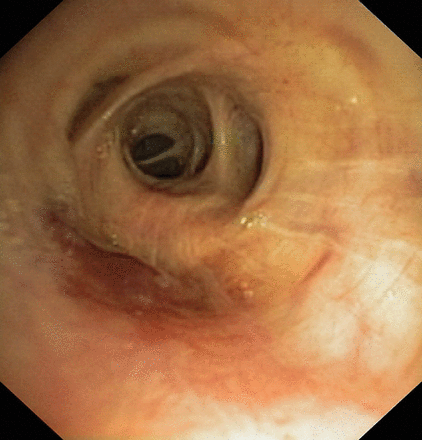
卡波西肉瘤支气管定位的内窥镜图。
胸部卡波西肉瘤可累及内脏胸膜。胸膜穿刺显示出血清学渗出液或出血性液体,无细胞优势。在没有卡波西肉瘤胸膜定位的病例中,20%的胸腔积液可能是乳糜胸。胸膜液细胞学检查和经皮胸膜活检均无帮助。如有需要,胸膜镜可显示典型的红色或紫色病灶进行诊断[47].如果没有可触及的支气管病变,手术肺活检可能是必要的。经BALF和CT扫描评估后,这种情况极为罕见。
诊断
皮肤发现,CD4计数<200个细胞·mm−3,不受控制的HIV感染,胸部影像学和支气管镜检查结果与BALF分析通常足以诊断卡波西肉瘤[48].
没有必要对血液进行HHV-8血清学和PCR检测,可能会出现假阴性结果(表1) [10].胸膜HHV-8感染的PCR分析尚未被证实是有用的,但可能有助于诊断。胸膜中较低的HHV-8病毒载量将排除PEL [49].
鉴别诊断
除了罕见的肺淋巴瘤(例如.在皮肤卡皮西肉瘤的患者中,泛刺血管和隔膜增厚,CD4计数<200个细胞·mm−3BALF分析排除机会性感染[42])。
最常见的差异诊断是机会性感染,例如,巴尔通氏体属henselae、淋巴样间质性肺炎、癌性淋巴管炎及结节病[50].BALF分析是有帮助的,并显示在淋巴样间质性肺炎中,例如淋巴细胞性肺泡炎以CD8阳性为主。对于肺泡出血,最常见的鉴别诊断是心功能不全和机会性感染,尤其是曲霉属真菌或塞细胞病毒感染[50].
进化和治疗
除了呼吸功能不全的功能或重要风险外,在Kaposi Sarcoma中,必须首先控制HIV感染以快速逆转免疫缺陷(表2).一般来说,单独使用cART就足以治疗与HIV相关的卡波西肉瘤[51].然而,有报道称,在开始使用cART后不久,出现了一些矛盾恶化的病例[52].必须在使用至少一种蛋白酶抑制剂的cART治疗3个月后评估治疗效果。蛋白酶抑制剂在HHV-8感染实验模型中优于其他类抗逆转录病毒药物[53,54].因此,在没有咯血或呼吸功能不全的情况下,卡波西肉瘤的肺定位,一线治疗是单独使用cART。
抗hhv -8抗病毒治疗(西多福韦、更昔洛韦或膦甲酸)已经证实体外抗HHV-8感染的活性,但对卡波西肉瘤无效[55].可考虑用长春碱,冷冻疗法,激光治疗,放疗或手术切除的局部治疗用于皮肤卡皮肉瘤,但从未研究过肺酸肺癌[56].
如有必要,肺卡波西肉瘤局部可采用全身化疗,如蒽环类(聚乙二醇脂质体阿霉素或柔红霉素脂质体)、长春碱、博莱霉素或紫杉醇(表2).尽管存在心脏毒性的风险,但蒽环类药物的耐受性良好;应答率接近50%,中位数为5个月应答[57].紫杉醇化疗显示了几乎相同的疗效,但可能与蛋白酶抑制剂相互作用[58,59].蛋白酶抑制剂,如利托那韦,是最有效的抗病毒药物之一,通常是cART的组成部分[60].蛋白酶抑制剂由细胞色素P450系统代谢。它们可能抑制或诱导该系统,并改变其他药物的代谢,如紫杉醇,通过这一途径代谢[61].事实上,接受蛋白酶抑制剂的患者紫杉醇暴露(曲线下面积)增加。然而,这种治疗并不总是导致毒性增加[62].最简单的选择是将蛋白酶抑制剂换成另一种抗病毒药物;如有必要,紫杉醇可能与蛋白酶抑制剂相关,密切监测[63].博莱霉素和长春碱单药化疗疗效较差,常与聚乙二醇脂质体阿霉素联用[59].此外,化疗引起额外的免疫缺陷,这需要预防肺囊虫病和弓形虫病。化疗引起的血液毒性可能需要造血生长因子治疗[64].
其他可能有效治疗卡波西肉瘤的疗法,目前正在评估,包括干扰素-α, mTOR抑制剂如雷帕霉素,或血管生成抑制剂如来那度胺,贝伐单抗,舒尼替尼或索拉非尼[57,65].
多中心Castleman病
定义
Castleman病的定义是组织学:Angiofollicular淋巴结增生。局部疾病,在非免疫表情患者中最常见的Castleman病,与HHV-8感染无关。HHV-8相关的MCD与古典透明血管或血浆细胞类型Castleman病。HHV-8被认为是大多数艾滋病毒相关MCD的Aetiological Agent和非HIV相关MCD的一半[2,66].
文章里是罕见的。评估20世纪90年代中期cART引入后MCD的患病率非常困难,特别是因为同时描述了与hiv相关的MCD [67].MCD可发生在控制或不控制HIV感染的患者中。在法国,与mcd相关的艾滋病毒感染的最大系列包括173名患者,而在法国,有近15万名患者感染了艾滋病毒[66,68].
临床检查和补充检查
MCD的最初表现可能提示淋巴瘤伴发热、多腺病和肝脾肿大。MCD的爆发可能会自行解决,而质疑可能会揭示之前的耀斑仍然没有诊断出来。
卡波西肉瘤的皮肤或黏液定位可能存在于近75%的病例[69].鼻塞经常发生,肺部症状(咳嗽、呼吸困难和咳痰)在33-75%的病例中出现。咯血是罕见的。肺听诊可见杂音[67,69,70].当出现呼吸系统症状时,胸片显示双侧间质混浊,可巩固为肺泡混浊。可能有纵隔淋巴结肿大及少量胸腔积液(图6).
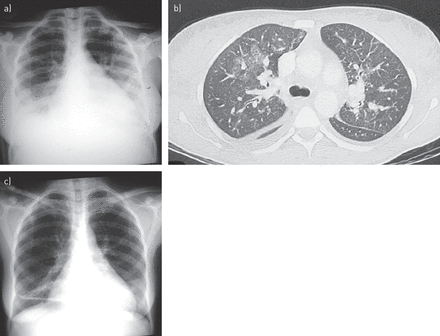
a)胸部放射线照相和b)多中心Castleman疾病眩光的患者的计算机断层扫描图像,显示具有小的双侧胸腔积液的Bibasal磨碎玻璃不透。c)胸部射线照相结果在用依托泊苷的火炬分离后几乎是正常的。
胸部CT显示胸膜下、支气管血管周围或中隔网状及小结节样混浊,伴淋巴分布。结节状或毛玻璃样混浊。CT显示1 - 3cm纵隔淋巴结病变。可能有少量胸腔积液。CT扫描结果显示耀斑分辨率正常[71].
生物试验通常显示血症患有炎症综合征,C反应蛋白质水平几乎总是> 200毫克·L.−1[72].威胁危及生命形式的MCD与血糖综合征有关[73].可以存在高肝酶水平和肾功能不全[74].蛋白质电泳显示约50%的病例出现多克隆高球蛋白血症和低蛋白血症。通过直接抗球蛋白试验或使用抗心磷脂和/或抗磷脂抗体,近30%患者的生物试验结果显示自身免疫。自身免疫表现更多地与MCD相关,而不是HIV。事实上,除了特发性或血栓性血小板减少性紫癜,自身免疫性疾病在HIV感染期间很少见。
PCR评估的HHV-8病毒载体总体血液始终增加,并且具有良好的负面预测值(表1) [10,72].高HHV-8病毒载量可能预示MCD耀斑[75].HHV-8病毒载量通常为每10个2-4个log拷贝5PBMCS [28因此,HHV-8血清学没有帮助。
很少需要支气管镜检查。在12例患者中,没有出现肉眼异常,特别是卡波西肉瘤病变。BALF分析显示,11名患者中有5人的细胞计数增加,7人的肺泡淋巴细胞增加。均无同时发生肺部机会性感染[70].
诊断
MCD通常是通过淋巴结活检的组织学检查确诊的[76].结果典型表现为卵泡增生、透明质化和生发中心退化;地幔带增生表现为同心环状的淋巴细胞,“洋葱皮层”。血管增多,毛细血管增生和内皮细胞增生。滤泡间区可见浆细胞片。只有一例手术肺活检的结果被报道,显示病变类似于淋巴结[71].
用LANA-1抗体免疫组化检测HHV-8感染细胞。受感染的细胞分散在地幔带[77,78].Lana测定证实了诊断,特别是在困难的组织学案件中。HHV-8感染细胞没有感染EBV,原位用EBV编码的RNA(EBER)杂交给出了负面结果。eBV似乎在MCD中没有发挥作用。Kaposi Sarcoma和MCD病变可能在近三分之二的案例中在同一淋巴结中共存[79].
在MCD病变中,HHV-8感染的细胞是具有浆细胞分化的b细胞。以前,它们被称为浆细胞;然而,它们是naïve b细胞。表面免疫球蛋白的特征为单型IgM-λ b细胞,但为多克隆[26].b细胞可以聚集成单克隆细胞,称为微淋巴瘤。该观察的临床和治疗意义仍有待确定[78].
鉴别诊断
主要鉴别诊断是结核和霍奇金或非霍奇金淋巴瘤,这需要组织学诊断。pcr检测的HHV-8病毒载量高,有可能出现HHV-8相关疾病,不太可能出现非HHV-8相关疾病。然而,在缺乏组织学证据的情况下,随着治疗的不同寻常发展,应重新考虑诊断。PCR和血清学是有用的[80].在HIV感染期间,MCD的肺部表现应排除可以通过BALF分析进行支气管镜检查的感染[70].噬血症可引起水肿伴胸腔积液。然而,胸腔积液可能继发于卡波西肉瘤或PEL,必须通过胸膜液分析排除。
进化和治疗
虽然MCD喇叭口可能会自发地解决,但它们可能会重现并且没有特定治疗的终身危险。审查报告报告11个月的中位生存率和47%的死亡率[69].报告的死亡原因为感染(24%)、器官功能障碍(15%)、非霍奇金淋巴瘤(15%)和MCD(9%)。此外,许多报告的感染或器官功能障碍可能继发于MCD失控。MCD诊断的长时间延迟可能与预后不良有关,但尚未得到证实[69].然而,德国最近的系列报告了2005年之前的平均存活率为1.5岁,但2005年后77%的生存率[81].
过去MCD患者发生淋巴瘤的风险是hiv感染患者的10-20倍[82].大多数MCD后发生的淋巴瘤与HHV-8感染有关[82].自cART引入以来,风险可能已经降低,而利妥昔单抗治疗则大大降低了风险[83].
MCD治疗的建议只依赖于专家的意见。他们建议进行以下治疗:1)减少艾滋病毒感染;2)淋巴样增生;3) HHV-8感染(表2) [76,84].
动物实验证实MCD的发生需要同时感染猴免疫缺陷病毒[85].MCD通常出现在CD4计数<350细胞·mm的患者−3.然而,cART在MCD中的作用尚未被证实。此外,已报道了许多cART启动后不久出现MCD的病例[86].然而,开始推车似乎是必要的,因为活性HIV复制会增加免疫缺陷,特别是淋巴瘤的风险。最近的综述表明,自推测推出以来的存活率增加[69,82].更昔洛韦和西多福韦对HHV-8感染有活性体外.西多福韦对MCD没有作用。最近的一系列研究显示,大剂量齐多夫定和缬更昔洛韦的治疗有短暂缓解,但只有23%的患者长期有反应[87,88].
MCD不是单克隆淋巴细胞增殖,但具有侵略性和致命的。这支持使用化疗。在紧急情况下可能需要化学疗法,并诱导快速缓解。实际上,在重症监护单位中,MCD诊断与血肿患者的良好预后有关[89].MCD症状几乎在24-48小时内得到缓解注射。依托泊苷。之后可每周口服依托泊苷一次。然而,依托泊苷长期治疗增加了骨髓增生异常的风险,需要讨论替代的长期治疗[90].避免复发需要其他疗法[69,91].在用环磷酰胺,adriamycin,vincristine和泼尼松(Chec)或等同物中,在聚铬疗法后获得延长缓解[69,92,93].
利妥昔单抗(一种针对b细胞中CD20蛋白的人源单克隆抗体)疗法很有吸引力。利妥昔单抗,375 mg·m,四次注射−2,导致近80%的MCD缓解期延长[76,81,94,95].自Rituximab的使用以来,MCD的整体存活率大大提高,5年可达90%[81].在几乎一半的病例中,注射利妥昔单抗后卡波西肉瘤病变恶化。没有其他副作用的报道。相比之下,对于淋巴瘤相关的艾滋病,利妥昔单抗与严重感染的高风险相关[96].值得注意的是,两种小系列报告的rituximab在活性MCD中用作一线治疗的疗效差[49,97].
一些MCD专家将依托泊苷作为控制疾病的一线疗法,作为与多种疗法相结合的多疗法,依托哌妥和利妥昔单抗以及优化的推车[76,84].皮质类固醇对MCD有部分作用,但会增加卡波西肉瘤病变恶化的风险,不推荐使用[76].
主要积液淋巴瘤
流行病学和定义
1995年,HHV-8感染在特定类型的间皮淋巴瘤中发现,涉及免疫表明患者的胸膜,心包或腹膜[3.].它被称为世界卫生组织分类中的肉肉,将其与次级积液定位的固体淋巴瘤区分开[98].自第一次描述PEL以来,PEL一直以固体形式被描述。固体PEL可能作为液体PEL的复发或作为初始表现出现[99].
PEL是一种罕见的淋巴瘤,占所有淋巴瘤的0.5%,占艾滋病相关淋巴瘤的3% [One hundred.].PEL可能发生在病毒学控制或不控制艾滋病毒感染的患者。平均CD4计数为150个细胞·mm−3[27].在器官移植继发免疫缺陷的患者或>80岁的患者中,很少有PEL的报道[101,102].
临床表现
患者大多表现为发热、行为状态改变和呼吸困难[27].胸腔积液在85%的病例中存在,并且在50%的病例中与腹水有关[24].继发于特定心包定位的心包填塞也可显示心包狭窄[27].2 / 3的病例有肝肿大和脾肿大[27].Kaposi Sarcoma的皮肤或粘膜定位在30-70%的病例中存在。MCD和PEL可能会相关。扩大的外周淋巴结很少见。神经功能缺陷或上颌病变应导致怀疑疾病的具体定位[24].
生物学检查常显示贫血,在50%的病例中伴有血小板减少和低白蛋白血症[24].乳酸脱氢酶的浓度一般是升高的[27].骨髓活检可发现噬血细胞,但很少发现肿瘤细胞[24,27].
胸膜流体分析显示血清血液渗出性液体,该分析是诊断的强制性[27].CT扫描显示没有肺部病变的胸腔积液或可检测的质量。可能存在小的胸膜增厚。心包或腹膜积液可能存在[103].
诊断
没有实体肿瘤存在,并且诊断是通过培养的细胞学家进行的细胞学。胸腔活检通常不需要或有用。细胞是多晶态且大的,有时是免疫细胞,具有一定程度的血浆细胞分化和不规则的波动细胞核。细胞质是丰富的和高胆无止的。短暂的众多。细胞通常不表达B细胞标记物(CD19或CD20)或T细胞标记物(CD3),但表达CD45,其证实淋巴源,也可以表达异常的T细胞标记物,例如血管上质CD3或CD4。它们可以共用激活标记,例如CD30,CD38或CD71,Mum1和等离子体 - 细胞标记,例如CD138 [104,105].b细胞是单克隆的,但诊断时不需要用PCR分析来确认单克隆性。此外,一些克隆分析技术可能产生假阴性结果,因为大量体细胞突变影响免疫球蛋白基因可变区[106].
HHV-8感染必须通过肿瘤细胞上的LANA抗原免疫组化和/或胸膜液中病毒载量的PCR评估(表1).PCR通常显示胸膜和血液之间的3-4 log比率[10].在血液中,HHV-8病毒载量通常是>4 log拷贝每10个5PBMCS [28].
在70%的病例中,肿瘤细胞同时感染了EBV。EBV感染处于1型潜伏期。事实上,免疫组化检测潜伏膜蛋白对肿瘤细胞是阴性的。原位需要用EBER探针进行肿瘤细胞杂交或对胸膜液进行PCR分析来证实EBV的存在[24].
细胞遗传学分析显示一个复杂的核型,或7、8或12三体。它从未显示其他结构异常,如c-Myc或Bcl-2蛋白[107].
鉴别诊断
差异化蛋白质和另一个具有胸膜定位的淋巴瘤可能是困难的。因此,HHV-8的检测有助于将PEL与其他淋巴瘤分化[108,109].
在免疫缺陷患者中,伴发热或表现状态改变的胸腔积液更常继发于卡波西肉瘤或感染性疾病,如肺结核,而非PEL。胸膜液分析没有显示肿瘤细胞和HHV-8病毒载量在胸膜液中将较弱。
进化和治疗
没有推荐的治疗PEL存在。中位生存率为6个月,1年生存率为39% [24].诊断时缺乏cART与预后不良有关,单独优化的cART可具有抗肿瘤活性,并可能导致缓解[24,110].一项文献回顾性研究表明,受累腔的数量与中位生存期相关[111].单腔受累患者的中位生存期比多腔受累患者的中位生存期长(18相对4个月)。对于只有一个腔受累的患者,心包受累和胸膜受累的患者比腹膜受累的患者中位生存期更长(分别为40个月、27个月和5个月)。
通常的治疗是多化疗,如CHOP,可能使用甲氨蝶呤。即使发病率很高,通常也能达到完全缓解(表2) [24,112].具有滑石或胸腔内侧卵巢的血液瘤化在姑息情况下可以讨论[113].
不推荐利妥昔单抗,因为肿瘤细胞不表达CD20,而利妥昔单抗会增加免疫缺陷。此外,cART与化疗相互作用。事实上,化疗必须在专门的中心进行。
有报道称,在胸膜内注射抗hhv -8药物西多福韦后,一些病例的缓解时间延长[114,115].在轶事病例中研究或报告了其他疗法,例如雷帕霉素,抗血管内皮生长因子治疗或干扰素[24,116,117].
结论
hiv感染患者HHV-8感染的呼吸道表现多种多样。HHV-8最常见的肺部表现是卡波西肉瘤,但自从引入cART后,卡波西肉瘤的患病率大大降低。呼吸系统表现在卡波西肉瘤,MCD或PEL中很常见。它们往往是这些疾病的最初表现,可能需要紧急治疗。这些疾病需要证明HHV-8感染。延迟诊断可能与MCD和PEL的不良预后有关。hiv感染患者或其他高危患者如免疫抑制或来自HHV-8流行国家的老年人的不明原因肺部疾病应提示HHV-8相关疾病。由于护理的稀缺性和复杂性,有理由向专业中心寻求建议。
脚注
利益冲突:无声明。
- 收到了2012年9月28日。
- 接受2012年11月27日。
- ©2013年