抽象
该假设是哮喘发作的儿童该预测可能通过呼出挥发性有机化合物(VOC)的剖面,气道炎症的非侵入性测量。本研究的目的是确定:1)呼出气体中的挥发性有机化合物是否能够预测哮喘发作;2)时间进程和最有预测挥发性有机化合物的化学背景。
对40名哮喘患儿进行了为期1年的前瞻性研究。在标准的2个月间隔,呼出一氧化氮分数(F依诺),呼出气样本,肺功能和症状在VOC型材以标准化的方式进行测定。VOC型材通过色谱 - 时间飞行气体质谱分析。
16出40名儿童的经历加重。随着支持向量机分析,基线测量的最优化模型对患者的病情加重基于6个VOCs(正确分类96%,敏感性100%,特异性93%)。与未加重者相比,患者基线值模型由7个VOCs组成(正确分类91%,敏感性79%,特异性100%)。F依诺肺功能不能预测病情的恶化。
这项研究表明,不同的VOCs呼出的组合能够预测儿童哮喘的发作。
介绍
哮喘治疗的目的是使疾病得到最佳控制[1]。几项横断面调查显示,哮喘控制的实际水平远远低于国家和国际准则的目标[2- - - - - -4]。H阿默尔等. [3.据报道,在荷兰,55%的哮喘儿童控制不良。哮喘控制不良和频繁发作可导致气道发生不可逆、病理和功能改变[5]。儿童哮喘往往有自己的抱怨相对于正常的肺功能,这导致的不良观感报告不足的症状,甚至漏诊哮喘[1,3.,6]。哮喘控制不良的另一种解释可能是,尽管哮喘的特征是慢性气道炎症,但目前还没有使用气道炎症的测量方法进行监测[7,8]。确实,有迹象表明,痰中嗜酸性粒细胞或呼出的呼吸中的一氧化氮可预测哮喘的加重[9,10]。
一个相对较新无创技术来评估在气道的气道炎症/氧化应激仿形呼出气中的挥发性有机化合物(VOC)的。在哮喘患者,生产活性氧物质(ROS)增加[11],导致细胞膜脂质过氧化,并产生挥发性有机化合物[12]。Dallinga等. [13]表明,呼出气中的VOCs可以哮喘儿童和对照之间具有高灵敏度和特异性鉴别。Dragonieri等。(14]研究了10名患有轻度哮喘的年轻人、10名患有严重哮喘的老年人和20名年龄相仿的对照组通过“电子鼻”对VOCs进行“嗅印”。他们发现,电子鼻可以区分哮喘患者和健康对照组,而不同哮喘严重程度等级之间的区别更加困难。
本纵向研究调查的假设哮喘患儿呼出气中挥发性有机化合物的具体能够预测加重他们临床表现之前。具体目标是研究:1)呼出气体中的挥发性有机化合物是否能够可靠地预测哮喘加重,并评估其VOC的组合是最能预测;和2)发作期当然VOC的时间。
方法
耐心
患有哮喘的年龄6-16岁的儿童从儿科呼吸科,马斯特里赫特大学医学中心(MUMC +),马斯特里赫特,荷兰系的门诊选定。所有的孩子都被称为在我们诊所有过哮喘的诊断≥6个月。哮喘是基于全球倡议的哮喘(GINA)和荷兰儿科协会肺病[以下标准定义1,15]:1)反复发作喘鸣、气促、胸闷或咳嗽;2)一次或多次可逆性气道阻塞(1s内用力呼气量增加(FEV1)400μg沙丁胺醇≥9%后预测[15]);和/或3)支气管对组胺的高反应性(定义为引起20% FEV下降所需的刺激性组胺浓度)1<8毫克·毫升−1)。
所有儿童均按GINA指引接受治疗[1]. 仅根据症状和肺功能进行治疗。当phadiatop试验和/或放射过敏原试验(RAST)呈阳性(至少两个RAST等级)时,儿童被视为特应性。排除标准为:1)可能干扰研究结果的疾病(如。其它慢性炎症性疾病);2)不能正确地执行测量;或3)主动吸烟。
研究设计
研究设计是一项为期一年的前瞻性纵向研究。除每2个月定期到门诊就诊外,患者在病情恶化时还要再去门诊就诊4次。在研究期间,这些额外的访问最多计划两次。在病情恶化的第1天、第3天和第5天以及FEV恢复后计划进行额外的测量1基线值及症状改善(表1)。
道德
这项研究得到了医学伦理委员会,MUMC+的批准。这个www.clinicaltrials.gov注册号为NCT00404859号。所有家长均给予书面知情同意。
呼气样本采集
至少在实验前1小时,不允许进食或体育锻炼。受试者被要求深吸一口气,然后呼气进入前面描述的无阻力的Tedlar袋(5升)[13,16,17]。通常一次到三次呼气就足以使袋子膨胀。有关呼气压力、采样时间及程序重现性的详情载于其他网页[16,17]。袋的内容物的标准化条件下转移到含有活性炭不锈钢两床吸附管(Markes国际公司,兰特里森特,UK)。挥发性有机化合物被困到碳部件,直到样品的分析。为了分析样品,挥发性有机化合物从该管通过热脱附在270℃(; Markes国际公司UNITY解吸单元)释放。挥发性有机化合物然后通过气相色谱法(GC)(赛默飞世科学,奥斯汀,TX,USA)分离,随后检测由时间飞行质谱(TOF-MS)(热电的Tempus加;赛默飞科学)如先前报道[13,16,17]。
成果措施
主要结果度量:哮喘恶化
哮喘发作是主要的预后指标。哮喘恶化的定义(中度和重度)是基于标准的美国胸腔学会和欧洲呼吸学会(人):1)增加哮喘症状(呼吸困难、咳嗽和喘息)和/或使用短效β188bet官网地址2激动剂为≥2天;和/或2)需要具有口服皮质类固醇治疗;和/或3)需要住院[18]。
以识别发作的早期阶段,AM1家庭监视器(CareFusion,Hoechberg,德国)和调制解调器(HCl; CareFusion)被使用。FEV1测量,使用急救药物和存在和肺部症状严重程度均在一个固定的时间每天记录。症状强度进行评分从0到3,所有患者的比例被要求进行演习10分钟内三次,最高FEV1(升)被储存。数据通过电话调制解调器以数字方式发送到MUMC+的个人计算机上,每周一次。在FEV恶化的情况下1值,和/或肺部症状的存在和严重程度的增加,患者被要求到医院进行额外的测量和咨询负责的儿科肺病医生。在门诊,评估哮喘控制分数和肺功能测试,收集呼吸样本。
次要成果措施
分析的数据
数据采集与挖掘
如前面详细描述的在连续的步骤中进行从GC-TOF-MS中的数据输出文件的分析[17]。总之,第一个步骤是在所有分析的输出文件中执行的峰值检测和基线校正。使用基于所述检测到的峰下的累积区域的区域缩放因子进行计算的峰面积进行归一化。所有样品的保留时间进行了评估。最后,输出文件由基于对应的质谱的相似度对应化合物组合合并,通过确定匹配因子值和保留时间相似性。使用基于所述相似性索引匹配因子的S描述质谱相似度计算TEIN和S科特(20]。
分析
为了分析其中的VOC是预测的哮喘加重的,分子内和个体间进行了比较。双方进行了比较研究,因为他们可能会提供不同的信息与问候,有助于早期发现哮喘患者病情加重的化合物。
个体内比较
第一探索比较是基线测量之间的个体内的比较(t=0)和恶化的第一次测量(t= E1). 基线测量是指在病情恶化开始前(测量0)平均在测量e前1个月采集的样本1。恶化时的测量结果按时间顺序表示为e1,E2,E3.和e4。之前的基线测量t= 0被表示为t= -1时,一个是t之前= -2,等等,如表1。
主体间的比较
第二项分析是主体间比较。基线样本(t= 0)的痛苦恶化受试者相比,受试者患有不恶化基线测量。所有纳入样本的抽样日期被选为彼此接近越好。
组件选择
随后的组分选择和感兴趣化合物的测定通过三种方式进行。1) 根据P新奥集团等。(21]。2)选取有或无加重的患儿中VOCs强度有显著差异的患儿(采用Bonferroni校正t检验)。样品在测量t=0来自于有恶化的患者,与没有恶化的组的样本进行比较(表1)。这些样本相匹配的日期t= 0的样品。3)支持向量机(SVM)分类模型来分析VOC的预测的哮喘恶化的能力。甲SVM是在统计和其分析数据和识别模式,并且用于分类和回归分析计算机科学的方法。标准SVM采用一组的输入数据和预测,对于每个给定的输入,其中两个可能的类形成输入,使得SVM一个非概率二元线性分类器。给定一组训练示例,每一个标记为属于两个类别中的一个,一个SVM的训练算法建立一个模型,分配新的实例为一类或其他。一个SVM模型是的例子如在空间中的点的表示,被映射,使得单独的类别的例子是由一个明显的差距是尽可能宽划分。然后新的例子被映射到相同的空间和预测的基础上,他们落入间隙哪边属于一个类别[22- - - - - -24]。
之所以选择SVM方法为它建造大型推广功率预测模型,即使在大维数据的情况下,当能力可用于训练的观测数低[22]。支持向量机是特别有用的,因为它们寻求全局优化的解决方案,避免过度拟合,允许大量的特性或化合物。为了获得化合物的最佳子集,使用了在Weka(怀卡托大学,汉密尔顿,新西兰)实现的属性选择选项[23]。化合物使用的SVM属性评估器选择。属性评估器通过考虑与它们之间的冗余沿着各化合物的单独的预测能力评价的化合物的一个子集的价值。优选地,被选择的化合物示出了类和低互相关内的高的相关性。排名最高的化合物的一个子集被实现为与P的顺序最小优化算法来训练SVM分类器LATT(24]。所述SVM分类进行了验证和性能,用10倍交叉验证,其中整个数据集重复分成测试组(90%的样品)和验证组(样品的10%)进行试验。
挥发性有机化合物的鉴定
通过从NIST库(标准与技术研究所的数据库),并通过质谱的解释由专门spectrometrist数据的质谱进行比较来进行VOC的鉴定。
动力分析
为了找到独立预测因子和至少0.6的恶化率之间临床上有意义的相关性,35名儿童有必要评估与0.05的双侧α和98%的功率这样的关系。在为期12个月的随访中,假设10%的辍学率。40名例哮喘患儿被纳入这项研究。
结果
病人的特点
在纳入研究的临床特征显示在表2。该组中大多数是特应性的:40名儿童中有29名(73%)是特应性的。除一名患者外,所有患者均接受吸入性糖皮质激素维持治疗。40名儿童中有38名完成了研究,两名患者退出了研究。一名患者离开了该地区。在他退学之前,他经历了一次病情恶化。这种恶化的数据包括在分析中。另一个孩子没有进一步参与的动机。她有稳定的哮喘。
恶化率
在1年的研究期间,16名儿童出现了病情加重,其中10名为中度,6名为重度。只有3名患者出现第二次恶化。均值±SE前述标准的测量和恶化的开始之间的时间间隔为39±4天。
挥发性有机化合物
数据分析中包含的挥发性有机物
在39名哮喘儿童中,共检测到3434种不同的VOCs。平均每个人检测到343种挥发性有机物。每名受试者根据病情恶化的情况提供7到15份样本。
明显不同的挥发性有机化合物的仪器
总的来说,经Bonferroni校正后,独立t检验显示30个VOCs有显著差异(p<0.001)。这些VOCs被确定为与病情恶化相关的标志物。
Timecourse的挥发性有机化合物的仪器
的显著不同的化合物的选择之后,这些挥发性有机化合物的所有其他样品中的跟踪(t= -2到e4)。在所有样本中测定了它们的相对强度,以便更深入地了解这些化合物在恶化前和恶化期间强度的时间进程。例如,三种VOCs在加重期间的强度过程如图所示图1。
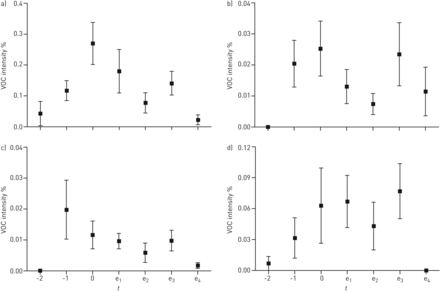
四种不同挥发性有机化合物(VOCs)的强度显示了它们在哮喘发作前和发作期间的时间进程。一)p二甲苯(弗里德曼检验p = 0.005);B)8,11- octadecadiynoic酸甲酯(弗里德曼检验p = 0.01);C)3,6- octadecadiynoic酸甲酯(弗里德曼检验p = 0.004);d)十八烷(弗里德曼检验p = 0.01)。数据表示为平均值±SE。对于时间点的定义(t),见表1。
预测哮喘恶化的能力
所有样本中≥8%的VOCs均纳入支持向量机分析,以评估VOCs预测哮喘发作的能力[16,17]。SVM模型的结果是基于综合考虑挥发性有机化合物。在SVM模型不同VOC的数目和相应的灵敏度和特异性之间的关系示于表3和4。在个体内的比较(基线对患者在发作期),在最佳运行状况的SVM是基于六个挥发性有机化合物。恶化被正确分类的样本中(100灵敏度%,特异性为93%,阳性预测值89%,阴性预测值100%)的96%,如图表3。最优的受试者间比较支持向量机(基线导致恶化对没有造成恶化基线,患者之间)是基于七个挥发性有机化合物。的91%A的正确分类率为78%和100%的相应的灵敏度和特异性实测值(正预测值100%,阴性预测值86%),分别为(表4)。既不F依诺也不肺功能是病情加重的无显著预测。的时间,直到病情恶化单变量Cox回归分析显示,无论是F依诺也不是FEV1是哮喘加重的重要预测因子(p=0.43和p=0.60)。
讨论
这项研究表明,呼出气中的VOC能够预测哮喘加重的儿童。我们发现,六和,七挥发性有机化合物的组合能够在两者之间和患者具有高灵敏度和特异性内预测病情加重。它也可以识别挥发性有机化合物是显著“跟踪”恶化的过程中。鉴定的挥发性有机化合物主要分为碳氢化合物。都F依诺本研究中肺功能对病情加重无显著预测价值。
据我们所知,这是首个分析呼出气体中挥发性有机化合物预测儿童哮喘恶化能力的纵向研究,并研究了挥发性有机化合物在哮喘恶化过程中的过程。在最近的一项研究中,I卜拉欣等。(25]研究了VOC谱在35例成人哮喘患者和23例对照组哮喘诊断、痰炎细胞谱和哮喘控制中的应用价值。他们证明,VOC图谱能够准确识别痰嗜酸性粒细胞增多症和疾病控制不良的患者,交叉验证的准确率分别为83%和80%。在对120名儿童(57名对照组和63名哮喘患者)的横断面研究中,我们发现在呼气中8种挥发性有机化合物的最佳组合基础上,哮喘和对照组之间有很好的区分[13]。在成人中,维ragonieri等。(14]利用电子鼻评估呼气中的挥发性有机化合物模式。他们发现哮喘可以与对照组进行鉴别,但不同程度哮喘严重程度的鉴别不能令人满意。与我们研究中使用的GC-TOF-MS不同,电子鼻用于Dragonieri等。(14]用于评估不同挥发性有机物的气味。这些技术是根本不同的,因为气味指纹是基于模式识别而不是评估单一质谱。气味指纹的缺点是它可能无法测量对鉴别很重要的特定挥发性有机化合物。在本研究中使用的方法的优点是能够检测出最具预测性的VOCs,并且能够阐明化合物的化学背景。这些信息可以在将来用来构建一个电子鼻,专门用于某种疾病(如。儿童哮喘)和一个特定的临床问题(如。早期发现病情恶化)。
定期评估两个月F依诺在这项研究并不能预测病情加重。
在Fritsch等。(26] 47名儿童患有轻度至中度哮喘,F依诺在截止29 PPB的点是最能预测具有80%的灵敏度和60%的特异性的恶化。在P的吸入糖皮质激素撤药研究ijnenburg等。(27]F依诺值> 49 ppb的4周停药后不得不为71%的哮喘复发和93%的特异性的灵敏度。在非特哮喘患者,F依诺可以不升高[28]. 呼气中VOC分析的优点是在呼气中同时测定多种炎症标志物,并可选择最具预测性的生物标志物,这表明VOCs组合在本研究中具有较高的敏感性和特异性。
讨论我们研究的几个要素是相关的。首先,纳入40名哮喘儿童,其中16名儿童在随访年内病情加重。虽然我们的研究通过10倍的交叉验证进行了内部验证,并且可以用良好的敏感性和特异性预测病情的恶化,但我们的研究需要在更大的研究人群中进行外部验证,以确定VOCs的最佳组合[29]。40名儿童中有29名患有特应症,但我们的儿童数量太少,无法进行a治疗事后本组分析。
其次,VOC的存在可以通过本征(性别,年龄,体重,特应性和肺功能)和外在因素(影响如。环境空气或药物)。在我们的研究中,这些内在因素大部分得到了很好的控制。此外,在研究过程中,这些内在因素、药物和病情恶化之间没有发现任何关系。这几乎排除了这些因素对本研究结果的可能影响。目前,对于环境空气中的VOC对呼出气体中VOC谱的作用还没有统一的认识。在每一阶段,所有的孩子都在同一个房间里接受测量,因此,他们都受到了环境空气的影响。正如V之前所报道的一个Berkel等。(17]和dallinga等。(13,我们并没有校正我们对样品中化学背景的测量。这是由于这样一个事实,即通过简单地减去从呼出的空气中吸入的挥发性有机化合物,不可能纠正排泄和吸收挥发性有机化合物之间复杂的相互依赖关系。此外,背景噪声将随机分布在受试者的样本之间,因此,不会产生任何歧视性的力量,也不会干扰分析的结果。我们的目标是进行鉴别分析,只选择那些对疾病或条件有特异性的化合物,因此,主要不依赖于背景化学物质。我们的研究小组较早前的一份报告认为,抽样、化学分析、数据处理和准确数据挖掘的程序是高度可重复的[17]。此外,所使用药物的化学结构和代谢物没有反映在显著预测VOCs。
第三,确定挥发性有机化合物的起源仍然在一些情况下不确定的。我们能够识别大部分的预测挥发性有机化合物的。
我们假设鉴别反映挥发性有机化合物的气道炎症和氧化应激的程度。呼出气中的饱和烃(VOCs)是细胞膜的脂肪酸成分的脂质过氧化过程中形成的。这个过程是通过ROS [触发17,三十- - - - - -35]。
在未来,它是相关研究的VOC的基础上抗炎治疗的滴定是预防哮喘的发作有帮助。此外,研究是必要的澄清生化起源,病理生理功能和测量预测VOC的最佳方式。
呼吸分析反映了人体肺部的生化和免疫过程。本研究表明VOC谱可预测儿童哮喘发作。未来的研究需要在更大的患者样本中对结果进行外部验证,以探索这些VOCs的性质,并研究在日常临床实践中将呼气分析作为一个参数时,是否可以更好地控制哮喘。
脚注
利益冲突:未申报。
- 收到2012年1月17日。
- 接受2012年10月15日。
- ©ERS 2013















